Дейтерий - Deuterium
 | |
| Общий | |
|---|---|
| Символ | 2ЧАС |
| Имена | дейтерий, H-2, водород-2, D |
| Протоны | 1 |
| Нейтронов | 1 |
| Данные о нуклидах | |
| Природное изобилие | 0,0115% (Земля)[1] |
| Изотопная масса | 2.01410177811[2] ты |
| Вращение | 1+ |
| Избыточная энергия | 13135.720± 0.001 кэВ |
| Связующая энергия | 2224,52 ± 0,20 кэВ |
| Изотопы водорода Полная таблица нуклидов | |
Дейтерий (или же водород-2, символ 2
ЧАС
или же
D
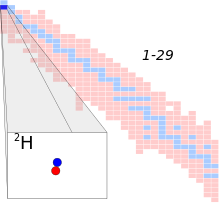
, также известный как тяжелый водород) является одним из двух стабильные изотопы из водород (другое существо протий, или водород-1). В ядро дейтерия атом, называется дейтрон, содержит один протон и один нейтрон, тогда как гораздо более распространенный протий не имеет нейтронов в ядре. Дейтерий имеет природное изобилие в земных океаны около одного атома в 6420 водорода. Таким образом, дейтерий составляет примерно 0,02% (0,03% по массе) от всего природного водорода в океанах, в то время как на протий приходится более 99,98%. Содержание дейтерия незначительно меняется от одной природной воды к другой (см. Венская стандартная средняя океанская вода ).
Название дейтерий происходит от греческого Deuteros, что означает «вторая», для обозначения двух частиц, составляющих ядро.[3] Дейтерий был открыт и назван в 1931 г. Гарольд Юри. Когда в 1932 году был открыт нейтрон, это сделало ядерную структуру дейтерия очевидной, и Юри выиграл Нобелевская премия в 1934 г. «за открытие тяжелого водорода». Вскоре после открытия дейтерия Юри и другие получили образцы "тяжелая вода "в котором содержание дейтерия было высоко концентрированным.
Дейтерий разрушается в недрах звезд быстрее, чем производится. Считается, что другие естественные процессы производят лишь незначительное количество дейтерия. Почти весь дейтерий, встречающийся в природе, был произведен в Большой взрыв 13,8 миллиарда лет назад, так как основное или изначальное отношение водорода-1 к дейтерию (около 26 атомов дейтерия на миллион атомов водорода) возникло с того времени. Это соотношение наблюдается у планет газовых гигантов, таких как Юпитер. Анализ отношений дейтерия и протия в кометах показал, что результаты очень похожи на среднее отношение в океанах Земли (156 атомов дейтерия на миллион атомов водорода). Это подкрепляет теории о том, что большая часть океанской воды Земли имеет кометное происхождение.[4][5] Отношение дейтерия к протию кометы 67П / Чурюмов-Герасименко, как измерено Розетта Космический зонд, примерно в три раза больше земной воды. Это самый высокий показатель для кометы.[6]
Таким образом, отношения дейтерия к протию продолжают оставаться активной темой исследований как в астрономии, так и в климатологии.
Отличия от обычного водорода (протия)
Химический символ

Дейтерий часто представлен химический символ D. Поскольку это изотоп водород с массовое число 2, он также представлен 2
ЧАС
. ИЮПАК позволяет как D, так и 2
ЧАС
, несмотря на то что 2
ЧАС
является предпочтительным.[7] Для удобства используется отчетливый химический символ, поскольку изотоп широко используется в различных научных процессах. Кроме того, его большая разница в массе с протий (1H) (дейтерий имеет массу 2.014102 тыпо сравнению с иметь в виду водород атомный вес из 1.007947 ты, а масса протия 1.007825 ты) дает существенные химические различия с протийсодержащими соединениями, тогда как массовые отношения изотопов в других химических элементах в этом отношении в значительной степени незначительны.
Спектроскопия
В квантовая механика уровни энергии электронов в атомах зависят от уменьшенная масса системы электрона и ядра. Для атом водорода, роль приведенной массы проще всего увидеть в Модель Бора атома, где приведенная масса появляется в простом вычислении Постоянная Ридберга и уравнение Ридберга, но приведенная масса также появляется в Уравнение Шредингера, а Уравнение Дирака для расчета уровней атомной энергии.
Приведенная масса системы в этих уравнениях близка к массе отдельного электрона, но отличается от нее на небольшую величину, примерно равную отношению массы электрона к массе ядра атома. Для водорода это количество составляет примерно 1837/1836, или 1.000545, а для дейтерия еще меньше: 3671/3670, или 1.0002725. Энергии спектроскопических линий дейтерия и легкого водорода (водород-1 ) поэтому различаются соотношением этих двух чисел, которое составляет 1.000272. Длины волн всех спектральных линий дейтерия короче соответствующих линий легкого водорода в 1.000272 раз. В астрономических наблюдениях это соответствует синему доплеровскому смещению, в 0,000272 раза превышающему скорость света, или 81,6 км / с.[8]
Различия более выражены в колебательной спектроскопии, такой как ИК-спектроскопия и Рамановская спектроскопия,[9] и во вращательных спектрах, таких как микроволновая спектроскопия поскольку уменьшенная масса дейтерия заметно выше, чем протия. В спектроскопия ядерного магнитного резонанса, дейтерий имеет совсем другое ЯМР частота (например, 61 МГц при частоте протия 400 МГц) и намного менее чувствительна. Дейтерированные растворители обычно используются в протиевом ЯМР для предотвращения перекрытия растворителя с сигналом, хотя дейтерий ЯМР само по себе также возможно.
Нуклеосинтез Большого взрыва
Считается, что дейтерий сыграл важную роль в определении количества и соотношений элементов, которые образовались в Большой взрыв. Объединение термодинамика и изменения, вызванные космическим расширением, можно вычислить долю протоны и нейтроны основанный на температуре в точке, когда Вселенная остыла достаточно, чтобы позволить образование ядра. Этот расчет показывает семь протонов на каждый нейтрон в начале нуклеогенез, соотношение, которое останется стабильным даже после завершения нуклеогенеза. Первоначально эта доля была в пользу протонов, прежде всего потому, что меньшая масса протона способствовала их образованию. По мере расширения Вселенная остывала. Свободные нейтроны и протоны менее стабильны, чем гелий ядер, а протоны и нейтроны имели сильную энергетическую причину для образования гелий-4. Однако для образования гелия-4 требуется промежуточный этап образования дейтерия.
В течение большей части нескольких минут после Большого взрыва, во время которых мог произойти нуклеосинтез, температура была достаточно высокой, так что средняя энергия, приходящаяся на одну частицу, была больше энергии связи слабосвязанного дейтерия; поэтому любой образовавшийся дейтерий немедленно разрушался. Эта ситуация известна как узкое место дейтерия. Узкое место задерживало образование любого гелия-4 до тех пор, пока Вселенная не стала достаточно холодной, чтобы образовался дейтерий (примерно при температуре, эквивалентной 100 ° C). кэВ ). В этот момент произошел внезапный всплеск образования элементов (сначала дейтерий, который немедленно слился с гелием). Однако вскоре после этого, через двадцать минут после Большого взрыва, Вселенная стала слишком холодной для дальнейшего термоядерная реакция и произойдет нуклеосинтез. К этому моменту содержание элементов было почти фиксированным, с единственным изменением, так как некоторые из радиоактивный продукты нуклеосинтеза Большого взрыва (такие как тритий ) разлагаться.[10] Дейтерий-узкое место в образовании гелия вместе с отсутствием стабильных способов соединения гелия с водородом или с самим собой (стабильных ядер с массовыми числами пять или восемь) означало, что незначительное количество углерода или каких-либо элементов тяжелее углерода, образовавшегося в результате Большого взрыва. Таким образом, эти элементы требовали образования звезд. В то же время отказ от значительной части нуклеогенеза во время Большого взрыва гарантировал, что в более поздней Вселенной будет достаточно водорода, доступного для образования долгоживущих звезд, таких как наше Солнце.
Избыток
Дейтерий встречается в следовых количествах в природе в виде дейтерия. газ, написано 2
ЧАС
2 или D2, но большинство естественных атомов в Вселенная связаны с типичным 1
ЧАС
атом, газ, называемый дейтерид водорода (HD или 1
ЧАС
2
ЧАС
).[11]
Существование дейтерия на Земле, в других местах Солнечная система (что подтверждено планетными зондами), а в спектрах звезды, также является важным элементом в космология. Гамма-излучение от обычного ядерного синтеза диссоциирует дейтерий на протоны и нейтроны, и нет никаких известных естественных процессов, кроме Нуклеосинтез Большого взрыва, который мог бы произвести дейтерий в количестве, близком к его наблюдаемому естественному содержанию. Дейтерий производится редкими кластерный распад и случайное поглощение естественных нейтронов легким водородом, но это тривиальные источники. Считается, что внутри Солнца и других звезд мало дейтерия, так как при таких температурах реакции ядерного синтеза которые потребляют дейтерий, происходят намного быстрее, чем протон-протонная реакция что создает дейтерий. Однако дейтерий сохраняется во внешней атмосфере Солнца в примерно той же концентрации, что и на Юпитере, и это, вероятно, не изменилось с момента возникновения Солнечной системы. Естественное содержание дейтерия, кажется, очень похоже на долю водорода, где бы водород ни находился, если только не работают очевидные процессы, которые его концентрируют.
Существование дейтерия с низкой, но постоянной первичной долей во всем водороде - еще один аргумент в пользу Большой взрыв теория над Теория устойчивого состояния Вселенной. Наблюдаемое соотношение водорода, гелия и дейтерия во Вселенной трудно объяснить, кроме как с помощью модели Большого взрыва. По оценкам, содержание дейтерия существенно не изменилось с момента его производства около 13,8 миллиарда лет назад.[12] Измерения галактического дейтерия в Млечном Пути с помощью ультрафиолетового спектрального анализа показывают соотношение целых 23 атомов дейтерия на миллион атомов водорода в невозмущенных газовых облаках, что всего на 15% ниже WMAP По оценкам, изначальное соотношение около 27 атомов на миллион от Большого взрыва. Это было интерпретировано как означающее, что при звездообразовании в нашей галактике было разрушено меньше дейтерия, чем ожидалось, или, возможно, дейтерий был восполнен за счет большого поступления первичного водорода из-за пределов галактики.[13] В космосе в нескольких сотнях световых лет от Солнца содержание дейтерия составляет всего 15 атомов на миллион, но на это значение предположительно влияет дифференциальная адсорбция дейтерия на зернах углеродной пыли в межзвездном пространстве.[14]
Обилие дейтерия в атмосфере Юпитер был напрямую измерен Космический зонд Галилео как 26 атомов на миллион атомов водорода. Наблюдения ISO-SWS обнаружили 22 атома на миллион атомов водорода в Юпитере.[15] и это изобилие, как полагают, соответствует соотношению, близкому к изначальной солнечной системе.[5] Это примерно 17% земного отношения дейтерия к водороду, составляющего 156 атомов дейтерия на миллион атомов водорода.
Кометные тела, такие как Комета Хейла-Боппа и Комета Галлея было измерено, что они содержат относительно больше дейтерия (около 200 атомов D на миллион водородов), отношения, которые обогащены по отношению к предполагаемому соотношению протосолнечной туманности, вероятно, из-за нагрева, и которые аналогичны отношениям, обнаруженным в морской воде Земли. Недавнее измерение количества дейтерия в 161 атоме D на миллион водорода в комете 103P / Hartley (бывший Пояс Койпера объект), соотношение почти точно такое же, как в океанах Земли, подчеркивает теорию, согласно которой поверхностные воды Земли могут быть в значительной степени образованы кометами.[4][5] Совсем недавно отношение дейтерия к протию (D – H) составляло 67P / Чурюмов – Герасименко как измерено Розетта примерно в три раза больше земной воды, и это высокий показатель.[6] Это вызвало новый интерес к предположениям о том, что вода на Земле может иметь частично астероидное происхождение.
Также наблюдалось, что концентрация дейтерия превышает среднюю солнечную концентрацию на других планетах земной группы, в частности на Марсе и Венере.
Производство
Дейтерий производят для промышленных, научных и военных целей, начиная с обычной воды, небольшая часть которой встречается в природе. тяжелая вода - а затем отделить тяжелую воду Сульфидный процесс Гирдлера, дистилляция или другие методы.
Теоретически дейтерий для тяжелой воды может быть получен в ядерном реакторе, но отделение от обычной воды - самый дешевый процесс массового производства.
Ведущим мировым поставщиком дейтерия был Атомная энергия Канады Лимитед до 1997 года, когда была остановлена последняя установка по производству тяжелой воды. Канада использует тяжелую воду в качестве замедлитель нейтронов для работы Реактор CANDU дизайн.
Другой крупный производитель тяжелой воды - Индия. Все атомные электростанции Индии, кроме одной, представляют собой установки с тяжелой водой под давлением, в которых используется природный (то есть необогащенный) уран. В Индии восемь заводов по производству тяжелой воды, семь из которых находятся в эксплуатации. Шесть установок, пять из которых находятся в эксплуатации, основаны на обмене D – H в газообразном аммиаке. Два других завода извлекают дейтерий из природной воды в процессе, в котором используется сероводород под высоким давлением.
В то время как Индия самодостаточна тяжелой водой для собственного использования, Индия теперь также экспортирует тяжелую воду реакторного качества.
Характеристики
Физические свойства
Физические свойства соединений дейтерия могут существенно различаться. кинетические изотопные эффекты а также другие отличия физических и химических свойств от аналогов протия. D2О, например, больше вязкий чем ЧАС2О.[16] В химическом отношении существуют различия в энергии и длине связи для соединений тяжелых изотопов водорода по сравнению с протием, которые больше, чем изотопные различия в любом другом элементе. Связи с участием дейтерия и тритий несколько сильнее, чем соответствующие связи в протии, и этих различий достаточно, чтобы вызвать существенные изменения в биологических реакциях. Фармацевтические фирмы заинтересованы в том, что дейтерий сложнее удалить из углерода, чем протий.[17]
Дейтерий может заменять протий в молекулах воды с образованием тяжелой воды (D2O), которая примерно на 10,6% плотнее, чем обычная вода (так что лед, сделанный из нее, тонет в обычной воде). Тяжелая вода немного токсична в эукариотический животных, при этом 25% замещения воды в организме вызывают проблемы с делением клеток и бесплодие, а замещение 50% вызывает смерть от цитотоксического синдрома (недостаточность костного мозга и повреждение слизистой оболочки желудочно-кишечного тракта). Прокариотический организмы, однако, могут выжить и расти в чистой тяжелой воде, хотя и развиваются медленно.[18] Несмотря на эту токсичность, потребление тяжелой воды при нормальных обстоятельствах не представляет опасности. угроза здоровью людям. Подсчитано, что человек весом 70 кг (154 фунта) может выпить 4,8 литра (1,3 галлона США) тяжелой воды без серьезных последствий.[19] Небольшие дозы тяжелой воды (несколько граммов для людей, содержащие количество дейтерия, сравнимое с тем, которое обычно присутствует в организме) обычно используются в качестве безвредных метаболических индикаторов для людей и животных.
Квантовые свойства
Дейтрон имеет вращение +1 ("триплетное состояние ") и, таким образом, бозон. В ЯМР частота дейтерия существенно отличается от обычного легкого водорода. ИК-спектроскопия также легко различает многие дейтерированные соединения из-за большой разницы в частоте ИК-поглощения, наблюдаемой при колебании химической связи, содержащей дейтерий, по сравнению с легким водородом. Два стабильных изотопа водорода также можно различить, используя масс-спектрометрии.
Нуклон триплетного дейтрона практически не связан в EB = 2,23 МэВ, и ни одно из состояний с более высокой энергией не связано. Синглетный дейтрон представляет собой виртуальное состояние с отрицательной энергией связи ~ 60 кэВ. Такой стабильной частицы нет, но эта виртуальная частица временно существует во время неупругого рассеяния нейтрона на протоне, что объясняет необычно большое сечение рассеяния нейтронов протоном.[20]
Ядерные свойства (дейтрон)
Масса и радиус дейтрона
Ядро дейтерия называется дейтрон. Он имеет массу 2.013553212745(40) ты (чуть более 1,875 ГэВ).[21][22]
В радиус заряда дейтрона 2.12799(74) FM.[23]
Словно радиус протона, измерения с использованием мюонный дейтерий дает меньший результат: 2.12562(78) FM.[24]
Спин и энергия
Дейтерий - один из пяти стабильных нуклиды с нечетным числом протонов и нечетным числом нейтронов. (2
ЧАС
, 6
Ли
, 10
B
, 14
N
, 180 м
Та
; также долгоживущие радиоактивные нуклиды 40
K
, 50
V
, 138
Ла
, 176
Лу
происходят естественно.) Большинство нечетно-нечетные ядра нестабильны по отношению к бета-распад, потому что продукты распада даже-даже, и поэтому связаны более сильно из-за эффекты спаривания ядер. Дейтерий, однако, выигрывает от того, что его протон и нейтрон связаны со спином 1, что дает более сильное ядерное притяжение; соответствующее состояние со спином 1 не существует в двухнейтронной или двухпротонной системе из-за Принцип исключения Паули что потребовало бы, чтобы одна или другая идентичная частица с тем же спином имела другое квантовое число, например орбитальный угловой момент. Но орбитальный угловой момент любой частицы дает меньшее энергия связи для системы, прежде всего из-за увеличения расстояния между частицами в крутом градиенте ядерной силы. В обоих случаях это вызывает дипротон и динейтрон ядро быть неустойчивый.
Протон и нейтрон, составляющие дейтерий, могут быть диссоциированный через нейтральный ток взаимодействие с нейтрино. В поперечное сечение поскольку это взаимодействие сравнительно велико, и дейтерий успешно использовался в качестве нейтринной мишени в Нейтринная обсерватория Садбери эксперимент.
Двухатомный дейтерий (D2) имеет орто и пара ядерные спиновые изомеры как двухатомный водород, но с различия в количестве и заселенности спиновых состояний и вращательных уровней, которые происходят из-за того, что дейтрон является бозон с ядерным спином, равным единице.[25]
Изоспин-синглетное состояние дейтрона
Из-за сходства массы и ядерных свойств между протоном и нейтроном их иногда рассматривают как два симметричных типа одного и того же объекта: нуклон. Хотя электрический заряд есть только у протона, им часто можно пренебречь из-за слабости электромагнитное взаимодействие относительно сильное ядерное взаимодействие. Симметрия, связывающая протон и нейтрон, известна как изоспин и обозначен я (или иногда Т).
Изоспин - это SU (2) симметрия, как обычная вращение, поэтому полностью аналогичен ему. Протон и нейтрон, каждый из которых имеет изоспин-1⁄2, образуют изоспиновый дублет (аналог спин дублет ), где «нижнее» состояние (↓) - нейтрон, а «верхнее» состояние (↑) - протон.[нужна цитата ] Пара нуклонов может находиться в антисимметричном состоянии изоспина, называемом синглет, или в симметричном состоянии, называемом триплет. Что касается состояния «вниз» и «вверх», синглет
- , что также можно записать:
Это ядро с одним протоном и одним нейтроном, то есть ядро дейтерия. Тройка
и, таким образом, состоит из трех типов ядер, которые должны быть симметричными: ядро дейтерия (на самом деле сильно возбужденное состояние его), ядро с двумя протонами и ядро с двумя нейтронами. Эти состояния нестабильны.
Приближенная волновая функция дейтрона
Волновая функция дейтрона должна быть антисимметричной, если используется изоспиновое представление (поскольку протон и нейтрон не являются идентичными частицами, волновая функция не должна быть антисимметричной в целом). Помимо изоспина, два нуклона также имеют спиновые и пространственные распределения своей волновой функции. Последний симметричен, если дейтрон симметричен относительно паритет (т.е. иметь "четную" или "положительную" четность) и антисимметричный, если дейтрон антисимметричен относительно четности (т.е. имеет "нечетную" или "отрицательную" четность). Четность полностью определяется полным орбитальным угловым моментом двух нуклонов: если он четный, то четность четная (положительная), а если она нечетная, то четность нечетная (отрицательная).
Дейтрон, будучи изоспиновым синглетом, антисимметричен по отношению к обмену нуклонами из-за изоспина и, следовательно, должен быть симметричным по отношению к двойному обмену их спина и местоположения. Следовательно, он может находиться в одном из следующих двух разных состояний:
- Симметричный спин и симметричный относительно четности. В этом случае обмен двумя нуклонами умножит волновую функцию дейтерия на (-1) из-за изоспинового обмена, (+1) из-за спинового обмена и (+1) из-за четности (обмен местоположения), в сумме (-1 ) по мере необходимости для антисимметрии.
- Антисимметричный спин и антисимметричный по четности. В этом случае обмен двумя нуклонами будет умножать волновую функцию дейтерия на (-1) из-за изоспинового обмена, (-1) из-за спинового обмена и (-1) из-за четности (обмен местоположения), снова в сумме (- 1) для антисимметрии.
В первом случае дейтрон представляет собой спиновый триплет, так что его полный спин s равно 1. Он также имеет четность и, следовательно, орбитальный угловой момент. л ; Чем меньше его орбитальный угловой момент, тем меньше его энергия. Следовательно, самое низкое возможное энергетическое состояние имеет s = 1, л = 0.
Во втором случае дейтрон является синглетом спина, так что его полный спин s равно 0. Он также имеет нечетную четность и, следовательно, нечетный орбитальный угловой момент. л. Следовательно, самое низкое возможное энергетическое состояние имеет s = 0, л = 1.
С s = 1 дает более сильное ядерное притяжение, дейтерий основное состояние находится в s =1, л = 0 государственный.
Те же соображения приводят к возможным состояниям изоспинового триплета, имеющего s = 0, л = даже или же s = 1, л = нечетный. Таким образом, состояние с наименьшей энергией s = 1, л = 1, выше, чем у изоспинового синглета.
Только что приведенный анализ на самом деле является лишь приблизительным, потому что изоспин не является точной симметрией, и, что более важно, потому что сильное ядерное взаимодействие между двумя нуклонами связано с угловой момент в спин-орбитальное взаимодействие это смешивает разные s и л состояния. То есть, s и л непостоянны во времени (они не ездить с Гамильтониан ), а со временем такое состояние, как s = 1, л = 0 может стать состоянием s = 1, л = 2. Четность остается постоянной во времени, поэтому они не смешиваются с нечетными л состояния (например, s = 0, л = 1). Следовательно квантовое состояние дейтерия - это суперпозиция (линейная комбинация) s = 1, л = 0 государство и s = 1, л = 2 состояние, хотя первый компонент намного больше. Поскольку полный угловой момент j это тоже хорошо квантовое число (это постоянная во времени), оба компонента должны иметь одинаковые j, и поэтому j = 1. Это полный спин ядра дейтерия.
Таким образом, ядро дейтерия антисимметрично по изоспину, имеет спин 1 и четность (+1). Относительный угловой момент его нуклонов л не очень хорошо определен, и дейтрон является суперпозицией в основном л = 0 с некоторыми л = 2.
Магнитные и электрические мультиполи
Чтобы теоретически найти дейтерий магнитный дипольный момент μ используется формула для ядерный магнитный момент
с
грамм(l) и г(s) находятся g-факторы нуклонов.
Поскольку протон и нейтрон имеют разные значения для g(l) и г(s), необходимо разделить их вклады. Каждый получает половину орбитального углового момента дейтерия. и вращать . Один прибывает в
где нижние индексы p и n обозначают протон и нейтрон, а грамм(l)п = 0.
Используя те же идентификаторы, что и здесь и используя значение грамм(l)п = 1, мы приходим к следующему результату в единицах ядерный магнитный момент
Для s = 1, л = 0 государственный (j = 1), мы получаем
Для s = 1, л = 2 государственный (j = 1), мы получаем
Измеренное значение дейтерия магнитный дипольный момент, является 0,857 мкмN, что составляет 97,5% от 0,879 мкмN значение, полученное простым сложением моментов протона и нейтрона. Это говорит о том, что состояние дейтерия действительно в хорошем приближении. s = 1, л = 0 состояние, которое возникает, когда оба нуклона вращаются в одном направлении, но их магнитные моменты вычитаются из-за отрицательного момента нейтрона.
Но немного меньшее экспериментальное число, чем то, которое получается в результате простого сложения протонного и (отрицательного) нейтронного моментов, показывает, что дейтерий на самом деле представляет собой линейную комбинацию в основном s = 1, л = 0 состояние с небольшой примесью s = 1, л = 2 государственный.
В электрический диполь ноль как обычно.
Измеряемая электрическая квадруполь дейтерия 0.2859 е ·FM2. Хотя порядок величины разумный, поскольку радиус дейтерия составляет порядка 1 фемтометра (см. Ниже) и его электрический заряд is e, приведенная выше модель не подходит для ее расчета. В частности, электрический квадруполь не получает взнос от л = 0 (которое является доминирующим) и действительно получает вклад от члена, смешивающего л = 0 и л = 2 состояния, поскольку электрический квадруполь оператор не ездить с угловой момент.
Последний вклад является доминирующим при отсутствии чистого л = 0 вклад, но не может быть вычислен без знания точной пространственной формы нуклонов волновая функция внутри дейтерия.
Высшее магнитное и электрическое мультипольные моменты не может быть рассчитан по вышеуказанной модели по аналогичным причинам.
Приложения
Дейтерий имеет ряд коммерческих и научных применений. К ним относятся:
Ядерные реакторы
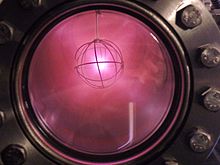
Дейтерий используется в реакторы деления с тяжеловодным замедлителем, обычно в виде жидкости D2О, чтобы замедлить нейтроны без высокого поглощения нейтронов, как у обычного водорода.[26] Это обычное коммерческое использование больших количеств дейтерия.
В исследовательские реакторы, жидкость D2 используется в источники холода умерять нейтроны до очень низких энергий и длин волн, подходящих для эксперименты по рассеянию.
Экспериментально дейтерий является наиболее распространенным нуклидом, используемым в термоядерная реакция конструкции реакторов, особенно в сочетании с тритий, из-за большой скорости реакции (или ядерное сечение ) и высокий энергия выход D – T реакции. Есть еще более доходный D–3
Он
реакция синтеза, хотя точка равновесия из D–3
Он
выше, чем у большинства других реакций синтеза; вместе с нехваткой 3
Он
, это делает его неприемлемым в качестве практического источника энергии до тех пор, пока, по крайней мере, реакции синтеза D – T и D – D не будут выполнены в промышленном масштабе. Коммерческий ядерный синтез еще не реализован.
ЯМР-спектроскопия
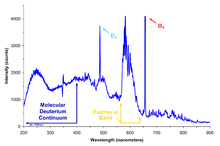
Дейтерий чаще всего используется в водороде. спектроскопия ядерного магнитного резонанса (протонный ЯМР ) следующим образом. ЯМР обычно требует, чтобы интересующие соединения анализировались как растворенные в растворе. Из-за ядерных спиновых свойств дейтерия, которые отличаются от легкого водорода, обычно присутствующего в органических молекулах, спектры ЯМР водорода / протия сильно отличаются от спектров дейтерия, и на практике дейтерий не «виден» прибором ЯМР, настроенным на легкий водород. . Дейтерированные растворители (включая тяжелую воду, а также такие соединения, как дейтерированный хлороформ, CDCl3) поэтому обычно используются в ЯМР-спектроскопии, чтобы можно было измерить только спектры легкого водорода интересующего соединения без интерференции сигнала растворителя.
Спектроскопия ядерного магнитного резонанса также может быть использована для получения информации об окружении дейтрона в образцах, меченных изотопами (ЯМР дейтерия ). Например, гибкость хвоста, представляющего собой длинную углеводородную цепь, в молекулах липидов, меченных дейтерием, можно количественно оценить с помощью твердотельного дейтериевого ЯМР.[27]
Спектры ЯМР дейтерия особенно информативны в твердом состоянии из-за его относительно небольшого квадрупольного момента по сравнению с более крупными квадрупольными ядрами, такими как, например, хлор-35.
Отслеживание
В химия, биохимия и науки об окружающей среде, дейтерий используется как нерадиоактивный, стабильный изотопный индикатор, например, в тест воды с двойной меткой. В химические реакции и метаболические пути, дейтерий ведет себя подобно обычному водороду (с некоторыми химическими отличиями, как уже отмечалось). Его легче всего отличить от обычного водорода по массе, используя масс-спектрометрии или же инфракрасная спектрометрия. Дейтерий может быть обнаружен фемтосекунда инфракрасный спектроскопия, так как разница масс резко влияет на частоту молекулярных колебаний; Колебания связи дейтерий-углерод обнаруживаются в спектральных областях, свободных от других сигналов.
Измерения небольших вариаций естественного содержания дейтерия и стабильных тяжелых изотопов кислорода. 17O и 18O важны в гидрология, чтобы проследить географическое происхождение вод Земли. Тяжелые изотопы водорода и кислорода в дождевой воде (так называемые метеорная вода ) обогащаются в зависимости от температуры окружающей среды в регионе, в котором выпадают осадки (и, таким образом, обогащение связано со средней широтой). Относительное обогащение тяжелыми изотопами в дождевой воде (по отношению к средней воде океана) при нанесении на график зависимости от температуры предсказуемо падает вдоль линии, называемой глобальная линия метеорной воды (GMWL). Этот график позволяет идентифицировать образцы воды, образовавшейся в результате атмосферных осадков, а также общую информацию о климате, в котором они возникли. Процессы испарения и другие процессы в водоемах, а также процессы в грунтовых водах также по-разному изменяют соотношения тяжелых изотопов водорода и кислорода в пресных и соленых водах характерными и часто регионально различимыми способами.[28] Соотношение концентрации 2H к 1H обычно обозначается с дельтой как δ2H и географические модели этих значений нанесены на карты, называемые изоскопами. Стабильные изотопы входят в состав растений и животных, и анализ соотношений у перелетных птиц или насекомых может помочь предложить приблизительное руководство к их происхождению.[29][30]
Контрастные свойства
Рассеяние нейтронов методы особенно выигрывают от наличия дейтерированных образцов: сечения H и D очень четкие и различаются по знаку, что позволяет варьировать контраст в таких экспериментах. Кроме того, неприятной проблемой обычного водорода является его большое некогерентное нейтронное сечение, которое равно нулю для D. Таким образом, замещение атомов водорода атомами дейтерия снижает шум рассеяния.
Водород - важный и главный компонент во всех материалах органической химии и биологических наук, но он почти не взаимодействует с рентгеновскими лучами. Поскольку водород (и дейтерий) сильно взаимодействуют с нейтронами, методы рассеяния нейтронов вместе с современной установкой дейтерирования,[31] заполняет нишу во многих исследованиях макромолекул в биологии и многих других областях.
Ядерное оружие
Это обсуждается ниже. Примечательно, что, хотя большинство звезд, включая Солнце, генерируют энергию на протяжении большей части своей жизни, превращая водород в более тяжелые элементы, такой синтез легкого водорода (протия) никогда не был успешным в условиях, достижимых на Земле. Таким образом, весь искусственный синтез, включая синтез водорода, который происходит в так называемых водородных бомбах, требует тяжелого водорода (трития или дейтерия, либо того и другого) для того, чтобы этот процесс работал.
Наркотики
Дейтерированный препарат - это малая молекула лекарственный препарат, в котором один или несколько из водород атомы, содержащиеся в молекуле лекарства, заменены дейтерием. Из-за кинетический изотопный эффект дейтерийсодержащие препараты могут иметь значительно более низкие показатели метаболизм, и, следовательно, более длинный период полураспада.[32][33][34] В 2017 г. дейетрабеназин стал первым дейтерированным препаратом, получившим одобрение FDA.[35]
Усиление основных питательных веществ
Дейтерий можно использовать для усиления определенных уязвимых к окислению связей C-H в основных или условных пределах. основные питательные вещества,[36] такие как определенные аминокислоты, или же полиненасыщенные жирные кислоты (ПНЖК), что делает их более устойчивыми к окислительному повреждению. Дейтерированный полиненасыщенный жирные кислоты, Такие как линолевая кислота, замедлить цепную реакцию перекисное окисление липидов повреждают живые клетки.[37][38] Дейтерированный этиловый эфир линолевой кислоты (RT001 ), разработанный Retrotope, находится в испытание на сострадание в детская нейроаксональная дистрофия и успешно завершил испытание фазы I / II в Атаксия Фридрейха.[39][35]
Термостабилизация
Живые вакцины, такие как пероральная вакцина против полиовируса, может быть стабилизирован дейтерием отдельно или в сочетании с другими стабилизаторами, такими как MgCl2.[40]
Замедление циркадных колебаний
Было показано, что дейтерий удлиняет период колебаний циркадных часов при введении крыс, хомяков и других животных. Гоньяулакс динофлагелляты.[41][42][43][44] У крыс при хроническом приеме 25% D2O нарушает циркадную ритмику, удлиняя циркадный период супрахиазматическое ядро -зависимые ритмы в гипоталамусе головного мозга.[45] Эксперименты на хомяках также подтверждают теорию о том, что дейтерий действует непосредственно на супрахиазматическое ядро для удлинения циркадного периода без перерыва.[46]
История
Подозрение на изотопы легких элементов
Существование нерадиоактивных изотопов более легких элементов подозревалось в исследованиях неона еще в 1913 году и доказано масс-спектрометрией легких элементов в 1920 году. Преобладающая теория в то время заключалась в том, что изотопы элемента различаются наличием дополнительных протоны в ядре в сопровождении равного количества ядерные электроны. Согласно этой теории, ядро дейтерия с массой два и зарядом один будет содержать два протона и один ядерный электрон. Однако ожидалось, что элемент водород с измеренной средней атомной массой очень близок к 1 ты, известная масса протона, всегда имеет ядро, состоящее из одного протона (известной частицы), и не может содержать второй протон. Таким образом, считалось, что водород не содержит тяжелых изотопов.
Обнаружен дейтерий

Впервые он был обнаружен спектроскопически в конце 1931 г. Гарольд Юри, химик в Колумбийский университет. Соавтор Юри, Фердинанд Брикведде, дистиллированный пять литры из cryogenically produced жидкий водород к 1 мл of liquid, using the low-temperature physics laboratory that had recently been established at the National Bureau of Standards in Washington, D.C. (now the Национальный институт стандартов и технологий ). The technique had previously been used to isolate heavy isotopes of neon. The cryogenic boiloff technique concentrated the fraction of the mass-2 isotope of hydrogen to a degree that made its spectroscopic identification unambiguous.[47][48]
Naming of the isotope and Nobel Prize
Urey created the names протий, дейтерий, и тритий in an article published in 1934. The name is based in part on advice from G. N. Lewis who had proposed the name "deutium". Название происходит от греческого deuteros ('second'), and the nucleus to be called "deuteron" or "deuton". Isotopes and new elements were traditionally given the name that their discoverer decided. Some British scientists, such as Эрнест Резерфорд, wanted the isotope to be called "diplogen", from the Greek diploos ('double'), and the nucleus to be called "diplon".[3][49]
The amount inferred for normal abundance of this heavy isotope of hydrogen was so small (only about 1 atom in 6400 hydrogen atoms in ocean water (156 deuteriums per million hydrogens)) that it had not noticeably affected previous measurements of (average) hydrogen atomic mass. This explained why it hadn't been experimentally suspected before. Urey was able to concentrate water to show partial enrichment of deuterium. Lewis had prepared the first samples of pure heavy water in 1933. The discovery of deuterium, coming before the discovery of the нейтрон in 1932, was an experimental shock to theory, but when the neutron was reported, making deuterium's existence more explainable, deuterium won Urey the Нобелевская премия по химии in 1934. Lewis was embittered by being passed over for this recognition given to his former student.[3]
"Heavy water" experiments in World War II
Shortly before the war, Ганс фон Хальбан и Лью Коварски moved their research on neutron moderation from France to Britain, smuggling the entire global supply of heavy water (which had been made in Norway) across in twenty-six steel drums.[50][51]
В течение Вторая Мировая Война, нацистская Германия was known to be conducting experiments using heavy water as moderator for a ядерный реактор дизайн. Such experiments were a source of concern because they might allow them to produce плутоний для Атомная бомба. Ultimately it led to the Союзник operation called the "Норвежский саботаж тяжелой воды ", the purpose of which was to destroy the Веморк deuterium production/enrichment facility in Norway. At the time this was considered important to the potential progress of the war.
After World War II ended, the Allies discovered that Germany was not putting as much serious effort into the program as had been previously thought. They had been unable to sustain a chain reaction. The Germans had completed only a small, partly built experimental reactor (which had been hidden away). By the end of the war, the Germans did not even have a fifth of the amount of heavy water needed to run the reactor,[требуется разъяснение ] partially due to the Norwegian heavy water sabotage operation. However, even had the Germans succeeded in getting a reactor operational (as the U.S. did with a graphite reactor in late 1942), they would still have been at least several years away from development of an Атомная бомба with maximal effort. The engineering process, even with maximal effort and funding, required about two and a half years (from first critical reactor to bomb) in both the U.S. and СССР, Например.
In thermonuclear weapons

The 62-ton Айви Майк device built by the United States and exploded on 1 November 1952, was the first fully successful "hydrogen bomb " (thermonuclear bomb). In this context, it was the first bomb in which most of the energy released came from ядерная реакция stages that followed the primary ядерное деление этап Атомная бомба. The Ivy Mike bomb was a factory-like building, rather than a deliverable weapon. At its center, a very large cylindrical, insulated vacuum flask или же криостат, держал криогенный liquid deuterium in a volume of about 1000 литры (160 kilograms in mass, if this volume had been completely filled). Then, a conventional Атомная бомба (the "primary") at one end of the bomb was used to create the conditions of extreme temperature and pressure that were needed to set off the thermonuclear reaction.
Within a few years, so-called "dry" hydrogen bombs were developed that did not need cryogenic hydrogen. Released information suggests that all термоядерное оружие built since then contain химические соединения of deuterium and lithium in their secondary stages. The material that contains the deuterium is mostly дейтерид лития, with the lithium consisting of the isotope литий-6. When the lithium-6 is bombarded with fast нейтроны from the atomic bomb, тритий (hydrogen-3) is produced, and then the deuterium and the tritium quickly engage in термоядерный синтез, releasing abundant energy, helium-4, and even more free neutrons.
Modern research
In August 2018, scientists announced the transformation of gaseous deuterium into a liquid metallic form. This may help researchers better understand giant gas planets, such as Jupiter, Saturn and related экзопланеты, since such planets are thought to contain a lot of liquid metallic hydrogen, which may be responsible for their observed powerful магнитные поля.[52][53]
Data for elemental deuterium
Formula: D2 или же 2
1ЧАС
2
- Плотность: 0.180 kg/m3 в STP (0 ° C, 101.325 kPa).
- Atomic weight: 2.0141017926 ты.
- Mean abundance in ocean water (from VSMOW ) 155.76 ± 0.1 ppm (a ratio of 1 part per approximately 6420 parts), that is, about 0.015% of the atoms in a sample (by number, not weight)
Data at approximately 18 K для D2 (тройная точка ):
- Плотность:
- Liquid: 162.4 kg/m3
- Gas: 0.452 kg/m3
- Viscosity: 12.6 μPa·s в 300 К (газовая фаза)
- Specific heat capacity at constant pressure cп:
- Solid: 2950 J/(kg·K)
- Gas: 5200 J/(kg·K)
Antideuterium
An антидейтрон это антивещество counterpart of the nucleus of deuterium, consisting of an антипротон и антинейтрон. The antideuteron was first produced in 1965 at the Proton Synchrotron в ЦЕРН[54] и Синхротрон с переменным градиентом в Брукхейвенская национальная лаборатория.[55] A complete atom, with a позитрон orbiting the nucleus, would be called антидейтерий, но по состоянию на 2019 год[Обновить] antideuterium has not yet been created. The proposed symbol for antideuterium is
D
, that is, D with an overbar.[56]
Смотрите также
Рекомендации
- ^ "Nudat 2".
- ^ Wang, M .; Audi, G .; Кондев, Ф. Г .; Huang, W. J .; Naimi, S .; Xu, X. (2017). "The AME2016 atomic mass evaluation (II). Tables, graphs, and references" (PDF). Chinese Physics C. 41 (3): 030003-1–030003-442. Дои:10.1088/1674-1137/41/3/030003.
- ^ а б c O'Leary D (February 2012). "The deeds to deuterium". Nature Chemistry. 4 (3): 236. Bibcode:2012NatCh...4..236O. Дои:10.1038/nchem.1273. PMID 22354440.
- ^ а б Hartogh P, Lis DC, Bockelée-Morvan D, de Val-Borro M, Biver N, Küppers M, et al. (Октябрь 2011 г.). «Океаноподобная вода в комете семейства Юпитера 103P / Hartley 2». Природа. 478 (7368): 218–20. Bibcode:2011Натура.478..218H. Дои:10.1038 / природа10519. PMID 21976024.
- ^ а б c Hersant F, Gautier D, Hure J (2001). "A Two-dimensional Model for the Primordial Nebula Constrained by D/H Measurements in the Solar System: Implications for the Formation of Giant Planets". Астрофизический журнал. 554 (1): 391–407. Bibcode:2001ApJ...554..391H. Дои:10.1086/321355.
see fig. 7. for a review of D/H ratios in various astronomical objects
- ^ а б Altwegg K, Balsiger H, Bar-Nun A, Berthelier JJ, Bieler A, Bochsler P, et al. (Январь 2015 г.). "Cometary science. 67P/Churyumov-Gerasimenko, a Jupiter family comet with a high D/H ratio" (PDF). Наука. 347 (6220): 1261952. Bibcode:2015Научный ... 347А.387А. Дои:10.1126 / science.1261952. PMID 25501976. retrieved 12 Dec 2014
- ^ "§ IR-3.3.2 Provisional Recommendations". Номенклатура неорганической химии. Chemical Nomenclature and Structure Representation Division, ИЮПАК. Архивировано из оригинал 27 октября 2006 г.. Получено 3 октября 2007.
- ^ Hébrard G, Péquignot D, Vidal-Madjar A, Walsh JR, Ferlet R (7 February 2000). "Detection of deuterium Balmer lines in the Orion Nebula". Астрономия и астрофизика. 354: L79. arXiv:astro-ph/0002141. Bibcode:2000A&A...354L..79H.
- ^ Water Absorption Spectrum. lsbu.ac.uk
- ^ Weiss A. "Equilibrium and change: The physics behind Big Bang Nucleosynthesis". Einstein Online. Получено 24 февраля 2007.
- ^ IUPAC Commission on Nomenclature of Inorganic Chemistry (2001). "Names for Muonium and Hydrogen Atoms and their Ions" (PDF). Чистая и прикладная химия. 73 (2): 377–380. Дои:10.1351/pac200173020377.
- ^ "Космические детективы". Европейское космическое агентство (ЕКА). 2 апреля 2013 г.. Получено 15 апреля 2013.
- ^ NASA FUSE Satellite Solves the Case of the Missing Deuterium. НАСА
- ^ graph of deuterium with distance in our galactic neighborhood В архиве 5 декабря 2013 г. Wayback Machine Смотрите также Linsky JL, Draine BT, Moos HW, Jenkins EB, Wood BE, Oliveira C, et al. (2006). "What is the Total Deuterium Abundance in the Local Galactic Disk?". Астрофизический журнал. 647 (2): 1106–1124. arXiv:astro-ph/0608308. Bibcode:2006ApJ...647.1106L. Дои:10.1086/505556.
- ^ Lellouch E, Bézard B, Fouchet T, Feuchtgruber H, Encrenaz T, de Graauw T (2001). "The deuterium abundance in Jupiter and Saturn from ISO-SWS observations" (PDF). Астрономия и астрофизика. 670 (2): 610–622. Bibcode:2001A&A...370..610L. Дои:10.1051/0004-6361:20010259.
- ^ Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ Halford B (4 July 2016). "The deuterium switcheroo". Новости химии и машиностроения. Американское химическое общество. С. 32–36.
- ^ Kushner DJ, Baker A, Dunstall TG (February 1999). "Pharmacological uses and perspectives of heavy water and deuterated compounds". Канадский журнал физиологии и фармакологии. 77 (2): 79–88. Дои:10.1139/cjpp-77-2-79. PMID 10535697.
- ^ Vertes, Attila, ed. (2003). "Physiological effect of heavy water". Elements and isotopes: formation, transformation, distribution. Dordrecht: Kluwer. С. 111–112. ISBN 978-1-4020-1314-0.
- ^ Neutron-Proton Scattering. (PDF). mit.edu. Проверено 23 ноября 2011.
- ^ deuteron mass in u. Physics.nist.gov. Retrieved on 2020-09-18.
- ^ deuteron mass energy equivalent in MeV. Physics.nist.gov. Retrieved on 2020-09-18.
- ^ deuteron rms charge radius. Physics.nist.gov. Retrieved on 2020-09-18.
- ^ Pohl R, Nez F, Fernandes LM, Amaro FD, Biraben F, Cardoso JM, et al. (The CREMA Collaboration) (August 2016). "Laser spectroscopy of muonic deuterium". Наука. 353 (6300): 669–73. Bibcode:2016Sci...353..669P. Дои:10.1126/science.aaf2468. HDL:10316/80061. PMID 27516595.
- ^ Hollas JM (1996). Современная спектроскопия (3-е изд.). Джон Уайли и сыновья. п. 115. ISBN 0-471-96523-5.
- ^ Видеть нейтронное сечение # Типичные сечения
- ^ Seelig J (October 1971). "On the flexibility of hydrocarbon chains in lipid bilayers". Журнал Американского химического общества. 93 (20): 5017–22. Дои:10.1021/ja00749a006. PMID 4332660.
- ^ "Oxygen – Isotopes and Hydrology". САХРА. Архивировано из оригинал 2 января 2007 г.. Получено 10 сентября 2007.
- ^ West JB (2009). Isoscapes: Understanding movement, pattern, and process on Earth through isotope mapping. Springer.
- ^ Hobson KA, Van Wilgenburg SL, Wassenaar LI, Larson K (2012). "Linking hydrogen (δ2H) isotopes in feathers and precipitation: sources of variance and consequences for assignment to isoscapes". PLOS ONE. 7 (4): e35137. Bibcode:2012PLoSO...735137H. Дои:10.1371/journal.pone.0035137. ЧВК 3324428. PMID 22509393.
- ^ "NMI3 – Deuteration". NMI3. Получено 23 января 2012.
- ^ Sanderson K (March 2009). "Big interest in heavy drugs". Природа. 458 (7236): 269. Дои:10.1038/458269a. PMID 19295573.
- ^ Katsnelson A (June 2013). "Heavy drugs draw heavy interest from pharma backers". Природа Медицина. 19 (6): 656. Дои:10.1038/nm0613-656. PMID 23744136.
- ^ Gant TG (May 2014). "Using deuterium in drug discovery: leaving the label in the drug". Журнал медицинской химии. 57 (9): 3595–611. Дои:10.1021/jm4007998. PMID 24294889.
- ^ а б Schmidt C (June 2017). "First deuterated drug approved". Природа Биотехнологии. 35 (6): 493–494. Дои:10.1038/nbt0617-493. PMID 28591114.
- ^ Demidov VV (September 2007). "Heavy isotopes to avert ageing?". Тенденции в биотехнологии. 25 (9): 371–5. Дои:10.1016/j.tibtech.2007.07.007. PMID 17681625.
- ^ Halliwell, Barry; Gutteridge, John M.C. (2015). Free Radical Biology and Medicine (5th ed.). Оксфорд: Clarendon Press. ISBN 9780198717485.
- ^ Hill S, Lamberson CR, Xu L, To R, Tsui HS, Shmanai VV, et al. (Август 2012 г.). «Небольшие количества усиленных изотопами полиненасыщенных жирных кислот подавляют автоокисление липидов». Свободная радикальная биология и медицина. 53 (4): 893–906. Дои:10.1016 / j.freeradbiomed.2012.06.004. ЧВК 3437768. PMID 22705367.
- ^ https://clinicaltrials.gov/ct2/show/NCT02445794
- ^ Wu R, Georgescu MM, Delpeyroux F, Guillot S, Balanant J, Simpson K, Crainic R (August 1995). "Thermostabilization of live virus vaccines by heavy water (D2O)". Вакцина. 13 (12): 1058–63. Дои:10.1016/0264-410X(95)00068-C. PMID 7491812.
- ^ Lesauter J, Silver R (September 1993). "Heavy water lengthens the period of free-running rhythms in lesioned hamsters bearing SCN grafts". Физиология и поведение. 54 (3): 599–604. Дои:10.1016/0031-9384(93)90255-E. ISSN 0031-9384.
- ^ McDaniel M, Sulzman FM, Hastings JW (November 1974). "Heavy water slows the Gonyaulax clock: a test of the hypothesis that D2O affects circadian oscillations by diminishing the apparent temperature". Труды Национальной академии наук Соединенных Штатов Америки. 71 (11): 4389–91. Дои:10.1073/pnas.71.11.4389. ЧВК 433889. PMID 4530989.
- ^ Petersen CC, Mistlberger RE (August 2017). "Interval Timing Is Preserved Despite Circadian Desynchrony in Rats: Constant Light and Heavy Water Studies". Журнал биологических ритмов. 32 (4): 295–308. Дои:10.1177/0748730417716231. PMID 28651478.
- ^ Richter CP (March 1977). "Heavy water as a tool for study of the forces that control length of period of the 24-hour clock of the hamster". Труды Национальной академии наук Соединенных Штатов Америки. 74 (3): 1295–9. Дои:10.1073/pnas.74.3.1295. ЧВК 430671. PMID 265574.
- ^ Petersen CC, Mistlberger RE (August 2017). "Interval Timing Is Preserved Despite Circadian Desynchrony in Rats: Constant Light and Heavy Water Studies". Журнал биологических ритмов. 32 (4): 295–308. Дои:10.1177/0748730417716231. PMID 28651478.
- ^ Lesauter J, Silver R (September 1993). "Heavy water lengthens the period of free-running rhythms in lesioned hamsters bearing SCN grafts". Физиология и поведение. 54 (3): 599–604. Дои:10.1016/0031-9384(93)90255-E.
- ^ Brickwedde FG (1982). "Harold Urey and the discovery of deuterium". Физика сегодня. 35 (9): 34. Bibcode:1982PhT....35i..34B. Дои:10.1063/1.2915259.
- ^ Urey H, Brickwedde F, Murphy G (1932). "A Hydrogen Isotope of Mass 2". Физический обзор. 39 (1): 164–165. Bibcode:1932PhRv...39..164U. Дои:10.1103/PhysRev.39.164.
- ^ "Science: Deuterium v. Diplogen". Время. 19 February 1934.
- ^ Sherriff L (1 June 2007). "Royal Society unearths top secret nuclear research". Реестр. Situation Publishing Ltd. Получено 3 июн 2007.
- ^ "The Battle for Heavy Water Three physicists' heroic exploits". Бюллетень ЦЕРН. Европейская организация ядерных исследований. 25 марта 2002 г.. Получено 2 ноября 2015.
- ^ Chang K (16 August 2018). "Settling Arguments About Hydrogen With 168 Giant Lasers". Нью-Йорк Таймс. Получено 18 августа 2018.
- ^ "Under pressure, hydrogen offers a reflection of giant planet interiors". Carnegie Institution for Science. 15 августа 2018 г.. Получено 19 августа 2018.
- ^ Massam T, Muller T, Righini B, Schneegans M, Zichichi A (1965). "Experimental observation of antideuteron production". Il Nuovo Cimento. 39 (1): 10–14. Bibcode:1965NCimS..39...10M. Дои:10.1007/BF02814251.
- ^ Dorfan DE, Eades J, Lederman LM, Lee W, Ting CC (June 1965). "Observation of Antideuterons". Phys. Rev. Lett. 14 (24): 1003–1006. Bibcode:1965PhRvL..14.1003D. Дои:10.1103/PhysRevLett.14.1003.
- ^ Chardonnet P, Orloff J, Salati P (1997). "The production of anti-matter in our galaxy". Письма по физике B. 409 (1–4): 313–320. arXiv:astro-ph/9705110. Bibcode:1997PhLB..409..313C. Дои:10.1016/S0370-2693(97)00870-8.
внешняя ссылка
- Nuclear Data Center at KAERI
- "Annotated bibliography for deuterium". ALSOS: The Digital Library for Nuclear Issues. Архивировано из оригинал 5 мая 2010 г.. Получено 26 ноября 2019.
- Mullins, Justin (27 April 2005). "Desktop nuclear fusion demonstrated". Новый ученый.
- Lloyd, Robin (21 August 2006). "Missing Gas Found in Milky Way". Space.com.
| Более легкий: hydrogen-1 | Deuterium is an изотоп из водород | Тяжелее: hydrogen-3 |
| Продукт распада из: — | Цепочка распада of deuterium | Распада к: Стабильный |









![{ displaystyle mu = { frac {1} {4 (j + 1)}} left [({g ^ {(s)}} _ {p} + {g ^ {(s)}} _ { n}) { big (} j (j + 1) -l (l + 1) + s (s + 1) { big)} + { big (} j (j + 1) + l (l + 1) -s (s + 1) { big)} right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a3c23357e4baf596b679ef024306fab09a5396a8)


