Гипофтористая кислота - Hypofluorous acid
 Газофазная структура | |
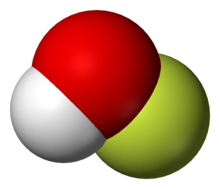 | |
| Имена | |
|---|---|
| Название ИЮПАК Гипофтористая кислота | |
| Другие имена Гипофторит водорода Фтористый водород (-I) Плавиковая (-I) кислота Монофтороксигенат водорода (0) гидроксил фторид | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| HOF | |
| Молярная масса | 36,0057 г моль−1 |
| Внешность | бледно-желтая жидкость выше −117 ° C белое твердое вещество ниже −117 ° C |
| Температура плавления | -117 ° С (-179 ° F, 156 К) |
| Точка кипения | разлагается при 0 ° C[нужна цитата ] |
| Структура | |
| Cs | |
| Опасности | |
| Главный опасности | сильный окислитель, коррозионный |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другой катионы | гипофторит лития |
Родственные соединения | хлорноватистая кислота нитроксил цианистый водород формальдегид |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гипофтористая кислота, химическая формула ЧАСОF, это единственный известный оксокислота фтора и единственной известной оксикислоты, из которой основной атом получает электроны кислород для создания отрицательной степени окисления. Степень окисления кислорода в гипофторитах равна 0. Это также единственный гипогалогеновая кислота который можно выделить как твердый. HOF - это средний в окисление из воды к фтор, который производит фтороводород, дифторид кислорода, пероксид водорода, озон и кислород. HOF взрывоопасен при комнатной температуре, образуя HF и O2:
- 2 HOF → 2 HF + O2[1]
Он был выделен в чистом виде путем передачи F2газ над льдом при -40 ° C, собирая газ HOF и конденсируя его:
- F2 + H2O → HOF + HF
В твердой фазе соединение характеризуется: Рентгеновская кристаллография[1] как изогнутая молекула с углом 101 °. Длины связей O – F и O – H составляют 144,2 и 96,4. пикометры, соответственно. Твердый каркас состоит из цепочек со связями O – H ··· O. Структура также была проанализирована в газовой фазе, состоянии, в котором валентный угол H – O – F немного уже (97,2 °).
Гипофтористая кислота в ацетонитриле (образуется на месте пропусканием газообразного фтора через «мокрый» ацетонитрил ) широко известен как Реактив Розена.[2][3][4]
Гипофлюориты
Гипофториты формально являются производными OF−, какой сопряженное основание гипофтористой кислоты. Одним из примеров является трифторметилгипофторит (CF3ИЗ).
Смотрите также
- Хлорноватистая кислота, родственное соединение, которое является более технологически важным, но не было получено в чистом виде.
Рекомендации
- ^ а б W. Poll; Г. Павелке; Д. Муц; Э. Х. Аппельман (1988). "Кристаллическая структура гипофтористой кислоты: образование цепей водородными связями O-H · · · O". Энгью. Chem. Int. Эд. Англ. 27 (3): 392–3. Дои:10.1002 / anie.198803921.
- ^ Розен, Шломо (2001). «Гипофтористоводородная кислота». Энциклопедия реагентов для органического синтеза. Дои:10.1002 / 047084289X.rh074. ISBN 0471936235.
- ^ Розен, Шломо (2014). «HOF · CH3CN: возможно, лучший агент переноса кислорода, который может предложить органическая химия». Соотв. Chem. Res. 47 (8): 2378–2389. Дои:10.1021 / ar500107b. PMID 24871453.
- ^ Сингх, Раман; Каур, Раджниш; Гупта, Таранг; Кульбир, Кульбир; Сингх, Калдип (2019). "Применение реагента Розена в реакциях переноса кислорода и активации C-H". Синтез. 51 (2): 371–383. Дои:10.1055 / с-0037-1609638.

