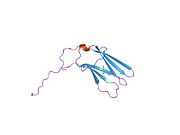
Киназа рецептора тропомиозина А - Tropomyosin receptor kinase A
Киназа рецептора тропомиозина А (TrkA),[5] также известный как рецептор фактора роста нервов с высоким сродством, нейротрофический рецептор тирозинкиназы типа 1, или же TRK1-трансформирующий белок тирозинкиназы это белок что у людей кодируется НТРК1 ген.[6]
Этот ген кодирует член семейство нейротрофических тирозинкиназных рецепторов (NTKR). Эта киназа представляет собой мембранно-связанный рецептор, который при нейротрофин связывание, фосфорилирует себя (аутофосфорилирование ) и члены Путь MAPK. Присутствие этой киназы приводит к дифференцировке клеток и может играть роль в определении подтипов сенсорных нейронов. Мутации в этом гене были связаны с врожденная нечувствительность к боли при ангидрозе, членовредительство, умственная отсталость и / или когнитивные нарушения и некоторые раки. Обнаружены альтернативные варианты транскрипционного сплайсинга этого гена, но на сегодняшний день охарактеризованы только три.[7]
Функция
TrkA это высокое сродство каталитический рецептор для нейротрофин, Фактор роста нервов, или «NGF». Таким образом, он опосредует множественные эффекты NGF, которые включают: нейронный дифференциация и избегание запрограммированная гибель клеток.
Члены семьи
TrkA является частью подсемейства протеинкиназ, которое включает: TrkB и TrkC. Также существуют другие нейротрофические факторы, структурно связанные с NGF: BDNF (для нейротрофического фактора мозга), NT-3 (для нейротрофина-3) и NT-4 (для нейротрофина-4). Хотя TrkA опосредует эффекты NGF, TrkB связан и активируется BDNF, NT-4 и NT-3. Дальше, TrkC связывается и активируется NT-3.[8]
Помимо TrkA, существует еще один рецептор NGF, который называется "СПГФР " (за "Рецептор фактора роста нервов с низким сродством "). В отличие от TrkA, LNGFR играет несколько менее очевидную роль в биологии NGF. Некоторые исследователи показали, что LNGFR связывается и служит" приемником "для нейротрофинов. Следовательно, клетки, которые экспрессируют рецепторы LNGFR и Trk, могут иметь большую активность - поскольку они имеют более высокую «микроконцентрацию» нейротрофина. Однако также было показано, что в отсутствие коэкспрессируемого TrkA LNGFR может сигнализировать клетке о смерти через апоптоз - поэтому клетки, экспрессирующие LNGFR в отсутствие рецепторов Trk может скорее погибнуть, чем жить в присутствии нейротрофина.
Роль в болезни
TrkA был первоначально клонирован из опухоли толстой кишки; рак произошел в результате транслокации, которая привела к активации киназного домена TrkA. Однако сам TrkA не выглядит онкоген.[нужна цитата ]
В одном исследовании было обнаружено полное отсутствие рецептора TrkA у кератоконус -поврежденные роговицы, наряду с повышенным уровнем репрессорной изоформы Фактор транскрипции Sp3.[9]
Было показано, что слияния генов с участием NTRK1 являются онкогенными, что приводит к конститутивной активации TrkA.[10] В исследовании, проведенном Вайшнави А. и др., Слияние NTRK1, по оценкам, встречается в 3,3% случаев рака легких. секвенирование следующего поколения или же флуоресценция in situ гибридизация.[10]
Регулирование
Уровни различных белков можно регулировать с помощью "убиквитин /протеасома "система. В этой системе небольшой (7–8 кДа) белок, называемый"убиквитин "прикреплен к белку-мишени и, таким образом, нацелен на разрушение структурой, называемой"протеасома ". TrkA нацелен на опосредованное протеасомами разрушение" E3 убиквитинлигаза " называется NEDD4-2.[11] Этот механизм может быть отличным способом контролировать выживание нейрона. Степень и, возможно, тип убиквитиниации TrkA могут регулироваться другим, неродственным рецептором NGF, p75NTR.
Взаимодействия
TrkA был показан взаимодействовать с:
Лиганды
Небольшие молекулы, такие как амитриптилин и гамбожовая кислота производные, как утверждается, активируют TrkA. Амитриптилин активирует TrkA и способствует гетеродимеризации TrkA и TrkB в отсутствие NGF. Связывание амитриптилина с TrkA происходит с богатой лейцином областью (LRR) внеклеточного домена рецептора, который отличается от сайта связывания NGF. Амитриптилин обладает нейротрофической активностью как in vitro и in vivo (модель мыши).[29] Гамбогический амид, производное гамбожьей кислоты, избирательно активирует TrkA (но не TrkB и TrkC ) обе in vitro и in vivo путем взаимодействия с цитоплазматическим юкстамембранным доменом TrkA.[30]
Роль в раке
Первоначально идентифицированный как онкогенное слияние в 1982 году,[31] только недавно возобновился интерес к семейству Trk, поскольку оно связано с его ролью в раковых заболеваниях человека из-за идентификации слияния генов NTRK1 (TrkA), NTRK2 (TrkB) и NTRK3 (TrkC) и других онкогенных изменений в ряде типы опухолей. Номер Ингибиторы Trk находятся (в 2015 г.) в клинических испытаниях и показали первые результаты в уменьшении опухолей человека.[32]
Ингибиторы в развитии
Энтректиниб (ранее RXDX-101) - исследуемый препарат, разработанный Ignyta, Inc., обладающий потенциальной противоопухолевой активностью. Это селективный рецептор pan-trk. ингибитор тирозинкиназы (TKI), нацеленные на слияние генов в trkA, trkB, и trkC (закодировано НТРК1, НТРК2, и НТРК3 гены), который в настоящее время проходит фазу 2 клинических испытаний.[33]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000198400 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000028072 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 8: Атипичные нейротрансмиттеры». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. ISBN 9780071481274.
Другой общей особенностью нейротрофинов является то, что они оказывают свое физиологическое действие посредством семейства рецепторов рецепторной киназы тропомиозина (Trk) (также известного как семейство рецепторов тирозиновых киназ). ...
Рецепторы Trk
Все нейротрофины связываются с классом высокогомологичных рецепторных тирозинкиназ, известных как рецепторы Trk, из которых известны три типа: TrkA, TrkB и TrkC. Эти трансмембранные рецепторы представляют собой гликопротеины с молекулярными массами от 140 до 145 кДа. Каждый тип рецептора Trk имеет тенденцию связывать определенные нейротрофины: TrkA является рецептором для NGF, TrkB является рецептором для BDNF и NT-4, а TrkC является рецептором для NT-3. Однако было отмечено некоторое совпадение специфичности этих рецепторов. . - ^ Мартин-Занка Д., Хьюз С.Х., Барбакид М. (апрель 1986 г.). «Онкоген человека, образованный путем слияния усеченных последовательностей тропомиозина и протеинтирозинкиназы». Природа. 319 (6056): 743–8. Дои:10.1038 / 319743a0. PMID 2869410.
- ^ «Ген Entrez: нейротрофическая тирозинкиназа NTRK1, рецептор, тип 1».
- ^ Бенито-Гутьеррес Э., Гарсия-Фернандес Дж., Комелла Дж. Х (февраль 2006 г.). «Происхождение и эволюция семейства нейротрофических рецепторов Trk». Мол. Клетка. Неврологи. 31 (2): 179–92. Дои:10.1016 / j.mcn.2005.09.007. PMID 16253518.
- ^ Ламбиасе А, Мерло Д., Моллинари С., Бонини П., Ринальди А.М., Д'Амато М., Мицера А., Коассин М., Рама П., Бонини С., Гарачи Е. (ноябрь 2005 г.). «Молекулярная основа кератоконуса: отсутствие экспрессии TrkA и его репрессия транскрипции с помощью Sp3». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 102 (46): 16795–800. Дои:10.1073 / pnas.0508516102. ЧВК 1283852. PMID 16275928.
- ^ а б Вайшнави, Ария; Капеллетти, Марция; Le, Anh T .; Како, Северина; Бутани, Мохит; Эркан, Далия; Махале, Сакши; Дэвис, Куртис Д .; Айснер, Дара Л. (01.11.2013). «Онкогенные и лекарственно-чувствительные перестройки NTRK1 при раке легких». Природа Медицина. 19 (11): 1469–1472. Дои:10,1038 / нм.3352. ISSN 1546–170X. ЧВК 3823836. PMID 24162815.
- ^ Ю. Т., Кальво Л., Анта Б., Лопес-Бенито С., Саутон Е., Чао М. В., Тессаролло Л., Аревало Дж. К. (апрель 2011 г.). «Регулирование трафика активированного TrkA имеет решающее значение для функций, опосредованных NGF». Трафик. 12 (4): 521–34. Дои:10.1111 / j.1600-0854.2010.01156.x. ЧВК 3547592. PMID 21199218.
- ^ а б c d Кох А., Манчини А., Стефан М., Ниденталь Р., Ниманн Х., Тамура Т. (март 2000 г.). «Прямое взаимодействие рецептора фактора роста нервов, TrkA, с нерецепторной тирозинкиназой, c-Abl, через петлю активации». FEBS Lett. 469 (1): 72–6. Дои:10.1016 / S0014-5793 (00) 01242-4. PMID 10708759.
- ^ Яно Х., Конг Ф., Бирге Р. Б., Гофф С. П., Чао М. В. (февраль 2000 г.). «Ассоциация тирозинкиназы Abl с рецептором фактора роста нервов Trk». J. Neurosci. Res. 59 (3): 356–64. Дои:10.1002 / (SICI) 1097-4547 (20000201) 59: 3 <356 :: AID-JNR9> 3.0.CO; 2-G. PMID 10679771.
- ^ а б c Мекин С.О., Макдональд Д.И., Грыз Е.А., Кубу С.Дж., Верди Дж.М. (апрель 1999 г.). «Адаптер передачи сигналов FRS-2 конкурирует с Shc за связывание с рецептором фактора роста нервов TrkA. Модель для различения пролиферации и дифференцировки». J. Biol. Chem. 274 (14): 9861–70. Дои:10.1074 / jbc.274.14.9861. PMID 10092678.
- ^ Песня C, Perides G, Лю Ю.Ф. (февраль 2002 г.). «Экспрессия полноразмерного удлиненного полиглутамином Хантингтина нарушает передачу сигналов рецептора фактора роста в клетках феохромоцитомы крысы (PC12)». J. Biol. Chem. 277 (8): 6703–7. Дои:10.1074 / jbc.M110338200. PMID 11733534.
- ^ Макдональд Дж. И., Грыз Е. А., Кубу С. Дж., Верди Дж. М., Микин С. О. (июнь 2000 г.). «Прямое связывание сигнального адаптивного белка Grb2 с тирозинами петли активации на тирозинкиназе рецептора фактора роста нервов, TrkA». J. Biol. Chem. 275 (24): 18225–33. Дои:10.1074 / jbc.M001862200. PMID 10748052.
- ^ Ямасита Х., Авраам С., Цзян С., Дикич И., Авраам Х. (май 1999 г.). «Гомологичная киназа Csk связывается с рецепторами TrkA и участвует в росте нейритов из клеток PC12». J. Biol. Chem. 274 (21): 15059–65. Дои:10.1074 / jbc.274.21.15059. PMID 10329710.
- ^ Никьяер А., Ли Р., Тенг К.К., Янсен П., Мадсен П., Нильсен М.С., Якобсен К., Климаннель М., Шварц Э., Вилнов Т.Е., Хемпстед Б.Л., Петерсен С.М. (февраль 2004 г.). «Сортилин необходим для индуцированной proNGF гибели нейрональных клеток». Природа. 427 (6977): 843–8. Дои:10.1038 / природа02319. PMID 14985763.
- ^ Ли Р., Кермани П., Тэн К.К., Хемпстед Б.Л. (ноябрь 2001 г.). «Регулирование выживаемости клеток секретируемыми пронейротрофинами». Наука. 294 (5548): 1945–8. Дои:10.1126 / science.1065057. PMID 11729324.
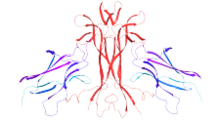
- ^ Wiesmann C, Ultsch MH, Bass SH, de Vos AM (сентябрь 1999 г.). «Кристаллическая структура фактора роста нервов в комплексе с лиганд-связывающим доменом рецептора TrkA». Природа. 401 (6749): 184–8. Дои:10.1038/43705. PMID 10490030.
- ^ Ohmichi M, Decker SJ, Pang L, Saltiel AR (август 1991). «Фактор роста нервов связывается с продуктом протоонкогена trk 140 кДа и стимулирует его ассоциацию с доменом гомологии src фосфолипазы C гамма 1» (PDF). Biochem. Биофиз. Res. Сообщество. 179 (1): 217–23. Дои:10.1016 / 0006-291X (91) 91357-I. HDL:2027.42/29169. PMID 1715690.
- ^ а б c d Цянь X, Риччио А., Чжан И, Джинти Д.Д. (ноябрь 1998 г.). «Идентификация и характеристика новых субстратов рецепторов Trk в развивающихся нейронах». Нейрон. 21 (5): 1017–29. Дои:10.1016 / S0896-6273 (00) 80620-0. PMID 9856458.
- ^ а б Накамура Т., Комия М., Сон К., Хиросэ Э, Гото Н., Мори Х, Охта Й, Мори Н. (декабрь 2002 г.). «Grit, белок, активирующий GTPase для семейства Rho, регулирует расширение нейритов посредством ассоциации с рецептором TrkA и адапторными молекулами N-Shc и CrkL / Crk». Мол. Клетка. Биол. 22 (24): 8721–34. Дои:10.1128 / MCB.22.24.8721-8734.2002. ЧВК 139861. PMID 12446789.
- ^ Wooten MW, Seibenhener ML, Mamidipudi V, Diaz-Meco MT, Barker PA, Moscat J (март 2001 г.). «Атипичный протеин-протеин p62, взаимодействующий с протеинкиназой C, представляет собой основу для активации NF-kappaB фактором роста нервов». J. Biol. Chem. 276 (11): 7709–12. Дои:10.1074 / jbc.C000869200. PMID 11244088.
- ^ Гита Т., Вутен М.В. (февраль 2003 г.). «Ассоциация атипичного белка p62 / ZIP, взаимодействующего с протеинкиназой С, с рецептором фактора роста нервов TrkA регулирует перенос рецепторов и передачу сигналов Erk5». J. Biol. Chem. 278 (7): 4730–9. Дои:10.1074 / jbc.M208468200. PMID 12471037.
- ^ Джадхав Т., Гита Т., Цзян Дж., Вутен М.В. (июль 2008 г.). «Идентификация консенсусного сайта полиубиквитинирования TRAF6 / p62». Biochem. Биофиз. Res. Сообщество. 371 (3): 521–4. Дои:10.1016 / j.bbrc.2008.04.138. ЧВК 2474794. PMID 18457658.
- ^ Wooten MW, Geetha T, Babu JR, Seibenhener ML, Peng J, Cox N, Diaz-Meco MT, Moscat J (март 2008 г.). «Существенная роль секвестосомы 1 / p62 в регуляции накопления Lys63-убиквитинированных белков». J. Biol. Chem. 283 (11): 6783–9. Дои:10.1074 / jbc.M709496200. PMID 18174161.
- ^ Borrello MG, Pelicci G, Arighi E, De Filippis L, Greco A, Bongarzone I, Rizzetti M, Pelicci PG, Pierotti MA (июнь 1994). «Онкогенные версии тирозинкиназ Ret и Trk связывают адаптерные белки Shc и Grb2». Онкоген. 9 (6): 1661–8. PMID 8183561.
- ^ Jang SW, Liu X, Chan CB, Weinshenker D, Hall RA, Xiao G, Ye K (июнь 2009 г.). «Амитриптилин является агонистом рецепторов TrkA и TrkB, который способствует гетеродимеризации TrkA / TrkB и обладает сильной нейротрофической активностью». Chem. Биол. 16 (6): 644–656. Дои:10.1016 / j.chembiol.2009.05.010. ЧВК 2844702. PMID 19549602.
- ^ Чан С.В., Окада М., Сайид И., Сяо Дж., Стейн Д., Джин П., Е К. (октябрь 2007 г.). «Гамбогический амид, селективный агонист рецептора TrkA, который обладает сильной нейротрофической активностью, предотвращает гибель нейрональных клеток». Proc Natl Acad Sci U S A. 104 (41): 16329–16334. Дои:10.1073 / pnas.0706662104. ЧВК 2042206. PMID 17911251.
- ^ Пульчиани С., Сантос Э., Ловер А.В., Лонг Л.К., Ааронсон С.А., Барбакид М. (декабрь 1982 г.). «Онкогены в солидных опухолях человека». Природа. 300 (5892): 539–42. Дои:10.1038 / 300539a0. PMID 7144906.
- ^ Добеле Р.С., Дэвис Л.Э., Вайшнави А., Ле А.Т., Эстрада-Бернал А., Кейсар С., Джимено А., Варелла-Гарсия М., Айснер Д.Л., Ли Й., Стивенс П.Дж., Морозини Д., Туч Б.Б., Фернандес М., Нанда Н., Лоу JA (октябрь 2015 г.). «Онкогенное слияние NTRK у пациента с саркомой мягких тканей с ответом на ингибитор тропомиозин-родственной киназы LOXO-101». Открытие рака. 5 (10): 1049–57. Дои:10.1158 / 2159-8290.CD-15-0443. ЧВК 4635026. PMID 26216294.
- ^ «Многообещающие данные клинических исследований энтректиниба». ScienceDaily. 18 апреля 2016 г.
внешняя ссылка
дальнейшее чтение
- Индо Y (2002). «Генетика врожденной нечувствительности к боли с ангидрозом (CIPA) или наследственной сенсорной и вегетативной нейропатии IV типа. Клинические, биологические и молекулярные аспекты мутаций в гене TRKA (NTRK1), кодирующем рецепторную тирозинкиназу фактора роста нервов». Clin. Auton. Res. 12 (Приложение 1): I20–32. Дои:10.1007 / с102860200016. PMID 12102460.
- Micera A, Lambiase A, Stampachiacchiere B, Bonini S, Bonini S, Levi-Schaffer F (2007). «Фактор роста нервов и ремоделирование восстановления тканей: trkA (NGFR) и p75 (NTR), два рецептора - одна судьба». Фактор роста цитокинов Rev. 18 (3–4): 245–56. Дои:10.1016 / j.cytogfr.2007.04.004. PMID 17531524.