Тиосульфат натрия - Sodium thiosulfate
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Тиосульфат натрия | |
| Другие имена Гипосульфит натрия Гипосульфит соды | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ |
|
| ChemSpider | |
| ECHA InfoCard | 100.028.970 |
| Номер E | E539 (регуляторы кислотности, ...) |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| Na 2S 2О 3 | |
| Молярная масса | 158,11 г / моль (безводный) 248,18 г / моль (пентагидрат) |
| Внешность | Белые кристаллы |
| Запах | Без запаха |
| Плотность | 1,667 г / см3 |
| Температура плавления | 48,3 ° С (118,9 ° F, 321,4 К) (пентагидрат) |
| Точка кипения | 100 ° С (212 ° F, 373 К) (пентагидрат, - 5H2O разложение) |
| 70,1 г / 100 мл (20 ° С)[1] 231 г / 100 мл (100 ° С) | |
| Растворимость | незначительный в алкоголь |
| 1.489 | |
| Структура | |
| моноклинический | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
| R-фразы (устарело) | R21 R36 R37 R38 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тиосульфат натрия (тиосульфат натрия) является неорганическое соединение с формулой Na2S2О3.ИксЧАС2О. Обычно он бывает белого или бесцветного цвета. пентагидрат, Na2S2О3·5ЧАС2О. Твердое тело цветущий (легко теряет воду) кристаллическое вещество, хорошо растворяющееся в воде.[2]
Тиосульфат натрия используется в золотодобыча, очистка воды, аналитическая химия, развитие серебро -основан фотопленка и отпечатки, и лекарство. В медицинское использование тиосульфата натрия включать лечение отравление цианидом и отрубевидный лишай.[3] Это на Список основных лекарственных средств Всемирной организации здравоохранения, самые безопасные и эффективные лекарства, необходимые в система здоровья.[4]
Использует
Медицинское использование
Тиосульфат натрия используется при лечении отравление цианидом.[3] Другие применения включают местное лечение стригущий лишай и разноцветный лишай,[3][5] и лечение некоторых побочных эффектов гемодиализ[6] и химиотерапия.[7]
Йодометрия
В аналитической химии наиболее важное применение происходит потому, что тиосульфат анион реагирует стехиометрически с йод в водном растворе, уменьшив его до йодид как тиосульфат окисляется до тетратионат:
- 2 ю.ш.
2О2−
3 + Я
2 → S
4О2−
6 + 2 я−
Из-за количественного характера этой реакции, а также из-за того, что Na
2S
2О
3· 5H2О имеет отличный срок хранения, используется как титрант в йодометрия. Na
2S
2О
3· 5H2О также является компонентом часы с йодом эксперименты.
Это конкретное использование может быть настроено для измерения содержания кислорода в воде через длинную серию реакций в Тест Винклера на растворенный кислород. Он также используется для объемной оценки концентраций определенных соединений в растворе (пероксид водорода, например), а также при оценке содержания хлора в коммерческом обесцвечивающем порошке и воде.
Фотографическая обработка
Серебро галогениды, например, AgBr, типичные компоненты фотоэмульсий, растворяются при обработке водным тиосульфатом:
Это приложение как фотографический фиксатор был обнаружен Джон Гершель. Он используется как для фильм и фотобумага обработка; тиосульфат натрия известен как фотографический фиксатор, и часто упоминается как «гипо», от первоначального химического названия - гипосульфит соды.[8] Тиосульфат аммония для этого применения обычно предпочтительнее тиосульфата натрия.[2]
Добыча золота
Тиосульфат натрия и тиосульфат аммония являются составной частью альтернативы выщелачиватели к цианид для добычи золото.[9][2] Тиосульфат образует прочные растворимые комплексы с ионами золота (I), [Au (S
2О
3)
2]3−. Преимущества этого подхода заключаются в том, что (i) тиосульфат по существу нетоксичен и (ii) типы руд, которые огнеупорный к цианирование золота (например. углеродистый или же Руды карлинского типа ) может выщелачиваться тиосульфатом. Некоторые проблемы с этим альтернативным процессом включают высокое потребление тиосульфата и отсутствие подходящей техники восстановления, поскольку [Au (S
2О
3)
2]3− не адсорбировать к Активированный уголь, который является стандартным методом, используемым при цианировании золота для отделения комплекса золота от рудной суспензии.
Нейтрализация хлорированной воды
Используется для дехлорирования водопроводной воды, включая хлор уровни для использования в аквариумах, бассейнах и спа (например, следующие суперхлорирование ) и внутри очистка воды установки для очистки отстоявшейся промывной воды перед сбросом в реки.[2] Реакция восстановления аналогична реакции восстановления йода.
В pH тестирование отбеливать веществ, тиосульфат натрия нейтрализует эффект отбеливания, удаляющий цвет, и позволяет проверять pH отбеливающих растворов с помощью жидких индикаторов. Соответствующая реакция сродни йодной реакции: тиосульфат снижает гипохлорит (активный ингредиент в отбеливать ) и при этом окисляется до сульфата. Полная реакция:
- 4 NaClO + Na
2S
2О
3 + 2 NaOH → 4 NaCl + 2 Na
2ТАК
4 + H
2О
Аналогичным образом тиосульфат натрия реагирует с бром, удаляя из раствора свободный бром. Растворы тиосульфата натрия обычно используются в качестве меры предосторожности в химических лабораториях при работе с бромом и для безопасной утилизации брома, йода или других сильных окислителей.
Структура
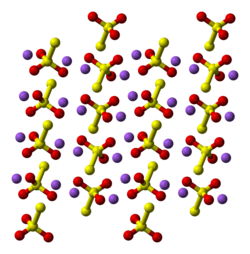
Известны два полиморфа пентагидрата. Безводная соль существует в нескольких полиморфных модификациях.[2] В твердом состоянии тиосульфат анион имеет тетраэдрическую форму и условно получается путем замены одного из атомов кислорода на атом серы в сульфат анион. Расстояние S-S указывает на одинарную связь, подразумевая, что терминальная сера имеет значительный отрицательный заряд, а взаимодействия S-O имеют более характер двойной связи.
Производство
В промышленных масштабах тиосульфат натрия производится в основном из жидких отходов сульфид натрия или сера краситель производство.[10]
В лаборатории эту соль можно приготовить путем нагревания водного раствора сульфит натрия с сера или кипячением водного едкий натр и сера согласно этому уравнению:[11]
- 6 NaOH + 4 S → 2 Na
2S + Na
2S
2О
3 + 3 часа
2О
Основные реакции
При нагревании до 300 ° C разлагается до сульфат натрия и натрий полисульфид:
- 4 Na
2S
2О
3 → 3 Na
2ТАК
4 + Na
2S
5
Соли тиосульфатов обычно разлагаются при обработке кислотами. Начальное протонирование происходит у серы. Когда протонирование проводится в диэтиловый эфир при −78 ° C, H2S2О3 (тиосерная кислота ) может быть получен. Это довольно сильная кислота с pKаs 0,6 и 1,7 для первой и второй диссоциации соответственно.
В нормальных условиях подкисление растворов этого избытка соли даже разбавленными кислотами приводит к полному разложению до сера, диоксид серы, и воды:[10]
- Na
2S
2О
3 + 2 HCl → 2 NaCl + S + SO
2 + H
2О
Эта реакция известна как "часы реакция ", потому что, когда сера достигает определенной концентрации, раствор превращается из бесцветного в бледно-желтый. Эта реакция использовалась для образования коллоидной серы. Этот процесс используется для демонстрации концепции скорость реакции на уроках химии.
Катионная реакция алюминия
Тиосульфат натрия используется в аналитическая химия.[12] При нагревании образца, содержащего катионы алюминия, может образоваться белый осадок:
- 2 Al3+ + 3 Ю
2О2−
3 + 3 часа
2O → 3 SO
2 + 3 S + 2 Al (OH)
3
Органическая химия
Алкилирование тиосульфата натрия дает S-алкилтиосульфаты, которые называются Соли Бунте.[13] Алкилтиосульфаты подвержены гидролизу с образованием тиола. Эта реакция иллюстрируется одним синтезом тиогликолевая кислота:
- ClCH
2CO
2H + Na
2S
2О
3 → Na [O
3S
2CH
2CO
2H] + NaCl - Na [O
3S
2CH
2CO
2H] + H
2O → HSCH
2CO
2Н + NaHSO
4
Рекомендации
- ^ Записывать в базе данных веществ GESTIS Институт охраны труда и здоровья
- ^ а б c d е Барбера Дж. Дж., Мецгер А., Вольф М. (2012). «Сульфиты, тиосульфаты и дитиониты». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a25_477. ISBN 9783527306732.CS1 maint: использует параметр авторов (связь)
- ^ а б c Всемирная организация здоровья (2009). Стюарт М.С., Куимци М., Хилл С.Р. (ред.). Типовой формуляр ВОЗ 2008 г.. Всемирная организация здоровья. п. 66. HDL:10665/44053. ISBN 9789241547659.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Саненшайн П.Дж., Шварц Р.А., Джаннигер К.К. (2002). «Разноцветный лишай». Int. J. Dermatol. 37 (9): 648–55. Дои:10.1046 / j.1365-4362.1998.00441.x. PMID 9762812. S2CID 75657768.
- ^ Auriemma M, Carbone A, Di Liberato L и др. (2011). «Лечение кальцифилаксии кожи тиосульфатом натрия: два сообщения о клинических случаях и обзор литературы». Являюсь. J. Clin. Дерматол. 12 (5): 339–46. Дои:10.2165/11587060-000000000-00000. PMID 21834598. S2CID 28366905.
- ^ Дики Д.Т., Ву Ю.Дж., Малдун Л.Л. и др. (2005). "Защита от токсичности, вызванной цисплатином, посредством N-Ацетилцистеин и тиосульфат натрия по оценке на молекулярном, клеточном уровне и уровне in vivo ». J. Pharmacol. Exp. Ther. 314 (3): 1052–8. Дои:10.1124 / jpet.105.087601. PMID 15951398. S2CID 11381393.
- ^ Гибсон CR (1908). Романтика современной фотографии, ее открытия и достижения. Seeley & Co., стр.37.
гипосульфит-содовый фиксатор herschel hypo.
- ^ Эйлмор MG, Muir DM (2001). «Тиосульфатное выщелачивание золота - обзор». Минерал Инжиниринг. 14 (2): 135–174. Дои:10.1016 / s0892-6875 (00) 00172-2.
- ^ а б Холлеман AF, Wiberg E, Wiberg N (2001). Неорганическая химия. Сан-Диего: Academic Press. ISBN 9780123526519.
- ^ Гордин HM (1913). Элементарная химия. Vol. 1. Неорганическая химия. Чикаго: Medico-Dental Publishing Co., стр. 162 и 287–288.
- ^ Дульский TR (1996). «Глава 8: Разделение путем подготовки». Руководство по химическому анализу металлов. Вест Коншохокен, Пенсильвания: ASTM. п. 99. ISBN 9781601194350. OCLC 180851384.
- ^ Алонсо М.Э., Арагона Х. (1978). «Сульфидный синтез в получении несимметричных диалкилдисульфидов: втор-бутил-изопропилдисульфид». Орг. Synth. 58: 147. Дои:10.15227 / orgsyn.058.0147.


