PLK1 - PLK1
Серин / треонин-протеинкиназа PLK1, также известный как поло-подобная киназа 1 (ПЛК-1) или серин / треонин-протеинкиназа 13 (STPK13), является фермент что у людей кодируется PLK1 (поло-подобная киназа 1) ген.[5]
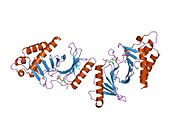
Структура
ПЛК1 состоит из 603 аминокислоты и составляет 66 кДа. В добавок к N-конец киназа домена есть две консервативные области полобокса из 30 аминокислот в C-конец. Активность киназы регулируется, по крайней мере частично, поло-боксами, которые функционально важны для обоих. автозапуск и субклеточная локализация.[6]
Локализация
Во время интерфазы PLK1 локализуется в центросомы. В рано митоз, это ассоциируется с митотическое веретено полюса. Рекомбинантный белок GFP-PLK1 располагается в центромера /кинетохора область, предполагая возможную роль для разделения хромосом.[7]
Регуляция клеточного цикла
Plk1 - это ранний триггер для перехода G2 / M. Plk1 поддерживает функциональное созревание центросомы в конце G2 / начале профаза и создание биполярного шпинделя. Plk1 фосфорилирует и активирует cdc25C, a фосфатаза который дефосфорилирует и активирует циклин B /cdc2 сложный. Plk фосфорилирует и активирует компоненты комплекс, способствующий анафазе (БТР). APC, который активируется белками семейства Fizzy-Cdc20, представляет собой клеточный цикл убиквитин-протеинлигаза (E3) деградирует митотические циклины, хромосомные белки, которые поддерживают сцепление сестринские хроматиды, и анафаза ингибиторы. Аномальное веретено (Asp), субстрат полокиназы, представляет собой микротрубочка -ассоциированный белок, необходимый для правильного поведения полюса шпинделя и микротрубочки М-фазы. Plk1 локализуется в центральной области веретена на позднем митозе и ассоциируется с кинезин -подобный белок CHO1 / MKLP1. Гомологичный моторный белок в Дрозофила является продуктом гена паваротти (PAR).[8]
Исследования показали, что потеря экспрессии PLK1 может вызывать проапоптотический пути и подавляют рост. На основе исследований на дрожжах и мышах мейоз PLK1 человека также может выполнять регуляторную функцию в мейозе. Полокиназа CDC5 S. cerevisiae необходима для фосфорилирования и удаления мейотической когезии во время первого деления клеток. В клетках с истощением CDC5 кинетохоры биориентированы во время мейоза I, а Mam1, белок, необходимый для коориентации, неспособен связываться с кинетохорами. CDC5, как полагают, играет роль в коориентации сестринских кинетохор и сегрегация хромосом во время мейоза I.[9]
Роль в онкогенезе
Plk1 считается протоонкоген, чей чрезмерное выражение часто наблюдается в опухоль клетки. Анеуплоидия и туморогенез также может быть результатом центросома аномалии, особенно дефекты амплификации центросомы. Дублирование и созревание центросом, регулируемое Plk1, происходит с позднего Фаза S профазировать. Аномальная амплификация центросом может привести к многополюсные шпиндели и приводит к неравной сегрегации хромосом. Сверхэкспрессия Plk1 также увеличивает размер центросом и / или количество центросом, что также приводит к неправильной сегрегации хромосом, анеуплоидии и туморогенезу.
Считается, что онкогенные свойства PLK1 связаны с его ролью в управлении автомобилем. клеточный цикл прогрессия. Подтверждающие доказательства получены из исследований сверхэкспрессии PLK1 в клеточной линии NIH3T3. Эти клетки становятся способными образовывать очаги и расти в мягких тканях. агар и, что более важно, эти клетки могут образовывать опухоли в голые мыши из-за сверхэкспрессии PLK1.[10]
PLK1 также был связан с известными путями, которые изменяются во время неопластическая трансформация. Ретинобластома подавитель опухолей (RB) активация пути приводит к репрессии промотора PLK1 в SWI / SNF ремоделирование хроматина сложный зависимый образ. В случае инактивации RB экспрессия PLK1, по-видимому, нарушена. Это новое открытие предполагает, что PLK1 может быть мишенью пути подавления опухоли ретинобластомы (RB).
Более того, PLK1, по-видимому, участвует в опухолевый супрессор p53 родственные пути. Данные свидетельствуют о том, что PLK1 может ингибировать трансактивация и проапоптотические функции р53 функционируют за счет физического взаимодействия и фосфорилирование.[11]
Клиническое значение
PLK1 изучается как цель для рак наркотики. Много двоеточие и рак легких вызваны мутациями K-RAS. Эти виды рака зависят от PLK1.
Когда экспрессия PLK1 подавлялась с помощью РНК-интерференция в культура клеток, Клетки K-RAS были избирательно убиты, не повреждая нормальные клетки.[12][13]
Ингибитор PLK1 Volasertib оценивается в клинические испытания для использования в острый миелоидный лейкоз (AML).[14] Комбинация ингибирования PLK1 и EGFR преодолевает лекарственную устойчивость, опосредованную T790M. in vitro и in vivo при немелкоклеточном раке легкого (НМРЛ).[15] В HNSCC мутации AJUBA опосредуют чувствительность к лечению ингибиторами клеточного цикла, включая ингибитор Plk1 воласертиб.[16]. В мезенхимальных клетках NSCLC фосфорилирование cMet регулируется с помощью Plk1-опосредованного фосфорилирования виментина через β1-интегрин. Комбинация ингибирования cMet и Plk1 приводила к значительной регрессии опухоли в моделях NSCLC in vivo, обработанных клинически значимыми лекарственными средствами.[17]
Ригосертиб экспериментальный ингибитор RAS / PI3K / PLK1.[18]
Взаимодействия
PLK1 был показан взаимодействовать с:
Структурный анализ был использован для объяснения широкой специфичности PLK1.[28]
Смотрите также
- Поло-подобные киназы, семейство генов, к которому принадлежит PLK1
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000166851 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000030867 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Holtrich U, Wolf G, Bräuninger A, Karn T., Böhme B, Rübsamen-Waigmann H, Strebhardt K (март 1994). «Индукция и подавление PLK, человеческой серин / треониновой киназы, экспрессируемой в пролиферирующих клетках и опухолях». Труды Национальной академии наук Соединенных Штатов Америки. 91 (5): 1736–40. Bibcode:1994PNAS ... 91.1736H. Дои:10.1073 / пнас.91.5.1736. ЧВК 43238. PMID 8127874.
- ^ Cheng KY, Lowe ED, Sinclair J, Nigg EA, Johnson LN (ноябрь 2003 г.). «Кристаллическая структура поло-бокс-домена человеческой поло-подобной киназы-1 и его фосфопептидного комплекса». Журнал EMBO. 22 (21): 5757–68. Дои:10.1093 / emboj / cdg558. ЧВК 275415. PMID 14592974.
- ^ Ли К.С., О ДЙ, Кан Й.Х., Пак Джей (январь 2008 г.). «Саморегулируемый механизм локализации Plk1 в кинетохорах: уроки взаимодействия Plk1-PBIP1». Отделение клеток. 3: 4. Дои:10.1186/1747-1028-3-4. ЧВК 2263035. PMID 18215321.
- ^ ван де Вердт BC, Medema RH (апрель 2006 г.). «Поло-подобные киназы: команда, контролирующая дивизион». Клеточный цикл. 5 (8): 853–64. Дои:10.4161 / cc.5.8.2692. PMID 16627997.
- ^ Сунг Н.К., Пак Дж. Э., Ю Л. Р., Ли К. Х., Ли Дж. М., Банг Дж. К. и др. (Апрель 2009 г.). «Plk1-зависимая и независимая роль варианта сплайсинга ODF2, hCenexin1, в центросоме соматических клеток». Клетка развития. 16 (4): 539–50. Дои:10.1016 / j.devcel.2009.02.004. ЧВК 2741019. PMID 19386263.
- ^ Malumbres M, Barbacid M (февраль 2007 г.). «Киназы клеточного цикла при раке». Текущее мнение в области генетики и развития. 17 (1): 60–5. Дои:10.1016 / j.gde.2006.12.008. PMID 17208431.
- ^ Лю X, Эриксон Р.Л. (май 2003 г.). «Истощение поло-подобной киназы (Plk) 1 вызывает апоптоз в раковых клетках». Труды Национальной академии наук Соединенных Штатов Америки. 100 (10): 5789–94. Bibcode:2003ПНАС..100.5789Л. Дои:10.1073 / pnas.1031523100. ЧВК 156279. PMID 12732729.
- ^ Downward J, Поиск слабости в раке, N Engl J Med, 361: 922, 27 августа 2009 г.
- ^ Луо Дж., Эмануэле М.Дж., Ли Д., Крейтон С.Дж., Шлабах М.Р., Вестбрук Т.Ф. и др. (Май 2009 г.). «Скрининг РНКи по всему геному выявляет множественные синтетические летальные взаимодействия с онкогеном Ras». Клетка. 137 (5): 835–48. Дои:10.1016 / j.cell.2009.05.006. ЧВК 2768667. PMID 19490893.
- ^ Van den Bossche J, Lardon F, Deschoolmeester V, De Pauw I, Vermorken JB, Specenier P и др. (Июль 2016 г.). «В центре внимания Volasertib: доклиническая и клиническая оценка перспективного ингибитора Plk1». Обзоры медицинских исследований. 36 (4): 749–86. Дои:10.1002 / med.21392. PMID 27140825. S2CID 3456912.
- ^ Ван И, Сингх Р., Ван Л., Нильссон М., Гунатилак Р., Тонг П. и др. (Июль 2016 г.). «Ингибирование поло-подобной киназы 1 снижает приобретенную устойчивость к ингибированию рецептора эпидермального фактора роста при немелкоклеточном раке легкого с мутациями T790M». Oncotarget. 7 (30): 47998–48010. Дои:10.18632 / oncotarget.10332. ЧВК 5216995. PMID 27384992.
- ^ Чжан М., Сингх Р., Пэн С., Мазумдар Т., Самбандам В., Шен Л. и др. (Апрель 2017 г.). «Мутации белка LIM AJUBA опосредуют чувствительность плоскоклеточного рака головы и шеи к лечению ингибиторами клеточного цикла». Письма о раке. 392: 71–82. Дои:10.1016 / j.canlet.2017.01.024. ЧВК 5404895. PMID 28126323.
- ^ а б Сингх Р., Пэн С., Вишванатх П., Самбандам В., Шен Л., Рао X и др. (Май 2019). «Неканоническая регуляция cMet с помощью виментина опосредует апоптоз, индуцированный ингибитором Plk1». EMBO Молекулярная медицина. 11 (5). Дои:10.15252 / emmm.201809960. ЧВК 6505578. PMID 31040125.
- ^ Nuthalapati S, Zhou Q, Guo P, Lv H, Cosenza S, Reddy MV и др. (Сентябрь 2012 г.). «Доклиническая фармакокинетическая и фармакодинамическая оценка новых противораковых агентов, ON01910.Na (Rigosertib, Estybon ™) и ON013105, для химиотерапии опухолей головного мозга». Фармацевтические исследования. 29 (9): 2499–511. Дои:10.1007 / s11095-012-0780-у. PMID 22678771. S2CID 15145715.
- ^ Цветков Л, Сюй Х, Ли Дж, Штерн Д.Ф. (март 2003 г.). «Поло-подобная киназа 1 и Chk2 взаимодействуют и совместно локализуются в центросомах и среднем теле». Журнал биологической химии. 278 (10): 8468–75. Дои:10.1074 / jbc.M211202200. PMID 12493754.
- ^ Чжоу Т., Аумайс Дж. П., Лю Х, Ю-Ли Л. Ю., Эриксон Р. Л. (июль 2003 г.). «Роль Plk1 фосфорилирования NudC в цитокинезе». Клетка развития. 5 (1): 127–38. Дои:10.1016 / с1534-5807 (03) 00186-2. PMID 12852857.
- ^ Шен М., Стукенберг П.Т., Киршнер М.В., Лу К.П. (март 1998 г.). «Существенная митотическая пептидил-пролилизомераза Pin1 связывает и регулирует митоз-специфические фосфопротеины». Гены и развитие. 12 (5): 706–20. Дои:10.1101 / gad.12.5.706. ЧВК 316589. PMID 9499405.
- ^ Лу Пи Джей, Чжоу XZ, Шен М., Лу КП (февраль 1999 г.). «Функция WW доменов как фосфосерин- или фосфотреонин-связывающих модулей». Наука. 283 (5406): 1325–8. Bibcode:1999Научный ... 283.1325Л. Дои:10.1126 / science.283.5406.1325. PMID 10037602.
- ^ Ли М., Дэниэлс М.Дж., Венкитараман А.Р. (январь 2004 г.). «Фосфорилирование BRCA2 Polo-подобной киназой Plk1 регулируется повреждением ДНК и митотической прогрессией». Онкоген. 23 (4): 865–72. Дои:10.1038 / sj.onc.1207223. PMID 14647413.
- ^ Лин Х.Р., Тинг Н.С., Цинь Дж., Ли У.Х. (сентябрь 2003 г.). «Специфическое для фазы M фосфорилирование BRCA2 поло-подобной киназой 1 коррелирует с диссоциацией комплекса BRCA2-P / CAF». Журнал биологической химии. 278 (38): 35979–87. Дои:10.1074 / jbc.M210659200. PMID 12815053.
- ^ а б c d Фэн Й, Лонго Д.Л., Феррис Д.К. (январь 2001 г.). «Поло-подобная киназа взаимодействует с протеасомами и регулирует их активность». Рост и дифференциация клеток. 12 (1): 29–37. PMID 11205743.
- ^ Astrinidis A, Senapedis W, Henske EP (январь 2006 г.). «Гамартин, продукт гена комплекса 1 туберозного склероза, взаимодействует с поло-подобной киназой 1 зависимым от фосфорилирования образом». Молекулярная генетика человека. 15 (2): 287–97. Дои:10.1093 / hmg / ddi444. PMID 16339216.
- ^ Ли Дж., Ван Р., Ганнон О. Дж., Рези А. С., Цзян С., Герлах Б. Д. и др. (Ноябрь 2016 г.). «Поло-подобная киназа 1 регулирует фосфорилирование виментина по Ser-56 и сокращение гладких мышц». Журнал биологической химии. 291 (45): 23693–23703. Дои:10.1074 / jbc.M116.749341. ЧВК 5095422. PMID 27662907.
- ^ Huggins DJ, McKenzie GJ, Robinson DD, Narváez AJ, Hardwick B, Roberts-Thomson M и др. (Август 2010 г.). «Вычислительный анализ связывания фосфопептида с полобокс-доменом митотической киназы PLK1 с использованием моделирования молекулярной динамики». PLOS вычислительная биология. 6 (8): e1000880. Bibcode:2010PLSCB ... 6E0880H. Дои:10.1371 / journal.pcbi.1000880. ЧВК 2920843. PMID 20711360.