PD-L1 - PD-L1
Запрограммированная смерть-лиганд 1 (PD-L1), также известный как кластер дифференциации 274 (CD274) или B7 гомолог 1 (B7-H1) - это белок что у людей кодируется CD274 ген.[5]
Лиганд запрограммированной смерти 1 (PD-L1) - это 40 кДа типа 1. трансмембранный белок который, как предполагалось, играет важную роль в подавлении адаптивный рука иммунная система во время определенных событий, таких как беременность, ткань аллотрансплантаты, аутоиммунное заболевание и другие болезненные состояния, такие как гепатит. Обычно адаптивная иммунная система реагирует на антигены которые связаны с активацией иммунной системы экзогенными или эндогенными сигналы опасности. В свою очередь, клональная экспансия антиген -специфический CD8 + Т-клетки и / или CD4 + клетки-помощники размножается. Связывание PD-L1 с молекулой ингибиторной контрольной точки ПД-1 передает тормозной сигнал, основанный на взаимодействии с фосфатазами (ШП-1 или же ШП-2 ) через иммунорецепторный тирозиновый переключающий мотив (ITSM).[6] Это снижает пролиферацию антиген-специфических Т-клеток в лимфатических узлах, одновременно уменьшая апоптоз в регуляторных Т-клетках (противовоспалительные, супрессивные Т-клетки) - дополнительно опосредовано более низкой регуляцией гена Bcl-2.[нужна цитата ]
История
PD-L1 был охарактеризован в клинике Мэйо как иммунорегуляторная молекула B7-H1. Позже эта молекула была переименована в PD-L1, потому что она была идентифицирована как лиганд PD-1.[7] Некоторые раковые клетки человека экспрессировали высокие уровни B7-H1, а блокада B7-H1 уменьшала рост опухолей в присутствии иммунных клеток. На тот момент был сделан вывод, что B7-H1 помогает опухолевым клеткам уклоняться от противоопухолевого иммунитета.[8] В 2003 году было показано, что B7-H1 экспрессируется на миелоидных клетках в качестве белка контрольной точки и был предложен в качестве потенциальной мишени в иммунотерапии рака в клинике человека. [9]
Привязка
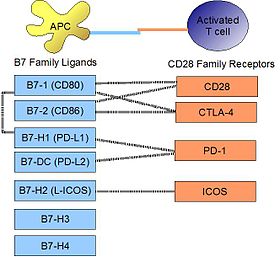
PD-L1 связывается со своим рецептором, ПД-1, обнаруженный на активированных Т-клетках, В-клетках и миелоидных клетках, чтобы модулировать активацию или ингибирование. Сродство между PD-L1 и PD-1, как определено константа диссоциации Kd, составляет 770 нм. PD-L1 также имеет заметное сродство к костимулирующей молекуле. CD80 (B7-1), но не CD86 (В7-2).[10] Сродство CD80 к PD-L1, 1,4 мкМ, является промежуточным между его сродством к CD28 и CTLA-4 (4,0 мкМ и 400 нМ соответственно). Родственная молекула PD-L2 не имеет такого сродства к CD80 или CD86, но разделяет PD-1 в качестве рецептора (с более сильным Kd 140 нМ). Said et al. показали, что PD-1, активированный на активированных Т-клетках CD4, может связываться с PD-L1, экспрессируемым на моноцитах, и индуцирует продукцию IL-10 последними.[11]
Сигнализация
Взаимодействие PD-L1 с его рецептором ПД-1 на Т-клетках доставляет сигнал, который подавляет TCR -опосредованная активация Ил-2 производство и пролиферация Т-клеток. Механизм предполагает ингибирование ZAP70 фосфорилирование и его связь с CD3ζ.[12] Сигнал PD-1 ослабляется PKC-θ цикл активации фосфорилирование (в результате передачи сигналов TCR), необходимое для активации факторов транскрипции NF-κB и АП-1, и для производства Ил-2. Связывание PD-L1 с PD-1 также способствует индуцированной лигандом понижающей модуляции TCR во время презентации антигена наивным Т-клеткам, индуцируя повышающую регуляцию CBL-b убиквитинлигазы E3.[13]
Регулирование
Интерферонами
На IFN-γ При стимуляции PD-L1 экспрессируется на Т-клетках, NK-клетках, макрофагах, миелоидных DC, В-клетках, эпителиальных клетках и эндотелиальных клетках сосудов.[14] Промоторная область гена PD-L1 имеет элемент ответа на IRF-1, регуляторный фактор интерферона.[15] Интерфероны I типа может также активировать PD-L1 в гепатоцитах, моноцитах, DC и опухолевых клетках мыши.[16]
На макрофаги и моноциты
PD-L1 особенно экспрессируется на макрофаги. У мышей было показано, что классически активированные макрофаги (индуцированные типом I хелперные Т-клетки или комбинация LPS и интерферон-гамма ) значительно активизируют PD-L1.[17] В качестве альтернативы макрофаги активируются Ил-4 (альтернативные макрофаги), немного активируют PD-L1, в то же время значительно повышая регуляцию PD-L2. Это было показано STAT1 - мышей с недостаточным нокаутом, что STAT1 в основном отвечает за активацию PD-L1 на макрофагах с помощью ЛПС или гамма-интерферона, но совершенно не отвечает за его конститутивную экспрессию до активации у этих мышей. Также было показано, что PD-L1 постоянно экспрессируется на Ly6C мышивот неклассический моноциты в устойчивом состоянии. [18]
Роль микроРНК
Отдыхающий человек холангиоциты экспрессируют мРНК PD-L1, но не белок, из-за подавления трансляции микроРНК miR-513.[19] После обработки гамма-интерфероном, miR-513 подавлялась, тем самым снимая подавление белка PD-L1. Таким образом, гамма-интерферон может индуцировать экспрессию белка PD-L1 путем ингибирования опосредованного генами подавления трансляции мРНК. В то время как латентный мембранный белок-1 (LMP1) вируса Эпштейна-Барра (EBV) является известным мощным индуктором PD-L1, было показано, что фрагмент H miRNA miR-BamH1 EBV, открытая вправо рамка считывания 1 (BHRF1) 2-5p, может регулируют экспрессию PD-L1, индуцированную LMP1.[20]
Эпигенетическая регуляция
Метилирование ДНК промотора PD-L1 может предсказывать выживаемость при некоторых формах рака после операции.[21]
Клиническое значение
Рак

Похоже, что активация PD-L1 может позволить раку уклоняться от иммунной системы хозяина. Анализ 196 образцов опухолей от пациентов с карцинома почек обнаружили, что высокая экспрессия PD-L1 в опухоли была связана с повышенной агрессивностью опухоли и в 4,5 раза повышенным риском смерти.[22]Много Ингибиторы PD-L1 находятся в разработке как иммуноонкологические методы лечения и показывают хорошие результаты в клинических испытаниях.[23] Клинически доступные примеры включают: Дурвалумаб, пембролизумаб, атезолизумаб и авелумаб.[24]В нормальной ткани обратная связь между факторами транскрипции, такими как STAT3 и NF-κB, ограничивает иммунный ответ, чтобы защитить ткань хозяина и ограничить воспаление. При раке потеря ограничения обратной связи между факторами транскрипции может привести к повышенной локальной экспрессии PD-L1, что может ограничивать эффективность системного лечения агентами, нацеленными на PD-L1.[25]
Listeria monocytogenes
В мышиной модели внутриклеточной инфекции L. monocytogenes индуцировал экспрессию белка PD-L1 в Т-клетках, NK-клетках и макрофагах. Блокада PD-L1 (с использованием блокирующих антител) привела к увеличению смертности инфицированных мышей. Блокада снижает продукцию TNFα и оксида азота макрофагами, снижает продукцию гранзима B NK-клетками и снижает пролиферацию L. monocytogenes антиген-специфические Т-клетки CD8 (но не Т-клетки CD4).[26] Эти данные свидетельствуют о том, что PD-L1 действует как положительная костимулирующая молекула при внутриклеточной инфекции.
Аутоиммунитет
Взаимодействие PD-1 / PD-L1 вовлечено в аутоиммунитет по нескольким линиям доказательств. NOD мыши, на животной модели аутоиммунитета, которая проявляет предрасположенность к спонтанному развитию диабета I типа и других аутоиммунных заболеваний, было показано, что в результате блокады PD-1 или PD-L1 (но не PD-L2) развивается ускоренное начало диабета.[27]
У людей было обнаружено изменение экспрессии PD-L1 у педиатрических пациентов с Системная красная волчанка (СКВ). Изучение изолированно PBMC от здоровых детей, незрелых миелоидные дендритные клетки и моноциты при первоначальном выделении экспрессирует мало PD-L1, но спонтанно активирует PD-L1 через 24 часа. Напротив, ни мДК, ни моноциты пациентов с активной СКВ не смогли активировать PD-L1 в течение 5-дневного курса, экспрессируя этот белок только во время ремиссии заболевания.[28] Это может быть один из механизмов потери периферической толерантности при СКВ.
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000120217 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000016496 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ген Энтреза: CD274 молекула CD274».
- ^ Chemnitz JM, Parry RV, Николс KE, июнь CH, Riley JL (июль 2004 г.). «SHP-1 и SHP-2 связываются с иммунорецепторным мотивом переключения на основе тирозина запрограммированной смерти 1 при первичной стимуляции Т-клеток человека, но только лигирование рецептора предотвращает активацию Т-клеток». Журнал иммунологии. 173 (2): 945–54. Дои:10.4049 / jimmunol.173.2.945. PMID 15240681.
- ^ Донг Х., Чжу Г., Тамада К., Чен Л. (декабрь 1999 г.). «B7-H1, третий член семейства B7, костимулирует пролиферацию Т-клеток и секрецию интерлейкина-10». Природа Медицина. 5 (12): 1365–9. Дои:10.1038/70932. PMID 10581077. S2CID 21397460.
- ^ Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, Roche PC, Lu J, Zhu G, Tamada K, Lennon VA, Celis E, Chen L (август 2002). «Связанный с опухолью B7-H1 способствует апоптозу Т-клеток: потенциальному механизму уклонения от иммунитета». Природа Медицина. 8 (8): 793–800. Дои:10,1038 / нм 730. PMID 12091876. S2CID 27694471.
- ^ Curiel TJ, Wei S, Dong H, Alvarez X, Cheng P, Mottram P, Krzysiek R, Knutson KL, Daniel B, Zimmermann MC, David O, Burow M, Gordon A, Dhurandhar N, Myers L, Berggren R, Hemminki A , Альварес Р.Д., Эмили Д., Куриэль Д.Т., Чен Л., Цзоу В. (май 2003 г.). «Блокада B7-H1 улучшает противоопухолевый иммунитет, опосредованный миелоидными дендритными клетками». Природа Медицина. 9 (5): 562–7. Дои:10,1038 / нм 863. PMID 12704383. S2CID 12499214.
- ^ Бьютт MJ, Пенья-Крус V, Ким MJ, Freeman GJ, Sharpe AH (август 2008 г.). «Взаимодействие PD-L1 и B7-1 человека». Молекулярная иммунология. 45 (13): 3567–72. Дои:10.1016 / j.molimm.2008.05.014. ЧВК 3764616. PMID 18585785.
- ^ Саид Э.А., Дюпюи Ф.П., Траутманн Л., Чжан Й., Ши И, Эль-Фар М, Хилл Б.Дж., Ното А, Анкута П., Перец Й., Фонсека С.Г., Ван Гревенинге Дж., Буласель М.Р., Бруно Дж., Шукри Н.Х., Роути Дж. , Douek DC, Haddad EK, Sekaly RP (апрель 2010 г.). «Вызванная запрограммированной смертью-1 продукция интерлейкина-10 моноцитами снижает активацию CD4 + Т-клеток во время ВИЧ-инфекции». Природа Медицина. 16 (4): 452–9. Дои:10,1038 / нм. 2106. ЧВК 4229134. PMID 20208540.
- ^ Шеппард К.А., Фитц Л.Дж., Ли Дж. М., Бенандер С., Джордж Дж. А., Вутерс Дж., Цю Й., Джуссиф Дж. М., Картер Л.Л., Вуд К.Р., Чаудхари Д. (сентябрь 2004 г.). «PD-1 ингибирует индуцированное Т-клеточным рецептором фосфорилирование сигнальной сомы ZAP70 / CD3zeta и последующую передачу сигнала к PKCtheta». Письма FEBS. 574 (1–3): 37–41. Дои:10.1016 / j.febslet.2004.07.083. PMID 15358536. S2CID 85034305.
- ^ Karwacz K, Bricogne C, MacDonald D, Arce F, Bennett CL, Collins M, Escors D (октябрь 2011 г.). «Костимуляция PD-L1 способствует понижающей модуляции Т-клеточного рецептора, индуцированной лигандом, на CD8 + Т-клетках». EMBO Молекулярная медицина. 3 (10): 581–92. Дои:10.1002 / emmm.201100165. ЧВК 3191120. PMID 21739608.
- ^ Мухи Д. Б., Чен Л. (апрель 2007 г.). «Новые B7: играют ключевую роль в противоопухолевом иммунитете». Журнал иммунотерапии. 30 (3): 251–60. Дои:10.1097 / CJI.0b013e31802e085a. PMID 17414316.
- ^ Lee SJ, Jang BC, Lee SW, Yang YI, Suh SI, Park YM, Oh S, Shin JG, Yao S, Chen L, Choi IH (февраль 2006 г.). «Фактор-1, регулирующий интерферон, является предпосылкой конститутивной экспрессии и индуцированной IFN-гамма активации B7-H1 (CD274)». Письма FEBS. 580 (3): 755–62. Дои:10.1016 / j.febslet.2005.12.093. PMID 16413538. S2CID 11169726.
- ^ Ямадзаки Т., Акиба Х, Иваи Х, Мацуда Х, Аоки М, Танно Й, Шин Т, Цучия Х, Пардолл Д.М., Окумура К., Адзума М., Ягита Х (ноябрь 2002 г.). «Экспрессия лигандов запрограммированной смерти 1 мышиными Т-клетками и APC». Журнал иммунологии. 169 (10): 5538–45. Дои:10.4049 / jimmunol.169.10.5538. PMID 12421930.
- ^ Локи П., Эллисон Дж. П. (апрель 2003 г.). «PD-L1 и PD-L2 по-разному регулируются клетками Th1 и Th2». Труды Национальной академии наук Соединенных Штатов Америки. 100 (9): 5336–41. Дои:10.1073 / pnas.0931259100. ЧВК 154346. PMID 12697896.
- ^ Bianchini M, Duchene J, Santovito D, Schloss MJ, Evrard M, Winkels H, Aslani M, Mohanta SK, Horckmans M, Blanchet X, Lacy M, von Hundelshausen P, Atzler D, Habenicht A, Gerdes N, Pelisek J, Ng LG, Steffens S, Weber C, Megens RT (июнь 2019 г.). «Экспрессия PD-L1 на неклассических моноцитах раскрывает их происхождение и иммунорегуляторную функцию». Научная иммунология. 4 (36): eaar3054. Дои:10.1126 / sciimmunol.aar3054. PMID 31227596. S2CID 195259881.
- ^ Гонг А.Ю., Чжоу Р., Ху Джи, Ли Х, Сплинтер П.Л., О'Хара С.П., ЛаРуссо Н.Ф., Соукуп Г.А., Донг Х., Чен ХМ (февраль 2009 г.). «МикроРНК-513 регулирует трансляцию B7-H1 и участвует в индуцированной IFN-гамма экспрессии B7-H1 в холангиоцитах». Журнал иммунологии. 182 (3): 1325–33. Дои:10.4049 / jimmunol.182.3.1325. ЧВК 2652126. PMID 19155478.
- ^ Cristino AS, Nourse J, West RA, Sabdia MB, Law SC, Gunawardana J, Vari F, Mujaj S, Thillaiyampalam G, Snell C, Gough M, Keane C, Gandhi MK (декабрь 2019 г.). «МикроРНК EBV-BHRF1-2-5p нацелена на 3'UTR лигандов иммунных контрольных точек PD-L1 и PD-L2». Кровь. 134 (25): 2261–2270. Дои:10.1182 / кровь.2019000889. ЧВК 6923667. PMID 31856276.
- ^ Гевенслебен Х, Холмс Э., Гольц Д., Дитрих Дж., Зайлер В., Эллингер Дж., Дитрих Д., Кристиансен Г. (ноябрь 2016 г.). «Метилирование промотора PD-L1 является прогностическим биомаркером выживаемости без биохимического рецидива у пациентов с раком простаты после радикальной простатэктомии». Oncotarget. 7 (48): 79943–79955. Дои:10.18632 / oncotarget.13161. ЧВК 5346762. PMID 27835597.
- ^ Thompson RH, Gillett MD, Cheville JC, Lohse CM, Dong H, Webster WS, Krejci KG, Lobo JR, Sengupta S, Chen L, Zincke H, Blute ML, Strome SE, Leibovich BC, Kwon ED (декабрь 2004 г.). «Костимулятор B7-H1 у пациентов с почечно-клеточной карциномой: индикатор агрессивности опухоли и потенциальная терапевтическая цель». Труды Национальной академии наук Соединенных Штатов Америки. 101 (49): 17174–9. Дои:10.1073 / pnas.0406351101. ЧВК 534606. PMID 15569934.
- ^ Велчети В., Шальпер К.А., Карвахаль Д.Е., Анагносту В.К., Сиригос К.Н., Сзнол М., Хербст Р.С., Геттингер С.Н., Чен Л., Римм Д.Л. (январь 2014 г.). «Экспрессия лиганда-1 запрограммированной смерти при немелкоклеточном раке легкого». Лабораторные исследования; Журнал технических методов и патологии. 94 (1): 107–16. Дои:10.1038 / labinvest.2013.130. ЧВК 6125250. PMID 24217091.
- ^ «Ингибиторы иммунных контрольных точек для лечения рака». www.cancer.org. Получено 2017-03-27.
- ^ Влахопулос, С.А. (15 августа 2017 г.). «Аберрантный контроль NF-κB при раке разрешает транскрипционную и фенотипическую пластичность, сокращая зависимость от ткани хозяина: молекулярный режим». Биология и медицина рака. 14 (3): 254–270. Дои:10.20892 / j.issn.2095-3941.2017.0029. ЧВК 5570602. PMID 28884042.
- ^ Со СК, Чон Х.Й., Пак С.Г., Ли С.В., Чхве И.В., Чен Л., Чхве И. (январь 2008 г.). «Блокада эндогенного B7-H1 подавляет антибактериальную защиту после первичной инфекции Listeria monocytogenes». Иммунология. 123 (1): 90–9. Дои:10.1111 / j.1365-2567.2007.02708.x. ЧВК 2433284. PMID 17971153.
- ^ Ансари М.Дж., Салама А.Д., Читнис Т., Смит Р.Н., Ягита Х., Акиба Х., Ямазаки Т., Азума М., Иваи Х., Хури С.Дж., Очинклосс Х., Сайег М.Х. (июль 2003 г.). «Путь запрограммированной смерти-1 (PD-1) регулирует аутоиммунный диабет у мышей, не страдающих ожирением и диабетом (NOD)». Журнал экспериментальной медицины. 198 (1): 63–9. Дои:10.1084 / jem.20022125. ЧВК 2196083. PMID 12847137.
- ^ Мозаффариан Н., Видеман А. Е., Стивенс А. М. (сентябрь 2008 г.). «Активная системная красная волчанка связана с неспособностью антигенпрезентирующих клеток экспрессировать лиганд-1 запрограммированной смерти». Ревматология. 47 (9): 1335–41. Дои:10.1093 / ревматология / ken256. ЧВК 2722808. PMID 18650228.
внешняя ссылка
- CD274 + белок, + человек в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: Q9NZQ7 (Запрограммированная гибель клеток 1 лиганд 1) на PDBe-KB.




