Генная инженерия - Genetic engineering
| Часть серия на |
| Генная инженерия |
|---|
 |
| Генетически модифицированные организмы |
| История и регулирование |
| Процесс |
| Приложения |
| Споры |
Генная инженерия, также называемый генетическая модификация или же генетическая манипуляция, является прямым воздействием на организм гены с помощью биотехнология. Это набор технологии используется для изменения генетического состава клеток, включая перенос генов внутри и за границы видов для получения улучшенных или новых организмы. Новый ДНК получается путем выделения и копирования интересующего генетического материала с использованием рекомбинантная ДНК методы или искусственно синтезирующий ДНК. А строить обычно создается и используется для вставки этой ДНК в организм-хозяин. Первая рекомбинантная молекула ДНК была создана Пол Берг в 1972 году путем объединения ДНК вируса обезьяны SV40 с лямбда-вирус. А также вставка гены, процесс можно использовать для удаления, или "нокаутировать ", гены. Новая ДНК может быть вставлена случайным образом или целевой к определенной части геном.
Организм, созданный с помощью генной инженерии, считается генетически модифицированным (ГМ), и полученный объект является генетически модифицированный организм (ГМО). Первый ГМО был бактерия создано Герберт Бойер и Стэнли Коэн в 1973 г. Рудольф Яениш создал первое ГМ-животное, вставив чужеродную ДНК в мышь в 1974 году. Первая компания, специализирующаяся на генной инженерии, Genentech, была основана в 1976 году и начала производство человеческих белков. Генно-инженерный человек инсулин был произведен в 1978 году, а инсулинпродуцирующие бактерии начали коммерциализировать в 1982 году. Генетически модифицированная пища продается с 1994 г., с выпуском Флавр Савр помидор. Flavr Savr был разработан для более длительного хранения, но большинство современных ГМ-культур модифицированы для повышения устойчивости к насекомым и гербицидам. GloFish первый ГМО, созданный в виде домашнего животного, был продан в США в декабре 2003 года. В 2016 году лосось модифицированные гормоном роста.
Генная инженерия применяется во многих областях, включая исследования, медицину, промышленную биотехнологию и сельское хозяйство. В исследованиях ГМО используются для изучения функции и экспрессии генов через потерю функции, усиление функции, отслеживание и эксперименты по экспрессии. Вырубая гены, отвечающие за определенные условия, можно создать животные модельные организмы болезней человека. Генная инженерия может не только производить гормоны, вакцины и другие лекарства, но и лечить генетические заболевания с помощью генная терапия. Те же методы, которые используются для производства лекарств, могут также иметь промышленное применение, например, производство ферментов для стиральных порошков, сыров и других продуктов.
Рост коммерциализированных генетически модифицированные культуры принесла экономическую выгоду фермерам во многих разных странах, но также была источником большинства полемика окружающие технологии. Это было с самого начала использования; первые полевые испытания были уничтожены активистами против ГМ. Хотя есть научный консенсус что доступные в настоящее время продукты питания, полученные из ГМ-культур, не представляют большего риска для здоровья человека, чем обычные продукты питания, безопасность ГМ-продуктов вызывает наибольшее беспокойство у критиков. Генетический поток, воздействие на нецелевые организмы, контроль над поставками пищи и интеллектуальная собственность права также были подняты как потенциальные проблемы. Эти опасения привели к разработке нормативной базы, которая началась в 1975 году. Это привело к заключению международного договора, Картахенский протокол по биобезопасности, который был принят в 2000 году. Отдельные страны разработали свои собственные системы регулирования в отношении ГМО, причем наиболее заметные различия наблюдаются между США и Европой.
Обзор
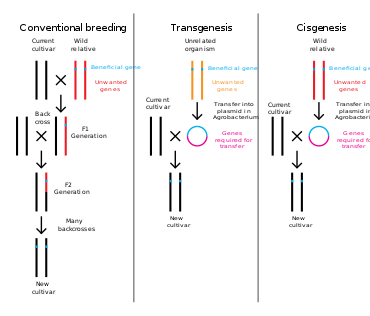
Генная инженерия - это процесс, который изменяет генетическую структуру организма путем удаления или введения ДНК. В отличие от традиционных животное и селекция растений, который включает в себя выполнение нескольких скрещиваний с последующим отбором организма с желаемым фенотип генная инженерия берет ген непосредственно из одного организма и доставляет его в другой. Это намного быстрее, с его помощью можно вставить любые гены из любого организма (даже из разных домены ) и предотвращает добавление других нежелательных генов.[3]
Генная инженерия потенциально может исправить серьезные генетические нарушения у человека путем замены дефектного гена на работающий.[4] Это важный инструмент в исследованиях, который позволяет изучать функцию определенных генов.[5] Лекарства, вакцины и другие продукты были получены из организмов, созданных для их производства.[6] Культуры были разработаны, что помощь Продовольственная безопасность за счет повышения урожайности, пищевой ценности и устойчивости к стрессам окружающей среды.[7]
ДНК может быть введена непосредственно в организм-хозяин или в клетку, которая затем сплавлен или же гибридизированный с хозяином.[8] Это зависит от рекомбинантная нуклеиновая кислота методы формирования новых комбинаций наследуемого генетического материала с последующим включением этого материала либо косвенно через вектор систему или напрямую через микроинъекция, макроинъекция или микрокапсулирование.[9]
Генная инженерия обычно не включает традиционное разведение, экстракорпоральное оплодотворение, индукция полиплоидия, мутагенез и методы слияния клеток, в которых не используются рекомбинантные нуклеиновые кислоты или генетически модифицированный организм.[8] Однако некоторые широкие определения генной инженерии включают: селекция.[9] Клонирование и стволовая клетка исследования, хотя и не считающиеся генной инженерией,[10] тесно связаны, и в них можно использовать генную инженерию.[11] Синтетическая биология это развивающаяся дисциплина, которая делает шаг вперед в генной инженерии, вводя в организм искусственно синтезированный материал.[12] Такой синтетическая ДНК в качестве Искусственно расширенная система генетической информации и ДНК Хатимодзи сделано в этой новой области.
Растения, животные или микроорганизмы, которые были изменены с помощью генной инженерии, называются генетически модифицированные организмы или ГМО.[13] Если к хозяину добавляется генетический материал другого вида, полученный организм называется трансгенный. Если используется генетический материал одного и того же вида или вида, который может естественным образом размножаться с хозяином, полученный организм называется цисгенный.[14] Если генная инженерия используется для удаления генетического материала из организма-мишени, полученный организм называется нокаутировать организм.[15] В Европе генетическая модификация синоним с генной инженерией, в то время как в Соединенных Штатах Америки и Канаде генетическая модификация также может использоваться для обозначения более традиционных методов разведения.[16][17][18]
История
Люди изменяли геномы видов на протяжении тысячелетий. селекция, или искусственный отбор[19]:1[20]:1 в отличие от естественный отбор. В последнее время, мутационное разведение использовал воздействие химикатов или радиации для получения высокой частоты случайных мутаций в целях селекции. Генная инженерия как прямое манипулирование ДНК людьми вне разведения и мутаций существует только с 1970-х годов. Термин «генная инженерия» впервые был введен Джек Уильямсон в его научная фантастика Роман Остров Дракона, опубликовано в 1951 г.[21] - за год до роли ДНК в наследственность был подтвержден Альфред Херши и Марта Чейз,[22] и два года назад Джеймс Уотсон и Фрэнсис Крик показал, что ДНК молекула имеет структуру двойной спирали, хотя общая концепция прямого генетического манипулирования исследовалась в зачаточной форме в Стэнли Г. Вайнбаум Научно-фантастический рассказ 1936 года Остров Протея.[23][24]

В 1972 г. Пол Берг создал первый рекомбинантная ДНК молекулы путем объединения ДНК из вируса обезьяны SV40 с тем из лямбда-вирус.[25] В 1973 г. Герберт Бойер и Стэнли Коэн создал первый трансгенный организм вставив гены устойчивости к антибиотикам в плазмида из кишечная палочка бактерия.[26][27] Год спустя Рудольф Яениш создал трансгенная мышь введя чужеродную ДНК в свой эмбрион, что сделало его первым в мире трансгенное животное[28] Эти достижения вызвали озабоченность в научном сообществе по поводу потенциальных рисков генной инженерии, которые впервые подробно обсуждались на Асиломарская конференция в 1975 году. Одна из основных рекомендаций этого совещания заключалась в том, что государственный надзор за исследованиями рекомбинантной ДНК должен быть установлен до тех пор, пока технология не будет признана безопасной.[29][30]
В 1976 г. Genentech, первая компания генной инженерии, была основана Гербертом Бойером и Роберт Свонсон а через год компания произвела человеческий белок (соматостатин ) в Кишечная палочка. Genentech объявила о производстве генетически модифицированного человека. инсулин в 1978 г.[31] В 1980 г. Верховный суд США в Даймонд против Чакрабарти дело постановило, что генетически измененная жизнь может быть запатентована.[32] В инсулин произведенный бактериями был одобрен для выпуска Управление по контролю за продуктами и лекарствами (FDA) в 1982 году.[33]
В 1983 году биотехнологическая компания Advanced Genetic Sciences (AGS) подала заявку на разрешение правительства США на проведение полевых испытаний с лед минус напряжение из Pseudomonas syringae чтобы защитить посевы от заморозков, но экологические организации и протестующие отложили полевые испытания на четыре года из-за юридических проблем.[34] В 1987 году штамм Ice-minus P. syringae стал первым генетически модифицированный организм (ГМО) для выброса в окружающую среду[35] когда им опрыскали клубничное и картофельное поля в Калифорнии.[36] Оба полигона подверглись нападению со стороны групп активистов в ночь перед проведением тестов: «Первый в мире полигон привлек первого в мире полевого мусорщика».[35]
Первые полевые испытания генно-инженерные растения произошло во Франции и США в 1986 году, табачные растения были спроектированы так, чтобы быть устойчивыми к гербициды.[37] Китайская Народная Республика была первой страной, которая начала коммерциализацию трансгенных растений, представив устойчивый к вирусам табак в 1992 году.[38] В 1994 г. Calgene получено разрешение на коммерческий выпуск первого генетически модифицированная пища, то Флавр Савр, помидор, рассчитанный на более длительный срок хранения.[39] В 1994 году Европейский Союз одобрил табак, устойчивый к гербициду. бромоксинил, что делает его первым выращенным в Европе генетически модифицированным урожаем.[40] В 1995 г. Bt Картофель был одобрен безопасным Агентство по охране окружающей среды после одобрения FDA, что делает его первой культурой для производства пестицидов, одобренной в США.[41] В 2009 году 11 трансгенных культур коммерчески выращивались в 25 странах, крупнейшими из которых по площади были США, Бразилия, Аргентина, Индия, Канада, Китай, Парагвай и Южная Африка.[42]
В 2010 году ученые из Институт Дж. Крейга Вентера создал первый синтетический геном и вставил в пустую бактериальную клетку. Образовавшаяся бактерия, названная Лаборатория микоплазм, мог копировать и производят белки.[43][44] Четыре года спустя это был шаг вперед, когда была разработана бактерия, которая воспроизводила плазмида содержащий уникальный базовая пара, создав первый организм, спроектированный для использования расширенного генетического алфавита.[45][46] В 2012, Дженнифер Дудна и Эммануэль Шарпантье сотрудничали в разработке CRISPR / Cas9 система,[47][48] метод, который можно использовать для легкого и специфического изменения генома практически любого организма.[49]
Процесс

Создание ГМО - это многоэтапный процесс. Генные инженеры должны сначала выбрать, какой ген они хотят вставить в организм. Это обусловлено тем, что является целью полученного организма, и основано на более ранних исследованиях. Генетические экраны могут быть выполнены для определения потенциальных генов, а затем использованы дальнейшие тесты для определения лучших кандидатов. Развитие микрочипы, транскриптомика и секвенирование генома значительно упростили поиск подходящих генов.[50] Удача тоже играет свою роль; Ген готовности к сбору информации был обнаружен после того, как ученые заметили, что бактерия процветает в присутствии гербицида.[51]
Выделение и клонирование генов
Следующим шагом является выделение гена-кандидата. В клетка содержащий ген, раскрывается, и ДНК очищается.[52] Ген отделяется с помощью рестрикционные ферменты разрезать ДНК на фрагменты[53] или же полимеразной цепной реакции (ПЦР) для амплификации генного сегмента.[54] Затем эти сегменты можно извлечь через гель-электрофорез. Если выбранный ген или донорский организм геном был хорошо изучен, возможно, он уже доступен из генетическая библиотека. Если Последовательность ДНК известно, но нет доступных копий гена, он также может быть искусственно синтезированный.[55] После выделения ген перевязанный в плазмида который затем вводится в бактерию. Плазмида реплицируется при делении бактерий, обеспечивая доступность неограниченного количества копий гена.[56]
Прежде чем ген будет введен в организм-мишень, он должен быть скомбинирован с другими генетическими элементами. К ним относятся промоутер и терминатор регион, который начинается и заканчивается транскрипция. А выбираемый маркер добавлен ген, который в большинстве случаев дает устойчивость к антибиотикам, поэтому исследователи могут легко определить, какие клетки были успешно трансформированы. На этом этапе ген также можно модифицировать для лучшей экспрессии или эффективности. Эти манипуляции проводятся с помощью рекомбинантная ДНК методы, такие как ограничительные дайджесты, лигирование и молекулярное клонирование.[57]
Вставка ДНК в геном хозяина

Существует ряд методов, используемых для вставки генетического материала в геном хозяина. Некоторые бактерии могут естественным образом взять чужую ДНК. Эта способность может быть вызвана у других бактерий через стресс (например, тепловой или поражение электрическим током), что увеличивает проницаемость клеточной мембраны для ДНК; извлеченная ДНК может либо интегрироваться с геномом, либо существовать как внехромосомная ДНК. ДНК обычно вставляют в клетки животных с использованием микроинъекция, куда он может быть введен через ядерная оболочка прямо в ядро, или с помощью вирусные векторы.[58]
Геномы растений можно создать физическими методами или с помощью Агробактерии для доставки последовательностей, размещенных в Бинарные векторы Т-ДНК. В растения ДНК часто вставляют с помощью Агробактерии-опосредованная трансформация,[59] воспользовавшись Агробактерииs Т-ДНК последовательность, которая позволяет естественным образом внедрять генетический материал в клетки растений.[60] Другие методы включают биолистика, где частицы золота или вольфрама покрываются ДНК, а затем попадают в молодые клетки растений,[61] и электропорация, который включает использование электрического шока, чтобы сделать клеточную мембрану проницаемой для плазмидной ДНК.
Поскольку генетическим материалом трансформируется только одна клетка, организм должен быть регенерированный из этой единственной клетки. У растений это достигается за счет использования культура ткани.[62][63] У животных необходимо убедиться, что вставленная ДНК присутствует в эмбриональные стволовые клетки.[64] Бактерии состоят из одной клетки и размножаются клонально, поэтому в регенерации нет необходимости. Выбираемые маркеры используются для легкой дифференциации трансформированных клеток от нетрансформированных. Эти маркеры обычно присутствуют в трансгенном организме, хотя был разработан ряд стратегий, которые могут удалить селектируемый маркер из зрелого трансгенного растения.[65]

Дальнейшее тестирование с помощью ПЦР, Южная гибридизация, и Секвенирование ДНК проводится для подтверждения того, что организм содержит новый ген.[66] Эти тесты также могут подтвердить хромосомное расположение и количество копий встроенного гена. Наличие гена не гарантирует, что он будет выразил на соответствующих уровнях в целевой ткани, поэтому также используются методы, которые ищут и измеряют генные продукты (РНК и белок). К ним относятся северная гибридизация, количественный ОТ-ПЦР, Вестерн-блоттинг, иммунофлуоресценция, ELISA и фенотипический анализ.[67]
Новый генетический материал может быть случайным образом вставлен в геном хозяина или направлен в определенное место. Техника нацеливание на гены использует гомологичная рекомбинация внести желаемые изменения в конкретный эндогенный ген. Это, как правило, происходит с относительно низкой частотой у растений и животных и обычно требует использования выбираемые маркеры. Частота нацеливания на гены может быть значительно увеличена за счет редактирование генома. Для редактирования генома используются искусственно созданные нуклеазы которые создают конкретные двухцепочечные разрывы в желаемых местах в геноме, и использовать эндогенные механизмы клетки для восстановления вызванного разрыва естественными процессами гомологичная рекомбинация и негомологичное соединение концов. Существует четыре семейства сконструированных нуклеаз: мегануклеазы,[68][69] нуклеазы цинковых пальцев,[70][71] эффекторные нуклеазы, подобные активаторам транскрипции (ТАЛЕНЫ),[72][73] и система Cas9-guideRNA (адаптированная из CRISPR).[74][75] TALEN и CRISPR - два наиболее часто используемых, и каждый из них имеет свои преимущества.[76] TALEN обладают большей целевой специфичностью, тогда как CRISPR проще в разработке и более эффективен.[76] В дополнение к усилению нацеливания на гены, сконструированные нуклеазы можно использовать для введения мутаций в эндогенные гены, которые генерируют нокаут гена.[77][78]
Приложения
Генная инженерия находит применение в медицине, исследованиях, промышленности и сельском хозяйстве и может использоваться на широком спектре растений, животных и микроорганизмов. Бактерии, первые организмы, которые будут генетически модифицированы, могут иметь вставленную плазмидную ДНК, содержащую новые гены, которые кодируют лекарства или ферменты, которые обрабатывают пищу и другие субстраты.[79][80] Растения были модифицированы для защиты от насекомых, устойчивости к гербицидам, устойчивости к вирусам, улучшенного питания, устойчивости к давлению окружающей среды и производства съедобные вакцины.[81] Большинство коммерчески выпускаемых ГМО - это культурные растения, устойчивые к насекомым или гербицидам.[82] Генетически модифицированные животные использовались для исследований, модельных животных и производства сельскохозяйственных или фармацевтических продуктов. К генетически модифицированным животным относятся животные с гены выбиты, повышенная восприимчивость к болезням, гормоны для дополнительного роста и способности экспрессировать белки с молоком.[83]
Лекарство
Генная инженерия имеет множество применений в медицине, включая производство лекарств, создание модельные животные которые имитируют человеческие условия и генная терапия. Одним из первых применений генной инженерии было массовое производство человеческого инсулина в бактериях.[31] Это приложение было применено к человеку гормоны роста, фолликулостимулирующие гормоны (для лечения бесплодия), человеческий альбумин, моноклональные антитела, антигемофильные факторы, вакцина и многие другие препараты.[84][85] Мышь гибридомы, клетки слились вместе, чтобы создать моноклональные антитела, были адаптированы с помощью генной инженерии для создания человеческих моноклональных антител.[86] В 2017 году генная инженерия химерные антигенные рецепторы самостоятельно Т-клетки был одобрен США FDA как лечение рака острый лимфобластный лейкоз. Генно-инженерные вирусы разрабатываются, которые по-прежнему могут давать иммунитет, но не имеют заразный последовательности.[87]
Генная инженерия также используется для создания животных моделей болезней человека. Генетически модифицированные мыши являются наиболее распространенными генно-инженерными моделями животных.[88] Они использовались для изучения и моделирования рака ( онкомышь ), ожирение, болезни сердца, диабет, артрит, токсикомания, беспокойство, старение и болезнь Паркинсона.[89] На этих моделях мышей можно проверить возможные лекарства. Также были выведены генетически модифицированные свиньи с целью увеличения успеха Свинья для трансплантации органов человека.[90]
Генная терапия - это генная инженерия человека, как правило, путем замены дефектных генов эффективными. Клинические исследования с помощью соматический генная терапия проводилась при нескольких заболеваниях, в том числе Х-сцепленный ТКИД,[91] хронический лимфолейкоз (CLL),[92][93] и болезнь Паркинсона.[94] В 2012, Алипоген типарвовец стал первым препаратом генной терапии, одобренным для клинического использования.[95][96] В 2015 году вирус был использован для внедрения здорового гена в клетки кожи мальчика, страдающего редким кожным заболеванием, буллезный эпидермолиз, чтобы вырасти, а затем пересадить здоровую кожу на 80 процентов тела мальчика, пострадавшего от болезни.[97]
Зародышевый генная терапия приведет к тому, что любые изменения будут переданы по наследству, что вызвало обеспокоенность в научном сообществе.[98][99] В 2015 году CRISPR использовался для редактирования ДНК нежизнеспособных человеческие эмбрионы,[100][101] ведущие ученые ведущих мировых академий призвали к мораторию на редактирование наследуемого генома человека.[102] Есть также опасения, что эту технологию можно использовать не только для лечения, но и для улучшения, модификации или изменения внешнего вида, приспособляемости, интеллекта, характера или поведения человека.[103] Также бывает сложно провести различие между лечением и улучшением.[104] В ноябре 2018 г. Хэ Цзянькуй объявил, что он отредактировал геномы двух человеческих эмбрионов, чтобы попытаться отключить CCR5 ген, который кодирует рецептор, ВИЧ используется для входа в клетки. Он сказал, что девочки-близнецы Лулу и Нана родились несколькими неделями ранее. Он сказал, что у девочек все еще есть функциональные копии CCR5 вместе с отключенным CCR5 (мозаика ) и все еще были уязвимы к ВИЧ. Работа была широко осуждена как неэтичная, опасная и преждевременная.[105] В настоящее время модификация зародышевой линии запрещена в 40 странах мира. Ученые, которые проводят такие исследования, часто позволяют эмбрионам расти в течение нескольких дней, не позволяя им развиться в ребенка. [106]
Исследователи изменяют геном свиней, чтобы стимулировать рост человеческих органов, которые будут использоваться при трансплантации. Ученые создают «генные двигатели», изменяя геномы комаров, чтобы сделать их невосприимчивыми к малярии, а затем стремятся распространить генетически измененных комаров по популяции комаров в надежде искоренить болезнь.[107]
Исследование
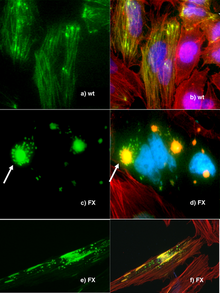
Генная инженерия - важный инструмент для естествоиспытатели, с созданием трансгенных организмов одним из важнейших инструментов для анализа функции генов.[108] Гены и другая генетическая информация от широкого круга организмов может быть вставлена в бактерии для хранения и модификации, создавая генетически модифицированные бактерии в процессе. Бактерии дешевы, их легко выращивать, клональный, быстро размножаются, относительно легко трансформируются и могут храниться при -80 ° C практически неограниченное время. После выделения гена его можно хранить внутри бактерий, обеспечивая неограниченный запас для исследований.[109]Организмы созданы с помощью генной инженерии, чтобы обнаружить функции определенных генов. Это может быть влияние на фенотип организма, где экспрессируется ген или с какими другими генами он взаимодействует. Эти эксперименты обычно включают потерю функции, усиление функции, отслеживание и выражение.
- Эксперименты с потерей функции, например, в нокаут гена эксперимент, в котором организм сконструирован так, чтобы не иметь активности одного или нескольких генов. При простом нокауте копия желаемого гена была изменена, чтобы сделать его нефункциональным. Эмбриональные стволовые клетки включить измененный ген, который заменяет уже существующую функциональную копию. Эти стволовые клетки вводятся в бластоцисты, которые вживляют суррогатным мамам. Это позволяет экспериментатору анализировать дефекты, вызванные этим мутация и тем самым определить роль конкретных генов. Особенно часто он используется в биология развития.[110] Когда это делается путем создания библиотеки генов с точечными мутациями в каждой позиции в интересующей области или даже в каждой позиции во всем гене, это называется «сканирующий мутагенез». Самым простым и первым из используемых методов является «сканирование аланина», при котором каждая позиция в свою очередь превращается в нереактивную аминокислоту. аланин.[111]
- Получение функциональных экспериментов, логический аналог нокаутов. Иногда их проводят в сочетании с экспериментами по нокауту, чтобы более точно установить функцию желаемого гена. Процесс во многом такой же, как и при нокаут-инженерии, за исключением того, что конструкция предназначена для увеличения функции гена, обычно путем предоставления дополнительных копий гена или более частого индуцирования синтеза белка. Прирост функции используется, чтобы определить, достаточно ли белка для выполнения функции, но не всегда означает, что это необходимо, особенно когда речь идет о генетической или функциональной избыточности.[110]
- Отслеживание экспериментов, которые стремятся получить информацию о локализации и взаимодействии желаемого белка. Один из способов сделать это - заменить ген дикого типа "гибридным" геном, который представляет собой сопоставление гена дикого типа с элементом сообщения, таким как зеленый флуоресцентный белок (GFP), что позволит легко визуализировать продукты генетической модификации. Хотя это полезный метод, манипуляции могут нарушить функцию гена, создавая вторичные эффекты и, возможно, ставя под сомнение результаты эксперимента. В настоящее время разрабатываются более сложные методы, позволяющие отслеживать белковые продукты без уменьшения их функции, такие как добавление небольших последовательностей, которые будут служить в качестве связывающих мотивов для моноклональных антител.[110]
- Исследования экспрессии стремятся узнать, где и когда производятся определенные белки. В этих экспериментах последовательность ДНК перед ДНК, которая кодирует белок, известный как ген промоутер, повторно вводится в организм с заменой кодирующей белок области на репортерный ген, такой как GFP, или фермент, который катализирует выработку красителя. Таким образом можно наблюдать время и место, где производится конкретный белок. Изучение экспрессии может быть продвинуто дальше, изменяя промотор, чтобы определить, какие части являются решающими для правильной экспрессии гена и фактически связаны белками факторов транскрипции; этот процесс известен как трепка промоутера.[112]
Промышленное

Организмы могут трансформировать свои клетки геном, кодирующим полезный белок, такой как фермент, чтобы они сверхэкспрессировать желаемый белок. Затем можно произвести массовые количества белка, выращивая трансформированный организм в биореактор оборудование, использующее промышленная ферментация, а потом очищающий белок.[113] Некоторые гены плохо работают у бактерий, поэтому также можно использовать клетки дрожжей, насекомых или млекопитающих.[114] Эти методы используются для производства таких лекарств, как инсулин, гормон роста человека, и вакцина, добавки, такие как триптофан, помощь в производстве продуктов питания (химозин в сыроварении) и топлива.[115] Другие приложения с генно-инженерными бактериями могут включать в себя выполнение задач, выходящих за рамки их естественного цикла, например создание биотопливо,[116] уборка разливов нефти, углерода и других токсичных отходов[117] и обнаружение мышьяка в питьевой воде.[118] Некоторые генетически модифицированные микробы также могут использоваться в биодобыча и биоремедиация из-за их способности извлекать тяжелые металлы из окружающей среды и включать их в соединения, которые легче восстановить.[119]
В материаловедение, генетически модифицированный вирус был использован в исследовательской лаборатории в качестве основы для создания более экологически чистого литий-ионный аккумулятор.[120][121] Бактерии также были созданы для работы в качестве сенсоров, экспрессируя флуоресцентный белок в определенных условиях окружающей среды.[122]
сельское хозяйство

Один из самых известных и спорный применения генной инженерии - создание и использование генетически модифицированные культуры или же генетически модифицированный скот производить генетически модифицированная пища. Культуры созданы для увеличения урожайности, повышения устойчивости к абиотические стрессы, изменить состав пищи или производить новые продукты.[124]
Первые культуры, которые будут выпущены в промышленном масштабе в больших масштабах, обеспечили защиту от насекомых-вредителей или устойчивость к гербициды. Также были созданы или разрабатываются устойчивые к грибам и вирусам культуры.[125][126] Это облегчает борьбу с насекомыми и сорняками в сельскохозяйственных культурах и может косвенно повысить урожайность сельскохозяйственных культур.[127][128] ГМ-культуры, которые напрямую повышают урожайность за счет ускорения роста или повышения устойчивости растений (за счет повышения устойчивости к соли, холоду или засухе), также находятся в стадии разработки.[129] В 2016 г. Лосось были генетически модифицированы гормонами роста, чтобы быстрее достигать нормального взрослого размера.[130]
Были разработаны ГМО, которые изменяют качество продукции, увеличивая пищевую ценность или обеспечивая более промышленно полезные качества или количества.[129] В Амфлора картофель производит более промышленно полезную смесь крахмалов. Соевые бобы и канола были генетически модифицированы для производства более полезных масел.[131][132] Первым коммерчески доступным генетически модифицированным кормом был помидор задержали созревание, увеличивая срок годности.[133]
Растения и животные созданы для производства материалов, которые они обычно не производят. Фарминг использует растения и животных в качестве биореакторов для производства вакцин, промежуточных лекарственных препаратов или самих лекарств; полезный продукт очищается от урожая и затем используется в стандартном фармацевтическом производственном процессе.[134] Коровы и козы были сконструированы для экспрессии лекарств и других белков в их молоке, а в 2009 году FDA одобрило лекарство, производимое на козьем молоке.[135][136]
Другие приложения
У генной инженерии есть потенциальные приложения для сохранения и управления природными территориями. Передача гена через вирусные векторы был предложен в качестве средства борьбы с инвазивными видами, а также для вакцинации угрожаемой фауны от болезней.[137] Были предложены трансгенные деревья как способ придать устойчивость к патогенам в диких популяциях.[138] С увеличением рисков дезадаптация У организмов в результате изменения климата и других возмущений облегченная адаптация путем корректировки генов могла бы стать одним из решений снижения рисков исчезновения.[139] Применение генной инженерии в области сохранения до сих пор носит в основном теоретический характер и еще не реализовано на практике.
Генная инженерия также используется для создания микробное искусство.[140] Некоторые бактерии были генетически модифицированы для создания черно-белых фотографий.[141] Новинки, например, цвета лаванды гвоздики,[142] синие розы,[143] и светящаяся рыба[144][145] также были получены с помощью генной инженерии.
Регулирование
Регулирование генной инженерии касается подходов, применяемых правительствами для оценки и управления рисками, связанными с разработкой и выпуском ГМО. Разработка нормативной базы началась в 1975 г. Асиломар, Калифорния.[146] В Встреча Асиломара рекомендовал набор добровольных руководящих принципов по использованию рекомбинантной технологии.[29] По мере совершенствования технологий в США был создан комитет в Управление науки и технологий,[147] который предоставил регулирующее одобрение ГМ-продуктов Министерству сельского хозяйства США, FDA и EPA.[148] В Картахенский протокол по биобезопасности, международный договор, регулирующий передачу, обработку и использование ГМО,[149] был принят 29 января 2000 г.[150] Сто пятьдесят семь стран являются участниками Протокола, и многие используют его в качестве ориентира для своих собственных правил.[151]
Правовой и нормативный статус ГМ-продуктов различается в зависимости от страны: некоторые страны запрещают или ограничивают их, а другие разрешают их с сильно различающейся степенью регулирования.[152][153][154][155] Некоторые страны разрешают импорт генетически модифицированных продуктов питания с разрешения, но либо не разрешают их выращивание (Россия, Норвегия, Израиль), либо имеют условия для выращивания, даже если продукты с ГМО еще не производятся (Япония, Южная Корея). Большинство стран, которые не разрешают выращивание ГМО, разрешают исследования.[156] Некоторые из наиболее заметных различий между США и Европой. Политика США фокусируется на продукте (а не на процессе), рассматривает только поддающиеся проверке научные риски и использует концепцию существенная эквивалентность.[157] В Евросоюз напротив, имеет, возможно, самые строгие правила в отношении ГМО в мире.[158] Все ГМО вместе с облученная еда, считаются «новой пищей» и подлежат всесторонней, индивидуальной, научно обоснованной оценке пищевых продуктов Европейское агентство по безопасности пищевых продуктов. Критерии авторизации делятся на четыре широкие категории: «безопасность», «свобода выбора», «маркировка» и «отслеживаемость».[159] Уровень регулирования в других странах, выращивающих ГМО, находится между Европой и США.
| Область, край | Регуляторы | Примечания |
|---|---|---|
| нас | USDA, FDA и EPA[148] | |
| Европа | Европейское агентство по безопасности пищевых продуктов[159] | |
| Канада | Министерство здравоохранения Канады и Канадское агентство по инспекции пищевых продуктов[160][161] | Регулируемые продукты с новыми характеристиками независимо от способа происхождения[162][163] |
| Африка | Общий рынок Восточной и Южной Африки[164] | Окончательное решение остается за каждой отдельной страной.[164] |
| Китай | Управление сельскохозяйственной генной инженерии, Управление по биобезопасности[165] | |
| Индия | Комитет по институциональной биобезопасности, Комитет по рассмотрению генетических манипуляций и Комитет по одобрению генной инженерии[166] | |
| Аргентина | Национальный консультативный комитет по сельскохозяйственной биотехнологии (воздействие на окружающую среду), Национальная служба здравоохранения и качества пищевых продуктов (безопасность пищевых продуктов) и Национальное управление агробизнеса (влияние на торговлю)[167] | Окончательное решение принял Секретариат сельского хозяйства, животноводства, рыболовства и продовольствия.[167] |
| Бразилия | Национальная техническая комиссия по биобезопасности (экологическая безопасность и безопасность пищевых продуктов) и Совет министров (коммерческие и экономические вопросы)[167] | |
| Австралия | Управление регулятора генных технологий (контролирует все продукты GM), Управление терапевтических товаров (ГМ-лекарства) и Стандарты пищевых продуктов Австралия Новая Зеландия (ГМО пища).[168][169] | Затем правительства отдельных штатов могут оценить влияние выпуска на рынки и торговлю и применить дальнейшее законодательство для контроля одобренных генетически модифицированных продуктов.[169] |
Один из ключевых вопросов, касающихся регулирующих органов, заключается в том, следует ли маркировать ГМ-продукты. В Европейская комиссия говорит, что обязательная маркировка и отслеживаемость необходимы для обеспечения осознанного выбора и предотвращения потенциальных ложная реклама[170] и облегчить изъятие продуктов при обнаружении неблагоприятного воздействия на здоровье или окружающую среду.[171] В Американская медицинская ассоциация[172] и Американская ассоциация развития науки[173] говорят, что при отсутствии научных доказательств вреда даже добровольная маркировка вводящий в заблуждение и будет ложно тревожить потребителей. Маркировка ГМО-продуктов на рынке требуется в 64 странах.[174] Маркировка может быть обязательной до порогового уровня содержания ГМ (который варьируется в зависимости от страны) или добровольным. В Канаде и США маркировка генетически модифицированных продуктов питания является добровольной,[175] в то время как в Европе вся еда (в том числе обработанная пища ) или же подача который содержит более 0,9% одобренных ГМО, должен быть маркирован.[158]
Полемика
Критики возражали против использования генной инженерии по нескольким причинам, включая этические, экологические и экономические соображения. Многие из этих проблем связаны с ГМ-культурами и безопасностью продуктов, произведенных из них, и о том, какое влияние их выращивание окажет на окружающую среду. Эти разногласия привели к судебным разбирательствам, международным торговым спорам и протестам, а также к ограничительному регулированию коммерческих продуктов в некоторых странах.[176]
Обвинения ученых "играющий Бог " и другие религиозные вопросы были приписаны технологии с самого начала.[177] Другие поднятые этические вопросы включают патентование жизни,[178] использование интеллектуальная собственность права[179] уровень маркировки продукции,[180][181] контроль поставок продуктов питания[182] и объективность процесса регулирования.[183] Хотя были сомнения,[184] С экономической точки зрения большинство исследований показало, что выращивание ГМ-культур приносит пользу фермерам.[185][186][187]
Генетический поток между ГМ-культурами и совместимыми растениями, наряду с более широким использованием селективных гербициды, может увеличить риск "суперсорняки "развивающийся.[188] Другие экологические проблемы связаны с потенциальным воздействием на нецелевые организмы, включая почвенные микробы,[189] и увеличение числа вторичных и устойчивых насекомых-вредителей.[190][191] Many of the environmental impacts regarding GM crops may take many years to be understood and are also evident in conventional agriculture practices.[189][192] With the commercialisation of генетически модифицированная рыба there are concerns over what the environmental consequences will be if they escape.[193]
There are three main concerns over the safety of genetically modified food: whether they may provoke an аллергическая реакция; whether the genes could transfer from the food into human cells; and whether the genes not approved for human consumption could outcross to other crops.[194] Существует научный консенсус[195][196][197][198] что доступные в настоящее время продукты питания, полученные из ГМ-культур, не представляют большего риска для здоровья человека, чем обычные продукты питания,[199][200][201][202][203] но каждый ГМО-продукт необходимо тестировать в индивидуальном порядке перед введением.[204][205][206] Nonetheless, members of the public are less likely than scientists to perceive GM foods as safe.[207][208][209][210]
В популярной культуре
Genetic engineering features in many научная фантастика рассказы.[211] Фрэнк Герберт роман The White Plague described the deliberate use of genetic engineering to create a возбудитель which specifically killed women.[211] Another of Herbert's creations, the Дюна series of novels, uses genetic engineering to create the powerful but despised Тлейлаксу.[212] Такие фильмы, как Остров и Бегущий по лезвию bring the engineered creature to confront the person who created it or the being it was cloned from. Few films have informed audiences about genetic engineering, with the exception of the 1978 Мальчики из Бразилии and the 1993 парк Юрского периода, both of which made use of a lesson, a demonstration, and a clip of scientific film.[213][214] Genetic engineering methods are weakly represented in film; Michael Clark, writing for The Wellcome Trust, calls the portrayal of genetic engineering and biotechnology "seriously distorted"[214] в таких фильмах, как 6 день. In Clark's view, the biotechnology is typically "given fantastic but visually arresting forms" while the science is either relegated to the background or fictionalised to suit a young audience.[214]
Смотрите также
- Биологическая инженерия
- Modifications (genetics)
- RNA editing#Therapeutic mRNA Editing
- Mutagenesis (molecular biology technique)
Рекомендации
- ^ "Terms and Acronyms". U.S. Environmental Protection Agency online. Получено 16 июля 2015.
- ^ Vert M, Doi Y, Hellwich KH, Hess M, Hodge P, Kubisa P, Rinaudo M, Schué F (2012). "Terminology for biorelated polymers and applications (IUPAC Recommendations 2012)". Чистая и прикладная химия. 84 (2): 377–410. Дои:10.1351 / PAC-REC-10-12-04. S2CID 98107080.
- ^ "How does GM differ from conventional plant breeding?". royalsociety.org. Получено 14 ноября 2017.
- ^ Erwin E, Gendin S, Kleiman L (22 December 2015). Ethical Issues in Scientific Research: An Anthology. Рутледж. п. 338. ISBN 978-1-134-81774-0.
- ^ Alexander DR (May 2003). "Uses and abuses of genetic engineering". Последипломный медицинский журнал. 79 (931): 249–51. Дои:10.1136/pmj.79.931.249. ЧВК 1742694. PMID 12782769.
- ^ Nielsen J (1 July 2013). "Production of biopharmaceutical proteins by yeast: advances through metabolic engineering". Bioengineered. 4 (4): 207–11. Дои:10.4161/bioe.22856. ЧВК 3728191. PMID 23147168.
- ^ Qaim M, Kouser S (5 June 2013). "Genetically modified crops and food security". PLOS ONE. 8 (6): e64879. Bibcode:2013PLoSO...864879Q. Дои:10.1371/journal.pone.0064879. ЧВК 3674000. PMID 23755155.
- ^ а б The European Parliament and the council of the European Union (12 March 2001). "Directive on the release of genetically modified organisms (GMOs) Directive 2001/18/EC ANNEX I A". Official Journal of the European Communities. Цитировать журнал требует
| журнал =(помощь) - ^ а б Сотрудники Economic Impacts of Genetically Modified Crops on the Agri-Food Sector; п. 42 Glossary – Term and Definitions В архиве 14 мая 2013 г. Wayback Machine The European Commission Directorate-General for Agriculture, "Genetic engineering: The manipulation of an organism's genetic endowment by introducing or eliminating specific genes through modern molecular biology techniques. A broad definition of genetic engineering also includes selective breeding and other means of artificial selection.", Retrieved 5 November 2012
- ^ Van Eenennaam A. "Is Livestock Cloning Another Form of Genetic Engineering?" (PDF). agbiotech. Архивировано из оригинал (PDF) on 11 May 2011.
- ^ Suter DM, Dubois-Dauphin M, Krause KH (July 2006). "Genetic engineering of embryonic stem cells" (PDF). Швейцарский медицинский еженедельник. 136 (27–28): 413–5. PMID 16897894. Архивировано из оригинал (PDF) 7 июля 2011 г.
- ^ Andrianantoandro E, Basu S, Karig DK, Weiss R (16 May 2006). "Synthetic biology: new engineering rules for an emerging discipline". Молекулярная системная биология. 2 (2006.0028): 2006.0028. Дои:10.1038/msb4100073. ЧВК 1681505. PMID 16738572.
- ^ "What is genetic modification (GM)?". CSIRO.
- ^ Jacobsen E, Schouten HJ (2008). "Cisgenesis, a New Tool for Traditional Plant Breeding, Should be Exempted from the Regulation on Genetically Modified Organisms in a Step by Step Approach". Картофельные исследования. 51: 75–88. Дои:10.1007/s11540-008-9097-y. S2CID 38742532.
- ^ Capecchi MR (October 2001). "Generating mice with targeted mutations". Природа Медицина. 7 (10): 1086–90. Дои:10.1038/nm1001-1086. PMID 11590420. S2CID 14710881.
- ^ Сотрудники Biotechnology – Glossary of Agricultural Biotechnology Terms В архиве 30 августа 2014 г. Wayback Machine United States Department of Agriculture, "Genetic modification: The production of heritable improvements in plants or animals for specific uses, via either genetic engineering or other more traditional methods. Some countries other than the United States use this term to refer specifically to genetic engineering.", Retrieved 5 November 2012
- ^ Maryanski JH (19 October 1999). "Genetically Engineered Foods". Center for Food Safety and Applied Nutrition at the Управление по контролю за продуктами и лекарствами.
- ^ Staff (28 November 2005) Health Canada – The Regulation of Genetically Modified Food В архиве 10 June 2017 at the Wayback Machine Glossary definition of Genetically Modified: "An organism, such as a plant, animal or bacterium, is considered genetically modified if its genetic material has been altered through any method, including conventional breeding. A 'GMO' is a genetically modified organism.", Retrieved 5 November 2012
- ^ Root C (2007). Одомашнивание. Greenwood Publishing Groups.
- ^ Zohary D, Hopf M, Weiss E (2012). Domestication of Plants in the Old World: The origin and spread of plants in the old world. Издательство Оксфордского университета.
- ^ Стейблфорд Б.М. (2004). Исторический словарь научно-фантастической литературы. п. 133. ISBN 978-0-8108-4938-9.
- ^ Херши А.Д., Чейз М. (май 1952 г.). «Независимые функции вирусного белка и нуклеиновой кислоты в росте бактериофага». Журнал общей физиологии. 36 (1): 39–56. Дои:10.1085 / jgp.36.1.39. ЧВК 2147348. PMID 12981234.
- ^ "Genetic Engineering". Энциклопедия научной фантастики. 2 апреля 2015 г.
- ^ Shiv Kant Prasad, Ajay Dash (2008). Modern Concepts in Nanotechnology, Volume 5. Издательство Discovery. ISBN 978-81-8356-296-6.CS1 maint: использует параметр авторов (связь)
- ^ Jackson DA, Symons RH, Berg P (October 1972). "Biochemical method for inserting new genetic information into DNA of Simian Virus 40: circular SV40 DNA molecules containing lambda phage genes and the galactose operon of Escherichia coli". Труды Национальной академии наук Соединенных Штатов Америки. 69 (10): 2904–9. Bibcode:1972PNAS...69.2904J. Дои:10.1073/pnas.69.10.2904. ЧВК 389671. PMID 4342968.
- ^ Arnold P (2009). "History of Genetics: Genetic Engineering Timeline".
- ^ Gutschi S, Hermann W, Stenzl W, Tscheliessnigg KH (1 May 1973). "[Displacement of electrodes in pacemaker patients (author's transl)]". Zentralblatt für Chirurgie. 104 (2): 100–4. PMID 433482.
- ^ Jaenisch R, Mintz B (April 1974). "Simian virus 40 DNA sequences in DNA of healthy adult mice derived from preimplantation blastocysts injected with viral DNA". Труды Национальной академии наук Соединенных Штатов Америки. 71 (4): 1250–4. Bibcode:1974PNAS...71.1250J. Дои:10.1073/pnas.71.4.1250. ЧВК 388203. PMID 4364530.
- ^ а б Berg P, Baltimore D, Brenner S, Roblin RO, Singer MF (June 1975). "Summary statement of the Asilomar conference on recombinant DNA molecules". Труды Национальной академии наук Соединенных Штатов Америки. 72 (6): 1981–4. Bibcode:1975PNAS...72.1981B. Дои:10.1073/pnas.72.6.1981. ЧВК 432675. PMID 806076.
- ^ "NIH Guidelines for research involving recombinant DNA molecules". Office of Biotechnology Activities. Министерство здравоохранения и социальных служб США. Архивировано из оригинал 10 сентября 2012 г.
- ^ а б Goeddel DV, Kleid DG, Bolivar F, Heyneker HL, Yansura DG, Crea R, Hirose T, Kraszewski A, Itakura K, Riggs AD (January 1979). "Expression in Escherichia coli of chemically synthesized genes for human insulin". Труды Национальной академии наук Соединенных Штатов Америки. 76 (1): 106–10. Bibcode:1979PNAS...76..106G. Дои:10.1073/pnas.76.1.106. ЧВК 382885. PMID 85300.
- ^ US Supreme Court Cases from Justia & Oyez (16 June 1980). "Diamond V Chakrabarty". 447 (303). Supreme.justia.com. Получено 17 июля 2010. Цитировать журнал требует
| журнал =(помощь) - ^ "Artificial Genes". ВРЕМЯ. 15 ноября 1982 г.. Получено 17 июля 2010.
- ^ Bratspies R (2007). "Some Thoughts on the American Approach to Regulating Genetically Modified Organisms". Kansas Journal of Law & Public Policy. 16 (3): 101–31. SSRN 1017832.
- ^ а б BBC News 14 June 2002 GM crops: A bitter harvest?
- ^ Thomas H. Maugh II for the Los Angeles Times. 9 June 1987. Altered Bacterium Does Its Job : Frost Failed to Damage Sprayed Test Crop, Company Says
- ^ Джеймс С. (1996). «Глобальный обзор полевых испытаний и коммерциализации трансгенных растений: 1986–1995» (PDF). Международная служба по приобретению агробиотехнологических приложений. Получено 17 июля 2010.
- ^ James C (1997). "Global Status of Transgenic Crops in 1997" (PDF). ISAAA Briefs No. 5.: 31.
- ^ Bruening G, Lyons JM (2000). "The case of the FLAVR SAVR tomato". Калифорнийское сельское хозяйство. 54 (4): 6–7. Дои:10.3733/ca.v054n04p6.
- ^ MacKenzie D (18 June 1994). "Transgenic tobacco is European first". Новый ученый.
- ^ Генетически измененный картофель, пригодный для выращивания сельскохозяйственных культур Lawrence Journal-World – 6 May 1995
- ^ Global Status of Commercialized Biotech/GM Crops: 2009 ISAAA Brief 41-2009, 23 February 2010. Retrieved 10 August 2010
- ^ Pennisi E (May 2010). "Genomics. Synthetic genome brings new life to bacterium". Наука. 328 (5981): 958–9. Дои:10.1126/science.328.5981.958. PMID 20488994.
- ^ Гибсон Д.Г., Гласс Дж. И., Лартиг С., Носков В.Н., Чуанг Р.Ю., Альгире М.А. и др. (Июль 2010 г.). "Creation of a bacterial cell controlled by a chemically synthesized genome". Наука. 329 (5987): 52–6. Bibcode:2010Sci...329...52G. CiteSeerX 10.1.1.167.1455. Дои:10.1126/science.1190719. PMID 20488990. S2CID 7320517.
- ^ Малышев Д.А., Дхами К., Лавергн Т., Чен Т., Дай Н., Фостер Дж. М., Корреа И. Р., Ромесберг Ф. Э. (май 2014 г.). «Полусинтетический организм с расширенным генетическим алфавитом». Природа. 509 (7500): 385–8. Bibcode:2014Натура.509..385M. Дои:10.1038 / природа13314. ЧВК 4058825. PMID 24805238.
- ^ Thyer R, Ellefson J (May 2014). "Synthetic biology: New letters for life's alphabet". Природа. 509 (7500): 291–2. Bibcode:2014Natur.509..291T. Дои:10.1038/nature13335. PMID 24805244. S2CID 4399670.
- ^ Pollack A (11 May 2015). "Jennifer Doudna, a Pioneer Who Helped Simplify Genome Editing". Нью-Йорк Таймс. Получено 15 ноября 2017.
- ^ Jinek M, Chylinski K, Fonfara I, Hauer M, Doudna JA, Charpentier E (August 2012). "A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity". Наука. 337 (6096): 816–21. Bibcode:2012Sci...337..816J. Дои:10.1126/science.1225829. ЧВК 6286148. PMID 22745249.
- ^ Ledford H (March 2016). "CRISPR: gene editing is just the beginning". Природа. 531 (7593): 156–9. Bibcode:2016Natur.531..156L. Дои:10.1038/531156a. PMID 26961639.
- ^ Koh H, Kwon S, Thomson M (26 August 2015). Current Technologies in Plant Molecular Breeding: A Guide Book of Plant Molecular Breeding for Researchers. Springer. п. 242. ISBN 978-94-017-9996-6.
- ^ "How to Make a GMO". Science in the News. 9 августа 2015 г.. Получено 29 апреля 2017.
- ^ Nicholl, Desmond S.T. (29 мая 2008 г.). An Introduction to Genetic Engineering. Издательство Кембриджского университета. п. 34. ISBN 978-1-139-47178-7.
- ^ Альбертс Б., Джонсон А., Льюис Дж. И др. (2002). "8". Isolating, Cloning, and Sequencing DNA (4-е изд.). Нью-Йорк: Наука Гарланд.
- ^ Kaufman RI, Nixon BT (July 1996). "Use of PCR to isolate genes encoding sigma54-dependent activators from diverse bacteria". Журнал бактериологии. 178 (13): 3967–70. Дои:10.1128/jb.178.13.3967-3970.1996. ЧВК 232662. PMID 8682806.
- ^ Liang J, Luo Y, Zhao H (2011). "Synthetic biology: putting synthesis into biology". Междисциплинарные обзоры Wiley: системная биология и медицина. 3 (1): 7–20. Дои:10.1002/wsbm.104. ЧВК 3057768. PMID 21064036.
- ^ "5. The Process of Genetic Modification". www.fao.org. Получено 29 апреля 2017.
- ^ Берг П., Мертц Дж. Э. (январь 2010 г.). «Личные размышления о происхождении и появлении технологии рекомбинантной ДНК». Генетика. 184 (1): 9–17. Дои:10.1534 / генетика.109.112144. ЧВК 2815933. PMID 20061565.
- ^ Chen I, Dubnau D (March 2004). "DNA uptake during bacterial transformation". Обзоры природы. Микробиология. 2 (3): 241–9. Дои:10.1038/nrmicro844. PMID 15083159. S2CID 205499369.
- ^ National Research Council (US) Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health (1 January 2004). Methods and Mechanisms for Genetic Manipulation of Plants, Animals, and Microorganisms. Национальная академия прессы (США).
- ^ Гельвин С.Б. (март 2003 г.). «Опосредованная Agrobacterium трансформация растений: биология, лежащая в основе инструмента« генной борьбы »». Обзоры микробиологии и молекулярной биологии. 67 (1): 16–37, содержание. Дои:10.1128/MMBR.67.1.16-37.2003. ЧВК 150518. PMID 12626681.
- ^ Head G, Hull RH, Tzotzos GT (2009). Genetically Modified Plants: Assessing Safety and Managing Risk. London: Academic Pr. п.244. ISBN 978-0-12-374106-6.
- ^ Tuomela M, Stanescu I, Krohn K (October 2005). "Validation overview of bio-analytical methods". Генная терапия. 12 Suppl 1 (S1): S131-8. Дои:10.1038/sj.gt.3302627. PMID 16231045.
- ^ Narayanaswamy, S. (1994). Культура растительных клеток и тканей. Тата Макгроу-Хилл Образование. стр. vi. ISBN 978-0-07-460277-5.
- ^ National Research Council (US) Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health (2004). Methods and Mechanisms for Genetic Manipulation of Plants, Animals, and Microorganisms. Национальная академия прессы (США).
- ^ Hohn B, Levy AA, Puchta H (April 2001). "Elimination of selection markers from transgenic plants". Текущее мнение в области биотехнологии. 12 (2): 139–43. Дои:10.1016/S0958-1669(00)00188-9. PMID 11287227.
- ^ Setlow JK (31 October 2002). Genetic Engineering: Principles and Methods. Springer Science & Business Media. п. 109. ISBN 978-0-306-47280-0.
- ^ Deepak S, Kottapalli K, Rakwal R, Oros G, Rangappa K, Iwahashi H, Masuo Y, Agrawal G (June 2007). "Real-Time PCR: Revolutionizing Detection and Expression Analysis of Genes". Текущая геномика. 8 (4): 234–51. Дои:10.2174/138920207781386960. ЧВК 2430684. PMID 18645596.
- ^ Grizot S, Smith J, Daboussi F, Prieto J, Redondo P, Merino N, Villate M, Thomas S, Lemaire L, Montoya G, Blanco FJ, Pâques F, Duchateau P (September 2009). "Efficient targeting of a SCID gene by an engineered single-chain homing endonuclease". Исследования нуклеиновых кислот. 37 (16): 5405–19. Дои:10.1093/nar/gkp548. ЧВК 2760784. PMID 19584299.
- ^ Gao H, Smith J, Yang M, Jones S, Djukanovic V, Nicholson MG, West A, Bidney D, Falco SC, Jantz D, Lyznik LA (January 2010). "Heritable targeted mutagenesis in maize using a designed endonuclease". Журнал растений. 61 (1): 176–87. Дои:10.1111/j.1365-313X.2009.04041.x. PMID 19811621.
- ^ Townsend JA, Wright DA, Winfrey RJ, Fu F, Maeder ML, Joung JK, Voytas DF (May 2009). "High-frequency modification of plant genes using engineered zinc-finger nucleases". Природа. 459 (7245): 442–5. Bibcode:2009Natur.459..442T. Дои:10.1038/nature07845. ЧВК 2743854. PMID 19404258.
- ^ Shukla VK, Doyon Y, Miller JC, DeKelver RC, Moehle EA, Worden SE, Mitchell JC, Arnold NL, Gopalan S, Meng X, Choi VM, Rock JM, Wu YY, Katibah GE, Zhifang G, McCaskill D, Simpson MA, Blakeslee B, Greenwalt SA, Butler HJ, Hinkley SJ, Zhang L, Rebar EJ, Gregory PD, Urnov FD (May 2009). "Precise genome modification in the crop species Zea mays using zinc-finger nucleases". Природа. 459 (7245): 437–41. Bibcode:2009Natur.459..437S. Дои:10.1038/nature07992. PMID 19404259. S2CID 4323298.
- ^ Christian M, Cermak T, Doyle EL, Schmidt C, Zhang F, Hummel A, Bogdanove AJ, Voytas DF (October 2010). "Targeting DNA double-strand breaks with TAL effector nucleases". Генетика. 186 (2): 757–61. Дои:10.1534/genetics.110.120717. ЧВК 2942870. PMID 20660643.
- ^ Li T, Huang S, Jiang WZ, Wright D, Spalding MH, Weeks DP, Yang B (January 2011). "TAL nucleases (TALNs): hybrid proteins composed of TAL effectors and FokI DNA-cleavage domain". Исследования нуклеиновых кислот. 39 (1): 359–72. Дои:10.1093/nar/gkq704. ЧВК 3017587. PMID 20699274.
- ^ Эсвелт К.М., Ван Х.Х. (2013). «Геномная инженерия для систем и синтетической биологии». Молекулярная системная биология. 9: 641. Дои:10.1038 / msb.2012.66. ЧВК 3564264. PMID 23340847.
- ^ Тан В.С., Карлсон Д.Ф., Уолтон М.В., Фаренкруг СК, Хакетт ПБ (2012). «Прецизионное редактирование геномов крупных животных». Успехи в генетике Том 80. Advances in Genetics. 80. С. 37–97. Дои:10.1016 / B978-0-12-404742-6.00002-8. ISBN 978-0-12-404742-6. ЧВК 3683964. PMID 23084873.
- ^ а б Malzahn A, Lowder L, Qi Y (24 April 2017). "Plant genome editing with TALEN and CRISPR". Cell & Bioscience. 7: 21. Дои:10.1186/s13578-017-0148-4. ЧВК 5404292. PMID 28451378.
- ^ Ekker SC (2008). "Zinc finger-based knockout punches for zebrafish genes". Данио. 5 (2): 121–3. Дои:10.1089/zeb.2008.9988. ЧВК 2849655. PMID 18554175.
- ^ Geurts AM, Cost GJ, Freyvert Y, Zeitler B, Miller JC, Choi VM, Jenkins SS, Wood A, Cui X, Meng X, Vincent A, Lam S, Michalkiewicz M, Schilling R, Foeckler J, Kalloway S, Weiler H, Ménoret S, Anegon I, Davis GD, Zhang L, Rebar EJ, Gregory PD, Urnov FD, Jacob HJ, Buelow R (July 2009). "Knockout rats via embryo microinjection of zinc-finger nucleases". Наука. 325 (5939): 433. Bibcode:2009Sci...325..433G. Дои:10.1126/science.1172447. ЧВК 2831805. PMID 19628861.
- ^ "Genetic Modification of Bacteria". Фонд Анненберга.
- ^ Panesar, Pamit et al. (2010) "Enzymes in Food Processing: Fundamentals and Potential Applications", Chapter 10, I K International Publishing House, ISBN 978-93-80026-33-6
- ^ "GM traits list". International Service for the Acquisition of Agri-Biotech Applications.
- ^ "ISAAA Brief 43-2011: Executive Summary". International Service for the Acquisition of Agri-Biotech Applications.
- ^ Connor S (2 November 2007). "The mouse that shook the world". Независимый.
- ^ Avise JC (2004). The hope, hype & reality of genetic engineering: remarkable stories from agriculture, industry, medicine, and the environment. Oxford University Press, США. п. 22. ISBN 978-0-19-516950-8.
- ^ "Engineering algae to make complex anti-cancer 'designer' drug". PhysOrg. 10 декабря 2012 г.. Получено 15 апреля 2013.
- ^ Roque AC, Lowe CR, Taipa MA (2004). "Antibodies and genetically engineered related molecules: production and purification". Прогресс биотехнологии. 20 (3): 639–54. Дои:10.1021/bp030070k. PMID 15176864. S2CID 23142893.
- ^ Rodriguez LL, Grubman MJ (November 2009). "Foot and mouth disease virus vaccines". Вакцина. 27 Suppl 4: D90-4. Дои:10.1016/j.vaccine.2009.08.039. PMID 19837296.
- ^ "Background: Cloned and Genetically Modified Animals". Center for Genetics and Society. 14 апреля 2005 г. Архивировано с оригинал 23 ноября 2016 г.. Получено 9 июля 2010.
- ^ "Knockout Mice". Nation Human Genome Research Institute. 2009 г.
- ^ "GM pigs best bet for organ transplant". Медицинские новости сегодня. 21 сентября 2003 г.
- ^ Fischer A, Hacein-Bey-Abina S, Cavazzana-Calvo M (June 2010). "20 years of gene therapy for SCID". Иммунология природы. 11 (6): 457–60. Дои:10.1038/ni0610-457. PMID 20485269. S2CID 11300348.
- ^ Ledford H (2011). «Клеточная терапия борется с лейкемией». Природа. Дои:10.1038 / новости.2011.472.
- ^ Brentjens RJ, Davila ML, Riviere I, Park J, Wang X, Cowell LG, et al. (Март 2013 г.). "CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia". Научная трансляционная медицина. 5 (177): 177ra38. Дои:10.1126/scitranslmed.3005930. ЧВК 3742551. PMID 23515080.
- ^ LeWitt PA, Rezai AR, Leehey MA, Ojemann SG, Flaherty AW, Eskandar EN, et al. (Апрель 2011 г.). «Генная терапия AAV2-GAD для запущенной болезни Паркинсона: двойное слепое рандомизированное исследование, контролируемое фиктивным хирургическим вмешательством». Ланцет. Неврология. 10 (4): 309–19. Дои:10.1016 / S1474-4422 (11) 70039-4. PMID 21419704. S2CID 37154043.
- ^ Галлахер, Джеймс. (2 November 2012) BBC News – Gene therapy: Glybera approved by European Commission. Bbc.co.uk. Проверено 15 декабря 2012 года.
- ^ Richards S. "Gene Therapy Arrives in Europe". Ученый. Получено 16 ноября 2012.
- ^ "Genetically Altered Skin Saves A Boy Dying of a Rare Disease". NPR.org. Получено 15 ноября 2017.
- ^ "1990 The Declaration of Inuyama". 5 August 2001. Archived from the original on 5 August 2001.CS1 maint: BOT: статус исходного URL-адреса неизвестен (связь)
- ^ Smith KR, Chan S, Harris J (October 2012). "Human germline genetic modification: scientific and bioethical perspectives". Archives of Medical Research. 43 (7): 491–513. Дои:10.1016/j.arcmed.2012.09.003. PMID 23072719.
- ^ Kolata G (23 April 2015). «Китайские ученые редактируют гены эмбрионов человека, вызывая опасения». Нью-Йорк Таймс. Получено 24 апреля 2015.
- ^ Liang P, Xu Y, Zhang X, Ding C, Huang R, Zhang Z, et al. (Май 2015 г.). "CRISPR / Cas9-опосредованное редактирование генов в трипроядерных зиготах человека". Protein & Cell. 6 (5): 363–372. Дои:10.1007 / s13238-015-0153-5. ЧВК 4417674. PMID 25894090.
- ^ Wade N (3 декабря 2015 г.). "Scientists Place Moratorium on Edits to Human Genome That Could Be Inherited". Нью-Йорк Таймс. Получено 3 декабря 2015.
- ^ Bergeson ER (1997). "The Ethics of Gene Therapy".
- ^ Hanna KE. "Genetic Enhancement". Национальный институт исследования генома человека.
- ^ Бегли С. (28 ноября 2018 г.). "Amid uproar, Chinese scientist defends creating gene-edited babies – STAT". СТАТ.
- ^ Li, Emily (31 July 2020). "Diagnostic Value of Spiral CT Chest Enhanced Scan". Journal of Clinical and Nursing Research.
- ^ Harmon A (26 November 2015). "Open Season Is Seen in Gene Editing of Animals". Нью-Йорк Таймс. ISSN 0362-4331. Получено 27 сентября 2017.
- ^ Praitis V, Maduro MF (2011). "Transgenesis in C. elegans". Методы клеточной биологии. 106: 161–85. Дои:10.1016/B978-0-12-544172-8.00006-2. ISBN 9780125441728. PMID 22118277.
- ^ "Rediscovering Biology – Online Textbook: Unit 13 Genetically Modified Organisms". www.learner.org. Получено 18 августа 2017.
- ^ а б c Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). "Studying Gene Expression and Function". Цитировать журнал требует
| журнал =(помощь) - ^ Park SJ, Cochran JR (25 September 2009). Protein Engineering and Design. CRC Press. ISBN 978-1-4200-7659-2.
- ^ Kurnaz IA (8 May 2015). Techniques in Genetic Engineering. CRC Press. ISBN 978-1-4822-6090-8.
- ^ "Applications of Genetic Engineering". Microbiologyprocedure. Архивировано из оригинал 14 июля 2011 г.. Получено 9 июля 2010.
- ^ "Biotech: What are transgenic organisms?". Easyscience. 2002. Архивировано с оригинал 27 мая 2010 г.. Получено 9 июля 2010.
- ^ Savage N (1 August 2007). "Making Gasoline from Bacteria: A biotech startup wants to coax fuels from engineered microbes". Обзор технологий. Получено 16 июля 2015.
- ^ Summers R (24 April 2013). "Bacteria churn out first ever petrol-like biofuel". Новый ученый. Получено 27 апреля 2013.
- ^ "Applications of Some Genetically Engineered Bacteria". Архивировано из оригинал 27 ноября 2010 г.. Получено 9 июля 2010.
- ^ Sanderson K (24 February 2012). "New Portable Kit Detects Arsenic in Wells". Новости химии и техники. Получено 23 января 2013.
- ^ Reece JB, Urry LA, Cain ML, Wasserman SA, Minorsky PV, Jackson RB (2011). Campbell Biology Ninth Edition. San Francisco: Pearson Benjamin Cummings. п.421. ISBN 978-0-321-55823-7.
- ^ «Новая вирусная батарея может питать автомобили и электронные устройства». Web.mit.edu. 2 апреля 2009 г.. Получено 17 июля 2010.
- ^ "Hidden Ingredient in New, Greener Battery: A Virus". Npr.org. Получено 17 июля 2010.
- ^ "Researchers Synchronize Blinking 'Genetic Clocks' – Genetically Engineered Bacteria That Keep Track of Time". ScienceDaily. 24 января 2010 г.
- ^ Suszkiw J (November 1999). "Tifton, Georgia: A Peanut Pest Showdown". Agricultural Research magazine. Получено 23 ноября 2008.
- ^ Magaña-Gómez JA, de la Barca AM (January 2009). "Risk assessment of genetically modified crops for nutrition and health". Отзывы о питании. 67 (1): 1–16. Дои:10.1111/j.1753-4887.2008.00130.x. PMID 19146501.
- ^ Islam A (2008). "Fungus Resistant Transgenic Plants: Strategies, Progress and Lessons Learnt". Plant Tissue Culture and Biotechnology. 16 (2): 117–38. Дои:10.3329/ptcb.v16i2.1113.
- ^ "Disease resistant crops". ГМО Компас. Архивировано из оригинал on 3 June 2010.
- ^ Demont M, Tollens E (2004). "First impact of biotechnology in the EU: Bt maize adoption in Spain". Анналы прикладной биологии. 145 (2): 197–207. Дои:10.1111/j.1744-7348.2004.tb00376.x.
- ^ Chivian E, Bernstein A (2008). Sustaining Life. Oxford University Press, Inc. ISBN 978-0-19-517509-7.
- ^ а б Whitman DB (2000). "Genetically Modified Foods: Harmful or Helpful?".
- ^ Pollack A (19 November 2015). "Genetically Engineered Salmon Approved for Consumption". Нью-Йорк Таймс. Получено 21 апреля 2016.
- ^ Rapeseed (canola) has been genetically engineered to modify its oil content with a gene encoding a "12:0 thioesterase" (TE) enzyme from the California bay plant (Зонтик калифорнийский ) to increase medium length fatty acids, see: Geo-pie.cornell.edu В архиве 5 июля 2009 г. Wayback Machine
- ^ Bomgardner MM (2012). "Replacing Trans Fat: New crops from Dow Chemical and DuPont target food makers looking for stable, heart-healthy oils". Новости химии и техники. 90 (11): 30–32. Дои:10.1021/cen-09011-bus1.
- ^ Kramer MG, Redenbaugh K (1 January 1994). "Commercialization of a tomato with an antisense polygalacturonase gene: The FLAVR SAVR™ tomato story". Euphytica. 79 (3): 293–97. Дои:10.1007/BF00022530. ISSN 0014-2336. S2CID 45071333.
- ^ Marvier M (2008). "Pharmaceutical crops in California, benefits and risks. A review" (PDF). Агрономия в интересах устойчивого развития. 28 (1): 1–9. Дои:10.1051/agro:2007050. S2CID 29538486.
- ^ "FDA Approves First Human Biologic Produced by GE Animals". Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
- ^ Rebêlo P (15 July 2004). "GM cow milk 'could provide treatment for blood disease'". SciDev.
- ^ Angulo E, Cooke B (December 2002). "First synthesize new viruses then regulate their release? The case of the wild rabbit". Молекулярная экология. 11 (12): 2703–9. Дои:10.1046/j.1365-294X.2002.01635.x. HDL:10261/45541. PMID 12453252. S2CID 23916432.
- ^ Adams JM, Piovesan G, Strauss S, Brown S (2 August 2002). "The Case for Genetic Engineering of Native and Landscape Trees against Introduced Pests and Diseases". Биология сохранения. 16 (4): 874–79. Дои:10.1046/j.1523-1739.2002.00523.x.
- ^ Thomas MA, Roemer GW, Donlan CJ, Dickson BG, Matocq M, Malaney J (September 2013). "Ecology: Gene tweaking for conservation". Природа. 501 (7468): 485–6. Дои:10.1038/501485a. PMID 24073449.
- ^ Pasko JM (4 March 2007). "Bio-artists bridge gap between arts, sciences: Use of living organisms is attracting attention and controversy". msnbc.
- ^ Jackson J (6 December 2005). "Genetically Modified Bacteria Produce Living Photographs". National Geographic News.
- ^ Phys.Org website. 4 апреля 2005 г. "Plant gene replacement results in the world's only blue rose".
- ^ Katsumoto Y, Fukuchi-Mizutani M, Fukui Y, Brugliera F, Holton TA, Karan M, Nakamura N, Yonekura-Sakakibara K, Togami J, Pigeaire A, Tao GQ, Nehra NS, Lu CY, Dyson BK, Tsuda S, Ashikari T, Kusumi T, Mason JG, Tanaka Y (November 2007). "Engineering of the rose flavonoid biosynthetic pathway successfully generated blue-hued flowers accumulating delphinidin". Plant & Cell Physiology. 48 (11): 1589–600. CiteSeerX 10.1.1.319.8365. Дои:10.1093 / pcp / pcm131. PMID 17925311.
- ^ Published PCT Application WO2000049150 "Chimeric Gene Constructs for Generation of Fluorescent Transgenic Ornamental Fish." Национальный университет Сингапура [1]
- ^ Stewart CN (April 2006). "Go with the glow: fluorescent proteins to light transgenic organisms" (PDF). Тенденции в биотехнологии. 24 (4): 155–62. Дои:10.1016/j.tibtech.2006.02.002. PMID 16488034.
- ^ Berg P, Baltimore D, Boyer HW, Cohen SN, Davis RW, Hogness DS, Nathans D, Roblin R, Watson JD, Weissman S, Zinder ND (July 1974). "Letter: Potential biohazards of recombinant DNA molecules" (PDF). Наука. 185 (4148): 303. Bibcode:1974Sci...185..303B. Дои:10.1126/science.185.4148.303. ЧВК 388511. PMID 4600381.
- ^ McHughen A, Smyth S (January 2008). "US regulatory system for genetically modified [genetically modified organism (GMO), rDNA or transgenic] crop cultivars". Журнал биотехнологии растений. 6 (1): 2–12. Дои:10.1111/j.1467-7652.2007.00300.x. PMID 17956539.
- ^ а б U.S. Office of Science and Technology Policy (June 1986). "Coordinated framework for regulation of biotechnology; announcement of policy; notice for public comment" (PDF). Федеральный регистр. 51 (123): 23302–50. PMID 11655807. Архивировано из оригинал (PDF) 16 мая 2011 г.
- ^ Redick, T.P. (2007). "The Cartagena Protocol on biosafety: Precautionary priority in biotech crop approvals and containment of commodities shipments, 2007". Колорадский журнал международного экологического права и политики. 18: 51–116.
- ^ «О протоколе». The Biosafety Clearing-House (BCH). 29 мая 2012 г.
- ^ "AgBioForum 13(3): Implications of Import Regulations and Information Requirements under the Cartagena Protocol on Biosafety for GM Commodities in Kenya". 28 октября 2010 г.
- ^ "Restrictions on Genetically Modified Organisms". Библиотека Конгресса. 9 июня 2015 г.. Получено 24 февраля 2016.
- ^ Bashshur R (February 2013). "FDA and Regulation of GMOs". Американская ассоциация адвокатов. Получено 24 февраля 2016.
- ^ Sifferlin A (3 October 2015). "Over Half of E.U. Countries Are Opting Out of GMOs". Время.
- ^ Lynch D, Vogel D (5 April 2001). "The Regulation of GMOs in Europe and the United States: A Case-Study of Contemporary European Regulatory Politics". Совет по международным отношениям. Архивировано из оригинал on 29 September 2016. Получено 24 февраля 2016.
- ^ "Restrictions on Genetically Modified Organisms - Law Library of Congress". 22 января 2017.
- ^ Emily Marden, Risk and Regulation: U.S. Regulatory Policy on Genetically Modified Food and Agriculture, 44 B.C.L. Rev. 733 (2003)[2]
- ^ а б Davison J (2010). "GM plants: Science, politics and EC regulations". Растениеводство. 178 (2): 94–98. Дои:10.1016/j.plantsci.2009.12.005.
- ^ а б GMO Compass: The European Regulatory System. В архиве 14 августа 2012 г. Wayback Machine Проверено 28 июля 2012 года.
- ^ Government of Canada, Canadian Food Inspection Agency (20 March 2015). "Information for the general public". www.inspection.gc.ca.
- ^ Forsberg, Cecil W. (23 April 2013). "Генномодифицированные продукты". Канадская энциклопедия. Получено 4 октября 2017.
- ^ Evans, Brent and Lupescu, Mihai (15 July 2012) Canada – Agricultural Biotechnology Annual – 2012 В архиве 15 декабря 2013 г. Wayback Machine GAIN (Global Agricultural Information Network) report CA12029, United States Department of Agriculture, Foreifn Agricultural Service, Retrieved 5 November 2012
- ^ McHugen A (14 September 2000). "Chapter 1: Hors-d'oeuvres and entrees/What is genetic modification? What are GMOs?". Pandora's Picnic Basket. Издательство Оксфордского университета. ISBN 978-0-19-850674-4.
- ^ а б "Editorial: Transgenic harvest". Природа. 467 (7316): 633–634. 2010. Bibcode:2010Natur.467R.633.. Дои:10.1038/467633b. PMID 20930796.
- ^ "AgBioForum 5(4): Agricultural Biotechnology Development and Policy in China". 5 сентября 2003 г.
- ^ "TNAU Agritech Portal: Bio Technology".
- ^ а б c "BASF presentation" (PDF). Архивировано из оригинал (PDF) 28 сентября 2011 г.
- ^ Agriculture – Department of Primary Industries В архиве 29 марта 2011 г. Wayback Machine
- ^ а б "Welcome to the Office of the Gene Technology Regulator Website". Управление регулятора генных технологий. Получено 25 марта 2011.
- ^ "Regulation (EC) No 1829/2003 of the European Parliament and of the Council of 22 September 2003 On Genetically Modified Food And Feed" (PDF). Официальный журнал Европейского Союза. The European Parliament and the Council of the European Union. 2003. Архивировано с оригинал (PDF) 20 января 2014 г.
The labeling should include objective information to the effect that a food or feed consists of, contains or is produced from GMOs. Clear labeling, irrespective of the detectability of DNA or protein resulting from the genetic modification in the final product, meets the demands expressed in numerous surveys by a large majority of consumers, facilitates informed choice and precludes potential misleading of consumers as regards methods of manufacture or production.
- ^ "Regulation (EC) No 1830/2003 of the European Parliament and of the Council of 22 September 2003 concerning the traceability and labeling of genetically modified organisms and the traceability of food and feed products produced from genetically modified organisms and amending Directive 2001/18/EC". Official Journal L 268. The European Parliament and the Council of the European Union. 2003. pp. 24–28.
(3) Traceability requirements for GMOs should facilitate both the withdrawal of products where unforeseen adverse effects on human health, animal health or the environment, including ecosystems, are established, and the targeting of monitoring to examine potential effects on, in particular, the environment. Traceability should also facilitate the implementation of risk management measures in accordance with the precautionary principle. (4) Traceability requirements for food and feed produced from GMOs should be established to facilitate accurate labeling of such products.
- ^ "Report 2 of the Council on Science and Public Health: Labeling of Bioengineered Foods" (PDF). Американская медицинская ассоциация. 2012. Архивировано с оригинал (PDF) 7 сентября 2012 г.
- ^ American Association for the Advancement of Science (AAAS), Board of Directors (2012). Statement by the AAAS Board of Directors On Labeling of Genetically Modified Foods, и связанные Press release: Legally Mandating GM Food Labels Could Mislead and Falsely Alarm Consumers В архиве 4 ноября 2013 г. Wayback Machine
- ^ Hallenbeck T (27 April 2014). "How GMO labeling came to pass in Vermont". Burlington Free Press. Получено 28 мая 2014.
- ^ "The Regulation of Genetically Modified Foods". Архивировано из оригинал 10 июня 2017 г.. Получено 5 ноября 2012.
- ^ Sheldon IM (1 March 2002). "Regulation of biotechnology: will we ever 'freely' trade GMOs?". Европейский обзор экономики сельского хозяйства. 29 (1): 155–76. CiteSeerX 10.1.1.596.7670. Дои:10.1093/erae/29.1.155. ISSN 0165-1587.
- ^ Dabrock P (December 2009). "Playing God? Synthetic biology as a theological and ethical challenge". Systems and Synthetic Biology. 3 (1–4): 47–54. Дои:10.1007/s11693-009-9028-5. ЧВК 2759421. PMID 19816799.
- ^ Brown C (October 2000). "Patenting life: genetically altered mice an invention, court declares". CMAJ. 163 (7): 867–8. ЧВК 80518. PMID 11033718.
- ^ Zhou W (10 August 2015). "The Patent Landscape of Genetically Modified Organisms". Science in the News. Получено 5 мая 2017.
- ^ Puckett L (20 April 2016). "Why The New GMO Food-Labeling Law Is So Controversial". Huffington Post. Получено 5 мая 2017.
- ^ Miller H (12 April 2016). "GMO food labels are meaningless". Лос-Анджелес Таймс. ISSN 0458-3035. Получено 5 мая 2017.
- ^ Savage S. "Who Controls The Food Supply?". Forbes. Получено 5 мая 2017.
- ^ Knight AJ (14 April 2016). Science, Risk, and Policy. Рутледж. п. 156. ISBN 978-1-317-28081-1.
- ^ Hakim D (29 October 2016). "Doubts About the Promised Bounty of Genetically Modified Crops". Нью-Йорк Таймс. ISSN 0362-4331. Получено 5 мая 2017.
- ^ Areal FJ, Riesgo L, Rodríguez-Cerezo E (1 February 2013). "Economic and agronomic impact of commercialized GM crops: a meta-analysis". Журнал сельскохозяйственных наук. 151 (1): 7–33. Дои:10.1017/S0021859612000111.
- ^ Finger R, El Benni N, Kaphengst T, Evans C, Herbert S, Lehmann B, Morse S, Stupak N (10 May 2011). "A Meta Analysis on Farm-Level Costs and Benefits of GM Crops" (PDF). Устойчивость. 3 (5): 743–62. Дои:10.3390 / su3050743.
- ^ Klümper W, Qaim M (3 ноября 2014 г.). «Мета-анализ воздействия генетически модифицированных культур». PLOS ONE. 9 (11): e111629. Bibcode:2014PLoSO ... 9k1629K. Дои:10.1371 / journal.pone.0111629. ЧВК 4218791. PMID 25365303.
- ^ Цю Дж (2013). «Генетически модифицированные культуры передают преимущества сорнякам». Природа. Дои:10.1038 / природа.2013.13517. S2CID 87415065.
- ^ а б «ГМО и окружающая среда». www.fao.org. Получено 7 мая 2017.
- ^ Dively GP, Venugopal PD, Finkenbinder C (30 декабря 2016 г.). «Выработанная в полевых условиях устойчивость кукурузных червей к Cry-белкам, выраженная трансгенной сладкой кукурузой». PLOS ONE. 11 (12): e0169115. Bibcode:2016PLoSO..1169115D. Дои:10.1371 / journal.pone.0169115. ЧВК 5201267. PMID 28036388.
- ^ Цю, Джейн (13 мая 2010 г.). «Использование ГМ-культур создает серьезную проблему для мелких вредителей». Новости природы. CiteSeerX 10.1.1.464.7885. Дои:10.1038 / новости.2010.242.
- ^ Гилберт Н. (май 2013 г.). «Тематические исследования: пристальный взгляд на ГМ-культуры». Природа. 497 (7447): 24–6. Bibcode:2013Натура 497 ... 24G. Дои:10.1038 / 497024a. PMID 23636378.
- ^ "Безопасна ли ГМО рыба для окружающей среды? | Накапливаются сбои | Изучите науку в Scitable". www.nature.com. Получено 7 мая 2017.
- ^ «Вопросы и ответы: генетически модифицированные продукты питания». Всемирная организация здоровья. Получено 7 мая 2017.
- ^ Николя А., Манзо А., Веронези Ф., Роселлини Д. (март 2014 г.). «Обзор генно-инженерных исследований безопасности сельскохозяйственных культур за последние 10 лет». Критические обзоры в биотехнологии. 34 (1): 77–88. Дои:10.3109/07388551.2013.823595. PMID 24041244. S2CID 9836802.
Мы проанализировали научную литературу по безопасности ГМ культур за последние 10 лет, в которой нашли отражение научный консенсус, сформировавшийся с тех пор, как ГМ растения стали широко культивироваться во всем мире, и мы можем сделать вывод, что проведенные до сих пор научные исследования не выявили какой-либо значительной опасности, напрямую связанной с использование ГМ-культур. Литература о биоразнообразии и потреблении генетически модифицированных продуктов питания / кормов иногда приводила к оживленным дебатам относительно пригодности экспериментальных схем, выбора статистических методов или доступности данных для общественности. Такие дебаты, даже если они положительные и являются частью естественного процесса обзора со стороны научного сообщества, часто искажаются средствами массовой информации и часто используются политически и неуместно в кампаниях против ГМ.
- ^ «Состояние продовольствия и сельского хозяйства 2003–2004 гг. Сельскохозяйственная биотехнология: удовлетворение потребностей бедных. Воздействие трансгенных культур на здоровье и окружающую среду». Продовольственная и сельскохозяйственная организация Объединенных Наций. Получено 8 февраля 2016.
Доступные в настоящее время трансгенные культуры и продукты, полученные из них, признаны безопасными для употребления в пищу, а методы, используемые для проверки их безопасности, считаются подходящими. Эти выводы представляют собой консенсус научных данных, исследованных ICSU (2003), и согласуются с взглядами Всемирной организации здравоохранения (ВОЗ, 2002). Эти продукты питания были оценены на предмет повышенного риска для здоровья человека несколькими национальными регулирующими органами (в частности, Аргентиной, Бразилией, Канадой, Китаем, Соединенным Королевством и США) с использованием их национальных процедур безопасности пищевых продуктов (ICSU). На сегодняшний день не было обнаружено никаких поддающихся проверке нежелательных токсических или вредных для питания эффектов, возникающих в результате употребления продуктов питания, полученных из генетически модифицированных культур, где-либо в мире (Группа экспертов GM Science Review). Многие миллионы людей употребляли продукты, полученные из ГМ-растений, в основном кукурузу, сою и масличный рапс, без каких-либо наблюдаемых побочных эффектов (ICSU).
- ^ Рональд П. (май 2011 г.). «Генетика растений, устойчивое сельское хозяйство и глобальная продовольственная безопасность». Генетика. 188 (1): 11–20. Дои:10.1534 / генетика.111.128553. ЧВК 3120150. PMID 21546547.
Существует широкий научный консенсус в отношении того, что в настоящее время на рынке есть генно-инженерные культуры, которые можно употреблять в пищу. После 14 лет культивирования и посевов общей площадью 2 миллиарда акров, коммерциализация генетически модифицированных культур не привела к неблагоприятным последствиям для здоровья или окружающей среды (Совет по сельскому хозяйству и природным ресурсам, Комитет по экологическим воздействиям, связанным с коммерциализацией трансгенных растений, Национальные исследования Совет и Отдел по исследованиям Земли и жизни 2002 г.). И Национальный исследовательский совет США, и Объединенный исследовательский центр (научно-техническая исследовательская лаборатория Европейского союза и неотъемлемая часть Европейской комиссии) пришли к выводу, что существует обширная база знаний, которая адекватно решает проблему безопасности пищевых продуктов для генетически модифицированных культур. (Комитет по выявлению и оценке непреднамеренного воздействия генетически модифицированных продуктов на здоровье человека и Национальный исследовательский совет, 2004 год; Объединенный исследовательский центр Европейской комиссии, 2008 год). В этих и других недавних отчетах делается вывод о том, что процессы генной инженерии и традиционной селекции ничем не отличаются с точки зрения непредвиденных последствий для здоровья человека и окружающей среды (Генеральный директорат Европейской комиссии по исследованиям и инновациям, 2010 г.).
- ^ Но см. Также:Доминго Дж. Л., Джине Бордонаба Дж. (Май 2011 г.). «Обзор литературы по оценке безопасности генетически модифицированных растений». Environment International. 37 (4): 734–42. Дои:10.1016 / j.envint.2011.01.003. PMID 21296423.
Несмотря на это, количество исследований, специально посвященных оценке безопасности ГМ-растений, все еще ограничено. Однако важно отметить, что впервые определенное равновесие в количестве исследовательских групп, предполагающих на основе своих исследований, что ряд разновидностей ГМ-продуктов (в основном кукуруза и соя) столь же безопасны и питательны. как соответствующее обычное растение, не являющееся генетически модифицированным, и те, которые вызывают серьезные опасения. Более того, стоит упомянуть, что большинство исследований, демонстрирующих, что ГМ-продукты столь же питательны и безопасны, как и продукты, полученные путем традиционного разведения, были выполнены биотехнологическими компаниями или партнерами, которые также несут ответственность за коммерциализацию этих ГМ-растений. Во всяком случае, это заметный прогресс по сравнению с отсутствием исследований, опубликованных в последние годы в научных журналах этих компаний.
Крымский С (2015). «Иллюзорный консенсус в оценке здоровья ГМО» (PDF). Наука, технологии и человеческие ценности. 40 (6): 883–914. Дои:10.1177/0162243915598381. S2CID 40855100. Архивировано из оригинал (PDF) 7 февраля 2016 г.. Получено 30 октября 2016.Я начал эту статью с отзывов уважаемых ученых о том, что буквально нет научных споров о влиянии ГМО на здоровье. Мое исследование научной литературы рассказывает другую историю.
И контраст:Панчин А.Ю., Тужиков А.И. (март 2017). «Опубликованные исследования ГМО не обнаруживают никаких доказательств вреда при корректировке с учетом множественных сравнений». Критические обзоры в биотехнологии. 37 (2): 213–217. Дои:10.3109/07388551.2015.1130684. PMID 26767435. S2CID 11786594.Здесь мы показываем, что ряд статей, некоторые из которых сильно и негативно повлияли на общественное мнение о ГМ-культурах и даже спровоцировали политические действия, такие как эмбарго на ГМО, имеют общие недостатки в статистической оценке данных. Объяснив эти недостатки, мы пришли к выводу, что данные, представленные в этих статьях, не предоставляют каких-либо существенных доказательств вреда ГМО. Представленные статьи о возможном вреде ГМО получили большое внимание общественности. Однако, несмотря на их заявления, они фактически ослабляют доказательства вреда и отсутствия существенной эквивалентности изученных ГМО. Мы подчеркиваем, что, поскольку за последние 10 лет было опубликовано более 1783 статей о ГМО, ожидается, что некоторые из них должны были сообщить о нежелательных различиях между ГМО и обычными культурами, даже если в действительности таких различий не существует.
иЯн Ю.Т., Чен Б. (апрель 2016 г.). «Управление ГМО в США: наука, право и общественное здравоохранение». Журнал продовольственной науки и сельского хозяйства. 96 (6): 1851–5. Дои:10.1002 / jsfa.7523. PMID 26536836.Поэтому неудивительно, что попытки потребовать маркировки и запретить ГМО стали растущей политической проблемой в США. (цитируется Доминго и Бордонаба, 2011 г.). В целом, широкий научный консенсус придерживается мнения, что продаваемые в настоящее время ГМО продукты не представляют большего риска, чем обычные продукты питания ... Крупные национальные и международные научные и медицинские ассоциации заявили, что никаких неблагоприятных последствий для здоровья человека, связанных с ГМО-продуктами питания, не было зарегистрировано или подтверждено коллегами изучил литературу на сегодняшний день. Несмотря на различные опасения, сегодня Американская ассоциация развития науки, Всемирная организация здравоохранения и многие независимые международные научные организации согласны с тем, что ГМО так же безопасны, как и другие продукты питания. По сравнению с традиционными методами селекции генная инженерия намного точнее и в большинстве случаев с меньшей вероятностью приведет к неожиданному результату.
- ^ «Заявление совета директоров AAAS по маркировке генетически модифицированных продуктов питания» (PDF). Американская ассоциация развития науки. 20 октября 2012 г.. Получено 8 февраля 2016.
ЕС, например, инвестировал более 300 миллионов евро в исследования биобезопасности ГМО. В ее недавнем отчете говорится: «Главный вывод, который можно сделать из усилий более чем 130 исследовательских проектов, охватывающих период более 25 лет исследований и с участием более 500 независимых исследовательских групп, заключается в том, что биотехнология, и в частности ГМО, сами по себе не более опасны, чем, например, традиционные технологии селекции растений ». Всемирная организация здравоохранения, Американская медицинская ассоциация, Национальная академия наук США, Британское королевское общество и все другие уважаемые организации, изучавшие доказательства, пришли к такому же выводу: употребление продуктов, содержащих ингредиенты, полученные из ГМ-культур, не опаснее. чем употребление тех же продуктов, содержащих ингредиенты из сельскохозяйственных культур, модифицированных обычными методами улучшения растений.
Pinholster G (25 октября 2012 г.). «Совет директоров AAAS: наличие обязательной маркировки генетически модифицированных пищевых продуктов может« ввести потребителей в заблуждение и вызвать ложную тревогу »"". Американская ассоциация развития науки. Получено 8 февраля 2016. - ^ Европейская комиссия. Генеральный директорат по исследованиям (2010 г.). Десятилетие финансируемых ЕС исследований ГМО (2001–2010 гг.) (PDF). Генеральный директорат по исследованиям и инновациям. Биотехнологии, сельское хозяйство, продукты питания. Европейская комиссия, Европейский союз. Дои:10.2777/97784. ISBN 978-92-79-16344-9. Получено 8 февраля 2016.
- ^ «Отчет AMA по генетически модифицированным культурам и продуктам питания (онлайн-резюме)». Американская медицинская ассоциация. Январь 2001. Получено 19 марта 2016.
В отчете, выпущенном научным советом Американской медицинской ассоциации (AMA), говорится, что при использовании трансгенных культур и генетически модифицированных пищевых продуктов не было обнаружено никаких долгосрочных последствий для здоровья, и что эти продукты практически эквивалентны своим традиционным аналогам. (из онлайн-резюме, подготовленного ISAAA )"" Культуры и продукты питания, полученные с использованием методов рекомбинантной ДНК, доступны менее 10 лет, и на сегодняшний день не было обнаружено никаких долгосрочных эффектов. Эти продукты практически эквивалентны своим традиционным аналогам. (из исходного отчета AMA: [3] )
«Отчет 2 Совета по науке и общественному здравоохранению (A-12): Маркировка биоинженерных пищевых продуктов» (PDF). Американская медицинская ассоциация. 2012. Архивировано 7 сентября 2012 года.. Получено 19 марта 2016.Биоинженерные продукты потребляются в течение почти 20 лет, и за это время никаких явных последствий для здоровья человека не сообщалось и / или не подтверждалось в рецензируемой литературе.
CS1 maint: BOT: статус исходного URL-адреса неизвестен (связь) - ^ «Ограничения на генетически модифицированные организмы: США. Общественное и научное мнение». Библиотека Конгресса. 9 июня 2015 г.. Получено 8 февраля 2016.
Несколько научных организаций в США опубликовали исследования или заявления относительно безопасности ГМО, указывающие на отсутствие доказательств того, что ГМО представляют уникальные риски для безопасности по сравнению с продуктами традиционного разведения. В их число входят Национальный исследовательский совет, Американская ассоциация развития науки и Американская медицинская ассоциация. Группы в США, выступающие против ГМО, включают некоторые экологические организации, организации органического земледелия и организации потребителей. Значительное количество ученых-юристов критиковали подход США к регулированию ГМО.
- ^ Национальные академии наук, инженерия; Отдел изучения земной жизни; Совет по сельскохозяйственным природным ресурсам; Комитет по генетически модифицированным культурам: прошлый опыт и перспективы на будущее (2016). Генно-инженерные культуры: опыт и перспективы. Национальные академии наук, инженерии и медицины (США). п. 149. Дои:10.17226/23395. ISBN 978-0-309-43738-7. PMID 28230933. Получено 19 мая 2016.
Общие данные о предполагаемом неблагоприятном воздействии на здоровье человека продуктов питания, полученных из генетически модифицированных культур: На основе подробного изучения сравнений коммерчески выпускаемых в настоящее время ГЭ продуктов с продуктами, не являющихся ГМ, в композиционном анализе, тестах на острую и хроническую токсичность животных, долгосрочных данных о здоровье скота, получающих ГМ продукты, и эпидемиологических данных по людям, комитет не обнаружил различий которые подразумевают более высокий риск для здоровья человека от продуктов GE, чем их аналоги, не являющиеся генетически модифицированными.
- ^ «Часто задаваемые вопросы о генетически модифицированных продуктах». Всемирная организация здоровья. Получено 8 февраля 2016.
Разные ГМ организмы включают разные гены, встроенные по-разному. Это означает, что отдельные ГМ-продукты и их безопасность должны оцениваться в индивидуальном порядке, и что невозможно сделать общие заявления о безопасности всех ГМ-продуктов. ГМ-продукты, доступные в настоящее время на международном рынке, прошли оценку безопасности и вряд ли представляют опасность для здоровья человека. Кроме того, не было показано никакого воздействия на здоровье человека в результате потребления таких продуктов населением в странах, где они были одобрены. Непрерывное применение оценок безопасности, основанных на принципах Codex Alimentarius, и, при необходимости, адекватный пострыночный мониторинг, должны стать основой для обеспечения безопасности ГМ-продуктов.
- ^ Haslberger AG (июль 2003 г.). «Руководящие принципы Кодекса для ГМ-продуктов включают анализ непредвиденных последствий». Природа Биотехнологии. 21 (7): 739–41. Дои:10.1038 / nbt0703-739. PMID 12833088. S2CID 2533628.
Эти принципы требуют проведения предмаркетной оценки в каждом конкретном случае, которая включает оценку как прямых, так и непредвиденных эффектов.
- ^ Некоторые медицинские организации, в том числе Британская медицинская ассоциация, выступаем за дальнейшую осторожность, основанную на Принцип предосторожности:«Генетически модифицированные продукты и здоровье: второе промежуточное заявление» (PDF). Британская медицинская ассоциация. Март 2004 г.. Получено 21 марта 2016.
На наш взгляд, вероятность того, что ГМ-продукты будут оказывать вредное воздействие на здоровье, очень мала, и многие из выраженных опасений в равной степени относятся к продуктам, полученным традиционным способом. Однако пока нельзя полностью отбросить опасения по поводу безопасности на основе имеющейся в настоящее время информации. Пытаясь оптимизировать баланс между преимуществами и рисками, разумно проявить осторожность и, прежде всего, извлечь уроки из накопленных знаний и опыта. Любая новая технология, такая как генетическая модификация, должна быть изучена на предмет возможных преимуществ и рисков для здоровья человека и окружающей среды. Как и в случае со всеми новыми продуктами питания, оценка безопасности в отношении ГМО-продуктов должна проводиться в каждом конкретном случае. Члены жюри проекта GM были проинформированы о различных аспектах генетической модификации разнообразной группой признанных экспертов в соответствующих областях. Жюри ГМ пришло к выводу, что продажу доступных в настоящее время ГМ-продуктов следует прекратить, а мораторий на коммерческое выращивание ГМ-культур должен быть сохранен. Эти выводы были основаны на принципе предосторожности и отсутствии доказательств какой-либо пользы. Жюри выразило озабоченность по поводу воздействия ГМ-культур на сельское хозяйство, окружающую среду, безопасность пищевых продуктов и других потенциальных последствий для здоровья. Обзор Королевского общества (2002) пришел к выводу, что риски для здоровья человека, связанные с использованием конкретных вирусных последовательностей ДНК в ГМ-растениях, незначительны, и, призывая к осторожности при внесении потенциальных аллергенов в пищевые культуры, подчеркнул отсутствие доказательств того, имеющиеся в продаже генетически модифицированные продукты вызывают клинические аллергические проявления. BMA разделяет мнение о том, что нет убедительных доказательств того, что ГМ-продукты небезопасны, но мы поддерживаем призыв к дальнейшим исследованиям и надзору, чтобы предоставить убедительные доказательства безопасности и пользы.
- ^ Funk C, Rainie L (29 января 2015 г.). «Взгляды общественности и ученых на науку и общество». Pew Research Center. Получено 24 февраля 2016.
Наибольшие различия между общественностью и учеными AAAS заключаются в убеждениях о безопасности употребления генетически модифицированных (ГМ) продуктов. Почти девять из десяти (88%) ученых считают, что употребление ГМО-продуктов в целом безопасно, по сравнению с 37% широкой публики, разница в 51 процентный пункт.
- ^ Маррис С. (июль 2001 г.). «Общественное мнение о ГМО: развенчание мифов. Заинтересованные стороны в дебатах о ГМО часто называют общественное мнение иррациональным. Но действительно ли они понимают общественность?». Отчеты EMBO. 2 (7): 545–8. Дои:10.1093 / embo-reports / kve142. ЧВК 1083956. PMID 11463731.
- ^ Заключительный отчет исследовательского проекта PABE (декабрь 2001 г.). «Общественное мнение о сельскохозяйственных биотехнологиях в Европе». Комиссия Европейских Сообществ. Получено 24 февраля 2016.
- ^ Скотт С.Е., Инбар Ю., Розин П. (май 2016 г.). «Доказательства абсолютной моральной оппозиции генетически модифицированной пище в Соединенных Штатах». Перспективы психологической науки. 11 (3): 315–324. Дои:10.1177/1745691615621275. PMID 27217243. S2CID 261060.
- ^ а б "Генная инженерия". Энциклопедия научной фантастики. 15 мая 2017. Получено 19 июля 2018.
- ^ Кобольдт Д. (29 августа 2017 г.). "Наука о научной фантастике: как научная фантастика предсказывала будущее генетики". Внешние места. В архиве из оригинала 19 июля 2018 г.. Получено 19 июля 2018.
- ^ Морага Р. (ноябрь 2009 г.). «Современная генетика в мире художественной литературы». Журнал Clarkesworld (38). В архиве из оригинала от 19 июля 2018 г.
- ^ а б c Кларк М. «Генетические темы в игровых фильмах: генетика встречается с Голливудом». Wellcome Trust. Архивировано из оригинал 18 мая 2012 г.. Получено 19 июля 2018.
дальнейшее чтение
- Британская медицинская ассоциация (1999). Влияние генетической модификации на сельское хозяйство, продукты питания и здоровье. BMJ Книги. ISBN 0-7279-1431-6.
- Доннеллан, Крейг (2004). Генетическая модификация (проблемы). Независимые образовательные издательства. ISBN 1-86168-288-3.
- Морган С (1 января 2009 г.). Суперпродукты: генетическая модификация продуктов питания. Библиотека Хайнемана. ISBN 978-1-4329-2455-3.
- Смайли, Софи (2005). Генетическая модификация: учебное пособие (изучение проблем). Независимые образовательные издательства. ISBN 1-86168-307-3.
- Уотсон Дж. Д. (2007). Рекомбинантная ДНК: гены и геномы: краткий курс. Сан-Франциско: W.H. Фримен. ISBN 978-0-7167-2866-5.
- Уивер С, Майкл М (2003). «Аннотированная библиография научных публикаций о рисках, связанных с генетической модификацией». Веллингтон, Новая Зеландия: Университет Виктории. Цитировать журнал требует
| журнал =(помощь) - Заид А., Хьюз Х.Г., Порседду Э., Николас Ф. (2001). Глоссарий биотехнологии для производства продовольствия и ведения сельского хозяйства - пересмотренное и дополненное издание Глоссария биотехнологии и генной инженерии. Рим, Италия: ФАО. ISBN 92-5-104683-2.
внешняя ссылка
| Библиотечные ресурсы о Генная инженерия |


