Наносенсор - Nanosensor
| Часть серия статей о |
| Нанотехнологии |
|---|
| Влияние и Приложения |
| Наноматериалы |
| Молекулярная самосборка |
| Наноэлектроника |
| Нанометрология |
| Молекулярная нанотехнология |
|
Наносенсоры представляют собой наноразмерные устройства, которые измеряют физические величины и преобразуют их в сигналы, которые могут быть обнаружены и проанализированы. Сегодня предлагается несколько способов изготовления наносенсоров; к ним относятся литография сверху вниз, сборка снизу вверх, и молекулярная самосборка.[1] На рынке и в разработке находятся различные типы наносенсоров для различных приложений, в первую очередь в оборонной, экологической и здравоохранительной отраслях. Эти датчики используют один и тот же базовый рабочий процесс: избирательное связывание аналита, генерация сигнала от взаимодействия наносенсора с биоэлементом и обработка сигнала в полезные показатели.
Характеристики
Датчики на основе наноматериалов имеют ряд преимуществ: чувствительность и специфичность по сравнению с датчиками, изготовленными из традиционных материалов, из-за свойств наноматериалов, отсутствующих в объемном материале, которые возникают на наномасштабе.[2] Наносенсоры могут иметь повышенную специфичность, поскольку они действуют в масштабе, аналогичном естественным биологическим процессам, позволяя функционализировать химическими и биологическими молекулами, с событиями распознавания, которые вызывают обнаруживаемые физические изменения. Повышение чувствительности обусловлено высоким отношением поверхности к объему наноматериалов, а также новыми физическими свойствами наноматериалов, которые могут использоваться в качестве основы для обнаружения, в том числе нанофотоника. Наносенсоры также потенциально могут быть интегрированы с наноэлектроника для добавления в наносенсор встроенных возможностей обработки.[3]:4–10
Помимо чувствительности и специфичности, наносенсоры обладают значительными преимуществами по стоимости и времени отклика, что делает их пригодными для высокопроизводительных приложений. Наносенсоры обеспечивают мониторинг в реальном времени по сравнению с традиционными методами обнаружения, такими как хроматография и спектроскопия. Эти традиционные методы могут занять от нескольких дней до недель для получения результатов и часто требуют вложений в капитальные затраты, а также времени на подготовку проб.[4][5][6][7]
Одномерные наноматериалы, такие как нанопровода и нанотрубки хорошо подходят для использования в наносенсорах по сравнению с объемными или тонкая пленка планарные устройства. Они могут работать как преобразователи, так и как провода для передачи сигнала. Их большая площадь поверхности может вызвать большие изменения сигнала при связывании аналита. Их небольшой размер позволяет мультиплексирование индивидуально адресуемых сенсорных блоков в небольшом устройстве. Их работа также "свободна от этикеток" в том смысле, что не требует флуоресцентных или радиоактивных меток на аналитах.[3]:12–26 Нанопроволока из оксида цинка используется для обнаружения газов, поскольку она демонстрирует высокую чувствительность к низкой концентрации газа в условиях окружающей среды и может быть легко изготовлена с низкой стоимостью.[8]
Перед наносенсорами стоит несколько проблем, включая предотвращение дрейфа и обрастание разработка воспроизводимых методов калибровки, применение методов предварительного концентрирования и разделения для достижения надлежащей концентрации анализируемого вещества, позволяющей избежать насыщения, и интеграция наносенсора с другими элементами сенсорного блока надежным производственным способом.[3]:4–10 Поскольку наносенсоры являются относительно новой технологией, остается много безответных вопросов, касающихся нанотоксикологии, что в настоящее время ограничивает их применение в биологических системах.
Потенциальные применения наносенсоров включают медицину, обнаружение загрязнителей и патогенов, а также мониторинг производственных процессов и транспортных систем.[3]:4–10 Измеряя изменения физических свойств (объем, концентрация, смещение и скорость, гравитационный, электрические, и магнитный силы давление, или же температура ) наносенсоры могут различать и распознавать определенные клетки на молекулярном уровне, чтобы доставить лекарство или контролировать развитие в определенные места в организме.[9] Тип передачи сигнала определяет основную систему классификации наносенсоров. Некоторые из основных типов считывающих устройств наносенсора включают оптические, механические, вибрационные или электромагнитные.[10]
В качестве примера классификации наносенсоры, использующие полимеры с молекулярным отпечатком (MIP) можно разделить на три категории: электрохимический, пьезоэлектрический, или же спектроскопический датчики. Электрохимические датчики вызывают изменение электрохимических свойств чувствительного материала, в том числе: обвинять, проводимость, и электрический потенциал. Пьезоэлектрические датчики либо преобразуют механическую силу в электрическую, либо наоборот. Эта сила тогда преобразованный в сигнал. Спектроскопические датчики MIP можно разделить на три подкатегории: хемилюминесцентный датчики, поверхностный плазмонный резонанс датчики и флуоресценция датчики. Как следует из названия, эти датчики производят световые сигналы в форме хемилюминесценции, резонанса и флуоресценции. Как описано в примерах, тип изменения, которое обнаруживает датчик, и тип сигнала, который он вызывает, зависят от типа датчика.[11]
Механизмы работы
Есть несколько механизмов, с помощью которых событие распознавания может быть преобразованный в измеримый сигнал; как правило, они используют чувствительность наноматериала и другие уникальные свойства для обнаружения селективно связанного аналита.
Электрохимические наносенсоры основаны на обнаружении сопротивление изменение наноматериала при связывании аналита из-за изменений в рассеяние или к истощению или накоплению носители заряда. Одна из возможностей - использовать нанопроволоки, такие как углеродные нанотрубки, проводящие полимеры, или нанопроволоки оксида металла в качестве ворот в полевые транзисторы, хотя по состоянию на 2009 год они еще не демонстрировались в реальных условиях.[3]:12–26 Химические наносенсоры содержат систему химического распознавания (рецептор) и физико-химический преобразователь, в котором рецептор взаимодействует с анализируемым веществом для выработки электрических сигналов.[12] В одном случае[13] при взаимодействии аналита с рецептором у нанопористого преобразователя наблюдалось изменение импеданса, которое определяли как сигнал датчика. Другие примеры включают электромагнитные или плазмонный наносенсоры, спектроскопические наносенсоры, такие как Рамановская спектроскопия с усилением поверхности, магнитоэлектронные или спинтроник наносенсоры и механические наносенсоры.[3]:12–26
Биологические наносенсоры состоят из биорецептора и преобразователя. В настоящее время предпочтительным методом трансдукции является флуоресценция из-за высокой чувствительности и относительной простоты измерения.[14][15] Измерение может быть достигнуто с помощью следующих методов: связывание активных наночастиц с активными белками внутри клетки с использованием сайт-направленный мутагенез для производства индикаторных белков, позволяющих проводить измерения в реальном времени, или путем создания наноматериала (например, нановолокон) с сайтами прикрепления для биорецепторов.[14] Хотя электрохимические наносенсоры можно использовать для измерения внутриклеточный свойств, они обычно менее селективны для биологических измерений, так как им не хватает высокой специфичности биорецепторов (например, антител, ДНК).[16][14]
Фотонный устройства также могут использоваться в качестве наносенсоров для количественного определения концентраций клинически значимых образцов. Принцип действия этих датчиков основан на химической модуляции объема пленки гидрогеля, включающей Решетка Брэгга. Поскольку гидрогель набухает или сжимается при химической стимуляции, решетка Брэгга меняет цвет и дифрагирует свет на разных длинах волн. Дифрагированный свет можно коррелировать с концентрацией целевого аналита.[17]
Другой тип наносенсора - датчик, работающий через колориметрический основание. Здесь наличие аналит вызывает химическая реакция или морфологическое изменение для появления видимого изменения цвета. Одно из таких приложений - это золото наночастицы может использоваться для обнаружения тяжелых металлов.[18] Многие вредные газы также можно обнаружить с помощью колориметрического изменения, например, с помощью имеющихся в продаже Dräger Tube. Они представляют собой альтернативу громоздким лабораторным системам, поскольку их можно уменьшить в размерах для использования в устройствах для отбора проб. Например, многие химические вещества регулируются Агентство по охране окружающей среды и требуют всестороннего тестирования, чтобы гарантировать загрязнитель уровни находятся в соответствующих пределах. Колориметрические наносенсоры обеспечивают метод определения многих загрязняющих веществ на месте.[19][20][21]
Методы производства
Метод производства играет центральную роль в определении характеристик производимого наносенсора, так как функция наносенсора может осуществляться за счет управления поверхностью наночастиц. Существует два основных подхода к производству наносенсоров: нисходящие методы, которые начинаются с шаблона, созданного в более крупном масштабе, а затем сокращаются до микромасштаба. Восходящие методы начинаются с атомов или молекул, которые образуют наноструктуры.
Нисходящие методы
Литография
Для этого нужно начать с большого блока из некоторого материала и вырезать желаемую форму. Эти резные устройства, особенно используемые в определенных микроэлектромеханические системы используются в качестве микросенсоров, обычно достигают микро размер, но самые последние из них начали включать наноразмерные компоненты.[1] Один из самых распространенных методов называется электронно-лучевой литографией. Хотя этот метод очень дорогостоящий, он эффективно формирует распределение круговых или эллипсоидальных графиков на двумерной поверхности. Другой метод - это электроосаждение, при котором для изготовления миниатюрных устройств требуются проводящие элементы.[22]
Вытягивание волокна
Этот метод заключается в использовании натяжного устройства для растягивания главной оси волокна во время его нагрева для получения наноразмерных масштабов. Этот метод специально используется в оптическом волокне для разработки наносенсоров на основе оптического волокна.[16]
Химическое травление
Сообщалось о двух различных типах химического травления. в Метод Тернера, волокно протравливается до точки, когда оно помещается в мениск между плавиковая кислота и органический наложение. Было показано, что этот метод позволяет производить волокна с большими углами сужения (таким образом, увеличивая свет, достигающий кончика волокна) и диаметром кончика, сопоставимым с методом вытягивания. Второй метод - травление трубки, которое включает травление оптического волокна однокомпонентным раствором фтороводород. Волокно диоксида кремния, окруженное органическим облицовка, полируется и один конец помещается в емкость с плавиковой кислотой. Затем кислота начинает вытравливать кончик волокна, не разрушая оболочки. Когда кварцевое волокно вытравливается, полимерная оболочка действует как стенка, создавая микротоки в фтористоводородной кислоте, которая в сочетании с капиллярное действие, заставляют волокно вытравливать форму конуса с большими гладкими конусами. Этот метод показывает гораздо меньшую чувствительность к параметрам окружающей среды, чем метод Тернера.[16]
Восходящие методы
Этот тип методов включает сборку датчиков из более мелких компонентов, обычно отдельных атомы или молекулы. Это достигается путем расположения атомов в определенных образцах, что было достигнуто в лабораторных испытаниях с использованием атомно-силовая микроскопия, но по-прежнему трудно достичь в массовом порядке и не является экономически выгодным.
Самостоятельная сборка
Этот метод, также известный как «выращивание», чаще всего включает в себя уже полный набор компонентов, которые автоматически собираются в готовый продукт. Возможность точно воспроизвести этот эффект для желаемого датчика в лаборатории будет означать, что ученые могли бы производить наносенсоры намного быстрее и потенциально гораздо дешевле, позволяя множеству молекул собираться самостоятельно с минимальным внешним влиянием или без него, вместо того, чтобы вручную собирать каждый датчик. .
Хотя традиционные методы изготовления доказали свою эффективность, дальнейшие усовершенствования способа производства могут привести к минимизации затрат и повышению производительности. Проблемы с современными методами производства включают неравномерное распределение, размер и форму наночастиц, что приводит к ограничению производительности. В 2006 году исследователи в Берлине запатентовали свое изобретение нового диагностического наносенсора, изготовленного с помощью наносферной литографии (NSL), который позволяет точно контролировать размер и форму наночастиц и создает наноостровки. Металлические наноостровки увеличивали передачу сигнала и, таким образом, повышали чувствительность датчика. Результаты также показали, что чувствительность и характеристики диагностического наносенсора зависят от размера наночастиц, что уменьшение размера наночастиц увеличивает чувствительность.[22]
Приложения
Один из первых рабочих примеров синтетического наносенсора был построен исследователями из Технологический институт Джорджии в 1999 году.[23] Это включало прикрепление одиночной частицы к концу углеродная нанотрубка и измерения частота колебаний нанотрубки как с частицей, так и без них. Несовпадение двух частот позволило исследователям измерить массу прикрепленной частицы.[1]
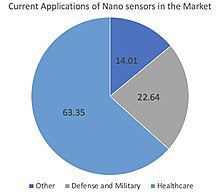
С тех пор все больше исследований проводилось в области наносенсоров, в результате чего современные наносенсоры были разработаны для многих приложений. В настоящее время применение наносенсоров на рынке включает в себя: здравоохранение, оборону и вооруженные силы, а также другие области, такие как продукты питания, окружающая среда и сельское хозяйство.[24]
Оборона и военные
Нанонаука в целом имеет множество потенциальных применений в оборонном и военном секторах, включая обнаружение химических веществ, дезактивацию и судебную экспертизу. Некоторые наносенсоры, разрабатываемые для оборонных приложений, включают наносенсоры для обнаружения взрывчатых веществ или токсичных газов. Такие наносенсоры работают по тому принципу, что молекулы газа можно различать по их массе с помощью, например, пьезоэлектрических датчиков. Если молекула газа адсорбируется на поверхности детектора, резонансная частота кристалла изменяется, и это можно измерить как изменение электрических свойств. Кроме того, полевые транзисторы, используемые в качестве потенциометры, могут обнаруживать токсичные газы, если их ворота чувствительны к ним.[25]
В аналогичном приложении наносенсоры могут использоваться в одежде и снаряжении военных и правоохранительных органов. Институт нанонауки Морской научно-исследовательской лаборатории изучил квантовые точки для применения в нанофотоника и идентификация биологических материалов. Наночастицы, состоящие из полимеров и других рецепторных молекул, меняют цвет при контакте с аналитами, такими как токсичные газы.[25] Это предупреждает пользователя, что он в опасности. Другие проекты включают в себя вшивку одежды с биометрический датчики для передачи информации о здоровье и жизненно важных функциях пользователя,[25] что было бы полезно для наблюдения за солдатами в бою.
Удивительно, но некоторые из наиболее сложных аспектов создания наносенсоров для обороны и военного использования носят политический, а не технический характер. Многие различные правительственные агентства должны работать вместе, чтобы распределять бюджеты и обмениваться информацией и прогрессом в тестировании; это может быть сложно с такими большими и сложными учреждениями. Кроме того, визы и иммиграционный статус могут стать проблемой для иностранных исследователей - поскольку предмет очень чувствительный, иногда может потребоваться разрешение правительства.[26] Наконец, в настоящее время нет четко определенных или четких правил тестирования или применения наносенсоров в сенсорной индустрии, что усложняет реализацию.
Еда и окружающая среда
Наносенсоры могут улучшить различные подотрасли пищевого и экологического секторов, включая пищевую промышленность, сельское хозяйство, мониторинг качества воздуха и воды, а также упаковку и транспорт. Благодаря своей чувствительности, а также возможности настройки и результирующей селективности связывания наносенсоры очень эффективны и могут быть разработаны для широкого спектра применений в окружающей среде. Такие применения наносенсоров помогают в удобной, быстрой и сверхчувствительной оценке многих типов загрязнителей окружающей среды.[27]
Химические датчики полезны для анализа запахов от образцов пищевых продуктов и обнаружения атмосферных газов. «Электронный нос» был разработан в 1988 году для определения качества и свежести образцов пищевых продуктов с использованием традиционных датчиков, но в последнее время чувствительная пленка была улучшена с помощью наноматериалов. Образец помещается в камеру, где летучие соединения концентрируются в газовой фазе, в результате чего газ затем прокачивается через камеру, чтобы передать аромат на датчик, который измеряет его уникальный отпечаток пальца. Высокое соотношение площади поверхности к объему наноматериалов позволяет лучше взаимодействовать с аналитами, а быстрое время отклика наносенсора позволяет разделить мешающие отклики.[28] Химические датчики также были построены с использованием нанотрубки для обнаружения различных свойств газовых молекул. Многие датчики на основе углеродных нанотрубок спроектированы как полевые транзисторы, что позволяет использовать их чувствительность. Электропроводность этих нанотрубок будет изменяться из-за переноса заряда и химического легирования другими молекулами, что позволяет их обнаруживать. Чтобы повысить их селективность, многие из них включают систему, с помощью которой наносенсоры создаются так, чтобы иметь специальный карман для другой молекулы. Углеродные нанотрубки использовались для определения ионизация молекул газа, в то время как нанотрубки, сделанные из титана, были использованы для обнаружения атмосферных концентраций водорода на молекулярном уровне.[29][30] Некоторые из них были разработаны как полевые транзисторы, в то время как другие используют возможности оптического считывания. Селективное связывание аналита обнаруживается посредством спектрального сдвига или модуляции флуоресценции.[31] Аналогичным образом Flood et al. показали, что супрамолекулярный химия хозяина и гостя предлагает количественное зондирование с использованием Рамановский рассеянный свет[32] а также SERS.[33]
Другие типы наносенсоров, в том числе квантовые точки и наночастицы золота, в настоящее время разрабатываются для обнаружения загрязнителей и токсинов в окружающей среде. Они используют преимущества локализованный поверхностный плазмонный резонанс (LSPR), который возникает на наномасштабе, что приводит к поглощению на длине волны.[34] Этот спектр LSPR особенно чувствителен, и его зависимость от размера наночастиц и окружающей среды может использоваться различными способами для разработки оптических датчиков. Чтобы воспользоваться преимуществом сдвига спектра LSPR, который происходит, когда молекулы связываются с наночастицей, их поверхности могут быть функционализированы, чтобы определять, какие молекулы будут связываться и запускать реакцию.[35] Для экологических приложений поверхности квантовых точек могут быть модифицированы антителами, которые специфически связываются с микроорганизмами или другими загрязнителями. Затем спектроскопию можно использовать для наблюдения и количественной оценки этого сдвига спектра, что дает возможность точного обнаружения, возможно, порядка молекул.[35] Точно так же флуоресцентные полупроводниковые наносенсоры могут использовать преимущества флуоресцентный резонансный перенос энергии (FRET) для оптического обнаружения. Квантовые точки можно использовать в качестве доноров, и они будут передавать энергию электронного возбуждения, когда расположены рядом с молекулами-акцепторами, тем самым теряя свою флуоресценцию. Эти квантовые точки можно функционализировать, чтобы определить, какие молекулы будут связываться, а флуоресценция будет восстанавливаться. Оптические сенсоры на основе наночастиц золота можно использовать для очень точного обнаружения тяжелых металлов; например, уровень ртути составляет всего 0,49 нанометра. Этот способ восприятия использует преимущество FRET, в котором присутствие металлов подавляет взаимодействие между квантовыми точками и наночастицами золота и подавляет реакцию FRET.[36] Другая потенциальная реализация использует зависимость спектра LSPR от размера для достижения ионного зондирования. В одном исследовании Liu et al. функционализированные наночастицы золота с Pb2+ чувствительный фермент для производства свинцового сенсора. Как правило, наночастицы золота объединяются по мере приближения друг к другу, и изменение размера приводит к изменению цвета. Взаимодействие между ферментом и Pb2+ ионы будут ингибировать эту агрегацию, и, таким образом, присутствие ионов может быть обнаружено.
Основная проблема, связанная с использованием наносенсоров в продуктах питания и окружающей среде, заключается в определении связанной с ними токсичности и общего воздействия на окружающую среду. В настоящее время недостаточно знаний о том, как внедрение наносенсоров повлияет на почву, растения и людей в долгосрочной перспективе. С этим трудно полностью справиться, поскольку токсичность наночастиц сильно зависит от типа, размера и дозировки частицы, а также от переменных окружающей среды, включая pH, температуру и влажность. Чтобы снизить потенциальный риск, проводятся исследования по производству безопасных, нетоксичных наноматериалов в рамках общих усилий по созданию зеленых нанотехнологий.[37]
Здравоохранение
Наносенсоры обладают огромным потенциалом для диагностической медицины, позволяя раннее выявить заболевание, не полагаясь на наблюдаемые симптомы. Идеальные реализации наносенсоров призваны имитировать реакцию иммунных клеток в организме, объединяя функции диагностики и иммунного ответа, при этом передавая данные, позволяющие контролировать входные данные датчика и реакцию. Однако эта модель остается долгосрочной целью, и в настоящее время исследования сосредоточены на непосредственных диагностических возможностях наносенсоров. Внутриклеточная реализация наносенсора, синтезированного из биоразлагаемых полимеров, вызывает сигналы, которые позволяют осуществлять мониторинг в реальном времени, и, таким образом, открывает путь для продвижения лекарств и лечения.[38]
Один из примеров этих наносенсоров включает использование флуоресцентных свойств селенид кадмия квантовые точки в качестве датчиков для обнаружения опухолей в организме. Однако недостатком точек селенида кадмия является то, что они очень токсичны для организма. В результате исследователи работают над созданием альтернативных точек, сделанных из другого, менее токсичного материала, сохраняя при этом некоторые флуоресцентные свойства. В частности, они изучали особые преимущества квантовых точек сульфида цинка, которые, хотя и не так флуоресцируют, как селенид кадмия, могут быть дополнены другими металлами, включая марганец и различные лантаноид элементы. Кроме того, эти новые квантовые точки становятся более флуоресцентными, когда связываются со своими клетками-мишенями.[31]
Еще одно применение наносенсоров включает использование кремниевых нанопроволок в линиях для внутривенного введения для контроля здоровья органов. Нанопроволоки чувствительны к обнаружению следовых биомаркеров, которые диффундируют в капельницу через кровь, что позволяет отслеживать почечную или органную недостаточность. Эти нанопроволоки позволят непрерывно измерять биомаркеры, что дает некоторые преимущества с точки зрения временной чувствительности по сравнению с традиционными анализами количественного определения биомаркеров, такими как ELISA.[39]
Наносенсоры также можно использовать для обнаружения загрязнения имплантатов органов. Наносенсор встроен в имплантат и обнаруживает загрязнение в клетках, окружающих имплант, с помощью электрического сигнала, отправляемого врачу или поставщику медицинских услуг. Наносенсор может определять, являются ли клетки здоровыми, воспалительными или загрязненными бактериями.[40] Однако главный недостаток заключается в длительном использовании имплантата, когда ткань растет поверх датчиков, ограничивая их способность сжиматься. Это препятствует производству электрических зарядов, сокращая, таким образом, срок службы этих наносенсоров, поскольку они используют пьезоэлектрический эффект для собственного питания.
Подобно тем, которые используются для измерения атмосферных загрязнителей, наносенсоры на основе золотых частиц используются для ранней диагностики нескольких типов рака путем обнаружения летучие органические соединения (ЛОС) в дыхании, поскольку рост опухоли связан с перекисное окисление клеточной мембраны.[41] Еще одно связанное с раком приложение, которое все еще находится на стадии исследования мышей, - это использование покрытый пептидом наночастицы как сенсоры на основе активности для обнаружения рака легких. Два основных преимущества использования наночастиц для обнаружения заболеваний заключаются в том, что они позволяют обнаруживать ранние стадии, поскольку они могут обнаруживать опухоли размером порядка миллиметров. Он также представляет собой экономичный, простой в использовании, портативный и неинвазивный диагностический инструмент.[41][42]
Недавние усилия по развитию технологии наносенсоров позволили молекулярный импринтинг, который представляет собой метод, используемый для синтеза полимерных матриц, которые действуют как рецепторы при молекулярном распознавании. Аналогично ферментно-субстратный замок и модель ключа Молекулярный импринтинг использует молекулы-шаблоны с функциональными мономерами для формирования полимерных матриц с определенной формой, соответствующей его молекулам-мишеням-шаблонам, что увеличивает селективность и сродство матриц. Этот метод позволил наносенсорам обнаруживать химические вещества. В области биотехнологии молекулярно импринтированные полимеры (MIP) представляют собой синтезированные рецепторы, показавшие многообещающие и экономически эффективные альтернативы природным антителам, поскольку они сконструированы так, чтобы иметь высокую селективность и аффинность. Например, эксперимент с датчиком MI, содержащим наноострия с непроводящими полифенол нанопокрытие (покрытие PPn) показало селективное обнаружение Белок E7 и таким образом продемонстрировали потенциальное использование этих наносенсоров для обнаружения и диагностики вируса папилломы человека, других патогенов человека и токсинов.[11] Как показано выше, наносенсоры с техникой молекулярного импринтинга способны избирательно обнаруживать сверхчувствительные химические вещества, поскольку путем искусственного изменения полимерных матриц молекулярный импринтинг увеличивает сродство и селективность.[11] Хотя полимеры с молекулярной печатью обеспечивают преимущества в селективном молекулярном распознавании наносенсоров, сама технология является относительно недавней, и все еще остаются проблемы, такие как ослабление сигналов, системы обнаружения, не имеющие эффективных преобразователей, и поверхности, не имеющие эффективного обнаружения. Дальнейшие исследования и исследования в области полимеров с молекулярной печатью имеют решающее значение для разработки высокоэффективных наносенсоров.[43]
Чтобы разработать интеллектуальное здравоохранение с помощью наносенсоров, необходимо создать сеть наносенсоров, часто называемую наносетью, чтобы преодолеть ограничения по размеру и мощности отдельных наносенсоров.[44] Наносети не только решают существующие проблемы, но и обеспечивают множество улучшений. Разрешение наносенсоров на клеточном уровне позволит устранить побочные эффекты при лечении, обеспечить непрерывный мониторинг и отчетность о состоянии пациентов.
Наносети требуют дальнейшего изучения тем, что наносенсоры отличаются от традиционных датчиков. Наиболее распространенный механизм сенсорных сетей - электромагнитная связь. Однако текущая парадигма неприменима к наноустройствам из-за их малого диапазона и мощности. Оптический сигнал преобразование было предложено как альтернатива классической электромагнитной телеметрии и имеет приложения для мониторинга человеческого тела. Другие предлагаемые механизмы включают биоинспирированные молекулярные коммуникации, проводной и беспроводной активный транспорт в молекулярных коммуникациях, передачу энергии Форстера и многое другое. Крайне важно построить эффективную наносеть, чтобы ее можно было применять в таких областях, как медицинские имплантаты, сети тела (БАН), Интернет нано вещей (IoNT), доставка лекарств и многое другое.[45] С помощью продуманной наносети биоимплантируемые наноустройства могут обеспечить более высокую точность, разрешение и безопасность по сравнению с имплантатами макромасштабов.Сети области тела (BAN) позволяют датчикам и исполнительным механизмам собирать физические и физиологические данные человеческого тела, чтобы лучше предвидеть любые заболевания, что, таким образом, облегчит лечение. Возможные применения BAN включают мониторинг сердечно-сосудистых заболеваний, лечение инсулином, искусственное зрение и слух, а также управление гормональной терапией. Интернет био-нано вещей относится к сетям наноустройств, к которым можно получить доступ через Интернет. Развитие IoBNT открыло путь к новым методам лечения и диагностики.[46] Наносети также могут помочь доставке лекарств за счет увеличения локализации и времени обращения лекарств.[44]
Существующие проблемы с вышеупомянутыми приложениями включают биосовместимость наноимплантатов, физические ограничения, приводящие к нехватке энергии и памяти, а также биосовместимость конструкции передатчика и приемника IoBNT. Концепция наносети имеет множество областей для улучшений: в их число входит разработка наномашины, проблемы стека протоколов, методы обеспечения питания и многое другое.[44]
По-прежнему действуют строгие правила для разработки стандартов для наносенсоров, которые будут использоваться в медицинской промышленности, из-за недостаточных знаний о побочных эффектах наносенсоров, а также о потенциальных цитотоксических эффектах наносенсоров.[47] Кроме того, может быть высокая стоимость сырья, такого как кремний, нанопроволоки и углеродные нанотрубки, что препятствует коммерциализации и производству наносенсоров, требующих масштабирования для внедрения. Чтобы уменьшить недостаток стоимости, исследователи изучают возможность производства наносенсоров из более экономичных материалов.[24] Также существует высокая степень точности, необходимая для воспроизводимого производства наносенсоров из-за их небольшого размера и чувствительности к различным методам синтеза, что создает дополнительные технические проблемы, которые необходимо преодолеть.
Смотрите также
Рекомендации
- ^ а б c Фостер Л. Е. (2006). Медицинские нанотехнологии: наука, инновации и возможности. Верхняя река Сэдл: образование Пирсона. ISBN 0-13-192756-6.
- ^ Гисбье, Грегори; Мехиа-Росалес, Серхио; Леонард Дипак, Фрэнсис (2012). «Свойства наноматериалов: зависимости размера и формы». Журнал наноматериалов. 2012: 1–2. Дои:10.1155/2012/180976. Получено 2020-05-05.
- ^ а б c d е ж "Зондирование с помощью нанотехнологий". Национальная нанотехнологическая инициатива. 2009. Получено 2017-06-22.
- ^ GarciaAnoveros, J; Кори, Д.П. (1997). «Молекулы механочувствительности». Ежегодный обзор нейробиологии. 20: 567–94. Дои:10.1146 / annurev.neuro.20.1.567. PMID 9056725.
- ^ Callaway DJ, Matsui T, Weiss T., Stingaciu LR, Stanley CB, Heller W.T., Bu ZM (7 апреля 2017 г.). «Контролируемая активация наноразмерной динамики в неупорядоченном белке изменяет кинетику связывания». Журнал молекулярной биологии. 427 (7): 987–998. Дои:10.1016 / j.jmb.2017.03.003. ЧВК 5399307. PMID 28285124.
- ^ Лангер, Роберт (2010). «Нанотехнологии в доставке лекарств и тканевой инженерии: от открытий до приложений». Nano Lett. 10 (9): 3223–30. Bibcode:2010NanoL..10.3223S. Дои:10.1021 / nl102184c. ЧВК 2935937. PMID 20726522.
- ^ Тангавелу, Раджа Мутурамалингам; Гунасекаран, Дхаранивасан; Джесси, Майкл Иммануэль; s.u, Мохаммед Рияз; Сундараджан, Дипан; Кришнан, Катираван (2018). «Нанобиотехнологический подход с использованием синтезированных гормоном корней растений наночастиц серебра в качестве« нанопуляций »для динамического применения в садоводстве - исследование in vitro и ex vitro». Арабский химический журнал. 11: 48–61. Дои:10.1016 / j.arabjc.2016.09.022.
- ^ Lupan, O .; Емельченко, Г. А .; Урсаки, В. В .; Chai, G .; Редькин, А. Н .; Грузинцев, А. Н .; Тигиняну, И. М .; Chow, L .; Оно, Л. К .; Roldan Cuenya, B .; Генрих, Х. (01.08.2010). «Синтез и характеристика нанопроволок ZnO для применения в наносенсорах». Бюллетень материаловедения. 45 (8): 1026–1032. Дои:10.1016 / j.materresbull.2010.03.027. ISSN 0025-5408.
- ^ Фрейтас младший РА (1999). Наномедицина, Том 1: Основные возможности. Остин: Landes Bioscience. ISBN 1-57059-680-8.
- ^ Lim, T.-C .; Рамакришна С. Концептуальный обзор наносенсоров. http://www.znaturforsch.com/aa/v61a/s61a0402.pdf.
- ^ а б c Кечили, Рустем; Бюйюктиряки, Сибел; Хуссейн, Чаудхери Мустансар (01.01.2018), Мустансар Хуссейн, Чаудхери (ред.), "Глава 57 - Разработанные наносенсоры на основе технологии молекулярного импринтинга", Справочник по наноматериалам для промышленного применения, Micro and Nano Technologies, Elsevier, pp. 1031–1046, Дои:10.1016 / b978-0-12-813351-4.00059-6, ISBN 978-0-12-813351-4, получено 2020-05-05
- ^ Химические датчики. http://nano-bio.ehu.es/files/chemical_sensors1.doc_definitivo.pdf (по состоянию на 6 декабря 2018 г.)
- ^ Агниво Госай, Брендан Шин Хау Да, Марит Нильсен-Гамильтон, Пранав Шротрия, Обнаружение тромбина без метки в присутствии высокой концентрации альбумина с использованием аптамерно-функционализированной нанопористой мембраны, Биосенсоры и биоэлектроника, Том 126,2019, страницы 88-95, ISSN 0956-5663,https://doi.org/10.1016/j.bios.2018.10.010.
- ^ а б c Fehr, M .; Окумото, S .; Deuschle, K .; Lager, I .; Looger, L. L .; Persson, J .; Кожух, Л .; Lalonde, S .; Фроммер, В. Б. (01.02.2005). «Разработка и использование флуоресцентных наносенсоров для визуализации метаболитов в живых клетках». Сделки Биохимического Общества. 33 (1): 287–290. Дои:10.1042 / BST0330287. ISSN 0300-5127. PMID 15667328.
- ^ Эйлотт, Джонатан В. (07.04.2003). «Оптические наносенсоры - эффективная технология для внутриклеточных измерений». Аналитик. 128 (4): 309–312. Bibcode:2003Ана ... 128..309А. Дои:10.1039 / b302174m. PMID 12741632.
- ^ а б c Каллум, Брайан М .; Во-Динь, Туан (1 сентября 2000 г.). «Разработка оптических наносенсоров для биологических измерений». Тенденции в биотехнологии. 18 (9): 388–393. Дои:10.1016 / S0167-7799 (00) 01477-3. ISSN 0167-7799. PMID 10942963.
- ^ Йетисен, АК; Монтелонго, Y; Васконселлос, ФК; Мартинес-Уртадо, JL; Neupane, S; Стык, H; Касим, ММ; Блит, Дж; Берлинг, К; Кармоди, JB; Эванс, М; Уилкинсон, Т. Д.; Кубота, LT; Монтейро, MJ; Лоу, CR (2014). «Многоразовый, надежный и точный лазерный фотонный нанодатчик». Nano Lett. 14 (6): 3587–3593. Bibcode:2014NanoL..14.3587Y. Дои:10.1021 / nl5012504. PMID 24844116.
- ^ Priyadarshini, E .; Прадхан, Н. (январь 2017 г.). «Наночастицы золота как эффективные сенсоры в колориметрическом обнаружении ионов токсичных металлов: обзор». Датчики и исполнительные механизмы B: химические. 238: 888–902. Дои:10.1016 / j.snb.2016.06.081.
- ^ Palomares, E .; Мартинес-Диас, М. В .; Торрес, Т .; Коронадо, Э. (06.06.2006). «Высокочувствительный гибридный колориметрический и флуорометрический молекулярный зонд для определения цианида на основе субфталоцианинового красителя». Современные функциональные материалы. 16 (9): 1166–1170. Дои:10.1002 / adfm.200500517. ISSN 1616-301X.
- ^ Вэй, Циншань; Наги, Ричи; Садеги, Кайвон; Фэн, Стив; Ян, Эдди; Ки, Со Юнг; Кэр, Ромен; Ценг, Дерек; Озджан, Айдоган (25 февраля 2014 г.). «Обнаружение и пространственное картирование загрязнения ртутью в пробах воды с помощью смартфона». САУ Нано. 8 (2): 1121–1129. Дои:10.1021 / nn406571t. ISSN 1936-0851. ЧВК 3949663. PMID 24437470.
- ^ Эль-Каутит, Хамид; Эстевес, Педро; Гарсия, Феликс С .; Серна, Фелипе; Гарсия, Хосе М. (2013). «Количественное определение Hg (ii) в водной среде с использованием как невооруженного глаза, так и цифровой информации из изображений колориметрической сенсорной полимерной мембраны, сделанных цифровой камерой обычного мобильного телефона». Анальный. Методы. 5 (1): 54–58. Дои:10.1039 / C2AY26307F. ISSN 1759-9660.
- ^ а б Писон, У., Гирсиг, М., и Шефер, Алекс. (2014). США 8846580 B2. Берлин, Германия.
- ^ Пончарал П; Wang ZL; Угарте Д; де Хеер WA (1999). «Электростатические отклонения и электромеханические резонансы углеродных нанотрубок». Наука. 283 (5407): 1513–1516. Bibcode:1999Научный ... 283.1513П. Дои:10.1126 / science.283.5407.1513. PMID 10066169.
- ^ а б Technavio. Инвестиции в глобальный рынок нанодатчиков. 2017 г.
- ^ а б c Нго К., Ван де Вурде М.Х. (2014) Нанотехнологии для обороны и безопасности. В кн .: Нанотехнологии в двух словах. Atlantis Press, Париж
- ^ Карафано, Дж. Нанотехнологии и национальная безопасность: небольшие изменения, большое влияние. https://www.heritage.org/defense/report/nanotechnology-and-national-security-small-changes-big-impact (по состоянию на 3 декабря 2018 г.)
- ^ Хэндфорд, Кэролайн Э .; Дин, Мойра; Хенчион, Мейв; Спенс, Мишель; Эллиотт, Кристофер Т .; Кэмпбелл, Катрина (декабрь 2014 г.). «Влияние нанотехнологий на агропродовольственную промышленность: возможности, преимущества и риски». Тенденции в пищевой науке и технологиях. 40 (2): 226–241. Дои:10.1016 / j.tifs.2014.09.007.
- ^ Рамгир, Н. С. ISRN Наноматериалы 2013, 2013, 1–21.
- ^ Моди А; Кораткар Н; Lass E; Вэй Б; Аджаян PM (2003). «Миниатюрные датчики ионизации газа с использованием углеродных нанотрубок». Природа. 424 (6945): 171–174. Bibcode:2003Натура.424..171М. Дои:10.1038 / природа01777. PMID 12853951.
- ^ Kong J; Франклин Н.Р .; Чжоу С; Чаплин MG; Peng S; Чо К; Дай Х. (2000). «Молекулярные нити нанотрубок как химические сенсоры». Наука. 287 (5453): 622–625. Bibcode:2000Sci ... 287..622K. Дои:10.1126 / science.287.5453.622. PMID 10649989.
- ^ а б Ратнер MA; Ратнер Д; Ратнер М. (2003). Нанотехнологии: мягкое введение в следующую большую идею. Река Верхнее Седл: Prentice Hall. ISBN 0-13-101400-5.
- ^ Witlicki, Edward H .; Hansen, Stinne W .; Кристенсен, Мартин; Hansen, Thomas S .; Nygaard, Sune D .; Jeppesen, Jan O .; Вонг, Эрик У .; Дженсен, Лассе; Флуд, Амар Х. (2009). «Определение силы связывания комплекса хозяин-гость с использованием резонансного комбинационного рассеяния света». J. Phys. Chem. А. 113 (34): 9450–9457. Bibcode:2009JPCA..113.9450 Вт. Дои:10.1021 / jp905202x. PMID 19645430.
- ^ Witlicki, Edward H .; Andersen, Sissel S .; Hansen, Stinne W .; Jeppesen, Jan O .; Вонг, Эрик У .; Дженсен, Лассе; Флуд, Амар Х. (2010). «Включение резонансного SERRS с использованием связи хромофор-плазмон, созданной комплексообразованием хост-гость на плазмонном наномассиве». Варенье. Chem. Soc. 132 (17): 6099–6107. Дои:10.1021 / ja910155b. PMID 20387841.
- ^ Йонзон, Чанда Ранджит; Стюарт, Дуглас А .; Чжан, Сяоюй; McFarland, Adam D .; Хейнс, Кристи Л .; Ван Дайн, Ричард П. (2005-09-15). «На пути к передовым химическим и биологическим наносенсорам - обзор». Таланта. Нанонаука и нанотехнологии. 67 (3): 438–448. Дои:10.1016 / j.talanta.2005.06.039. ISSN 0039-9140. PMID 18970187.
- ^ а б Риу, Хорди; Марото, Алисия; Риус, Ф. Ксавьер (15 апреля 2006 г.). «Наносенсоры в экологическом анализе». Таланта. 1-й семинар Swift-WFD по проверке устойчивости датчиков и биотестов для скрининга загрязнителей. 69 (2): 288–301. Дои:10.1016 / j.talanta.2005.09.045. ISSN 0039-9140. PMID 18970568.
- ^ Long, F .; Чжу, А .; Ши, Х (2013). «Последние достижения в области оптических биосенсоров для мониторинга окружающей среды и раннего предупреждения». Датчики. 13 (10): 13928–13948. Дои:10,3390 / с 131013928.
- ^ Оманович-Микличанин, Э .; Максимович, М. (2016). Бюллетень химиков и технологов Боснии и Герцеговины. 47: 59–70. Отсутствует или пусто
| название =(помощь) - ^ Йео, Дэвид; Вираджа, Кристиан; Чуах, Йон Джин; Гао, Ю; Сюй, Чэньцзе (06.10.2015). «Платформа датчиков на основе наночастиц для отслеживания клеток и оценки состояния / функций». Научные отчеты. 5 (1): 14768. Bibcode:2015НатСР ... 514768Y. Дои:10.1038 / srep14768. ISSN 2045-2322. ЧВК 4593999. PMID 26440504.
- ^ Бурзак, К. Наносенсоры для медицинского мониторинга. https://www.technologyreview.com/s/410426/nanosensors-for-medical-monitoring/. 2016 г.
- ^ МакИнтош, Дж. Наносенсоры: будущее диагностической медицины? https://www.medicalnewstoday.com/articles/299663.php. 2017 г.
- ^ а б Peng, G; Хаким, М; Броза, Y Y; Billan, S; Абдах-Бортняк, Р; Кутен, А; Tisch, U; Haick, H (август 2010 г.). «Обнаружение рака легких, молочной железы, толстой кишки и простаты на выдыхаемом воздухе с использованием единого набора наносенсоров». Британский журнал рака. 103 (4): 542–551. Дои:10.1038 / sj.bjc.6605810. ISSN 0007-0920. ЧВК 2939793. PMID 20648015.
- ^ «Наносенсоры позволяют проводить анализ мочи на рак легких». GEN - Новости генной инженерии и биотехнологии. 2020-04-02. Получено 2020-05-05.
- ^ Цай, Донг; Рен, Лу; Чжао, Хуайчжоу; Сюй, Чэньцзя; Чжан, Лу; Ю, Инь; Ван, Хэнчжи; Лань, Юйчэн; Робертс, Мэри Ф .; Чуанг, Джеффри Х .; Нотон, Майкл Дж. (Август 2010 г.). «Наносенсор с молекулярным отпечатком для сверхчувствительного обнаружения белков». Природа Нанотехнологии. 5 (8): 597–601. Bibcode:2010НатНа ... 5..597С. Дои:10.1038 / nnano.2010.114. ISSN 1748-3395. ЧВК 3064708. PMID 20581835.
- ^ а б c Хан, Туба; Civas, Meltem; Четинкая, Октябрь; Abbasi, Naveed A .; Акан, Озгур Б. (01.01.2020), Хан, Баогуо; Томер, Виджай К .; Нгуен, Туан Ань; Фармани, Али (ред.), «Глава 23 - Наносенсорные сети для умного здравоохранения», Наносенсоры для умных городов, Micro and Nano Technologies, Elsevier, pp. 387–403, Дои:10.1016 / b978-0-12-819870-4.00022-0, ISBN 978-0-12-819870-4, получено 2020-05-05
- ^ Галал, Акрам; Хессельбах, Ксавье (01.09.2018). «Коммуникационная архитектура наносетей: моделирование и функции». Нано-коммуникационные сети. 17: 45–62. Дои:10.1016 / j.nancom.2018.07.001. ISSN 1878-7789.
- ^ Акылдыз, И. Ф .; Pierobon, M .; Balasubramaniam, S .; Кучерявый Ю. (март 2015). «Интернет био-нано вещей». Журнал IEEE Communications. 53 (3): 32–40. Дои:10.1109 / MCOM.2015.7060516. ISSN 1558-1896.
- ^ Søndergaard, Rikke V .; Christensen, Nynne M .; Хенриксен, Йонас Р .; Кумар, Э. К. Прамод; Альмдал, Кристоффер; Андресен, Томас Л. (2015). «Столкнувшись с проблемами дизайна наносенсоров на основе частиц для количественного определения метаболитов в живых клетках». Химические обзоры. 115 (16): 8344–8378. Дои:10.1021 / cr400636x. PMID 26244372.
внешняя ссылка
- Взвешивание очень маленьких: «нанобаланс» на основе углеродных нанотрубок демонстрирует новое применение в наномеханике, Новости технических исследований Джорджии.
- Новые технологии и окружающая среда
- Нанотехнологии и социальная трансформация
- Нанотехнологии, конфиденциальность и меняющиеся социальные условности
- Нанотехнологии и наблюдение
