Молекулярное клонирование - Molecular cloning

Молекулярное клонирование представляет собой набор экспериментальных методов в молекулярной биологии, которые используются для сборки рекомбинантных молекул ДНК и управления их репликацией ДНК, репликацией внутри организма-хозяина (биология) | организмов-хозяев.[1] Использование слова клонирование относится к тому факту, что метод включает репликацию одной молекулы для получения популяции клеток с идентичными молекулами ДНК. Молекулярное клонирование обычно использует последовательности ДНК от двух разных организмов: вида, который является источником ДНК для клонирования, и вида, который будет служить живым. хозяин для репликации рекомбинантной ДНК. Методы молекулярного клонирования занимают центральное место во многих современных областях современной биологии и медицины.[2]
В обычном эксперименте по молекулярному клонированию ДНК, которую нужно клонировать, получают из интересующего организма, а затем обрабатывают ферментами в пробирке для получения более мелких фрагментов ДНК. Впоследствии эти фрагменты объединяются с вектор ДНК для создания рекомбинантных молекул ДНК. Затем рекомбинантная ДНК вводится в организм-хозяин (обычно это легко выращиваемый доброкачественный лабораторный штамм Кишечная палочка бактерии). Это создаст популяцию организмов, в которых молекулы рекомбинантной ДНК реплицируются вместе с ДНК хозяина. Поскольку они содержат фрагменты чужеродной ДНК, они трансгенный или генетически модифицированные микроорганизмы (ГМО ).[3] В этом процессе используется тот факт, что отдельная бактериальная клетка может быть побуждена принять и воспроизвести единственную молекулу рекомбинантной ДНК. Затем эта единственная клетка может быть увеличена экспоненциально, чтобы произвести большое количество бактерий, каждая из которых содержит копии исходной рекомбинантной молекулы. Таким образом, как полученная популяция бактерий, так и молекула рекомбинантной ДНК обычно называют «клонами». Строго говоря, рекомбинантная ДНК относится к молекулам ДНК, а молекулярное клонирование относится к экспериментальным методам, используемым для их сборки. Возникла идея, что различные последовательности ДНК могут быть вставлены в плазмиду и что эти чужеродные последовательности будут переноситься в бактерии и перевариваться как часть плазмиды. То есть эти плазмиды могут служить векторами клонирования для переноса генов. [4]
Практически любую последовательность ДНК можно клонировать и амплифицировать, но есть некоторые факторы, которые могут ограничить успех процесса. Примерами последовательностей ДНК, которые трудно клонировать, являются инвертированные повторы, точки начала репликации, центромеры и теломеры. Еще одна характеристика, ограничивающая шансы на успех, - это большой размер последовательности ДНК. Вставки размером более 10 кб имеют очень ограниченный успех, но бактериофаги, такие как бактериофаг λ, могут быть модифицированы для успешной вставки последовательности до 40 кб.[5]
История
До 1970-х годов понимание генетики и молекулярной биологии серьезно затруднялось из-за неспособности изолировать и изучать отдельные гены от сложных организмов. Ситуация резко изменилась с появлением методов молекулярного клонирования. Микробиологи, пытаясь понять молекулярные механизмы, с помощью которых бактерии ограничивают рост бактериофагов, изолировали эндонуклеазы рестрикции, ферменты, которые могут расщеплять молекулы ДНК только при обнаружении определенных последовательностей ДНК.[6] Они показали, что рестрикционные ферменты расщепляют молекулы ДНК длиной хромосомы в определенных местах, и что определенные участки более крупной молекулы можно очистить фракционированием по размеру. Используя второй фермент, ДНК лигаза, фрагменты, генерируемые рестрикционными ферментами, могут быть объединены в новые комбинации, называемые рекомбинантная ДНК. Путем рекомбинации представляющих интерес сегментов ДНК с векторной ДНК, такой как бактериофаг или плазмиды, которые естественным образом реплицируются внутри бактерий, можно получить большие количества очищенных рекомбинантных молекул ДНК в бактериальных культурах. Первые рекомбинантные молекулы ДНК были созданы и изучены в 1972 году.[7][8]
Обзор
Молекулярное клонирование использует тот факт, что химическая структура ДНК принципиально одинаков для всех живых организмов. Следовательно, если какой-либо сегмент ДНК от любого организма вставлен в сегмент ДНК, содержащий молекулярные последовательности, необходимые для Репликация ДНК, и в результате рекомбинантная ДНК вводится в организм, из которого были получены репликационные последовательности, то чужеродная ДНК будет реплицироваться вместе с ДНК клетки-хозяина в трансгенный организм.
Молекулярное клонирование похоже на полимеразной цепной реакции (ПЦР) в том смысле, что он позволяет репликацию последовательности ДНК. Принципиальное различие между двумя методами заключается в том, что молекулярное клонирование включает репликацию ДНК в живом микроорганизме, в то время как ПЦР реплицирует ДНК в in vitro раствор, свободный от живых клеток.
Шаги
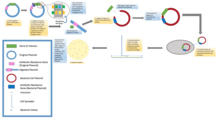
В стандартных экспериментах по молекулярному клонированию клонирование любого фрагмента ДНК по существу включает семь шагов: (1) выбор организма-хозяина и вектора клонирования, (2) получение векторной ДНК, (3) подготовка ДНК для клонирования, (4) создание рекомбинантной ДНК, (5) Введение рекомбинантной ДНК в организм-хозяин, (6) Отбор организмов, содержащих рекомбинантную ДНК, (7) Скрининг на клоны с желаемыми вставками ДНК и биологическими свойствами.
Хотя подробное планирование клонирования может быть выполнено в любом текстовом редакторе вместе с онлайн-утилитами, например, Дизайн праймера для ПЦР, для этой цели существует специальное программное обеспечение. Программное обеспечение для этой цели включает, например, ApE [1] (открытый исходный код), DNAStrider [2] (открытый исходный код), Serial Cloner [3] (бесплатно) и Коллаген [4] (Открытый исходный код).
Примечательно, что растущие возможности и точность платформ для синтеза ДНК позволяют создавать все более сложные конструкции в молекулярной инженерии. Эти проекты могут включать очень длинные цепи новой последовательности ДНК и / или тестировать целые библиотеки одновременно, в отличие от отдельных последовательностей. Эти сдвиги вносят сложность, которая требует от дизайна перехода от плоского представления на основе нуклеотидов к более высокому уровню абстракции. Примеры таких инструментов: GenoCAD, Теселаген [5] (бесплатно для академических кругов) или GeneticConstructor [6] (бесплатно для ученых).
Выбор организма-хозяина и вектора клонирования

Хотя используется очень большое количество организмов-хозяев и векторов молекулярного клонирования, подавляющее большинство экспериментов по молекулярному клонированию начинается с лабораторного штамма бактерии. Кишечная палочка (кишечная палочка ) и вектор клонирования плазмиды. Кишечная палочка и плазмидные векторы широко используются, поскольку они технически сложны, универсальны, широко доступны и обеспечивают быстрый рост рекомбинантных организмов с минимальным оборудованием.[3] Если клонируемая ДНК исключительно велика (от сотен тысяч до миллионов пар оснований), то бактериальная искусственная хромосома[10] или же искусственная хромосома дрожжей часто выбирается вектор.
Для специализированных приложений могут потребоваться специализированные векторные системы хоста. Например, если экспериментаторы хотят получить определенный белок из рекомбинантного организма, тогда вектор выражения выбран, который содержит соответствующие сигналы для транскрипции и трансляции в желаемом организме-хозяине. В качестве альтернативы, если желательна репликация ДНК у разных видов (например, перенос ДНК от бактерий к растениям), тогда вектор диапазона множества хозяев (также называемый шаттл вектор ) можно выбрать. Однако на практике специализированные эксперименты по молекулярному клонированию обычно начинаются с клонирования в бактериальную плазмиду, за которым следует субклонирование в специализированный вектор.
Какая бы комбинация хозяина и вектора ни использовалась, вектор почти всегда содержит четыре сегмента ДНК, которые критически важны для его функции и экспериментальной полезности:[3]
- ДНК источник репликации необходимо для вектора (и связанных с ним рекомбинантных последовательностей) для репликации внутри организма-хозяина
- один или несколько уникальных сайты узнавания рестрикционной эндонуклеазы служит местами, где может быть введена чужеродная ДНК
- а селектируемый генетический маркер ген, который можно использовать для обеспечения выживания клеток, которые приняли векторные последовательности
- а тег ген, который можно использовать для скрининга клеток, содержащих чужеродную ДНК

Подготовка векторной ДНК
Вектор клонирования обрабатывают эндонуклеазой рестрикции для расщепления ДНК в том месте, куда будет вставлена чужеродная ДНК. Рестрикционный фермент выбирается для создания конфигурации в сайте расщепления, совместимой с концами чужеродной ДНК (см. Конец ДНК ). Обычно это делается путем расщепления векторной ДНК и чужеродной ДНК одним и тем же рестрикционным ферментом, например EcoRI. Большинство современных векторов содержат множество удобных сайтов расщепления, которые уникальны внутри векторной молекулы (так что вектор может быть расщеплен только в одном сайте) и расположены внутри гена (часто бета-галактозидаза ), инактивация которых может быть использована для отличия рекомбинантных организмов от нерекомбинантных на более позднем этапе процесса. Чтобы улучшить соотношение рекомбинантных и нерекомбинантных организмов, расщепленный вектор можно обработать ферментом (щелочная фосфатаза ), который дефосфорилирует концы вектора. Векторные молекулы с дефосфорилированными концами не могут реплицироваться, и репликация может быть восстановлена только в том случае, если чужеродная ДНК интегрирована в сайт расщепления.[11]
Подготовка ДНК для клонирования
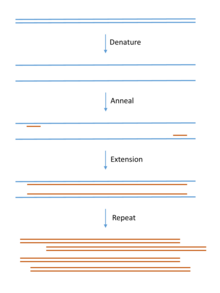
Для клонирования геномной ДНК клонируемую ДНК выделяют из интересующего организма. Можно использовать практически любой источник ткани (даже ткани из вымершие животные ),[12] пока ДНК не сильно деградировала. Затем ДНК очищают с использованием простых методов для удаления загрязняющих белков (экстракция фенолом), РНК (рибонуклеазы) и более мелких молекул (осаждение и / или хроматография). Полимеразной цепной реакции (ПЦР) методы часто используются для амплификации конкретной ДНК или РНК (ОТ-ПЦР ) последовательности до молекулярного клонирования.
ДНК для экспериментов по клонированию также может быть получена из РНК с использованием обратной транскриптазы (комплементарная ДНК или клонирование кДНК), или в виде синтетической ДНК (искусственный синтез генов ). Клонирование кДНК обычно используется для получения клонов, представляющих популяцию мРНК представляющих интерес клеток, в то время как синтетическая ДНК используется для получения любой точной последовательности, определенной разработчиком. Такая разработанная последовательность может потребоваться при перемещении генов через генетические коды (например, от митохрондрий к ядру)[13] или просто для увеличения выражения через оптимизация кодонов.[14]
Затем очищенную ДНК обрабатывают рестрикционным ферментом, чтобы получить фрагменты с концами, которые могут быть связаны с концами вектора. При необходимости короткие двухцепочечные сегменты ДНК (линкеры), содержащие желаемые сайты рестрикции, могут быть добавлены для создания концевых структур, совместимых с вектором.[3][11]
Создание рекомбинантной ДНК с ДНК-лигазой
Создание рекомбинантной ДНК во многих отношениях является самым простым этапом процесса молекулярного клонирования. ДНК, полученную из вектора и чужеродного источника, просто смешивают вместе в соответствующих концентрациях и подвергают действию фермента (ДНК-лигаза ), который ковалентно связывает концы вместе. Эту реакцию присоединения часто называют перевязка. Полученная смесь ДНК, содержащая произвольно соединенные концы, затем готова для введения в организм-хозяин.
ДНК-лигаза распознает только концы линейных молекул ДНК и воздействует на них, что обычно приводит к сложной смеси молекул ДНК со случайно соединенными концами. Желаемые продукты (векторная ДНК, ковалентно связанная с чужеродной ДНК) будут присутствовать, но обычно присутствуют и другие последовательности (например, чужеродная ДНК, связанная сама с собой, векторная ДНК, связанная сама с собой, и комбинации вектора и чужеродной ДНК более высокого порядка). Эта сложная смесь сортируется на последующих этапах процесса клонирования после того, как смесь ДНК вводится в клетки.[3][11]
Введение рекомбинантной ДНК в организм хозяина
Смесь ДНК, ранее обработанная in vitro, перемещается обратно в живую клетку, называемую организмом-хозяином. Методы, используемые для введения ДНК в клетки, разнообразны, и название этого этапа в процессе молекулярного клонирования часто будет зависеть от выбранного экспериментального метода (например, трансформация, трансдукция, трансфекция, электропорация ).[3][11]
Когда микроорганизмы могут поглощать и воспроизводить ДНК из своей локальной среды, этот процесс называется трансформация, а клетки, находящиеся в таком физиологическом состоянии, что они могут принимать ДНК, называются компетентный.[15] В культуре клеток млекопитающих аналогичный процесс введения ДНК в клетки обычно называют трансфекция. Как трансформация, так и трансфекция обычно требуют подготовки клеток с помощью специального режима роста и процесса химической обработки, который будет варьироваться в зависимости от конкретных видов и типов клеток, которые используются.
Электропорация использует электрические импульсы высокого напряжения для перемещения ДНК через клеточную мембрану (и клеточную стенку, если таковая имеется).[16] В отличие, трансдукция включает упаковку ДНК в частицы, полученные из вируса, и использование этих вирусоподобных частиц для введения инкапсулированной ДНК в клетку посредством процесса, напоминающего вирусную инфекцию. Хотя электропорация и трансдукция являются узкоспециализированными методами, они могут быть наиболее эффективными методами перемещения ДНК в клетки.
Отбор организмов, содержащих векторные последовательности
Какой бы метод ни использовался, введение рекомбинантной ДНК в выбранный организм-хозяин обычно является процессом с низкой эффективностью; то есть только небольшая часть клеток действительно будет принимать ДНК. Ученые-экспериментаторы решают эту проблему с помощью этапа искусственной генетической селекции, на котором клетки, которые не впитали ДНК, избирательно убиваются, и выживают только те клетки, которые могут активно реплицировать ДНК, содержащую ген селектируемого маркера, кодируемый вектором.[3][11]
Когда бактериальные клетки используются в качестве организмов-хозяев, выбираемый маркер обычно является геном, который придает устойчивость к антибиотик которые в противном случае убили бы клетки, обычно ампициллин. Клетки, несущие плазмиду, выживут при воздействии антибиотика, в то время как те, которые не смогли принять плазмидные последовательности, погибнут. Когда используются клетки млекопитающих (например, клетки человека или мыши), используется аналогичная стратегия, за исключением того, что маркерный ген (в этом случае обычно кодируется как часть kanMX кассета) придает устойчивость к антибиотику Генетицин.
Скрининг клонов с желаемыми вставками ДНК и биологическими свойствами
Современные векторы бактериального клонирования (например, pUC19 и более поздние производные, включая векторы pGEM) используют сине-белая система досмотра отличать колонии (клоны) трансгенных клеток от тех, которые содержат родительский вектор (т.е. вектор ДНК без вставленной рекомбинантной последовательности). В этих векторах чужеродная ДНК вставлена в последовательность, кодирующую существенную часть бета-галактозидаза, фермент, активность которого приводит к образованию колонии синего цвета на питательной среде, которая используется для этой работы. Введение чужеродной ДНК в последовательность, кодирующую бета-галактозидазу, отключает функцию фермента, так что колонии, содержащие трансформированную ДНК, остаются бесцветными (белыми). Таким образом, экспериментаторы могут легко идентифицировать и проводить дальнейшие исследования трансгенных бактериальных клонов, игнорируя при этом те, которые не содержат рекомбинантной ДНК.
Общую популяцию индивидуальных клонов, полученных в эксперименте по молекулярному клонированию, часто называют Библиотека ДНК. Библиотеки могут быть очень сложными (как при клонировании полной геномной ДНК из организма) или относительно простыми (как при перемещении ранее клонированного фрагмента ДНК в другую плазмиду), но почти всегда необходимо исследовать ряд различных клонов, чтобы быть уверенным. что желаемая конструкция ДНК получена. Это может быть достигнуто с помощью очень широкого набора экспериментальных методов, включая использование гибридизации нуклеиновых кислот, зонды антител, полимеразной цепной реакции, анализ рестрикционных фрагментов и / или Секвенирование ДНК.[3][11]
Приложения
Молекулярное клонирование предоставляет ученым практически неограниченное количество любых отдельных сегментов ДНК, полученных из любого генома. Этот материал можно использовать для самых разных целей, в том числе как в фундаментальной, так и в прикладной биологии. Здесь кратко излагаются некоторые из наиболее важных приложений.
Организация генома и экспрессия генов
Молекулярное клонирование привело непосредственно к выяснению полной последовательности ДНК геномов очень большого числа видов и к исследованию генетического разнообразия в пределах отдельных видов, работа, которая была проделана в основном путем определения последовательности ДНК большого числа случайных клонированные фрагменты генома и сборка перекрывающихся последовательностей.
На уровне отдельных генов молекулярные клоны используются для создания зонды которые используются для изучения того, как гены выразил и как это выражение связано с другими процессами в биологии, включая метаболическую среду, внеклеточные сигналы, развитие, обучение, старение и гибель клеток. Клонированные гены также могут служить инструментами для изучения биологической функции и важности отдельных генов, позволяя исследователям инактивировать гены, или сделать более тонкие мутации, используя региональный мутагенез или сайт-направленный мутагенез. Гены клонированы в векторы экспрессии для функциональное клонирование предоставить средства для скрининга генов на основе функции экспрессируемого белка.
Производство рекомбинантных белков
Получение молекулярного клона гена может привести к развитию организмов, которые продуцируют белковый продукт клонированных генов, называемый рекомбинантным белком. На практике часто сложнее разработать организм, который продуцирует активную форму рекомбинантного белка в желаемых количествах, чем клонировать ген. Это связано с тем, что молекулярные сигналы для экспрессии генов сложны и вариабельны, а также потому, что сворачивание, стабильность и транспорт белков могут быть очень сложными.
Многие полезные белки в настоящее время доступны в виде рекомбинантные продукты. К ним относятся - (1) полезные с медицинской точки зрения белки, введение которых может исправить дефектный или плохо экспрессируемый ген (например, рекомбинантный фактор VIII, фактор свертывания крови, дефицитный в некоторых формах гемофилия,[17] и рекомбинантный инсулин, используется для лечения некоторых форм сахарный диабет[18]), (2) белки, которые можно вводить для оказания помощи в угрожающих жизни чрезвычайных ситуациях (например, тканевый активатор плазминогена, используется для лечения инсультов[19]), (3) рекомбинантные субъединичные вакцины, в которых очищенный белок можно использовать для иммунизации пациентов против инфекционных заболеваний, не подвергая их воздействию самого инфекционного агента (например, вакцина против гепатита В[20]) и (4) рекомбинантные белки в качестве стандартного материала для диагностических лабораторных тестов.
Трансгенные организмы
После характеризации и обработки для обеспечения сигналов для соответствующей экспрессии клонированные гены могут быть вставлены в организмы, генерируя трансгенные организмы, также называемые генетически модифицированные организмы (ГМО). Хотя большинство ГМО генерируются для целей фундаментальных биологических исследований (см., Например, трансгенная мышь ), ряд ГМО был разработан для коммерческого использования, начиная от животных и растений, которые производят фармацевтические препараты или другие соединения (фарминг ), культурные растения, устойчивые к гербицидам, и флуоресцентные тропические рыбы (GloFish ) для домашних развлечений.[1]
Генная терапия
Генная терапия включает введение функционального гена в клетки, лишенные этой функции, с целью исправления генетического нарушения или приобретенного заболевания. Генную терапию можно условно разделить на две категории. Первый - это изменение половых клеток, то есть сперматозоидов или яйцеклеток, которое приводит к постоянным генетическим изменениям для всего организма и последующих поколений. Многие считают эту «генную терапию зародышевой линии» неэтичной для людей.[21] Второй тип генной терапии, «генная терапия соматических клеток», аналогичен трансплантации органов. В этом случае одна или несколько конкретных тканей подвергаются прямому лечению или удалению ткани, добавлению терапевтического гена или генов в лаборатории и возвращению обработанных клеток пациенту. Клинические испытания генной терапии соматических клеток начались в конце 1990-х годов, в основном для лечения рака и заболеваний крови, печени и легких.[22]
Несмотря на широкую огласку и обещания, история генной терапии человека характеризовалась относительно ограниченным успехом.[22] Эффект введения гена в клетки часто способствует лишь частичному и / или временному облегчению симптомов заболевания, которое лечат. Некоторые пациенты, проходящие испытания генной терапии, испытали неблагоприятные последствия самого лечения, включая смерть. В некоторых случаях побочные эффекты возникают в результате нарушения работы основных генов в геноме пациента путем инсерционной инактивации. В других случаях вирусные векторы, используемые для генной терапии, были заражены инфекционным вирусом. Тем не менее, генная терапия по-прежнему считается многообещающей областью медицины будущего и областью, где существует значительный уровень исследований и разработок.
Рекомендации
- ^ а б Уотсон Дж. Д. (2007). Рекомбинантная ДНК: гены и геномы: краткий курс. Сан-Франциско: W.H. Фримен. ISBN 978-0-7167-2866-5.
- ^ Паттен С.Л., Глик Б.Р., Пастернак Дж. (2009). Молекулярная биотехнология: принципы и применение рекомбинантной ДНК. Вашингтон, округ Колумбия: ASM Press. ISBN 978-1-55581-498-4.
- ^ а б c d е ж грамм час Браун Т. (2006). Клонирование генов и анализ ДНК: введение. Кембридж, Массачусетс: Blackwell Pub. ISBN 978-1-4051-1121-8.
- ^ М., Гришэм, Чарльз (01.01.2013). Биохимия. Брукс / Коул, Cengage Learning. ISBN 978-1133106296. OCLC 777722371.
- ^ Гаррет, Гришем (2010). Биохимия. Бельмонт, Калифорния, Брукс / Коул: обучение Cengage. п. 380.
- ^ Натанс Д., Смит Х.О. (1975). «Эндонуклеазы рестрикции в анализе и реструктуризации молекул ДНК». Ежегодный обзор биохимии. 44: 273–93. Дои:10.1146 / annurev.bi.44.070175.001421. PMID 166604.
- ^ Коэн С.Н., Чанг А.С., Бойер Х.В., Хеллинг РБ (ноябрь 1973 г.). «Конструирование биологически функциональных бактериальных плазмид in vitro». Труды Национальной академии наук Соединенных Штатов Америки. 70 (11): 3240–4. Bibcode:1973PNAS ... 70.3240C. Дои:10.1073 / пнас.70.11.3240. ЧВК 427208. PMID 4594039.
- ^ Джексон Д.А., Саймонс Р.Х., Берг П. (октябрь 1972 г.). «Биохимический метод встраивания новой генетической информации в ДНК обезьяньего вируса 40: кольцевые молекулы ДНК SV40, содержащие гены лямбда-фага и оперон галактозы Escherichia coli». Труды Национальной академии наук Соединенных Штатов Америки. 69 (10): 2904–9. Bibcode:1972PNAS ... 69.2904J. Дои:10.1073 / пнас.69.10.2904. ЧВК 389671. PMID 4342968.
- ^ "плазмиды / плазмиды | Изучение науки в Scitable". www.nature.com. Получено 2017-12-06.
- ^ Шизуя Х., Биррен Б., Ким У. Дж., Мансино В., Слепак Т., Тачиири И., Саймон М. (сентябрь 1992 г.). «Клонирование и стабильное поддержание фрагментов ДНК человека длиной 300 тыс. Пар оснований в Escherichia coli с использованием вектора на основе F-фактора». Труды Национальной академии наук Соединенных Штатов Америки. 89 (18): 8794–7. Bibcode:1992PNAS ... 89.8794S. Дои:10.1073 / пнас.89.18.8794. ЧВК 50007. PMID 1528894.
- ^ а б c d е ж Рассел Д. В., Сэмбрук Дж. (2001). Молекулярное клонирование: лабораторное руководство. Колд-Спринг-Харбор, штат Нью-Йорк: Лаборатория Колд-Спринг-Харбор. ISBN 978-0-87969-576-7.
- ^ Хигучи Р., Боуман Б., Фрейбергер М., Райдер О.А., Уилсон А.С. (1984). «Последовательности ДНК квагги, вымершего члена семейства лошадиных». Природа. 312 (5991): 282–4. Bibcode:1984Натура.312..282H. Дои:10.1038 / 312282a0. PMID 6504142. S2CID 4313241.
- ^ Boominathan, A; Vanhoozer, S; Басисты, Н; Пауэрс, К; Крэмптон, Алабама; Ван, Х; Фридрикс, N; Шиллинг, B; Бренд, MD; О'Коннор, MS (2 ноября 2016 г.). «Стабильная ядерная экспрессия генов ATP8 и ATP6 спасает нулевой мутант Комплекса V мтДНК». Исследования нуклеиновых кислот. 44 (19): 9342–9357. Дои:10.1093 / нар / gkw756. ЧВК 5100594. PMID 27596602.
- ^ Плоткин, Дж. Б .; Кудла, Г. (2011). «Синоним, но не одно и то же: причины и последствия смещения кодонов». Природа Обзоры Генетика. 12 (1): 32–42. Дои:10.1038 / nrg2899. ЧВК 3074964. PMID 21102527.
- ^ Ледерберг Дж (февраль 1994 г.). «Трансформация генетики с помощью ДНК: празднование годовщины Эйвери, Маклауда и Маккарти (1944)». Генетика. 136 (2): 423–6. ЧВК 1205797. PMID 8150273.
- ^ Вирт Р., Фризенеггер А., Фидлер С. (март 1989 г.). «Трансформация различных видов грамотрицательных бактерий, принадлежащих к 11 различным родам, путем электропорации». Молекулярная и общая генетика. 216 (1): 175–7. Дои:10.1007 / BF00332248. PMID 2659971. S2CID 25214157.
- ^ Ольденбург Дж., Долан Дж., Лемм Дж. (Январь 2009 г.). «Лечение гемофилии тогда, сейчас и в будущем». Гемофилия. 15 Дополнение 1: 2–7. Дои:10.1111 / j.1365-2516.2008.01946.x. PMID 19125934. S2CID 29118026.
- ^ MJ (ноябрь 1989 г.). «Человеческий инсулин: первый препарат ДНК-технологии». Американский журнал больничной аптеки. 46 (11 Прил. 2): S9-11. PMID 2690608.
- ^ Левандовски С., Барсан В. (февраль 2001 г.). «Лечение острого ишемического инсульта». Анналы неотложной медицины. 37 (2): 202–16. Дои:10.1067 / mem.2001.111573. PMID 11174240.
- ^ Chang MH, Chen CJ, Lai MS, Hsu HM, Wu TC, Kong MS, Liang DC, Shau WY, Chen DS (июнь 1997 г.). «Универсальная вакцинация против гепатита В на Тайване и заболеваемость гепатоцеллюлярной карциномой у детей. Тайваньская группа по изучению гепатомы у детей». Медицинский журнал Новой Англии. 336 (26): 1855–9. Дои:10.1056 / NEJM199706263362602. PMID 9197213.
- ^ Август JT (1997). Генная терапия. 40. Академическая пресса. п. 508. ISBN 978-0-08-058132-3.
- ^ а б Пфейфер А, Верма И.М. (2001). «Генная терапия: перспективы и проблемы». Ежегодный обзор геномики и генетики человека. 2: 177–211. Дои:10.1146 / annurev.genom.2.1.177. PMID 11701648.
дальнейшее чтение
- Мацумура, Ичиро (сентябрь 2015 г.). «Почему Джонни не может клонировать: распространенные ошибки и не очень распространенные решения». Биотехнологии. 53 (3): IV – XIII. Дои:10.2144/000114324. PMID 26345511. Получено 2 февраля 2016.
внешняя ссылка
| Библиотечные ресурсы о Молекулярное клонирование |
 СМИ, связанные с Молекулярное клонирование в Wikimedia Commons
СМИ, связанные с Молекулярное клонирование в Wikimedia Commons
