Токсин сибирской язвы - Anthrax toxin
| Средний домен летального фактора токсина сибирской язвы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
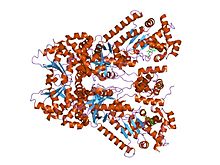 Рентгеновская кристаллическая структура летального фактора сибирской язвы, связанного с низкомолекулярным ингибитором bi-mfm3, 3- {5- [5- (4-хлорфенил) фуран-2-илметилен] -4-оксо-2- тиоксотиазолидин-3-ил} пропионовая кислота. | |||||||||
| Идентификаторы | |||||||||
| Символ | Anthrax-tox_M | ||||||||
| Pfam | PF09156 | ||||||||
| ИнтерПро | IPR015239 | ||||||||
| SCOP2 | 1j7n / Объем / СУПФАМ | ||||||||
| OPM суперсемейство | 35 | ||||||||
| |||||||||
| N- и C-концевые домены летального фактора сибирской язвы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
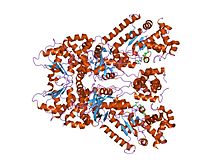 кристаллическая структура летального фактора сибирской язвы в комплексе с тиоацетил-тир-прометамидом, металлохелатирующим пептидиловым ингибитором малых молекул | |||||||||
| Идентификаторы | |||||||||
| Символ | ATLF | ||||||||
| Pfam | PF07737 | ||||||||
| ИнтерПро | IPR014781 | ||||||||
| МЕРОПЫ | M34 | ||||||||
| SCOP2 | 1pwq / Объем / СУПФАМ | ||||||||
| |||||||||
| Субъединица LF сибирской язвы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Anthrax_toxA | ||||||||
| Pfam | PF03497 | ||||||||
| SCOP2 | 1jky / Объем / СУПФАМ | ||||||||
| |||||||||

Токсин сибирской язвы это трех-белок экзотоксин секретно ядовитый штаммы бактерия, бацилла сибирской язвы - возбудитель сибирская язва. Токсин был впервые обнаружен Гарри Смитом в 1954 году.[1] Токсин сибирской язвы состоит из связывающего клетки белка, известного как защитный антиген (PA), и два компонента фермента, называемые фактором отека (EF) и смертельный фактор (LF). Эти три белковых компонента действуют вместе, чтобы передать свои физиологические эффекты. Собранные комплексы, содержащие компоненты токсина, представляют собой эндоцитозированный. в эндосома, ферментные компоненты токсина перемещать в цитоплазма целевой клетки. Попадая в цитозоль, ферментные компоненты токсина нарушают различные функции иммунных клеток, а именно передачу сигналов и миграцию клеток. Токсин может даже вызывать лизис клеток, как это наблюдается при макрофаг клетки. Токсин сибирской язвы позволяет бактериям избегать иммунная система, размножаются и в конечном итоге убивают животное-хозяина.[2] Исследование токсина сибирской язвы также дает представление о генерации макромолекулярные сборки, и дальше транслокация белков, порообразование, эндоцитоз, и другие биохимический процессы.
бацилла сибирской язвы факторы вирулентности
Сибирская язва - это заболевание, вызываемое: бацилла сибирской язвы, спорообразующий, Грамм положительный, палочковидная бактерия (рис. 1). Летальность болезни обусловлена двумя основными факторами вирулентности бактерии: (i) полиглутаминовая кислота капсула, которая анти-фагоцитарный и (ii) трехкомпонентный белковый токсин, называемый токсином сибирской язвы. Токсин сибирской язвы представляет собой смесь трех белок компоненты: (i) защитные антиген (PA), (ii) отек фактор (EF) и (iii) летальный фактор (LF).
Токсин сибирской язвы - это А / Б токсин
Каждый отдельный белок токсина сибирской язвы нетоксичен. Симптомы токсичности не наблюдаются при индивидуальном введении этих белков лабораторным животным. Совместное введение PA и EF вызывает отек, а совместная инъекция PA и LF смертельна. Первая комбинация называется отечным токсином, а вторая комбинация - летальным токсином. Таким образом, проявление физиологических симптомов в любом случае требует ПА.
Потребность в PA, наблюдаемая в экспериментах на животных моделях, демонстрирует общую парадигму для бактериальных токсинов, называемую А / B парадигма. В А компонент ферментативно активен, а B Компонент является компонентом связывания клеток. Токсин сибирской язвы имеет форму А2B, где два ферменты, EF и LF, являются А компонентов, а PA - это B компонент. Таким образом, PA действует как Троянский конь, который переносит EF и LF через плазматическая мембрана в цитозоль, где они могут затем катализировать реакции, нарушающие нормальную физиологию клетки.[нужна цитата ]
Сборка и перемещение токсина сибирской язвы

Для функционирования белковые компоненты токсина сибирской язвы должны собираться в комплексы голотоксина. Чтобы LF и EF функционировали внутри клетки-мишени, они должны локализоваться в клетке и проникать в ее цитоплазму. Посредством ряда шагов PA может перемещать EF и LF в ячейку (рис. 2). Этот процесс начинается, когда форма PA 83 кДа, называемая PA83, связывается с рецептор токсина сибирской язвы. Есть два известных гомологичных рецептора, которые связываются с PA83, которые называются опухолевыми. эндотелий маркер-8 (ТЕМ8 ) и капилляр морфогенез белок 2 (CMG2 ).[3] Затем фрагмент 20 кДа (PA20) отщепляется от аминоконца PA83 мембранными эндопротеазами из семейства фуринов. Когда PA20 диссоциирует, оставшаяся часть PA, связанная с рецептором, называемая PA63, может собираться в любой гептамерный[4] или октамерный[5] кольцеобразный олигомер. Этот кольцеобразный олигомер часто называют пре-поровой (или преканальной) формой PA, поскольку позже на своем пути он станет порой (или каналом) транслоказы. Поверхность препорового олигомера, которая подверглась воздействию при высвобождении фрагмента PA20, затем может связываться с LF и EF.[6] Гептамерная и октамерная формы олигомера PA могут затем связываться с тремя или четырьмя молекулами EF и / или LF соответственно.[5][7] Затем клетка эндоцитозирует эти собранные комплексы и переносит их в кислый отсек клетки. Низкий pH обнаруженный в эндосоме заставляет преканал PA63 превращаться в катион-селективный канал. EF и LF управляются через канал градиентом pH, позволяя факторам фермента проникать в цитозоль.[8]
Ферментативная функция LF и EF
Попав в цитозоль, EF и LF затем осуществляют свои соответствующие процессы, вызывающие повреждение.[9]
- EF действует как Ca2+ и кальмодулин зависимый аденилат циклаза что значительно увеличивает уровень лагерь в камере. Это увеличение цАМФ расстраивает воду гомеостаз, серьезно нарушает баланс внутриклеточного сигнальные пути, и ухудшает функцию макрофагов, позволяя бактериям еще больше уклоняться от иммунной системы.
- LF также помогает бактериям уклоняться от иммунной системы, убивая макрофаги. Попадая в эти клетки, LF действует как Zn2+-зависимый эндопротеаза который отрезает N-конец митоген-активируемые киназы протеинкиназы (MAPKK). Это ингибирует эти киназы, не позволяя им эффективно связываться со своими субстратами, что приводит к изменению сигнальных путей и, в конечном итоге, к апоптоз.
Таким образом, синергетический эффект этих трех белков приводит к гибели клетки в результате каскада событий, которые позволяют белкам проникать в клетку и нарушать клеточную функцию.
Взаимосвязь между структурой и функцией внеклеточного токсина
Механизм действия токсина сибирской язвы является результатом молекулярных структур трех токсиновых белков в сочетании с биомолекулами клетки-хозяина. Молекулярные взаимодействия становятся очевидными после выполнения детального анализа структур PA, EF, LF и клеточных рецепторов (ANTXR1 и ANTXR2 ). Структуры молекул токсина (рис. 3–5), рецептора и комплексов молекул позволяют понять синергетические действия этих белков. Анализ сайтов связывания и конформационных изменений дополнил структурные исследования, выяснив функции каждого домена PA, LF и EF, как кратко изложено в таблице 1.
Первой была определена структура ПА (рис. 3).[10] Эта структура и структура его клеточного рецептора проливают свет на специфичность распознавания и связывания.[11] Эта специфичность PA и рецептора CMG2 (аналогично интегинам типа I) обусловлена взаимодействиями через сайт зависимой от ионов металла адгезии (MIDAS), гидрофобную бороздку и выступ β-шпильки. Все они способствуют тесному взаимодействию, в котором большая часть поверхности белка на CMG2 (и TEM8) погребена.[12]

Petosa et al. решила структуру гептамера PA63 при 4,5 Å (0,45 нм).[10] Структура, которую они решили, представляла собой немембранно-связанную пре-пору, конформацию гептамера до того, как комплекс расширит β-бочку через плазматическую мембрану, чтобы перемещать LF и EF в цитозоль.
Фрагмент PA20 стерически препятствует гептамеризации и образованию пор, но когда он удаляется с верхней части мономера, пре-поры формируются быстро. Образование гептамера не вызывает серьезных изменений в конформации каждого отдельного мономера, но при объединении более 15400 Ų (154 нм2) поверхности белка похоронен. Эта скрытая поверхность состоит в основном из полярных или заряженных боковых групп из доменов 1 и 2.[10]
PA также образует октамерную предканальную структуру.[5] Было показано, что октамерная форма более термостабильна, чем гептамерная форма, и, следовательно, октамерный олигомер может сохраняться в плазме хозяина во время инфекции сибирской язвы.[5]

Во время олигомеризации PA63 молекулы EF и / или LF быстро и одновременно связываются с преканалом PA. Это связывание происходит потому, что после удаления домена PA20 открывается большая гидрофобная поверхность на домене 1 PA63. Домен 1 обеспечивает большую поверхность, которая взаимодействует с N-концом EF и LF,[13] который почти полностью гомологичен для первых ~ 36 остатков и аналогичен по третичной структуре для первых ~ 250 остатков.[14] Исследования области связывания LF и EF показали, что большая площадь поверхности контактирует с доменом 1 двух соседних молекул PA63, когда они находятся в конформации гептамера.[15] Эта большая область связывания объясняет, почему предыдущие исследования могли связывать только до трех молекул гептамера PA63. Сокристаллическая структура октамера PA в комплексе с N-концевым LF показала, что связывающее взаимодействие фактически представляет собой два прерывистых сайта.[13] Один сайт, названный C-концевым подсайтом, напоминает классическую «горячую точку» с предсказанными солевыми мостиками и электростатическими взаимодействиями. Другой сайт, называемый субсайтом альфа-зажима, представляет собой глубокую щель, которая неспецифически связывает N-концевую альфа-спираль и короткую бета-цепь LF, направляя N-конец субстрата к просвету преканала PA. Таким образом, альфа-зажим способствует транслокации белка, неспецифическому связыванию и последующему разворачиванию вторичной структуры по мере ее разворачивания из субстрата.[16] Сайт связывания LF / EF в настоящее время используется для доставки терапевтических средств посредством слитых белков.
После образования препоры и присоединения LF и / или EF гептамер мигрирует на липидный слой, где он быстро эндоцитозируется. Эндоцитоз происходит в результате серии событий. Это начинается, когда CMG2 или TEM8 пальмитоилированы, что ингибирует ассоциацию рецептора с липидными рафтами. Это препятствует эндоцитозу рецептора до того, как РА83 будет расщеплен и до того, как LF или EF смогут связываться с гептамером. Реассоциация рецептора с холестерин и микродомены, богатые гликосфиголипидами (липидные рафты ) возникает, когда PA63 связывается с рецептором и гептамеризируется. Как только рецептор и PA возвращаются на липидный слой, E3-убиквитинлигаза Cb1 убиквитинирует цитоплазматический хвост рецептора, передавая сигнал рецептору и связанным с ним токсиновым белкам для эндоцитоза. Dynamin и Eps15 необходимы для возникновения этого эндоцитоза, что указывает на то, что токсин сибирской язвы попадает в клетку через клатрин -зависимый путь.[17]
Как уже обсуждалось, каждая молекула взаимодействует с несколькими другими, чтобы вызвать эндоцитоз токсина сибирской язвы. Оказавшись внутри, комплекс переносится в кислый отсек, где гептамер, все еще находящийся в конформации препоры, не охватывающей мембраны, подготавливается для транслокации EF и LF в цитозоль.[18]
Отношение структура-функция от везикулы до цитозоля
Формирование пор
На первый взгляд, первичная последовательность PA не похожа на последовательность трансмембранного белка. А гидрофобность на графике отсутствуют какие-либо паттерны, общие для возможных мембранных доменов. Структуры других мультимерных мембранных белков (таких как дифтерийный токсин ) дают ответ на вопрос, как PA удается преодолеть мембрану. Считается, что PA действует как эти мультимерные мембранные белки, которые образуют β-бочки, состоящие из участков как полярных, так и неполярных аминокислоты от каждого мономера.[10]

Формированию поры β-цилиндра способствует снижение pH. Чтобы сформировать цилиндр, когда pH падает, домен 2 PA63 должен претерпеть наибольшее изменение конформации. При рассмотрении структуры домена 2 (рис. 7) видно, что этот домен содержит Греческий ключ мотив (золотая часть на рис. 7). Общая схема мотива с греческим ключом показана на рис. 8. К греческому ключу в домене 2 прикреплена большая неупорядоченная петля. Необходимость этой петли в порообразовании показана с помощью мутагенеза и протеолиза петли химотрипсином. Дополнительные электрофизиологические измерения замен цистеина помещают аминокислоты этой петли внутрь просвета поры, в которую вставлена мембрана. Неупорядоченная петля в домене 2 также имеет паттерн чередования гидрофобных и гидрофильных аминокислот, который является паттерном, сохраняющимся в покрывающих мембрану частях поринов. Единственная проблема заключается в том, что петля недостаточно велика, чтобы охватить мембрану β-цилиндра. Встраивание в мембрану могло происходить только при дополнительных конформационных изменениях. Большое конформационное изменение происходит там, где разворачивается мотив греческого ключа, образуя β-шпильку, которая выступает вниз в мембрану и образует β-бочку с другими 6 мономерами комплекса (рисунки 9a и 9b). Конечная пора имеет диаметр 12 Å (1,2 нм), что соответствует теоретическому значению этой модели.[10]
Эта модель потребует больших конформационных изменений в домене 2 наряду с разрывом многих водородных связей, поскольку мотив греческого ключа отслаивается от центра домена. Petosa et al. предложил модель того, как это происходит.[10] Встраивание ключевых мотивов PA греческого происхождения в мембрану происходит при подкислении гептамера. На искусственных двойных слоях это происходит, когда pH снижается с 7,4 до 6,5, что позволяет предположить, что триггер для введения включает титрование гистидинов. Это действительно соответствует последовательности PA, поскольку домен 2 содержит некоторое количество гистидинов (показано звездочками на рисунке 9a). В неупорядоченной петле обнаружены три остатка гистидина, один из которых находится с гистидином с греческим ключом в кластере полярных аминокислот. Этот кластер (включая два гистидина, три аргинина и один глутамат) встроен в верхнюю часть ключевого греческого мотива, поэтому легко увидеть, что протонирование этих гистидинов разрушило бы кластер. Кроме того, другой гистидин расположен в основании ключевого греческого мотива вместе с рядом гидрофобных остатков (в зеленом сегменте на фигурах 7 и 9a). При pH 7,4 этот сегмент упорядочен, но при выращивании кристаллов при pH 6,0 он становится неупорядоченным. Этот переход от порядка к беспорядку является начальным этапом введения мембраны ПА.
PA эндоцитозируется как растворимый гептамер, прикрепленный к его рецепторам, с LF или EF, присоединенными к гептамеру в качестве груза. Первым шагом после эндоцитоза является закисление эндоцитотического пузырька. Подкисление играет две роли в продолжительности жизни токсина. Во-первых, это помогает ослабить плотный захват рецептора CMG2 или TEM8 на PA, облегчая формирование пор (разные рецепторы допускают введение при немного другом pH).[12] Во-вторых, снижение pH приводит к тому, что неупорядоченная петля и мотив греческого ключа в домене PA 2 складываются из препоры гептамера и вставляются через стенку кислой везикулы, что приводит к образованию пор (рисунки 7–9). .
Santelli et al. объяснили больше о процессе после того, как они определили кристаллическую структуру комплекса PA / CMG2.[12] Структура этого комплекса показывает связывание CMG2 как доменами 2, так и 4 PA. Это взаимодействие демонстрирует меньшую свободу раскрытия греческого ключа. Дальнейший анализ показывает, что семь из девяти гистидинов в PA находятся на интерфейсе домен 2 / домен 4. Протонирование этих гистидинов приводит к тому, что домены разделяются в достаточной степени, чтобы позволить греческому ключу выскочить и помочь сформировать β-шпильку, участвующую в вставке. Кроме того, когда PA связывается с CMG2, вставка больше не происходит при pH 6,5, как при вставке в искусственную мембрану. Вместо этого для введения в естественные клетки требуется pH 5,0. Было объяснено, что это различие является результатом наличия кармана рядом с мотивом MIDAS в CMG2. Этот карман содержит гистидин, похороненный на дне, где прикрепляется домен 2. Этот гистидин протонируется при более низком pH и увеличивает стабильность PA. Эта дополнительная стабильность не дает греческому ключу двигаться до тех пор, пока не будут выполнены более кислые условия. Все эти гистидины работают вместе, чтобы предотвратить преждевременное внедрение гептамера до возникновения эндоцитоза.
Santelli et al. (Fig. 10) также построили гипотетическую структуру встроенной в мембрану структуры PA / CMG2. Эта модель показывает, что β-бочка имеет длину около 70 Å (7 нм), 30 Å (3 нм) из которых охватывают мембрану, а зазор 40 Å (4 нм) фактически заполнен остальной внеклеточной частью рецептор CMG2 (~ 100 остатков). CMG2 обеспечивает дополнительную поддержку пор.
Транслокация белков

Несколько недавних исследований демонстрируют, как пора PA63 позволяет EF и LF проникать в цитоплазму, когда ее просвет настолько мал. Просвет поры PA63 составляет всего 15 Å (1,5 нм) в поперечнике, что намного меньше диаметра LF или EF. Транслокация происходит в результате серии событий, которые начинаются в эндосоме, когда она подкисляется. LF и EF чувствительны к pH, и при снижении pH их структуры теряют стабильность. Ниже pH 6,0 (pH в эндосоме) LF и EF становятся неупорядоченными. расплавленные глобулы. Когда молекула находится в этой конформации, N-конец высвобождается и втягивается в пору за счет протонного градиента и положительного трансмембранного потенциала. Кольцо из семи фенилаланинов на эндосомной стороне рта поры (фенилаланиновый зажим) помогает разворачиванию LF или EF, взаимодействуя с гидрофобными остатками, обнаруженными в LF или EF. Затем протонный градиент начинает пронизывать белок через пору. Механизм шнуровки приводится в движение градиентом, но для храпового движения требуется фенилаланиновый зажим. Первые 250 остатков EF и LF имеют нерегулярную чередующуюся последовательность основных, кислотных и гидрофобных остатков. Взаимодействие между зажимом фенилаланина и состоянием протонирования вызывает эффект храповика, который приводит в движение белок, хотя до тех пор, пока в цитоплазму не пересечется достаточно, чтобы протащить остаток через поры, когда N-конец перегибается (Рис. 11).
Рекомендации
- ^ Смит Х, Кеппи Дж (1954). «Наблюдения за экспериментальной формой сибирской язвы: демонстрация конкретного летального фактора, продуцируемого in vivo Bacillus anthracis». Природа. 173 (4410): 869–70. Дои:10.1038 / 173869a0. PMID 13165673.
- ^ Мальдонадо-Арочо; и другие. (2009). «Токсин сибирской язвы». Микробные токсины: текущие исследования и будущие тенденции. Caister Academic Press. ISBN 978-1-904455-44-8.
- ^ Штернбах, Г. (2003). «История сибирской язвы». Журнал неотложной медицины. 24 (4): 463–467. Дои:10.1016 / S0736-4679 (03) 00079-9. PMID 12745053.
- ^ Green, B.D .; Battisti, L .; Koehler, T. M .; Thorne, C.B .; Айвинс, Б. Э. (1985). «Демонстрация капсульной плазмиды в Bacillus anthracis». Инфекция и иммунитет. 49 (2): 291–297. ЧВК 262013. PMID 3926644.
- ^ а б c d Кинцер, А. Ф .; Thoren, K. L .; Sterling, H.J .; Dong, K. C .; Feld, G.K .; Tang, I. I .; Zhang, T. T .; Уильямс, E. R .; Berger, J.M .; Кранц, Б.А. (2009). «Защитный антигенный компонент токсина сибирской язвы образует функциональные октамерные комплексы». Журнал молекулярной биологии. 392 (3): 614–629. Дои:10.1016 / j.jmb.2009.07.037. ЧВК 2742380. PMID 19627991.
- ^ Абрами Л., Рейг Н., ван дер Гут Ф. Г. (2005). «Токсин сибирской язвы: долгая и извилистая дорога, ведущая к смерти». Тенденции Microbiol. 13 (2): 72–78. Дои:10.1016 / j.tim.2004.12.004. PMID 15680766.
- ^ Гринберг Л.М., Абрамова Ф.А., Ямпольская О.В., Уокер Д.Х., Смит Дж. Х. (2001). «Количественная патология легочной формы сибирской язвы I: количественные микроскопические данные». Мод Pathol. 14 (5): 482–495. Дои:10.1038 / modpathol.3880337. PMID 11353060.
- ^ Фридлендер AM, Бхатнагар Р., Леппла С.Х., Джонсон Л., Сингх Y (1993). «Характеристика чувствительности макрофагов и устойчивости к летальному токсину сибирской язвы». Заразить иммунную. 61 (1): 245–252. ЧВК 302711. PMID 8380282.
- ^ Сингх Ю., Леппла С.Х., Бхатнагар Р., Фридлендер А.М. (1989). «Интернализация и переработка летального токсина Bacillus anthracis токсин-чувствительными и резистентными клетками». J Biol Chem. 264 (19): 11099–11102. PMID 2500434.
- ^ а б c d е ж Petosa, C .; Collier, R.J .; Климпель, К. Р .; Leppla, S. H .; Лиддингтон, Р. К. (1997). «Кристаллическая структура защитного антигена токсина сибирской язвы». Природа. 385 (6619): 833–838. Дои:10.1038 / 385833a0. PMID 9039918.
- ^ Lacy, D. B .; Wigelsworth, D. J .; Scobie, H.M .; Young, J. A .; Кольер, Р. Дж. Кристаллическая структура домена фактора фон Виллебранда А человеческого белка морфогенеза капилляров 2: рецептор токсина сибирской язвы. Proc. Natl. Акад. Sci. USA 2004, 101, 6367–6372.
- ^ а б c Santelli, E .; Bankston, L.A .; Leppla, S. H .; Liddington, R.C. Кристаллическая структура комплекса между токсином сибирской язвы и его рецептором клетки-хозяина. Природа. 2004, 430, 905–908.
- ^ а б Feld GK, Thoren KL, Kintzer AF, Sterling HJ, Tang II, Greenberg SG, Williams ER, Krantz BA. Структурная основа развертывания летального фактора сибирской язвы олигомерами защитных антигенов. Nat Struct Mol Biol. 2010, 17 (11): 1383-80.
- ^ Pannifer, A.D .; Wong, T. Y .; Schwarzenbacher, R .; Ренатус, М .; Petosa, C .; Bienkowska, J .; Lacy, D. B .; Collier, R.J .; Парк, С .; Leppla, S. H .; Hanna, P .; Лиддингтон, Р. К. Кристаллическая структура летального фактора сибирской язвы. Природа. 2001, 414, 230–233.
- ^ Мельник, Р. А .; Hewitt, K. M .; Lacy, D. B .; Lin, H.C .; Gessner, C.R .; Li, S .; Вудс, В. Л .; Collier, R.J. Структурные детерминанты связывания летального фактора сибирской язвы с олигомерным защитным антигеном. J. Biol. Chem. 2006, 281, 1630–1635.
- ^ Фельд Г.К., Браун М.Дж., Кранц Б.А. Увеличение транслокации белков с помощью токсина сибирской язвы. Prot Sci. 2012, 21 (5): 606-24.
- ^ Abrami, L .; Liu, S .; Cosson, P .; Leppla, S. H .; van der Goot, F. G. Токсин сибирской язвы запускает эндоцитоз своего рецептора через клатрин-зависимый процесс, опосредованный липидными рафтами. J. Cell Biol. 2003, 160, 321–328.
- ^ Mourez, M. Токсины сибирской язвы. Rev. Physiol. Biochem. Pharmacol. 2004, 152, 135–164.
внешняя ссылка
- «Молекула месяца» апрель 2012 г.
- Обзор всей структурной информации, доступной в PDB за UniProt: P15917 (Летальный фактор) при PDBe-KB.
