Цитохалазин - Cytochalasin
Цитохалазины находятся грибковый метаболиты которые имеют возможность связываться с актин волокна и блок полимеризация и удлинение актина. В результате ингибирования полимеризации актина цитохалазины могут изменять сотовый морфология, подавляют клеточные процессы, такие как деление клеток, и даже заставляют клетки подвергаться апоптоз.[1] Цитохалазины обладают способностью проникать через клеточные мембраны, предотвращать клеточную транслокацию и вызывать энуклеацию клеток.[2] Цитохалазины также могут оказывать влияние на другие аспекты биологических процессов, не связанные с полимеризацией актина. Например, цитохалазин А и цитохалазин B может также ингибировать транспорт моносахаридов через клеточную мембрану,[2] цитохалазин H было установлено, что регулирует рост растений,[3] цитохалазин D подавляет синтез белка[4] и цитохалазин E предотвращает ангиогенез.[5]
Связывание с актиновыми филаментами
Известно, что цитохалазины связываются с зазубренными, быстрорастущими плюс-концами микрофиламенты, который затем блокирует сборку и разборку отдельных мономеров актина на связанном конце. После связывания цитохалазины по существу закрывают конец новой актиновой нити. Один цитохалазин будет связываться с одной актиновой нитью.[2] Исследования выполнены с цитохалазин D (CD) обнаружили, что димеры CD-актина при образовании содержат связанный с АТФ актин.[6] Эти димеры CD-актина восстанавливаются до мономеров CD-актина в результате гидролиза АТФ. Полученный мономер CD-актина может связывать мономер АТФ-актина с преобразованием димера CD-актина.[2] CD очень эффективен; необходимы только низкие концентрации (0,2 мкМ) для предотвращения вздутия и разрушения мембраны беговая дорожка.[7] Было проанализировано влияние множества различных цитохалазинов на актиновые филаменты, и было обнаружено, что для удаления стрессовых волокон необходимы более высокие концентрации (2-20 мкМ) CD.[7]
В отличие, латрункулин ингибирует полимеризацию актиновых филаментов за счет связывания с мономерами актина.
Использование и применение цитохалазинов
Микрофиламенты актина были широко изучены с использованием цитохалазинов. Благодаря своей химической природе цитохалазины могут помочь исследователям понять важность актина в различных биологических процессах. Использование цитохалазинов позволило исследователям лучше понять полимеризацию актина, подвижность клеток, взъерошенность, деление клеток, сокращение и жесткость клеток. Использование цитохалазинов было настолько важно для понимания движения цитоскелета и многих других биологических процессов, что исследователи создали два синтетических цитохалазина.[1]
Цитохалазин нашел практическое применение в тромбоэластометрия (ТЕМ) анализы цельной крови для оценки фибриноген и нарушения полимеризации фибрина в анализе FIBTEM на ROTEM. Этот тест основан на принципе, что цитохалазин D очень эффективно подавляет тромбоцит функция за счет торможения сократительных элементов.[8] Ингибирование тромбоцитов более эффективно, чем когда тромбоциты блокируются GPIIb / IIIa антагонисты.[9] In vitro и клинические данные показывают, что сила сгустка в FIBTEM увеличивается в фибриноген зависимый от концентрации способ независимо от количества тромбоцитов.[10] Таким образом, можно быстро обнаружить дефицит фибриногена или нарушения полимеризации фибрина.
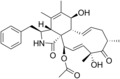
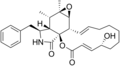
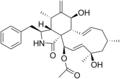
Химические структуры
Смотрите также
Рекомендации
- ^ а б Haidle, A.M .; Майерс, А. Г. (2004). «Энантиоселективный, модульный и общий путь к цитохалазинам: синтез L-696,474 и цитохалазина B» (PDF). Труды Национальной академии наук. 101 (33): 12048–12053. Дои:10.1073 / pnas.0402111101. ЧВК 514432. PMID 15208404.
- ^ а б c d Купер, Дж. А. (1987). «Влияние цитохалазина и фаллоидина на актин» (PDF). Журнал клеточной биологии. 105 (4): 1473–1478. Дои:10.1083 / jcb.105.4.1473. ЧВК 2114638. PMID 3312229.
- ^ Cox, R.H .; Cutler, H.G .; Hurd, R.E .; Коул, Р. Дж. (1983). "Протон и ядерный магнитный резонанс углерода-13 Исследования конформации производных цитохалазина H и регулирующих рост растений эффектов цитохалазинов". Журнал сельскохозяйственной и пищевой химии. 31 (2): 405–408. Дои:10.1021 / jf00116a055.
- ^ Орнеллес, Д. А .; Fey, E. G .; Пенман, С. (1986). «Цитохалазин высвобождает мРНК из каркаса цитоскелета и ингибирует синтез белка». Молекулярная и клеточная биология. 6 (5): 1650–1662. Дои:10.1128 / mcb.6.5.1650. ЧВК 367692. PMID 3785175.
- ^ Удагава, Т .; Yuan, J .; Panigrahy, D .; Chang, Y.-H .; Shah, J .; Д’Амато, Р. Дж. (2000). "Цитохалазин E, эпоксид, содержащий Аспергиллы-Полученный грибковый метаболит, ингибирует ангиогенез и рост опухоли » (PDF). Журнал фармакологии и экспериментальной терапии. 294 (2): 421–427. PMID 10900214.
- ^ Годдетт, Д. В .; Frieden, C. (1987). «Полимеризация актина - механизм действия цитохалазина D» (PDF). Журнал биологической химии. 261 (34): 15974–15980. PMID 3023337.
- ^ а б Yahara, I .; Harada, F .; Sekita, S .; Yoshihira, K .; Натори, С. (1982). «Корреляция между эффектами 24 различных цитохалазинов на клеточные структуры и клеточные события, а также на актин in vitro». Журнал клеточной биологии. 92 (1): 69–78. Дои:10.1083 / jcb.92.1.69. ЧВК 2112011. PMID 7199054.
- ^ May, J. A .; Ratan, H .; Glenn, J. R .; Lösche, W .; Spangenberg, P .; Хептинстолл, С. (1998). «Антагонисты GPIIb-IIIa вызывают быструю дезагрегацию тромбоцитов, предварительно обработанных цитохалазином D. Доказательства того, что стабильность агрегатов тромбоцитов зависит от нормальной сборки цитоскелета». Тромбоциты. 9 (3–4): 227–232. Дои:10.1080/09537109876744. PMID 16793707.
- ^ Lang, T .; Toller, W .; Gütl, M .; Mahla, E .; Metzler, H .; Rehak, P .; März, W .; Хальвакс-Бауманн, Г. (2004). «Различные эффекты абциксимаба и цитохалазина D на прочность сгустка при тромбэластографии». Журнал тромбоза и гемостаза. 2 (1): 147–153. Дои:10.1111 / j.1538-7836.2004.00555.x. PMID 14717978.
- ^ Lang, T .; Johanning, K .; Metzler, H .; Piepenbrock, S .; Соломон, С .; Rahe-Meyer, N .; Танака, К. А. (2009). «Влияние уровней фибриногена на тромбоэластометрические параметры при тромбоцитопении» (PDF). Анестезия и анальгезия. 108 (3): 751–758. Дои:10.1213 / ane.0b013e3181966675. PMID 19224779.