Ренин-ангиотензиновая система - Renin–angiotensin system

В ренин-ангиотензиновая система (РАН), или же ренин-ангиотензин-альдостероновая система (РАСН), это гормональная система что регулирует артериальное давление и жидкость и электролит сбалансированность, а также системная сосудистое сопротивление.[2]
Когда почечный кровоток уменьшен, юкстагломерулярные клетки в почках конвертируют предшественник проренин (уже присутствует в крови) в ренин и секретировать прямо в обращение. Ренин плазмы затем выполняет преобразование ангиотензиноген, выпущенный печень, к ангиотензин I.[3] Впоследствии ангиотензин I превращается в ангиотензин II посредством ангиотензин-превращающий фермент (АПФ), обнаруженный на поверхности эндотелиальных клеток сосудов, преимущественно клеток легкие.[4] Ангиотензин II - сильнодействующий сосудосуживающий пептид, вызывающий сужение кровеносных сосудов, что приводит к повышению артериального давления.[5] Ангиотензин II также стимулирует секрецию гормона. альдостерон[5] от кора надпочечников. Альдостерон вызывает почечные канальцы для увеличения реабсорбции натрий что, как следствие, вызывает реабсорбцию воды в кровь, в то же время вызывая выделение калий (поддерживать электролит баланс). Это увеличивает объем внеклеточной жидкости в организме, что также повышает кровяное давление.
Если РАС ненормально активен, артериальное давление будет слишком высоким. Есть несколько типов препаратов, в которые входят: Ингибиторы АПФ, БРА, и ингибиторы ренина которые прерывают различные этапы этой системы для повышения кровяного давления. Эти препараты являются одним из основных способов борьбы с высокое кровяное давление, сердечная недостаточность, почечная недостаточность, и вредное воздействие сахарный диабет.[6][7]Ренин активирует ренин-ангиотензиновую систему, расщепляя ангиотензиноген, продуцируемый печенью, с образованием ангиотензина I, который далее превращается в ангиотензин II под действием АПФ, ангиотензин-превращающего фермента, главным образом в капиллярах легких.
Активация
Дальнейшая информация: Саморегуляция
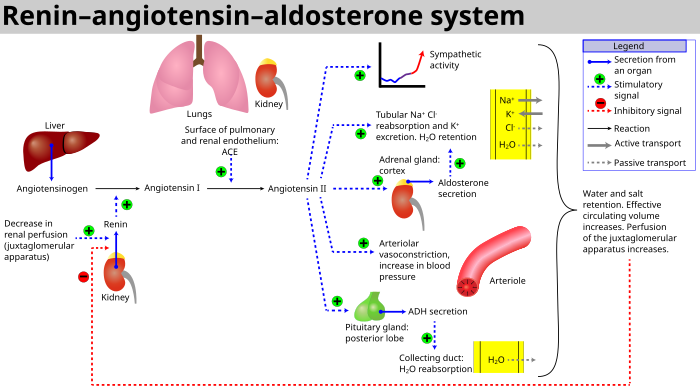
Система может быть активирована при потере объем крови или капля в артериальное давление (например, в кровоизлияние или же обезвоживание ). Эта потеря давления интерпретируется как барорецепторы в каротидный синус. Также может активироваться уменьшением фильтрата. хлорид натрия (NaCl) или пониженная скорость потока фильтрата, которая будет стимулировать плотное пятно сигнализировать юкстагломерулярные клетки освободить ренин.
- Если перфузия юкстагломерулярный аппарат в почках плотное пятно уменьшается, затем юкстагломерулярные клетки (зернистые клетки, модифицированные перициты в капилляре клубочков) высвобождают фермент ренин.
- Ренин раскалывает а декапептид из ангиотензиноген, а глобулярный белок. Декапептид известен как ангиотензин I.
- Затем ангиотензин I превращается в октапептид, ангиотензин II к ангиотензин-превращающий фермент (ТУЗ),[8] который, как полагают, находится в основном в эндотелиальных клетках капилляры по всему телу, в легких и эпителиальных клетках почек. Одно исследование 1992 года обнаружило АПФ во всех эндотелиальных клетках кровеносных сосудов.[9]
- Ангиотензин II является основным биологически активным продуктом ренин-ангиотензиновой системы, связывающимся с рецепторами на внутриклубочковые мезангиальные клетки, заставляя эти клетки сокращаться вместе с окружающими их кровеносными сосудами и вызывая высвобождение альдостерон от зона клубочков в кора надпочечников. Ангиотензин II действует как эндокринный, автокринный /паракринный, и внутрикринный гормон.
Сердечно-сосудистые эффекты
Дальнейшее чтение: Эффекты ангиотензина и Функция альдостерона

Ангиотензин I может иметь незначительную активность, но ангиотензин II является основным биологически активным продуктом. Ангиотензин II оказывает на организм множество эффектов:
- Во всем организме ангиотензин II является мощным сосудосуживающее средство из артериолы.
- В почках сужается ангиотензин II. клубочковый артериолы, оказывая большее влияние на эфферентные артериолы чем афферент. Как и в случае с большинством других капилляров в организме, сужение афферентные артериолы увеличивает сопротивление артериол, повышая системный артериальное давление и уменьшение кровотока. Тем не менее, почки должны продолжать фильтровать достаточное количество крови, несмотря на это падение кровотока, что требует механизмов для поддержания высокого кровяного давления в клубочках. Для этого ангиотензин II сужает эфферентные артериолы, что заставляет кровь скапливаться в клубочках, повышая гломерулярное давление. В скорость клубочковой фильтрации (СКФ), таким образом, сохраняется, и фильтрация крови может продолжаться, несмотря на снижение общего кровотока в почках. Поскольку фракция фильтрации, которая представляет собой отношение скорости клубочковой фильтрации (СКФ) к почечному потоку плазмы (ППФ), увеличилась, в нижних перитубулярных капиллярах остается меньше плазменной жидкости. Это, в свою очередь, приводит к уменьшению гидростатическое давление и увеличился онкотическое давление (из-за нефильтрованного белки плазмы ) в перитубулярных капиллярах. Эффект пониженного гидростатического давления и повышенного онкотического давления в перитубулярных капиллярах будет способствовать усилению реабсорбции канальцевой жидкости.
- Ангиотензин II снижает медуллярный кровоток через прямая ваза. Это уменьшает вымывание NaCl и мочевина в почке мозговое пространство. Таким образом, более высокие концентрации NaCl и мочевины в мозговом веществе способствуют увеличению абсорбции канальцевой жидкости. Кроме того, повышенная реабсорбция жидкости в мозговом веществе увеличивает пассивную реабсорбцию натрия вдоль толстой восходящей конечности Петля Генле.
- Ангиотензин II стимулирует Na+
/ЧАС+
обменники, расположенные на апикальных мембранах (обращенных к просвету канальцев) клеток в проксимальном канальце и толстой восходящей конечности петли Генле в дополнение к Na+
каналы в сборных каналах. В конечном итоге это приведет к увеличению реабсорбции натрия. - Ангиотензин II стимулирует гипертрофию клеток почечных канальцев, что приводит к дальнейшей реабсорбции натрия.
- в кора надпочечников, ангиотензин II вызывает высвобождение альдостерон. Альдостерон действует на канальцы (например, дистальные извитые канальцы и корковый сборные каналы ) в почках, заставляя их реабсорбировать больше натрий и вода с мочой. Это увеличивает объем крови и, следовательно, повышает кровяное давление. В обмен на реабсорбцию натрия в кровь, калий секретируется в канальцы, становится частью мочи и выводится из организма.
- Ангиотензин II вызывает выброс антидиуретического гормона (АДГ),[5] также называемый вазопрессин - АДГ производится в гипоталамусе и высвобождается из задней части гипофиз. Как следует из названия, он также проявляет сосудосуживающие свойства, но его основное действие - стимулировать реабсорбцию воды в почках. ADH также действует на Центральная нервная система для увеличения аппетита человека к соли и для стимулирования ощущения жажда.
Эти эффекты напрямую действуют вместе, повышая кровяное давление, и им противостоят: предсердный натрийуретический пептид (ANP).
Местные ренин-ангиотензиновые системы
Локально экспрессируемые ренин-ангиотензиновые системы были обнаружены в ряде тканей, включая почки, надпочечники, то сердце, сосудистая сеть и нервная система, и имеют множество функций, в том числе местная сердечно-сосудистая регуляция, в сочетании или независимо от системной ренин-ангиотензиновой системы, а также несердечно-сосудистых функций.[8][10][11] За пределами почек ренин преимущественно поступает из кровотока, но может секретироваться местно в некоторых тканях; его предшественник проренин высоко экспрессируется в тканях, и более половины циркулирующего проренина имеет внепочечное происхождение, но его физиологическая роль, помимо того, что он служит предшественником ренина, все еще неясна.[12] Вне печени ангиотензиноген улавливается из кровотока или локально экспрессируется в некоторых тканях; с ренином они образуют ангиотензин I и локально экспрессируются ангиотензин-превращающий фермент, химаза или другие ферменты могут преобразовать его в ангиотензин II.[12][13][14] Этот процесс может быть внутриклеточным или интерстициальным.[8]
В надпочечниках он, вероятно, участвует в паракринный регулирование альдостерон секреция; в сердце и сосудистой сети он может участвовать в ремоделировании или тонусе сосудов; и в мозг, где он в значительной степени не зависит от РАС кровообращения, он может участвовать в местной регуляции артериального давления.[8][11][15] Кроме того, как центральный и периферийный нервная система может использовать ангиотензин для симпатической нейротрансмиссии.[16] Другие места проявления включают репродуктивную систему, кожу и органы пищеварения. Лекарства, нацеленные на системную систему, могут положительно или отрицательно повлиять на экспрессию этих локальных систем.[8]
Ренин-ангиотензиновая система плода
в плод система ренин-ангиотензин является преимущественно системой с потерей натрия,[нужна цитата ] поскольку ангиотензин II практически не влияет на уровень альдостерона. Уровни ренина у плода высоки, тогда как уровни ангиотензина II значительно ниже; это происходит из-за ограниченного легочного кровотока, из-за которого АПФ (преимущественно в малом круге кровообращения) не дает максимального эффекта.
Клиническое значение

- Ингибиторы АПФ ангиотензин-превращающего фермента часто используются для уменьшения образования более мощного ангиотензина II. Каптоприл является примером ингибитора АПФ. АПФ расщепляет ряд других пептидов и в этом качестве является важным регулятором кинин – калликреиновая система, как таковая блокировка АПФ может привести к побочным эффектам.[нужна цитата ]
- Антагонисты рецепторов ангиотензина II, также известные как блокаторы рецепторов ангиотензина, могут использоваться для предотвращения воздействия ангиотензина II на его рецепторы.
- Прямой ингибиторы ренина также можно использовать при гипертонии.[17] Препараты, ингибирующие ренин: алискирен[18] и следственные ремикирен.[19]
- Вакцина против ангиотензина II, например CYT006-AngQb, были исследованы.[20][21]
Смотрите также
Рекомендации
- ^ Борон, Уолтер Ф. (2003). «Интеграция солевого и водного баланса (стр. 866–7); надпочечники (стр. 1059)». Медицинская физиология: клеточный и молекулярный подход. Elsevier / Saunders. ISBN 978-1-4160-2328-9.
- ^ Фонтан, Джон Х. (5 мая 2019 г.). «Физиология, ренин-ангиотензиновая система». NCBI. Национальные институты здравоохранения США. Получено 9 мая 2019.
- ^ Кумар, Аббас; Фаусто, Астер (2010). «11». Патологическая основа болезни (8-е изд.). Saunders Elsevier. п. 493. ISBN 978-1-4160-3121-5.
- ^ Голан, Дэвид; Ташджян, Армен; Армстронг, Эрин; Армстронг, апрель (15 декабря 2011 г.). ПРИНЦИПЫ ФАРМАКОЛОГИИ - ПАТОФИЗИОЛОГИЧЕСКАЯ ОСНОВА ЛЕКАРСТВЕННОЙ ТЕРАПИИ. LIPPINCOTT WILLIAMS & WILKINS, предприятие WOLTERS KLUWER. п. 335. ISBN 978-1-60831-270-2.
- ^ а б c Йи А.Х., Бернс Д.Д., Вейдикс Э.Ф. (апрель 2010 г.). «Церебральное солевое истощение: патофизиология, диагностика и лечение». Нейрохирургия Clin N Am. 21 (2): 339–52. Дои:10.1016 / j.nec.2009.10.011. PMID 20380974.
- ^ «Высокое кровяное давление: заболевания сердца и сосудов». Руководство Merck, домашнее издание.
- ^ Соломон, Скотт Д.; Анавекар, Нагеш (2005). «Краткий обзор ингибирования ренин-ангиотензиновой системы: акцент на блокаде рецептора ангиотензина II типа 1». Медицинская кардиология. 9 (2).
- ^ а б c d е Пол М., Поян Мехр А., Кройц Р. (июль 2006 г.). «Физиология местных ренин-ангиотензиновых систем». Physiol. Rev. 86 (3): 747–803. Дои:10.1152 / физрев.00036.2005. PMID 16816138.
- ^ Роджерсон Ф.М., Чай С.Ю., Шлаве I, Мюррей В.К., Марли П.Д., Мендельсон Ф.А. (июль 1992 г.). «Наличие ангиотензинпревращающего фермента в адвентиции крупных кровеносных сосудов». J. Hypertens. 10 (7): 615–20. Дои:10.1097/00004872-199207000-00003. PMID 1321187.
- ^ Kobori, H .; Nangaku, M .; Navar, L.G .; Нишияма, А. (1 сентября 2007 г.). «Внутрипочечная система ренин – ангиотензин: от физиологии к патобиологии гипертонии и заболеваний почек». Фармакологические обзоры. 59 (3): 251–287. Дои:10.1124 / пр.59.3.3. PMID 17878513.
- ^ а б Ehrhart-Bornstein, M; Hinson, JP; Bornstein, SR; Scherbaum, WA; Винсон, GP (апрель 1998 г.). «Интраадреналовые взаимодействия в регуляции стероидогенеза надпочечников» (PDF). Эндокринные обзоры. 19 (2): 101–43. Дои:10.1210 / edrv.19.2.0326. PMID 9570034.
- ^ а б Нгуен, Дж. (Март 2011 г.). «Ренин, (про) ренин и рецептор: обновление». Клиническая наука. 120 (5): 169–78. Дои:10.1042 / CS20100432. PMID 21087212.
- ^ Кумар, Р. Сингх, вице-президент; Бейкер, К.М. (март 2008 г.). «Внутриклеточная система ренин-ангиотензин: влияние на ремоделирование сердечно-сосудистой системы». Текущее мнение в нефрологии и гипертонии. 17 (2): 168–73. Дои:10.1097 / MNH.0b013e3282f521a8. PMID 18277150.
- ^ Кумар, Р. Сингх, вице-президент; Бейкер, К.М. (апрель 2009 г.). «Внутриклеточная ренин-ангиотензиновая система в сердце». Текущие отчеты о гипертонии. 11 (2): 104–10. Дои:10.1007 / s11906-009-0020-у. PMID 19278599.
- ^ МакКинли, MJ; Альбистон, Алабама; Аллен, AM; Mathai, ML; Май, CN; Макаллен, РМ; Олдфилд, Би Джей; Мендельсон, Ф.А.; Чай, SY (июнь 2003 г.). «Ренин-ангиотензиновая система мозга: расположение и физиологические роли». Международный журнал биохимии и клеточной биологии. 35 (6): 901–18. Дои:10.1016 / S1357-2725 (02) 00306-0. PMID 12676175.
- ^ Патил Дж., Хайнигер Э., Шаффнер Т., Мюлеманн О., Имбоден Х. (апрель 2008 г.). «Ангиотензинэргические нейроны в симпатических чревных ганглиях, иннервирующих кровеносные сосуды крысы и мезентериальное сопротивление человека». Regul. Пепт. 147 (1–3): 82–7. Дои:10.1016 / j.regpep.2008.01.006. PMID 18308407.
- ^ Презентация прямых ингибиторов ренина как антигипертензивных средств В архиве 7 декабря 2010 г. Wayback Machine
- ^ Градман А., Шмидер Р., Линс Р., Нуссбергер Дж., Чиангс Ю., Бедигиан М. (2005). «Алискирен, новый эффективный для перорального применения ингибитор ренина, обеспечивает дозозависимую антигипертензивную эффективность и переносимость, подобную плацебо, у пациентов с гипертонией». Тираж. 111 (8): 1012–8. Дои:10.1161 / 01.CIR.0000156466.02908.ED. PMID 15723979.
- ^ Рихтер WF, Whitby BR, Chou RC (1996). «Распространение ремикирена, мощного перорально активного ингибитора человеческого ренина, у лабораторных животных». Ксенобиотика. 26 (3): 243–54. Дои:10.3109/00498259609046705. PMID 8730917.
- ^ Tissot AC, Maurer P, Nussberger J, Sabat R, Pfister T, Ignatenko S, Volk HD, Stocker H, Müller P, Jennings GT, Wagner F, Bachmann MF (март 2008 г.). «Влияние иммунизации против ангиотензина II с помощью CYT006-AngQb на амбулаторное кровяное давление: двойное слепое рандомизированное плацебо-контролируемое исследование фазы IIa». Ланцет. 371 (9615): 821–7. Дои:10.1016 / S0140-6736 (08) 60381-5. PMID 18328929.
- ^ Браун, MJ (2009). «Успех и неудача вакцин против компонентов ренин-ангиотензиновой системы». Обзоры природы. Кардиология. 6 (10): 639–47. Дои:10.1038 / nrcardio.2009.156. PMID 19707182.
- Баник А., Сигурдссон Г. Х., Уитли А. М. (1993). «Влияние возраста на сердечно-сосудистую реакцию во время градуированного кровотечения у анестезированных крыс». Res Exp Med (Berl). 193 (5): 315–21. Дои:10.1007 / BF02576239. PMID 8278677.
внешняя ссылка
- Система Ренин-Ангиотензин + в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
