Потенциал действия - Action potential

В физиология, потенциал действия (AP) происходит, когда мембранный потенциал конкретного ячейка локация стремительно поднимается и опускается:[1] эта деполяризация затем вызывает аналогичную деполяризацию соседних участков. Потенциалы действия встречаются в нескольких типах клетки животных, называется возбудимый ячеек, которые включают нейроны, мышечные клетки, эндокринный клетки клетки клубочка, а в некоторых клетки растений.
В нейронах потенциалы действия играют центральную роль в связь между ячейками путем предоставления - или в отношении скачкообразное проведение, ассистирование - распространение сигналов по нейрону аксон к синаптические бутоны расположен на концах аксона; эти сигналы могут затем связываться с другими нейронами в синапсах, моторными клетками или железами. В других типах клеток их основная функция - активировать внутриклеточные процессы. В мышечных клетках, например, потенциал действия - это первый шаг в цепи событий, ведущих к сокращению. В бета-клетки из поджелудочная железа, они провоцируют выброс инсулин.[а] Потенциалы действия в нейронах также известны как "нервные импульсы" или "шипы", а временная последовательность потенциалов действия, генерируемых нейроном, называется его"шипованный поезд". Нейрон, который испускает потенциал действия или нервный импульс, часто говорят, что он" стреляет ".
Потенциалы действия порождаются особыми видами потенциалзависимые ионные каналы встроен в ячейку плазматическая мембрана.[b] Эти каналы закрываются, когда мембранный потенциал близок к (отрицательному) потенциал покоя ячейки, но они быстро начинают открываться, если мембранный потенциал увеличивается до точно определенного порогового напряжения, деполяризующий трансмембранный потенциал.[b] Когда каналы открываются, они пропускают внутрь поток натрий ионы, которые изменяют электрохимический градиент, что, в свою очередь, вызывает дальнейшее повышение мембранного потенциала до нуля. Это затем приводит к открытию большего количества каналов, создавая больший электрический ток через клеточную мембрану и так далее. Процесс продолжается до тех пор, пока не откроются все доступные ионные каналы, что приводит к большому скачку мембранного потенциала. Быстрый приток ионов натрия вызывает изменение полярности плазматической мембраны, и ионные каналы затем быстро инактивируются. Когда натриевые каналы закрываются, ионы натрия больше не могут проникать в нейрон, и они активно транспортируются обратно из плазматической мембраны. Калий каналы затем активируются, и происходит выходящий ток ионов калия, возвращающий электрохимический градиент в состояние покоя. После возникновения потенциала действия происходит переходный отрицательный сдвиг, называемый постгиперполяризация.
В клетках животных существует два основных типа потенциалов действия. Один тип создается напряжение-управляемые натриевые каналы, другой - по напряжению кальций каналы. Потенциалы действия на основе натрия обычно длятся менее одной миллисекунды, но потенциалы действия на основе кальция могут длиться до 100 миллисекунд или дольше.[нужна цитата ] В некоторых типах нейронов медленные выбросы кальция обеспечивают движущую силу для длительного выброса быстро выделяемых выбросов натрия. В клетках сердечной мышцы, с другой стороны, начальный быстрый выброс натрия обеспечивает «праймер», чтобы спровоцировать быстрое начало выброса кальция, которое затем вызывает сокращение мышц.[нужна цитата ]
Обзор

Почти все клеточные мембраны у животных, растений и грибов поддерживать Напряжение разница между внешним видом и интерьером клетки, называемая мембранный потенциал. Типичное напряжение на мембране животной клетки составляет -70 мВ. Это означает, что внутренняя часть ячейки имеет отрицательное напряжение по отношению к внешней стороне. В большинстве типов клеток мембранный потенциал обычно остается довольно постоянным. Однако некоторые типы элементов являются электрически активными в том смысле, что их напряжение колеблется со временем. В некоторых типах электрически активных ячеек, в том числе нейроны и в мышечных клетках колебания напряжения часто принимают форму быстрого всплеска вверх, за которым следует быстрое падение. Эти восходящие и нисходящие циклы известны как потенциалы действия. В некоторых типах нейронов весь цикл «вверх-вниз» занимает несколько тысячных долей секунды. В мышечных клетках типичный потенциал действия длится около одной пятой секунды. В некоторых других типах клеток и растений потенциал действия может длиться три секунды и более.[2]
Электрические свойства клетки определяются структурой окружающей ее мембраны. А клеточная мембрана состоит из липидный бислой молекул, в которые встроены более крупные молекулы белка. Липидный бислой очень устойчив к движению электрически заряженных ионов, поэтому он действует как изолятор. Напротив, крупные встроенные в мембрану белки обеспечивают каналы, через которые ионы могут проходить через мембрану. Потенциалы действия управляются белками каналов, конфигурация которых переключается между закрытым и открытым состояниями в зависимости от разности напряжений между внутренней и внешней частью клетки. Эти чувствительные к напряжению белки известны как потенциалзависимые ионные каналы.
Процесс в типичном нейроне
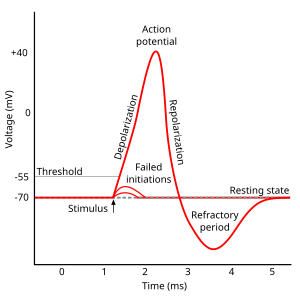
Все клетки тканей тела животных электрически поляризованный - другими словами, они поддерживают разность напряжений на плазматическая мембрана, известный как мембранный потенциал. Эта электрическая поляризация является результатом сложного взаимодействия белковых структур, встроенных в мембрану, называемого ионные насосы и ионные каналы. В нейронах типы ионных каналов в мембране обычно различаются в разных частях клетки, что дает дендриты, аксон, и Тело клетки разные электрические свойства. В результате некоторые части мембраны нейрона могут быть возбудимыми (способны генерировать потенциалы действия), а другие - нет. Недавние исследования показали, что наиболее возбудимая часть нейрона - это часть после аксональный бугорок (точка, где аксон покидает тело клетки), который называется начальным сегментом, но аксон и тело клетки также в большинстве случаев возбудимы.[3]
Каждый возбудимый участок мембраны имеет два важных уровня мембранного потенциала: потенциал покоя, которое представляет собой значение, которое мембранный потенциал поддерживает до тех пор, пока клетка не возмущается, и более высокое значение, называемое пороговый потенциал. На бугорке аксона типичного нейрона потенциал покоя составляет около -70 милливольт (мВ), а пороговый потенциал составляет около -55 мВ. Синаптические входы в нейрон заставляют мембрану деполяризовать или гиперполяризовать; то есть они вызывают повышение или понижение мембранного потенциала. Потенциалы действия срабатывают, когда накапливается достаточно деполяризации, чтобы довести мембранный потенциал до порогового значения. Когда срабатывает потенциал действия, мембранный потенциал резко поднимается вверх, а затем столь же резко возвращается вниз, часто заканчиваясь ниже уровня покоя, где он остается в течение некоторого периода времени. Форма потенциала действия стереотипна; это означает, что подъем и спад обычно имеют примерно одинаковую амплитуду и ход во времени для всех потенциалов действия в данной клетке. (Исключения обсуждаются далее в статье). В большинстве нейронов весь процесс происходит примерно за тысячную долю секунды. Многие типы нейронов постоянно излучают потенциалы действия со скоростью до 10–100 в секунду. Однако некоторые типы намного тише и могут длиться минуты или дольше, не испуская никаких потенциалов действия.
Биофизическая основа
Эта секция нужны дополнительные цитаты для проверка. (Февраль 2014 года) (Узнайте, как и когда удалить этот шаблон сообщения) |
Потенциалы действия возникают из-за присутствия в клеточной мембране особых типов потенциалзависимые ионные каналы.[4] Управляемый потенциалом ионный канал - это кластер белков, встроенных в мембрану, который обладает тремя ключевыми свойствами:
- Он способен принимать более одной конформации.
- По крайней мере, одна из конформаций создает канал через мембрану, проницаемый для определенных типов ионов.
- На переход между конформациями влияет мембранный потенциал.
Таким образом, потенциал-зависимый ионный канал имеет тенденцию быть открытым для одних значений мембранного потенциала и закрытым для других. Однако в большинстве случаев связь между мембранным потенциалом и состоянием канала является вероятностной и включает временную задержку. Ионные каналы переключаются между конформациями в непредсказуемые моменты времени: мембранный потенциал определяет скорость переходов и вероятность в единицу времени каждого типа перехода.

Управляемые по напряжению ионные каналы способны создавать потенциалы действия, потому что они могут вызывать положительный отзыв петли: мембранный потенциал контролирует состояние ионных каналов, но состояние ионных каналов контролирует мембранный потенциал. Таким образом, в некоторых ситуациях повышение мембранного потенциала может вызвать открытие ионных каналов, тем самым вызывая дальнейшее повышение мембранного потенциала. Когда этот цикл положительной обратной связи (Цикл Ходжкина ) происходит взрывоопасно. Время и амплитуда траектории потенциала действия определяются биофизическими свойствами потенциалзависимых ионных каналов, которые его создают. Существуют несколько типов каналов, способных производить положительную обратную связь, необходимую для создания потенциала действия. Управляемые напряжением натриевые каналы отвечают за быстрые потенциалы действия, участвующие в нервной проводимости. Потенциалы медленного действия в мышечных клетках и некоторых типах нейронов генерируются потенциалозависимыми кальциевыми каналами. Каждый из этих типов имеет несколько вариантов с разной чувствительностью к напряжению и разной временной динамикой.
Наиболее интенсивно изучаемый тип потенциалзависимых ионных каналов - это натриевые каналы, участвующие в быстрой нервной проводимости. Иногда их называют натриевые каналы Ходжкина-Хаксли, потому что они сначала были охарактеризованы Алан Ходжкин и Эндрю Хаксли в своих исследованиях биофизики потенциала действия, получивших Нобелевскую премию, но для удобства их можно назвать NaV каналы. («V» означает «напряжение».) NaV канал имеет три возможных состояния, известных как деактивирован, активирован, и инактивированный. Канал проницаем только для ионов натрия, когда он находится в активирован штат. Когда мембранный потенциал низкий, канал большую часть времени проводит в деактивирован (закрытое) состояние. Если мембранный потенциал поднимается выше определенного уровня, канал показывает повышенную вероятность перехода в активирован (открытое) состояние. Чем выше мембранный потенциал, тем больше вероятность активации. После активации канала он в конечном итоге перейдет в инактивированный (закрытое) состояние. Затем он имеет тенденцию оставаться неактивным в течение некоторого времени, но, если мембранный потенциал снова станет низким, канал в конечном итоге вернется к деактивирован штат. Во время потенциала действия большинство каналов этого типа проходят цикл деактивирован→активирован→инактивированный→деактивирован. Однако это только среднее поведение населения - отдельный канал, в принципе, может осуществить любой переход в любое время. Однако вероятность перехода канала из инактивированный заявить непосредственно в активирован состояние очень низкое: канал в инактивированный состояние является невосприимчивым, пока не перейдет обратно в деактивирован штат.
Результатом всего этого является то, что кинетика NaV каналы управляются переходной матрицей, скорость которой зависит от напряжения сложным образом. Поскольку эти каналы сами по себе играют важную роль в определении напряжения, глобальную динамику системы может быть довольно сложно определить. Ходжкин и Хаксли подошли к проблеме, разработав набор дифференциальные уравнения для параметров, которые управляют состояниями ионных каналов, известных как Уравнения Ходжкина-Хаксли. Эти уравнения были значительно изменены более поздними исследованиями, но они составляют отправную точку для большинства теоретических исследований биофизики потенциала действия.
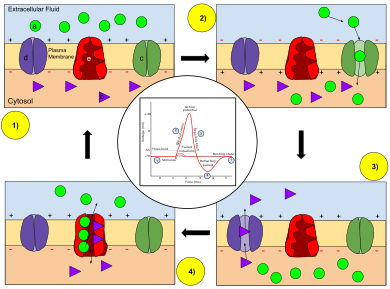
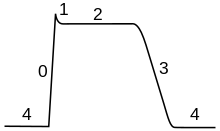
Ключ: а) Натрий (Na+) ион. б) Калий (K+) ион. в) Натриевый канал. г) Калиевый канал. д) Натрий-калиевый насос.
На этапах потенциала действия проницаемость мембраны нейрона изменяется. На состояние покоя (1), ионы натрия и калия имеют ограниченную способность проходить через мембрану, и нейрон имеет внутри отрицательный заряд. Как только потенциал действия срабатывает, деполяризация (2) нейрона активирует натриевые каналы, позволяя ионам натрия проходить через клеточную мембрану в клетку, что приводит к появлению в нейроне общего положительного заряда по сравнению с внеклеточной жидкостью. После достижения пика потенциала действия нейрон начинает реполяризация (3), где каналы натрия закрываются и каналы калия открываются, позволяя ионам калия пересекать мембрану во внеклеточную жидкость, возвращая мембранный потенциал к отрицательному значению. Наконец, есть период отражения (4), при котором потенциалзависимые ионные каналы инактивированный в то время как Na+ и K+ ионы возвращаются в свое состояние покоя, распределенные по мембране (1), и нейрон готов повторить процесс для следующего потенциала действия.
По мере увеличения мембранного потенциала ионные каналы натрия открыть, позволяя вход натрий ионы в клетку. Затем следует открытие ионные каналы калия которые позволяют выход калий ионы из клетки. Входящий поток ионов натрия увеличивает концентрацию положительно заряженных катионы в клетке и вызывает деполяризацию, когда потенциал клетки выше, чем у клетки потенциал покоя. На пике потенциала действия натриевые каналы закрываются, а калий продолжает покидать клетку. Отток ионов калия снижает мембранный потенциал или гиперполяризует клетку. При небольшом увеличении напряжения из состояния покоя ток калия превышает ток натрия, и напряжение возвращается к своему нормальному значению в состоянии покоя, обычно -70 мВ.[5][6][7] Однако, если напряжение превышает критический порог, обычно на 15 мВ выше значения покоя, преобладает натриевый ток. Это приводит к неуправляемому состоянию, при котором положительный отзыв от натриевого тока активируется еще больше натриевых каналов. Таким образом, ячейка пожары, производя потенциал действия.[5][8][9][примечание 1] Частоту, с которой нейрон выявляет потенциалы действия, часто называют скорострельность или скорость нейронной активации.
Токи, возникающие при открытии управляемых по напряжению каналов в ходе действия потенциала действия, обычно значительно превышают начальный стимулирующий ток. Таким образом, амплитуда, продолжительность и форма потенциала действия в значительной степени определяются свойствами возбудимой мембраны, а не амплитудой или продолжительностью стимула. Эта все или ничего свойство потенциала действия отличает его от градуированные потенциалы такие как рецепторные потенциалы, электротонические потенциалы, подпороговые колебания мембранного потенциала, и синаптические потенциалы, которые масштабируются с величиной стимула. Различные типы потенциала действия существуют во многих типах клеток и клеточных компартментах, что определяется типами потенциалзависимых каналов, каналы утечки, распределение каналов, концентрации ионов, емкость мембраны, температура и другие факторы.
Основными ионами, участвующими в потенциале действия, являются катионы натрия и калия; Ионы натрия попадают в клетку, а ионы калия уходят, восстанавливая равновесие. Относительно небольшое количество ионов должно пройти через мембрану, чтобы напряжение на мембране резко изменилось. Ионы, обмениваемые во время потенциала действия, поэтому вносят незначительное изменение во внутренние и внешние концентрации ионов. Немногочисленные пересекающиеся ионы снова откачиваются непрерывным действием натриево-калиевый насос, который вместе с другими ионные транспортеры, поддерживает нормальное соотношение концентраций ионов на мембране. Кальций катионы и хлористый анионы участвуют в нескольких типах потенциалов действия, таких как потенциал сердечного действия и потенциал действия в одноклеточной водоросль Ацетабулярия соответственно.
Хотя потенциалы действия генерируются локально на участках возбудимой мембраны, результирующие токи могут запускать потенциалы действия на соседних участках мембраны, ускоряя распространение, подобное домино. В отличие от пассивного распространения электрических потенциалов (электротонический потенциал ), потенциалы действия генерируются заново вдоль возбудимых участков мембраны и распространяются без распада.[10] Миелинизированные участки аксонов не возбудимы и не производят потенциалов действия, а сигнал распространяется пассивно, как электротонический потенциал. Регулярно расположенные немиелинизированные пятна, называемые узлы Ранвье, генерируйте потенциалы действия для усиления сигнала. Известный как скачкообразное проведение, этот тип распространения сигнала обеспечивает благоприятный компромисс между скоростью сигнала и диаметром аксона. Деполяризация терминалы аксонов, как правило, запускает выпуск нейротрансмиттер в синаптическая щель. Кроме того, потенциалы действия обратного распространения были зарегистрированы в дендритах пирамидные нейроны, которые повсеместно встречаются в неокортексе.[c] Считается, что они играют роль в пластичность, зависящая от времени всплеска.
в Модель емкости мембраны Ходжкина – Хаксли скорость передачи потенциала действия не была определена, и предполагалось, что соседние области становятся деполяризованными из-за высвобожденных ионных помех соседним каналам. Измерения диффузии ионов и радиусов с тех пор показали, что это невозможно.[нужна цитата ] Более того, противоречивые измерения изменений энтропии и времени оспаривают модель емкости как действующую самостоятельно.[нужна цитата ] С другой стороны, гипотеза адсорбции Гилберта Линга утверждает, что мембранный потенциал и потенциал действия живой клетки обусловлены адсорбцией подвижных ионов на адсорбционные сайты клеток.[11]
Созревание электрических свойств потенциала действия
А нейрон способность генерировать и распространять изменения потенциала действия во время развитие. Сколько мембранный потенциал изменения нейрона в результате импульса тока является функцией мембраны входное сопротивление. По мере роста клетки больше каналы добавляются к мембране, вызывая уменьшение входного сопротивления. Зрелый нейрон также претерпевает более короткие изменения мембранного потенциала в ответ на синаптические токи. Нейроны хорька латеральное коленчатое ядро иметь больше постоянная времени и больше Напряжение прогиб в P0, чем в P30.[12] Одним из следствий уменьшения продолжительности потенциала действия является то, что точность сигнала может быть сохранена в ответ на высокочастотную стимуляцию. Незрелые нейроны более склонны к синаптической депрессии, чем к потенциации после высокочастотной стимуляции.[12]
На раннем этапе развития многих организмов потенциал действия фактически изначально переносится кальциевый ток скорее, чем натриевой ток. В кинетика открытия и закрытия кальциевых каналов во время развития медленнее, чем у потенциалзависимых натриевых каналов, которые несут потенциал действия в зрелых нейронах. Более длительное время открытия кальциевых каналов может привести к тому, что потенциалы действия будут значительно ниже, чем у зрелых нейронов.[12] Xenopus нейроны изначально имеют потенциалы действия, которые занимают 60–90 мс. В процессе разработки это время уменьшается до 1 мс. Это резкое снижение объясняется двумя причинами. Во-первых, внутренний ток переносится преимущественно по натриевым каналам.[13] Во-вторых, выпрямитель с задержкой, а калиевый канал ток увеличивается в 3,5 раза от первоначальной силы.[12]
Для перехода от кальций-зависимого потенциала действия к натрий-зависимому потенциалу действия в мембрану должны быть добавлены новые каналы. Если нейроны Xenopus выращиваются в среде с Синтез РНК или синтез белка ингибиторы этого перехода предотвращаются.[14] Даже электрическая активность самой клетки может играть роль в экспрессии каналов. Если потенциалы действия в Xenopus миоциты блокируются, предотвращается или задерживается типичное повышение плотности тока натрия и калия.[15]
Это созревание электрических свойств наблюдается у всех видов. Потоки натрия и калия Xenopus резко увеличиваются после того, как нейрон проходит свою последнюю фазу митоз. Плотность натриевого тока крысы корковые нейроны увеличивается на 600% в течение первых двух послеродовых недель.[12]
Нейротрансмиссия
Анатомия нейрона
| Нейрон |
|---|
Некоторые типы клеток поддерживают потенциал действия, такие как клетки растений, мышечные клетки и специализированные клетки сердца (в которых происходит потенциал сердечного действия ). Однако основная возбудимая клетка - это нейрон, который также имеет простейший механизм действия.
Нейроны представляют собой электрически возбудимые клетки, состоящие, как правило, из одного или нескольких дендритов, одного сома, один аксон и один или несколько терминалы аксонов. Дендриты - это клеточные проекции, основной функцией которых является получение синаптических сигналов. Их выступы, известные как дендритные шипы, предназначены для захвата нейромедиаторов, выделяемых пресинаптическим нейроном. У них высокая концентрация ионные каналы, управляемые лигандами. Эти шипы имеют тонкую шейку, соединяющую луковичный выступ с дендритом. Это гарантирует, что изменения, происходящие внутри позвоночника, с меньшей вероятностью повлияют на соседние позвоночники. Дендритный отросток может, за редким исключением (см. LTP ), действуют как независимая единица. Дендриты отходят от сомы, в которой находится ядро, и многие из "нормальных" эукариотический органеллы. В отличие от шипов поверхность сомы заполнена ионными каналами, активируемыми напряжением. Эти каналы помогают передавать сигналы, генерируемые дендритами. Из сомы выходит аксональный бугорок. Эта область характеризуется очень высокой концентрацией активируемых напряжением натриевых каналов. В целом, это считается зоной инициирования всплеска для потенциалов действия,[16] то есть триггерная зона. Здесь сходятся многочисленные сигналы, генерируемые шипами и передаваемые сомой. Сразу после бугорка аксона находится аксон. Это тонкий трубчатый выступ, отходящий от сомы. Аксон изолирован миелин оболочка. Миелин состоит из Шванновские клетки (в периферической нервной системе) или олигодендроциты (в центральной нервной системе), оба из которых являются типами глиальные клетки. Хотя глиальные клетки не участвуют в передаче электрических сигналов, они общаются и обеспечивают важную биохимическую поддержку нейронов.[17] Точнее говоря, миелин несколько раз оборачивается вокруг аксонального сегмента, образуя толстый жировой слой, который предотвращает проникновение и выход ионов из аксона. Эта изоляция предотвращает значительное затухание сигнала, а также обеспечивает более высокую скорость сигнала. Эта изоляция, однако, имеет ограничение, заключающееся в том, что на поверхности аксона не может быть никаких каналов. Таким образом, существуют регулярно расположенные участки мембраны, не имеющие изоляции. Эти узлы Ранвье их можно рассматривать как «бугорки мини-аксонов», поскольку их цель - усилить сигнал, чтобы предотвратить его значительный распад. На самом дальнем конце аксон теряет изоляцию и начинает разветвляться на несколько терминалы аксонов. Эти пресинаптические терминалы, или синаптические бутоны, представляют собой специализированную область в аксоне пресинаптической клетки, которая содержит нейротрансмиттеры заключены в небольшие мембранные сферы, называемые синаптические везикулы.
Посвящение
Прежде чем рассматривать распространение потенциалов действия вдоль аксоны и их прекращение на синаптических ручках, полезно рассмотреть методы, с помощью которых потенциалы действия могут быть инициированы в аксональный бугорок. Основное требование - чтобы напряжение на мембране на бугре было выше порога стрельбы.[5][6][18][19] Эта деполяризация может происходить несколькими путями.

Динамика
Потенциалы действия чаще всего инициируются возбуждающие постсинаптические потенциалы от пресинаптического нейрона.[20] Обычно нейротрансмиттер молекулы высвобождаются пресинаптический нейрон. Затем эти нейротрансмиттеры связываются с рецепторами постсинаптической клетки. Эта привязка открывает различные типы ионные каналы. Это открытие имеет дальнейшее влияние на изменение локальной проницаемости клеточная мембрана и, следовательно, мембранный потенциал. Если связывание увеличивает напряжение (деполяризует мембрану), синапс становится возбуждающим. Однако, если связывание снижает напряжение (гиперполяризует мембрану), оно является тормозящим. Независимо от того, увеличивается или уменьшается напряжение, изменение пассивно распространяется на близлежащие области мембраны (как описано уравнение кабеля и его доработки). Обычно стимул напряжения спадает экспоненциально с расстоянием от синапса и со временем от связывания нейротрансмиттера. Некоторая часть возбуждающего напряжения может достигать аксональный бугорок и может (в редких случаях) деполяризовать мембрану настолько, чтобы вызвать новый потенциал действия. Как правило, возбуждающие потенциалы нескольких синапсов должны работать вместе в почти в то же время спровоцировать новый потенциал действия. Однако их совместным усилиям может помешать противодействие тормозящие постсинаптические потенциалы.
Нейротрансмиссия также может происходить через электрические синапсы.[21] Благодаря прямой связи между возбудимыми клетками в виде щелевые соединения, потенциал действия может передаваться напрямую от одной ячейки к другой в любом направлении. Свободный поток ионов между клетками обеспечивает быструю передачу, не опосредованную химическими веществами. Выпрямляющие каналы обеспечивают движение потенциалов действия только в одном направлении через электрический синапс.[нужна цитата ] Электрические синапсы присутствуют во всех нервных системах, включая человеческий мозг, хотя их меньшинство.[22]
Принцип «все или ничего»
В амплитуда потенциала действия не зависит от величины тока, который его произвел. Другими словами, большие токи не создают больших потенциалов действия. Следовательно, потенциалы действия называются все или ничего сигналов, так как они либо возникают полностью, либо не возникают вовсе.[d][e][f] Это в отличие от рецепторные потенциалы, амплитуды которых зависят от интенсивности стимула.[23] В обоих случаях частота потенциалов действия коррелирует с интенсивностью стимула.
Сенсорные нейроны
В сенсорные нейроны внешний сигнал, такой как давление, температура, свет или звук, связан с открытием и закрытием ионные каналы, которые, в свою очередь, изменяют ионную проницаемость мембраны и ее напряжение.[24] Эти изменения напряжения снова могут быть возбуждающими (деполяризующими) или тормозящими (гиперполяризационными), а в некоторых сенсорных нейронах их комбинированные эффекты могут деполяризовать бугорок аксона в достаточной степени, чтобы вызвать потенциалы действия. Некоторые примеры у людей включают нейрон обонятельного рецептора и Тельце Мейснера, которые имеют решающее значение для чувства запах и прикоснуться соответственно. Однако не все сенсорные нейроны преобразуют свои внешние сигналы в потенциалы действия; у некоторых нет даже аксона.[25] Вместо этого они могут преобразовать сигнал в выпуск нейротрансмиттер, или в непрерывный градуированные потенциалы, любой из которых может стимулировать последующий нейрон (ы) в возбуждении потенциала действия. Например, в человеческом ухо, волосковые клетки преобразовать входящий звук в открытие и закрытие механически управляемые ионные каналы, что может вызвать нейротрансмиттер высвобождаемые молекулы. Аналогичным образом в человеческом сетчатка, начальный фоторецепторные клетки и следующий слой ячеек (содержащий биполярные клетки и горизонтальные ячейки ) не производят потенциалов действия; только некоторые амакриновые клетки и третий слой, ганглиозные клетки, производят потенциалы действия, которые затем перемещаются вверх по оптический нерв.
Возможности кардиостимулятора
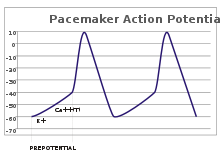
В сенсорных нейронах потенциалы действия возникают в результате внешнего раздражителя. Однако некоторым возбудимым клеткам не нужен такой стимул для срабатывания: они спонтанно деполяризуют бугорки аксонов и запускают потенциалы действия с регулярной скоростью, как внутренние часы.[26] Следы напряжения таких ячеек известны как потенциал кардиостимулятора.[27] В кардиостимулятор ячейки синоатриальный узел в сердце дайте хороший пример.[г] Хотя у таких кардиостимуляторов есть естественный ритм, его можно регулировать внешними раздражителями; например, частота сердцебиения могут быть изменены фармацевтическими препаратами, а также сигналами от симпатичный и парасимпатический нервы.[28] Внешние стимулы не вызывают повторяющихся срабатываний клетки, а просто изменяют их время.[27] В некоторых случаях регулирование частоты может быть более сложным, что приводит к паттернам потенциалов действия, таким как разрыв.
Фазы
Ход потенциала действия можно разделить на пять частей: фаза нарастания, фаза пика, фаза падения, фаза недорега и рефрактерный период. Во время фазы роста мембранный потенциал деполяризуется (становится более положительным). Точка, в которой деполяризация стопов называется пиковой фазой. На этом этапе мембранный потенциал достигает максимума. Вслед за этим наступает фаза падения. На этом этапе мембранный потенциал становится более отрицательным, возвращаясь к потенциалу покоя. Недостаток, или постгиперполяризация, фаза - это период, в течение которого мембранный потенциал временно становится более отрицательно заряженным, чем в состоянии покоя (гиперполяризован). Наконец, время, в течение которого последующий потенциал действия невозможно или трудно задействовать, называется период отражения, которые могут перекрываться с другими фазами.[29]
Ход потенциала действия определяется двумя связанными эффектами.[30] Во-первых, чувствительные к напряжению ионные каналы открываются и закрываются в ответ на изменения мембранное напряжение Vм. Это изменяет проницаемость мембраны для этих ионов.[31] Во-вторых, согласно Уравнение гольдмана, это изменение проницаемости изменяет равновесный потенциал Eм, а значит, и мембранное напряжение Vм.[час] Таким образом, мембранный потенциал влияет на проницаемость, которая затем дополнительно влияет на мембранный потенциал. Это создает возможность для положительный отзыв, который является ключевой частью фазы роста потенциала действия.[5][8] Осложняющим фактором является то, что один ионный канал может иметь несколько внутренних «ворот», которые реагируют на изменения в Vм противоположными способами или с разной скоростью.[32][я] Например, хотя повышение Vм открывается большинство ворот в чувствительном к напряжению натриевом канале, он также закрывается «ворота инактивации» канала, хотя и медленнее.[33] Следовательно, когда Vм поднимается внезапно, натриевые каналы сначала открываются, но затем закрываются из-за более медленной инактивации.
Напряжения и токи потенциала действия во всех его фазах точно смоделированы Алан Ллойд Ходжкин и Эндрю Хаксли в 1952 г.,[я] за что они были награждены Нобелевская премия по физиологии и медицине в 1963 г.[β] Однако, их модель рассматривает только два типа чувствительных к напряжению ионных каналов и делает несколько предположений о них, например, что их внутренние ворота открываются и закрываются независимо друг от друга. На самом деле существует много типов ионных каналов,[34] и они не всегда открываются и закрываются независимо.[j]
Фаза стимуляции и подъема
Типичный потенциал действия начинается с аксональный бугорок[35] при достаточно сильной деполяризации, например, раздражитель, увеличивающий Vм. Эта деполяризация часто вызывается инъекцией дополнительного количества натрия. катионы в камеру; эти катионы могут поступать из самых разных источников, таких как химические синапсы, сенсорные нейроны или потенциал кардиостимулятора.
Для нейрона в состоянии покоя существует высокая концентрация ионов натрия и хлорида в внеклеточной жидкости по сравнению с внутриклеточная жидкость, в то время как во внутриклеточной жидкости наблюдается высокая концентрация ионов калия по сравнению с внеклеточной жидкостью. Разница в концентрациях, которая заставляет ионы перемещаться от высокой до низкой концентрации, а электростатические эффекты (притяжение противоположных зарядов) ответственны за движение ионов внутрь нейрона и из него. Внутренняя часть нейрона имеет отрицательный заряд по отношению к внешней части клетки из-за движения K+ из клетки. Мембрана нейрона более проницаема для K+ чем к другим ионам, позволяя этому иону выборочно перемещаться из клетки, вниз по градиенту его концентрации. Этот градиент концентрации вместе с каналы утечки калия присутствует на мембране нейрона, вызывает отток ионов калия, что делает потенциал покоя близким к EK ≈ –75 мВ.[36] Поскольку Na+ ионы находятся в более высоких концентрациях за пределами ячейки, разница в концентрации и напряжении приводит их в ячейку, когда Na+ каналы открыты. Деполяризация открывает и натриевые, и калиевые каналы в мембране, позволяя ионам поступать в аксон и выходить из него соответственно. Если деполяризация мала (скажем, увеличивается Vм от -70 мВ до -60 мВ), выходящий калиевый ток подавляет входящий натриевый ток, и мембрана реполяризуется обратно до своего нормального потенциала покоя около -70 мВ.[5][6][7] Однако, если деполяризация достаточно велика, входящий натриевый ток увеличивается больше, чем выходящий калиевый ток, и возникает состояние убегания (положительный отзыв ) результаты: чем больше внутренний ток, тем больше Vм увеличивается, что, в свою очередь, еще больше увеличивает входящий ток.[5][8] Достаточно сильная деполяризация (увеличение Vм) вызывает открытие чувствительных к напряжению натриевых каналов; повышенная проницаемость для натриевых двигателей Vм ближе к напряжению равновесия натрия ENa≈ +55 мВ. Повышение напряжения, в свою очередь, вызывает открытие еще большего количества натриевых каналов, что подталкивает Vм еще дальше к ENa. Эта положительная обратная связь продолжается до тех пор, пока натриевые каналы не откроются полностью и Vм близко к ENa.[5][6][37][38] Резкий рост Vм и проницаемость натрия соответствуют фаза подъема потенциала действия.[5][6][37][38]
Критическое пороговое напряжение для этого состояния разгона обычно составляет около -45 мВ, но это зависит от недавней активности аксона. Клетка, которая только что активировала потенциал действия, не может немедленно запустить другую, так как Na+ каналы не вышли из неактивированного состояния. Период, в течение которого нельзя задействовать новый потенциал действия, называется периодом абсолютный рефрактерный период.[39][40][41] В более длительные периоды времени, после восстановления некоторых, но не всех ионных каналов, аксон можно стимулировать для создания другого потенциала действия, но с более высоким порогом, требующим гораздо более сильной деполяризации, например, до -30 мВ. Период, в течение которого необычно трудно вызвать потенциалы действия, называется периодом относительный рефрактерный период.[39][40][41]
Пиковая фаза
Положительная обратная связь нарастающей фазы замедляется и прекращается, когда каналы ионов натрия становятся максимально открытыми. На пике потенциала действия проницаемость для натрия максимальна, а напряжение на мембране Vм почти равно равновесному напряжению натрия ENa. Однако то же повышенное напряжение, которое первоначально открывало натриевые каналы, также медленно закрывает их, закрывая поры; натриевые каналы становятся инактивированный.[33] Это снижает проницаемость мембраны для натрия по сравнению с калием, возвращая мембранное напряжение обратно к значению покоя. В то же время повышенное напряжение открывает чувствительные к напряжению калиевые каналы; увеличение проницаемости калия мембраны приводит Vм в направлении EK.[33] В совокупности эти изменения проницаемости для натрия и калия вызывают: Vм быстро падать, переполяризуя мембрану и создавая «фазу падения» потенциала действия.[39][42][38][43]
После гиперполяризации
Деполяризованное напряжение открывает дополнительные зависимые от напряжения калиевые каналы, и некоторые из них не закрываются сразу же, когда мембрана возвращается к своему нормальному напряжению покоя. К тому же, дополнительные калиевые каналы открываются в ответ на приток ионов кальция во время потенциала действия. Внутриклеточная концентрация ионов калия временно необычно низка, из-за чего напряжение на мембране Vм еще ближе к напряжению равновесия калия EK. Мембранный потенциал опускается ниже мембранного потенциала покоя. Следовательно, есть недобор или гиперполяризация, названный постгиперполяризация, который сохраняется до тех пор, пока проницаемость мембраны для калия не вернется к своему обычному значению, восстанавливая мембранный потенциал до состояния покоя.[44][42]
Период отражения
За каждым потенциалом действия следует период отражения, которые можно разделить на абсолютный рефрактерный период, во время которого невозможно вызвать другой потенциал действия, а затем относительный рефрактерный период, во время которого требуется более сильный, чем обычно, стимул.[39][40][41] Эти два рефрактерных периода вызваны изменениями в состоянии молекул натриевого и калиевого каналов. При закрытии после потенциала действия натриевые каналы входят в «инактивированное» состояние, в котором они не могут открыться независимо от мембранного потенциала - это приводит к абсолютному рефрактерному периоду. Даже после того, как достаточное количество натриевых каналов перешло обратно в состояние покоя, часто случается, что часть калиевых каналов остается открытой, что затрудняет деполяризацию мембранного потенциала и, таким образом, приводит к возникновению относительного рефрактерного периода. Поскольку плотность и подтипы калиевых каналов могут сильно различаться между разными типами нейронов, продолжительность относительного рефрактерного периода сильно варьируется.
Абсолютный рефрактерный период в значительной степени отвечает за однонаправленное распространение потенциалов действия вдоль аксонов.[45] В любой данный момент участок аксона позади активно развивающейся части является рефрактерным, но участок впереди, который не был активирован в последнее время, способен стимулироваться деполяризацией от потенциала действия.
Распространение
Потенциал действия, генерируемый на бугорке аксона, распространяется по аксону в виде волны.[46] Токи, текущие внутрь в точке на аксоне во время потенциала действия, распространяются вдоль аксона и деполяризуют соседние участки его мембраны. Если эта деполяризация достаточно сильна, она вызывает аналогичный потенциал действия на соседних участках мембраны. Этот основной механизм был продемонстрирован Алан Ллойд Ходжкин в 1937. После раздавливания или охлаждения нервных сегментов и, таким образом, блокирования потенциалов действия, он показал, что потенциал действия, приходящий на одну сторону блока, может спровоцировать другой потенциал действия на другой, при условии, что заблокированный сегмент был достаточно коротким.[k]
Как только на участке мембраны проявился потенциал действия, мембранному участку требуется время для восстановления, прежде чем он сможет снова выстрелить. На молекулярном уровне это абсолютный рефрактерный период соответствует времени, необходимому для активации натриевых каналов, активируемых напряжением, для восстановления после инактивации, то есть возврата в свое закрытое состояние.[40] В нейронах существует много типов калиевых каналов, активируемых напряжением. Некоторые из них деактивируются быстро (токи А-типа), а некоторые инактивируются медленно или не деактивируются совсем; эта изменчивость гарантирует, что всегда будет доступный источник тока для реполяризации, даже если некоторые из калиевых каналов инактивированы из-за предшествующей деполяризации. С другой стороны, все нейронные активируемые напряжением натриевые каналы инактивируются в течение нескольких миллисекунд во время сильной деполяризации, что делает последующую деполяризацию невозможной до тех пор, пока значительная часть натриевых каналов не вернется в свое закрытое состояние. Хотя это ограничивает частоту стрельбы,[47] Абсолютный рефрактерный период гарантирует, что потенциал действия движется только в одном направлении вдоль аксона.[45] Токи, протекающие из-за потенциала действия, распространяются в обоих направлениях вдоль аксона.[48] Однако только незажженная часть аксона может ответить потенциалом действия; только что сработавшая часть не реагирует, пока потенциал действия не выйдет за пределы допустимого диапазона, и не сможет рестимулировать эту часть. В обычном ортодромная проводимость потенциал действия распространяется от бугорка аксона к синаптическим выступам (концам аксона); распространение в обратном направлении, известное как антидромная проводимость - очень редко.[49] Однако, если лабораторный аксон стимулируется в его середине, обе половины аксона остаются «свежими», т. Е. Необожженными; тогда будут генерироваться два потенциала действия: один движется к бугорку аксона, а другой - к синаптическим выступам.
Миелиновая и скачкообразная проводимость

Чтобы обеспечить быструю и эффективную передачу электрических сигналов в нервной системе, определенные нейрональные аксоны покрыты миелин ножны. Миелин представляет собой многослойную мембрану, которая охватывает аксон сегментами, разделенными интервалами, известными как узлы Ранвье. Его производят специализированные клетки: Шванновские клетки исключительно в периферическая нервная система, и олигодендроциты исключительно в Центральная нервная система. Миелиновая оболочка снижает емкость мембраны и увеличивает сопротивление мембраны в межузловых интервалах, тем самым обеспечивая быстрое скачкообразное движение потенциалов действия от узла к узлу.[l][м][n] Миелинизация встречается в основном у позвоночные, но аналогичная система была обнаружена у нескольких беспозвоночных, таких как некоторые виды креветка.[o] Не все нейроны у позвоночных миелинизированы; например, аксоны нейронов, составляющих автономную нервную систему, как правило, миелинизированы.
Миелин предотвращает попадание ионов в аксон и его выход из миелинизированных сегментов. Как правило, миелинизация увеличивает скорость проводимости потенциалов действия и делает их более энергоэффективными. Скачкообразно или нет, средняя скорость проведения потенциала действия колеблется от 1метр в секунду (м / с) до более 100 м / с и, как правило, увеличивается с увеличением диаметра аксона.[п]
Потенциалы действия не могут распространяться через мембрану в миелинизированных сегментах аксона. Однако по цитоплазме проводится ток, которого достаточно для деполяризации первого или второго последующего узел Ранвье. Вместо этого ионный ток от потенциала действия на одном узел Ранвье вызывает еще один потенциал действия в следующем узле; это очевидное «скачкообразное изменение» потенциала действия от узла к узлу известно как скачкообразное проведение. Хотя механизм скачкообразной проводимости был предложен в 1925 году Ральфом Лилли,[q] первые экспериментальные доказательства скачкообразной проводимости пришли из Ичидзи Тасаки[р] и Тайцзи Такеучи[s][50] и из Эндрю Хаксли и Роберт Штэмпфли.[т] Напротив, в немиелинизированных аксонах потенциал действия провоцирует другой потенциал в мембране, непосредственно прилегающей к нему, и непрерывно движется вниз по аксону, как волна.

Миелин имеет два важных преимущества: высокая скорость проводимости и энергоэффективность. Для аксонов больше минимального диаметра (примерно 1 микрометр ) миелинизация увеличивает скорость проводимости потенциала действия, как правило, десятикратного.[v] И наоборот, для данной скорости проводимости миелинизированные волокна меньше, чем их немиелинизированные аналоги. Например, потенциалы действия движутся примерно с одинаковой скоростью (25 м / с) в миелинизированном аксоне лягушки и немиелинизированном аксоне. гигантский аксон кальмара, но аксон лягушки имеет примерно в 30 раз меньший диаметр и в 1000 раз меньшую площадь поперечного сечения. Кроме того, поскольку ионные токи ограничиваются узлами Ранвье, гораздо меньше ионов «просачивается» через мембрану, экономя метаболическую энергию. Это значительная экономия селективное преимущество, поскольку нервная система человека использует примерно 20% метаболической энергии организма.[v]
Длина миелинизированных сегментов аксонов важна для успеха скачкообразной проводимости. Они должны быть как можно более длинными, чтобы максимизировать скорость проводимости, но не настолько длинными, чтобы приходящий сигнал был слишком слабым, чтобы вызвать потенциал действия в следующем узле Ранвье. В природе миелинизированные сегменты обычно достаточно длинные для того, чтобы пассивно распространяемый сигнал прошел по крайней мере два узла, сохраняя при этом достаточную амплитуду, чтобы запустить потенциал действия во втором или третьем узле. Таким образом коэффициент безопасности скачкообразной проводимости высока, позволяя в случае травмы обходить узлы. Однако потенциалы действия могут преждевременно заканчиваться в определенных местах, где коэффициент безопасности низкий, даже в немиелинизированных нейронах; распространенным примером является точка ветвления аксона, где он делится на два аксона.[52]
Некоторые заболевания разрушают миелин и нарушают скачкообразную проводимость, снижая скорость проведения потенциалов действия.[w] Самым известным из них является рассеянный склероз, при котором распад миелина нарушает скоординированные движения.[53]
Теория кабеля

Поток токов внутри аксона можно количественно описать следующим образом: теория кабеля[54] и его разработки, такие как компартментальная модель.[55] Теория кабеля была разработана в 1855 г. Лорд Кельвин смоделировать трансатлантический телеграфный кабель[Икс] и было показано, что имеет отношение к нейронам Ходжкин и Раштон в 1946 г.[y] В простой кабельной теории нейрон рассматривается как электрически пассивный, идеально цилиндрический передающий кабель, который можно описать как уравнение в частных производных[54]
где V(Икс, т) - напряжение на мембране в момент времени т и должность Икс вдоль длины нейрона, и где λ и τ - характерная длина и временные масштабы, на которых эти напряжения падают в ответ на стимул. Обращаясь к принципиальной схеме справа, эти масштабы можно определить по сопротивлению и емкости на единицу длины.[56]
Эти масштабы времени и длины можно использовать для понимания зависимости скорости проводимости от диаметра нейрона в немиелинизированных волокнах. Например, временной масштаб τ увеличивается с увеличением сопротивления мембраны. рм и емкость cм. По мере увеличения емкости для получения заданного трансмембранного напряжения должно быть передано больше заряда ( уравнение Q = резюме ); по мере увеличения сопротивления в единицу времени передается меньше заряда, что замедляет уравновешивание. Аналогичным образом, если внутреннее сопротивление на единицу длины ря в одном аксоне меньше, чем в другом (например, потому что радиус первого больше), длина пространственного распада λ становится больше, и скорость проводимости потенциала действия должен увеличиваться. Если трансмембранное сопротивление рм увеличивается, что снижает средний ток «утечки» через мембрану, что также вызывает λ становиться длиннее, увеличивая скорость проводимости.
Прекращение
Химические синапсы
В общем, потенциалы действия, которые достигают синаптических узлов, вызывают нейротрансмиттер быть выпущенным в синаптическую щель.[z] Нейротрансмиттеры - это небольшие молекулы, которые могут открывать ионные каналы в постсинаптической клетке; большинство аксонов имеют один и тот же нейромедиатор на всех концах. Прибытие потенциала действия открывает чувствительные к напряжению кальциевые каналы в пресинаптической мембране; приток кальция вызывает пузырьки заполнены нейротрансмиттером для миграции на поверхность клетки и выпустить их содержимое в синаптическая щель.[аа] Этот сложный процесс тормозится нейротоксины тетаноспазмин и ботулинический токсин, которые несут ответственность за столбняк и ботулизм соответственно.[ab]
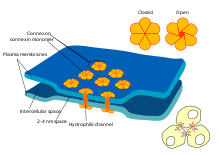
Электрические синапсы
Некоторые синапсы обходятся без «посредника» нейротрансмиттера и соединяют вместе пресинаптические и постсинаптические клетки.[ac] Когда потенциал действия достигает такого синапса, ионные токи, текущие в пресинаптическую клетку, могут пересечь барьер двух клеточных мембран и проникнуть в постсинаптическую клетку через поры, известные как коннексоны.[объявление] Таким образом, ионные токи пресинаптического потенциала действия могут напрямую стимулировать постсинаптическую клетку. Электрические синапсы обеспечивают более быструю передачу, потому что они не требуют медленной диффузии нейротрансмиттеры через синаптическую щель. Следовательно, электрические синапсы используются всякий раз, когда решающее значение имеют быстрый отклик и координация времени, как в спасательные рефлексы, то сетчатка из позвоночные, а сердце.
Нервно-мышечные соединения
Частным случаем химического синапса является нервно-мышечное соединение, в которой аксон из двигательный нейрон заканчивается на мышечное волокно.[ae] В таких случаях высвобожденный нейротрансмиттер ацетилхолин, который связывается с рецептором ацетилхолина, интегральным мембранным белком в мембране ( сарколемма ) мышечного волокна.[аф] Однако ацетилхолин не остается связанным; скорее, он диссоциирует и гидролизованный ферментом, ацетилхолинэстераза, расположенный в синапсе. Этот фермент быстро снижает раздражение мышц, что позволяет деликатно регулировать степень и время мышечного сокращения.Некоторые яды инактивируют ацетилхолинэстеразу для предотвращения этого контроля, например, нервно-паралитические вещества зарин и табун,[ag] и инсектициды диазинон и малатион.[ах]
Другие типы клеток
Потенциалы сердечного действия
Потенциал сердечного действия отличается от потенциала действия нейронов наличием расширенного плато, на котором мембрана удерживается под высоким напряжением в течение нескольких сотен миллисекунд, прежде чем будет реполяризована током калия, как обычно.[ai] Это плато связано с действием более медленных кальций каналы открываются и удерживают напряжение мембраны около их равновесного потенциала даже после того, как натриевые каналы инактивированы.
Потенциал сердечного действия играет важную роль в координации сокращений сердца.[ai] Сердечные клетки синоатриальный узел предоставить потенциал кардиостимулятора что синхронизирует сердце. Потенциалы действия этих клеток распространяются на и через атриовентрикулярный узел (АВ-узел), который обычно является единственным проводящим путем между предсердие и желудочки. Потенциалы действия от AV-узла проходят через связка Его и оттуда в Волокна Пуркинье.[заметка 2] И наоборот, аномалии потенциала сердечной деятельности - будь то из-за врожденной мутации или травмы - могут привести к патологиям человека, особенно аритмии.[ai] Некоторые антиаритмические препараты действуют на потенциал сердечного действия, например: хинидин, лидокаин, бета-блокаторы, и верапамил.[aj]
Потенциалы мышечного действия
Потенциал действия в нормальной клетке скелетных мышц аналогичен потенциалу действия в нейронах.[57] Потенциалы действия возникают в результате деполяризации клеточной мембраны ( сарколемма ), который открывает чувствительные к напряжению натриевые каналы; они становятся инактивированными, и мембрана реполяризуется за счет выходящего тока ионов калия. Потенциал покоя перед потенциалом действия обычно составляет -90 мВ, что несколько более отрицательно, чем у типичных нейронов. Потенциал действия мышцы длится примерно 2–4 мс, абсолютный рефрактерный период составляет примерно 1–3 мс, а скорость проводимости по мышце составляет примерно 5 м / с. Релизы с потенциалом действия кальций ионы, которые высвобождают тропомиозин и позвольте мышце сократиться. Потенциалы мышечного действия провоцируются приходом пресинаптического нейронального потенциала действия в нервно-мышечное соединение, что является общей целью для нейротоксины.[ag]
Потенциалы действия растений
Завод и грибковые клетки[ак] также электрически возбудимы. Принципиальное отличие от потенциалов действия животных состоит в том, что деполяризация в растительных клетках достигается не за счет поглощения положительных ионов натрия, а за счет высвобождения отрицательных ионов натрия. хлористый ионы.[al][утра][an] Увеличение количества ионов кальция в цитоплазме может быть причиной выброса анионов в клетку. Это делает кальций предшественником движений ионов, таких как приток отрицательных ионов хлора и отток положительных ионов калия, как это видно на листьях ячменя.[58]
Первоначальный приток ионов кальция также вызывает небольшую клеточную деполяризацию, вызывая открытие потенциалозависимых ионных каналов и позволяя полной деполяризации распространяться ионами хлорида.
Некоторые растения (например, Dionaea muscipula ) используют каналы с натриевыми воротами для управления движениями и, по сути, «счета». Dionaea muscipula, также известный как венерина мухоловка, встречается в субтропических заболоченных местах в Северной и Южной Каролине.[59] Когда в почве мало питательных веществ, мухоловка питается насекомыми и животными.[60] Несмотря на исследования этого растения, отсутствует понимание молекулярной основы венерианских мухоловок и хищных растений в целом.[61]
Тем не менее, было проведено множество исследований потенциалов действия и того, как они влияют на движение и часовой механизм венерианской мухоловки. Начнем с того, что мембранный потенциал покоя венерианской мухоловки ниже, чем у животных клеток.[61] Это упрощает активацию потенциала действия. Таким образом, когда насекомое попадает в ловушку растения, оно запускает механорецептор, похожий на волосы.[61] Затем этот рецептор активирует потенциал действия, который длится около 1,5 мс.[62] В конечном итоге это вызывает увеличение количества положительных ионов кальция в клетке, слегка деполяризуя ее.
Однако мухоловка не закрывается после одного срабатывания. Вместо этого требуется активация 2 или более волосков.[60][61] Если срабатывает только один волос, активация считается ложной. Кроме того, вторые волосы должны быть активированы в течение определенного интервала времени (0,75 - 40 с), чтобы они зарегистрировались при первой активации.[61] Таким образом, начинается накопление кальция и медленно падает с первого триггера. Когда второй потенциал действия срабатывает в течение временного интервала, он достигает порогового значения кальция, чтобы деполяризовать клетку, закрывая ловушку на добыче в течение доли секунды.[61]
Вместе с последующим высвобождением положительных ионов калия потенциал действия растений включает в себя осмотический потеря соли (KCl). Принимая во внимание, что потенциал действия животных осмотически нейтрален, потому что равные количества поступающего натрия и выходящего калия осмотически компенсируют друг друга. Взаимодействие электрических и осмотических отношений в клетках растений[ао] по-видимому, возникло из-за осмотической функции электрической возбудимости у общих одноклеточных предков растений и животных в условиях меняющейся засоленности. Кроме того, существующая функция быстрой передачи сигнала рассматривается как новое достижение многоклеточный клетки в более стабильной осмотической среде.[63] Вероятно, что знакомая сигнальная функция потенциалов действия у некоторых сосудистых растений (например, Мимоза стыдливая ) возникла независимо от таковой в возбудимых клетках многоклеточных животных.
Таксономическое распространение и эволюционные преимущества
Потенциалы действия встречаются повсюду многоклеточные организмы, в том числе растения, беспозвоночные такие как насекомые, и позвоночные такие как рептилии и млекопитающие.[ap] Губки кажется главным филюм многоклеточных эукариоты который не передает потенциалы действия, хотя некоторые исследования предполагают, что эти организмы также имеют форму электрических сигналов.[водный] Потенциал покоя, а также величина и продолжительность потенциала действия не сильно менялись в процессе эволюции, хотя скорость проводимости действительно сильно зависит от диаметра аксона и миелинизации.
| Животное | Тип ячейки | Потенциал покоя (мВ) | Увеличение АД (мВ) | Длительность AP (мс) | Скорость проводимости (м / с) |
|---|---|---|---|---|---|
| Кальмар (Лолиго) | Гигантский аксон | −60 | 120 | 0.75 | 35 |
| Земляной червь (Поясничный) | Срединное гигантское волокно | −70 | 100 | 1.0 | 30 |
| Таракан (Periplaneta) | Гигантское волокно | −70 | 80–104 | 0.4 | 10 |
| Лягушка (Рана) | Аксон седалищного нерва | От -60 до -80 | 110–130 | 1.0 | 7–30 |
| Кот (Фелис) | Спинальный мотонейрон | От -55 до -80 | 80–110 | 1–1.5 | 30–120 |
Учитывая его сохранение на протяжении эволюции, потенциал действия, по-видимому, дает эволюционные преимущества. Одна из функций потенциалов действия - это быстрая передача сигналов на большие расстояния внутри организма; скорость проводимости может превышать 110 м / с, что составляет треть от скорость звука. Для сравнения, молекула гормона, переносимая кровотоком, движется со скоростью примерно 8 м / с в крупных артериях. Частью этой функции является тесная координация механических событий, таких как сокращение сердца. Вторая функция - это вычисление, связанное с его генерацией. Будучи сигналом типа "все или ничего", который не затухает с увеличением расстояния передачи, потенциал действия имеет те же преимущества, что и цифровая электроника. Интеграция различных дендритных сигналов на бугорке аксона и их пороговая обработка для формирования сложной последовательности потенциалов действия - это еще одна форма вычислений, которая была использована биологически для формирования генераторы центральных паттернов и подражали в искусственные нейронные сети.
Считается, что общий предок прокариот / эукариот, который жил около четырех миллиардов лет назад, имел каналы, управляемые напряжением. Вероятно, что позже эта функция была перекрестной для обеспечения механизма связи. Даже современные одноклеточные бактерии могут использовать потенциалы действия для связи с другими бактериями в той же биопленке.[65]
Экспериментальные методы

Изучение потенциалов действия потребовало разработки новых экспериментальных методов. Первоначальная работа, до 1955 г., в основном выполнялась Алан Ллойд Ходжкин и Эндрю Филдинг Хаксли, которые были вместе Джон Кэрью Эклс награжден 1963 г. Нобелевская премия по физиологии и медицине за их вклад в описание ионной основы нервной проводимости. Он был сосредоточен на трех целях: изоляция сигналов от отдельных нейронов или аксонов, разработка быстрой и чувствительной электроники и сокращение электроды достаточно, чтобы можно было записать напряжение внутри отдельной ячейки.
Первая проблема была решена путем изучения гигантские аксоны обнаружены в нейронах Кальмар (Лолиго форбесии и Doryteuthis pealeii, в то время классифицированный как Лолиго палеи).[ар] Эти аксоны настолько велики в диаметре (примерно на 1 мм, или в 100 раз больше, чем у типичного нейрона), что их можно увидеть невооруженным глазом, что позволяет легко извлекать их и манипулировать ими.[я][так как] Однако они не являются репрезентативными для всех возбудимых клеток, и многие другие системы с потенциалами действия были изучены.
Вторая проблема была решена с решающим развитием зажим напряжения,[в] что позволило экспериментаторам изучать ионные токи, лежащие в основе потенциала действия изолированно, и устранило ключевой источник электронный шум, электрический ток яC связанный с емкость C мембраны.[67] Поскольку ток равен C умноженная на скорость изменения трансмембранного напряжения Vм, решение заключалось в разработке схемы, сохраняющей Vм фиксированная (нулевая скорость изменения) независимо от токов, протекающих через мембрану. Таким образом, ток, необходимый для сохранения Vм при фиксированном значении - прямое отражение тока, протекающего через мембрану. Другие достижения в области электроники включают использование Клетки Фарадея и электроника с высоким входное сопротивление, чтобы само измерение не влияло на измеряемое напряжение.[68]
Третья проблема, проблема получения электродов, достаточно маленьких для регистрации напряжений в пределах одного аксона, не нарушая его, была решена в 1949 году с изобретением стеклянного микропипеточного электрода.[au] который был быстро принят другими исследователями.[средний][aw] Усовершенствования этого метода позволяют производить наконечники электродов толщиной до 100 Å (10 нм ), что также обеспечивает высокий входной импеданс.[69] Потенциалы действия также могут быть записаны с помощью небольших металлических электродов, размещенных рядом с нейроном, с нейрочипы содержащий EOSFET, или оптически красителями, которые чувствителен к Ca2+ или к напряжению.[топор]

В то время как стеклянные электроды микропипетки измеряют сумму токов, проходящих через множество ионных каналов, изучение электрических свойств одного ионного канала стало возможным в 1970-х годах с развитием патч зажим от Эрвин Неер и Берт Сакманн. За это открытие они были награждены Нобелевская премия по физиологии и медицине в 1991 г.[γ] Фиксация патча подтвердила, что ионные каналы имеют дискретные состояния проводимости, такие как открытый, закрытый и инактивированный.
Оптическое изображение В последние годы были разработаны технологии для измерения потенциалов действия либо посредством одновременной записи на нескольких участках, либо с ультрапространственным разрешением. С помощью красители чувствительные к напряжению, потенциалы действия были оптически записаны с крошечного участка кардиомиоцит мембрана.[ай]
Нейротоксины

Несколько нейротоксины как натуральные, так и синтетические, предназначены для блокирования потенциала действия. Тетродотоксин от рыба фугу и сакситоксин от Гоньяулакс (в динофлагеллята род, ответственный за "красные приливы «) блокировать потенциалы действия, подавляя чувствительный к напряжению натриевый канал;[аз] так же, дендротоксин от Черная мамба змея подавляет чувствительный к напряжению калиевый канал. Такие ингибиторы ионных каналов служат важной исследовательской цели, позволяя ученым по желанию «отключать» определенные каналы, тем самым изолируя вклад других каналов; они также могут быть полезны для очистки ионных каналов путем аффинная хроматография или при определении их концентрации. Однако такие ингибиторы также вырабатывают эффективные нейротоксины и рассматриваются для использования в качестве химическое оружие. Нейротоксины, нацеленные на ионные каналы насекомых, оказались эффективными инсектициды; одним из примеров является синтетический перметрин, который продлевает активацию натриевых каналов, участвующих в потенциалах действия. Ионные каналы насекомых достаточно отличаются от своих собратьев у человека, поэтому у людей мало побочных эффектов.
История
Роль электричества в нервной системе животных впервые была обнаружена при вскрытии. лягушки от Луиджи Гальвани, изучавшие его с 1791 по 1797 год.[ба] Результаты Гальвани стимулировали Алессандро Вольта развивать Гальваническая свая - самый ранний из известных электрическая батарея - с помощью которых он изучал электричество животных (например, электрические угри ) и физиологические реакции на прикладываемые постоянный ток напряжения.[bb]
Ученые 19 века изучали распространение электрических сигналов в целом. нервы (т.е. пучки нейроны ) и продемонстрировал, что нервная ткань состоит из клетки, вместо взаимосвязанной сети трубок (a сеточка).[70] Карло Маттеуччи продолжил исследования Гальвани и продемонстрировал, что клеточные мембраны имели напряжение на них и могли производить постоянный ток. Работа Маттеуччи вдохновила немецкого физиолога, Эмиль дю Буа-Реймон, открывший потенциал действия в 1843 году.[71] В скорость проводимости потенциалов действия был впервые измерен в 1850 году другом дю Буа-Реймона, Герман фон Гельмгольц.[72] Чтобы установить, что нервная ткань состоит из отдельных клеток, испанский врач Сантьяго Рамон-и-Кахаль и его ученики использовали краситель, разработанный Камилло Гольджи чтобы выявить бесчисленные формы нейронов, которые они тщательно воспроизвели. За свои открытия Гольджи и Рамон-и-Кахаль были награждены орденом 1906 г. Нобелевская премия по физиологии.[δ] Их работа разрешила давние противоречия в нейроанатомия 19 века; Сам Гольджи выступал за сетевую модель нервной системы.
ХХ век был важной эпохой для электрофизиологии. В 1902 г. и снова в 1912 г. Юлиус Бернштейн выдвинул гипотезу о том, что потенциал действия возник в результате изменения проницаемость аксональной мембраны на ионы.[до н.э][73] Гипотезу Бернштейна подтвердил Кен Коул и Говард Кертис, который показал, что проводимость мембраны увеличивается во время потенциала действия.[bd] В 1907 г. Луи Лапик предположил, что потенциал действия генерировался при превышении порога,[быть] то, что позже будет показано как продукт динамические системы ионных проводимостей. В 1949 г. Алан Ходжкин и Бернард Кац уточнил гипотезу Бернштейна, считая, что аксональная мембрана может иметь разную проницаемость для разных ионов; в частности, они продемонстрировали решающую роль проницаемости для натрия для потенциала действия.[bf] Они сделали первую фактическую регистрацию электрических изменений мембраны нейронов, которые опосредуют потенциал действия.[ε] Кульминацией этого направления исследований стали пять работ Ходжкина, Каца и Эндрю Хаксли, в котором они применили зажим напряжения Методика определения зависимости проницаемости аксональной мембраны для ионов натрия и калия от напряжения и времени, на основе которой они смогли количественно восстановить потенциал действия.[я] Ходжкин и Хаксли коррелировали свойства своей математической модели с дискретными ионные каналы которые могут существовать в нескольких разных состояниях, включая «открыто», «закрыто» и «неактивно». Их гипотезы были подтверждены в середине 1970-х и 1980-х гг. Эрвин Неер и Берт Сакманн, который разработал технику патч зажим для исследования состояний проводимости отдельных ионных каналов.[bg] В 21 веке исследователи начинают понимать структурную основу этих состояний проводимости и селективности каналов для их разновидностей иона,[bh] через атомное разрешение кристаллические структуры,[би] измерения расстояния флуоресценции[bj] и криоэлектронная микроскопия исследования.[bk]
Юлиус Бернштейн также первым представил Уравнение Нернста для потенциал покоя через мембрану; это было обобщено Дэвид Э. Голдман одноименному Уравнение гольдмана в 1943 г.[час] В натриево-калиевый насос был идентифицирован в 1957 г.[bl][ζ] и его свойства постепенно выяснялись,[bm][млрд][бо] достигнув высшей точки в определении его структуры атомного разрешения Рентгеновская кристаллография.[bp] Также были решены кристаллические структуры связанных ионных насосов, что дает более широкое представление о том, как они молекулярные машины Работа.[bq]
Количественные модели

Математические и вычислительные модели необходимы для понимания потенциала действия и предлагают прогнозы, которые могут быть проверены на экспериментальных данных, обеспечивая строгую проверку теории. Самой важной и точной из ранних нейронных моделей является Модель Ходжкина – Хаксли, который описывает потенциал действия совокупностью из четырех обыкновенные дифференциальные уравнения (ОДУ).[я] Хотя модель Ходжкина – Хаксли может быть упрощением с некоторыми ограничениями[74] по сравнению с реалистичной нервной мембраной в том виде, в каком она существует в природе, ее сложность вдохновила на создание нескольких еще более упрощенных моделей,[75][br] такой как Модель Морриса – Лекара[bs] и Модель ФитцХью – Нагумо,[bt] оба имеют только два связанных ODE. Свойства моделей Ходжкина – Хаксли и ФитцХью – Нагумо и их родственников, таких как модель Бонхёффера – ван дер Поля,[bu] были хорошо изучены в математике,[76][bv] вычисление[77] и электроника.[чб] Однако простые модели потенциала генератора и потенциала действия не могут точно воспроизвести частоту нейронных импульсов, близкую к пороговой, и форму импульсов, особенно для механорецепторы словно Тельце Пачини.[78] Более современные исследования сосредоточены на более крупных и интегрированных системах; объединяя модели потенциала действия с моделями других частей нервной системы (например, дендритов и синапсов), исследователи могут изучать нейронные вычисления[79] и просто рефлексы, такие как спасательные рефлексы и другие, контролируемые генераторы центральных паттернов.[80][bx]
Смотрите также
Заметки
- ^ В целом, хотя это простое описание инициации потенциала действия является точным, оно не объясняет такие явления, как блокировка возбуждения (способность препятствовать тому, чтобы нейроны вызывали потенциалы действия, стимулируя их большими шагами тока) и способность вызывать потенциалы действия путем кратковременной стимуляции. гиперполяризация мембраны. Путем анализа динамики системы натриевых и калиевых каналов в мембранном пластыре с использованием вычислительные модели Однако эти явления легко объяснимы.[α]
- ^ Обратите внимание, что эти Волокна Пуркинье являются мышечными волокнами и не связаны с Клетки Пуркинье, которые нейроны найдено в мозжечок.
использованная литература
Сноски
- ^ Ходжкин А.Л., Хаксли А.Ф. (август 1952 г.). «Количественное описание мембранного тока и его применение к проводимости и возбуждению в нерве». Журнал физиологии. 117 (4): 500–44. Дои:10.1113 / jphysiol.1952.sp004764. ЧВК 1392413. PMID 12991237.
- ^ Пикард Б (июнь 1973 г.). «Возможности действия высших растений» (PDF). Ботанический обзор. 39 (2): 188. Дои:10.1007 / BF02859299. S2CID 5026557.
- ^ Летерье С (февраль 2018 г.). "Начальный сегмент аксона: обновленная точка зрения". Журнал неврологии. 38 (9): 2135–2145. Дои:10.1523 / JNEUROSCI.1922-17.2018. ЧВК 6596274. PMID 29378864.
- ^ Purves D, Augustine GJ, Fitzpatrick D, et al., Eds. (2001). "Ионные каналы, управляемые напряжением". Неврология (2-е изд.). Сандерленд, Массачусетс: Sinauer Associates. В архиве из оригинала 5 июня 2018 г.. Получено 29 августа 2017.
- ^ а б c d е ж г час Баллок, Орканд и Гриннелл 1977 г. С. 150–151.
- ^ а б c d е Junge 1981 С. 89–90.
- ^ а б Шмидт-Нильсен 1997, п. 484.
- ^ а б c Purves et al. 2008 г., стр. 48–49; Баллок, Орканд и Гриннелл 1977 г., п. 141; Шмидт-Нильсен 1997, п. 483; Junge 1981, п. 89.
- ^ Стивенс 1966, п. 127.
- ^ Шмидт-Нильсен, п. 484.
- ^ Тамагава Х., Фунатани М., Икеда К. (январь 2016 г.). «Теория адсорбции Линга как механизм генерации мембранного потенциала, наблюдаемый как в живых, так и в неживых системах». Мембраны. 6 (1): 11. Дои:10.3390 / мембраны6010011. ЧВК 4812417. PMID 26821050.
- ^ а б c d е Санес Д.Х., Рех Т.А. (1 января 2012 г.). Развитие нервной системы (Третье изд.). Elsevier Academic Press. С. 211–214. ISBN 9780080923208. OCLC 762720374.
- ^ Куропатка Д. (1991). Кальциевые каналы: их свойства, функции, регуляция и клиническое значение. CRC Press. С. 138–142. ISBN 9780849388071.
- ^ Черный I (1984). Клеточная и молекулярная биология развития нейронов | Ира Блэк | Springer. Springer. п. 103. ISBN 978-1-4613-2717-2. В архиве из оригинала 17 июля 2017 г.
- ^ Педерсен Р. (1998). Текущие темы биологии развития, том 39. Elsevier Academic Press. ISBN 9780080584621.
- ^ Баллок, Орканд и Гриннелл 1977 г., п. 11.
- ^ Сильверторн 2010, п. 253.
- ^ Purves et al. 2008 г., стр. 49–50; Баллок, Орканд и Гриннелл 1977 г., стр. 140–141; Шмидт-Нильсен 1997, с. 480-481.
- ^ Шмидт-Нильсен 1997 С. 483-484.
- ^ Баллок, Орканд и Гриннелл 1977 г., стр. 177–240; Шмидт-Нильсен 1997, pp. 490-499; Стивенс 1966, п. 47–68.
- ^ Баллок, Орканд и Гриннелл 1977 г., стр. 178–180; Шмидт-Нильсен 1997, стр. 490-491.
- ^ Purves et al. 2001 г..
- ^ Purves et al. 2008 г. С. 26–28.
- ^ Шмидт-Нильсен 1997, стр. 535–580; Баллок, Орканд и Гриннелл 1977 г., стр. 49–56, 76–93, 247–255; Стивенс 1966 С. 69–79.
- ^ Баллок, Орканд и Гриннелл 1977 г., стр. 53; Баллок, Орканд и Гриннелл 1977 г. С. 122–124.
- ^ Junge 1981 С. 115–132.
- ^ а б Баллок, Орканд и Гриннелл 1977 г. С. 152–153.
- ^ Баллок, Орканд и Гриннелл 1977 г. С. 444–445.
- ^ Purves et al. 2008 г., п. 38.
- ^ Стивенс 1966 С. 127–128.
- ^ Purves et al. 2008 г. С. 61–65.
- ^ Purves et al. 2008 г., стр. 64–74; Баллок, Орканд и Гриннелл 1977 г., стр. 149–150; Junge 1981, стр. 84–85; Стивенс 1966 С. 152–158.
- ^ а б c Purves et al. 2008 г., п. 47; Purves et al. 2008 г., п. 65; Баллок, Орканд и Гриннелл 1977 г., стр. 147–148; Стивенс 1966, п. 128.
- ^ Гольдин АЛ в Ваксман 2007, Нейрональные каналы и рецепторыС. 43–58.
- ^ Стивенс 1966, п. 49.
- ^ Purves et al. 2008 г., п. 34; Баллок, Орканд и Гриннелл 1977 г., п. 134; Шмидт-Нильсен 1997 С. 478–480.
- ^ а б Purves et al. 2008 г., стр. 49–50; Баллок, Орканд и Гриннелл 1977 г., стр. 140–141; Шмидт-Нильсен 1997 С. 480–481.
- ^ а б c Шмидт-Нильсен 1997 С. 483–484.
- ^ а б c d Purves et al. 2008 г., п. 49.
- ^ а б c d Стивенс 1966 С. 19–20.
- ^ а б c Баллок, Орканд и Гриннелл 1977 г., п. 151; Junge 1981, стр. 4–5.
- ^ а б Баллок, Орканд и Гриннелл 1977 г., п. 152.
- ^ Баллок, Орканд и Гриннелл 1977 г., стр. 147–149; Стивенс 1966 С. 126–127.
- ^ Purves et al. 2008 г., п. 37.
- ^ а б Purves et al. 2008 г., п. 56.
- ^ Баллок, Орканд и Гриннелл 1977 г. С. 160–164.
- ^ Стивенс 1966 С. 21–23.
- ^ Баллок, Орканд и Гриннелл 1977 г. С. 161–164.
- ^ Баллок, Орканд и Гриннелл 1977 г., п. 509.
- ^ Тасаки, я в Поле 1959, стр. 75–121
- ^ Шмидт-Нильсен 1997, Рисунок 12.13.
- ^ Баллок, Орканд и Гриннелл 1977 г., п. 163.
- ^ Ваксман, SG в Ваксман 2007, Рассеянный склероз как нейродегенеративное заболеваниеС. 333–346.
- ^ а б Ралл, З в Кох и Сегев 1989, Кабельная теория дендритных нейроновС. 9–62.
- ^ Сегев I, Fleshman JW, Burke RE (1989). «Компартментные модели сложных нейронов». В Кох С, Сегев I (ред.). Методы нейронного моделирования: от синапсов к сетям. Кембридж, Массачусетс: MIT Press. С. 63–96. ISBN 978-0-262-11133-1. LCCN 88008279. OCLC 18384545.
- ^ Purves et al. 2008 г. С. 52–53.
- ^ Ганонг 1991 С. 59–60.
- ^ Felle HH, Zimmermann MR (июнь 2007 г.). «Системная сигнализация ячменя через потенциалы действия». Planta. 226 (1): 203–14. Дои:10.1007 / s00425-006-0458-y. PMID 17226028. S2CID 5059716.
- ^ Люкен Дж.О. (декабрь 2005 г.). «Среда обитания Dionaea muscipula (ловушка Венеры), Droseraceae, ассоциированная с заливами Каролины». Юго-восточный натуралист. 4 (4): 573–584. Дои:10.1656 / 1528-7092 (2005) 004 [0573: HODMVF] 2.0.CO; 2. ISSN 1528-7092.
- ^ а б Бём Дж., Шерцер С., Крол Э., Крейцер И., фон Мейер К., Лори С. и др. (Февраль 2016). «Венерина мухоловка Dionaea muscipula учитывает индуцированные добычей действия, способствующие поглощению натрия». Текущая биология. 26 (3): 286–95. Дои:10.1016 / j.cub.2015.11.057. ЧВК 4751343. PMID 26804557.
- ^ а б c d е ж Хедрих Р., Нехер Э. (март 2018 г.). "Венерина мухоловка: как возбудимое, плотоядное растение работает". Тенденции в растениеводстве. 23 (3): 220–234. Дои:10.1016 / j.tplants.2017.12.004. PMID 29336976.
- ^ Волков А.Г., Адесина Т., Йованов Э. (май 2007 г.). «Закрытие венериной мухоловки путем электростимуляции моторных клеток». Сигнализация и поведение растений. 2 (3): 139–45. Дои:10.4161 / psb.2.3.4217. ЧВК 2634039. PMID 19516982.
- ^ Градманн, Д; Маммерт, H дюйм Спансвик, Лукас и Дэйнти 1980, Потенциалы действия растенийС. 333–344.
- ^ Буллок и Хорридж 1965.
- ^ Кристан ВБ (октябрь 2016 г.). «Ранняя эволюция нейронов». Текущая биология. 26 (20): R949 – R954. Дои:10.1016 / j.cub.2016.05.030. PMID 27780067.
- ^ Хеллье JL (2014). Мозг, нервная система и их болезни. ABC-Clio. п. 532. ISBN 9781610693387.
- ^ Junge 1981 С. 63–82.
- ^ Кеттенманн и Грантин 1992.
- ^ Снелл, FM в Лавале, Шанн и Эбер, 1969 г., Некоторые электрические свойства микроэлектродов для пипеток с тонкими наконечниками.
- ^ Мангал 1961; МакГенри и Гаррисон 1969; Уорден, Свази и Адельман, 1975 г..
- ^ Финкельштейн Г.В. (2013). Эмиль дю Буа-Реймон: нейробиология, личность и общество в Германии XIX века. Кембридж, Массачусетс. ISBN 9781461950325. OCLC 864592470.
- ^ Олеско, Кэтрин М., и Фредерик Л. Холмс. «Эксперимент, количественная оценка и открытие: ранние физиологические исследования Гельмгольца, 1843-50». В Герман фон Гельмгольц и основы науки девятнадцатого века, изд. Дэвид Кахан, 50-108. Беркли; Лос-Анджелес; Лондон: Калифорнийский университет, 1994.
- ^ Бернштейн 1912.
- ^ Баранаускас Г., Мартина М. (январь 2006 г.). «Натриевые токи активируются без задержки типа Ходжкина и Хаксли в центральных нейронах млекопитающих». Журнал неврологии. 26 (2): 671–84. Дои:10.1523 / jneurosci.2283-05.2006. ЧВК 6674426. PMID 16407565.
- ^ Хоппенстедт 1986.
- ^ Сато, S; Fukai, H; Номура, Т; Дои, S в Reeke et al. 2005 г., Бифуркационный анализ уравнений Ходжкина-Хаксли.С. 459–478.
* ФитцХью, Р в Шванн 1969, Математические модели возбуждения и распространения в нервеС. 12–16.
* Гуккенхаймер и Холмс 1986, стр. 12–16 - ^ Нельсон, Мэн; Ринзель, Дж в Бауэр и Биман 1995, Модель Ходжкина-ХакслиС. 29–49.
* Ринзель, Дж. И Эрментроут, Великобритания; в Кох и Сегев 1989, Анализ нервной возбудимости и колебанийС. 135–169. - ^ Бисвас А., Маниваннан М., Сринивасан М.А. (2015). «Порог вибротактильной чувствительности: нелинейная стохастическая механотрансдукционная модель тельца Пачини». Транзакции IEEE по тактильности. 8 (1): 102–13. Дои:10.1109 / TOH.2014.2369422. PMID 25398183. S2CID 15326972.
- ^ Маккалок 1988, стр. 19–39, 46–66, 72–141; Андерсон и Розенфельд 1988 С. 15–41.
- ^ Получение, ПА в Кох и Сегев 1989, Реконструкция малых нейронных сетейС. 171–194.
журнальные статьи
- ^ MacDonald PE, Rorsman P (февраль 2006 г.). «Колебания, межклеточное взаимодействие и секреция инсулина в бета-клетках поджелудочной железы». PLOS Биология. 4 (2): e49. Дои:10.1371 / journal.pbio.0040049. ЧВК 1363709. PMID 16464129.

- ^ а б Барнетт М.В., Ларкман П.М. (июнь 2007 г.). «Потенциал действия». Практическая неврология. 7 (3): 192–7. PMID 17515599. В архиве из оригинала от 8 июля 2011 г.
- ^ Голдинг Н.Л., Кэт В.Л., Спрустон Н. (декабрь 2001 г.). «Дихотомия обратного распространения потенциала действия в дендритах пирамидных нейронов CA1». Журнал нейрофизиологии. 86 (6): 2998–3010. Дои:10.1152 / ян.2001.86.6.2998. PMID 11731556.
- ^ Sasaki, T., Matsuki, N., Ikegaya, Y. 2011 Модуляция потенциала действия во время аксональной проводимости Science 331 (6017), стр. 599–601
- ^ Aur D, Коннолли CI, Jog MS (ноябрь 2005 г.). «Вычисление направленности спайков с тетродами». Журнал методов неврологии. 149 (1): 57–63. Дои:10.1016 / j.jneumeth.2005.05.006. PMID 15978667. S2CID 34131910.
- ^ Аур Д., Джог, МС., 2010 Нейроэлектродинамика: понимание языка мозга, IOS Press, 2010. Дои:10.3233 / 978-1-60750-473-3-я
- ^ Благородный D (ноябрь 1960 г.). «Сердечная деятельность и возможности водителя ритма на основе уравнений Ходжкина-Хаксли». Природа. 188 (4749): 495–7. Bibcode:1960Натура.188..495Н. Дои:10.1038 / 188495b0. PMID 13729365. S2CID 4147174.
- ^ а б Гольдман Д.Е. (сентябрь 1943 г.). «Потенциал, импеданс и выпрямление в мембранах». Журнал общей физиологии. 27 (1): 37–60. Дои:10.1085 / jgp.27.1.37. ЧВК 2142582. PMID 19873371.
- ^ а б c d е Ходжкин А.Л., Хаксли А.Ф., Кац Б (Апрель 1952 г.). «Измерение вольт-амперных отношений в мембране гигантского аксона Лолиго». Журнал физиологии. 116 (4): 424–48. Дои:10.1113 / jphysiol.1952.sp004716. ЧВК 1392219. PMID 14946712.
* Ходжкин А.Л., Хаксли AF (апрель 1952 г.). «Токи, переносимые ионами натрия и калия через мембрану гигантского аксона Лолиго». Журнал физиологии. 116 (4): 449–72. Дои:10.1113 / jphysiol.1952.sp004717. ЧВК 1392213. PMID 14946713.
* Ходжкин А.Л., Хаксли AF (апрель 1952 г.). «Компоненты проводимости мембраны в гигантском аксоне Лолиго». Журнал физиологии. 116 (4): 473–96. Дои:10.1113 / jphysiol.1952.sp004718. ЧВК 1392209. PMID 14946714.
* Ходжкин А.Л., Хаксли AF (апрель 1952 г.). «Двойное влияние мембранного потенциала на проводимость натрия в гигантском аксоне Лолиго». Журнал физиологии. 116 (4): 497–506. Дои:10.1113 / jphysiol.1952.sp004719. ЧВК 1392212. PMID 14946715.
* Ходжкин А.Л., Хаксли AF (август 1952 г.). «Количественное описание мембранного тока и его применение к проводимости и возбуждению в нерве». Журнал физиологии. 117 (4): 500–44. Дои:10.1113 / jphysiol.1952.sp004764. ЧВК 1392413. PMID 12991237. - ^ Наундорф Б., Вольф Ф., Волгушев М. (апрель 2006 г.). «Уникальные особенности инициации потенциала действия в корковых нейронах» (PDF). Природа. 440 (7087): 1060–3. Bibcode:2006Натура 440.1060Н. Дои:10.1038 / природа04610. PMID 16625198. S2CID 1328840.
- ^ Ходжкин А.Л. (Июль 1937 г.). "Доказательства передачи электрического тока в нерве: Часть I". Журнал физиологии. 90 (2): 183–210. Дои:10.1113 / jphysiol.1937.sp003507. ЧВК 1395060. PMID 16994885.
* Ходжкин А.Л. (Июль 1937 г.). "Доказательства передачи электрического тока в нерве: Часть II". Журнал физиологии. 90 (2): 211–32. Дои:10.1113 / jphysiol.1937.sp003508. ЧВК 1395062. PMID 16994886. - ^ Залц Б (2006). «Приобретение миелина: история успеха». Симпозиум Фонда Новартис. Симпозиумы Фонда Новартис. 276: 15–21, обсуждение 21–5, 54–7, 275–81. Дои:10.1002 / 9780470032244.ch3. ISBN 978-0-470-03224-4. PMID 16805421.
- ^ Поляк С., Пелеш Е. (декабрь 2003 г.). «Локальная дифференцировка миелинизированных аксонов в узлах Ранвье». Обзоры природы. Неврология. 4 (12): 968–80. Дои:10.1038 / nrn1253. PMID 14682359. S2CID 14720760.
- ^ Саймонс М., Троттер Дж. (Октябрь 2007 г.). «Подводя итог: клеточная биология миелинизации». Текущее мнение в нейробиологии. 17 (5): 533–40. Дои:10.1016 / j.conb.2007.08.003. PMID 17923405. S2CID 45470194.
- ^ Сюй К., Теракава С. (август 1999 г.). «Узлы фенестрации и широкое субмиелиновое пространство образуют основу для необычайно быстрого проведения импульсов миелинизированных аксонов креветок». Журнал экспериментальной биологии. 202 (Pt 15): 1979–89. PMID 10395528.
- ^ а б Гурш Дж.Б. (1939). «Скорость проведения и диаметр нервных волокон». Американский журнал физиологии. 127: 131–39. Дои:10.1152 / ajplegacy.1939.127.1.131.
- ^ Лилли Р.С. (март 1925 г.). «Факторы, влияющие на передачу и восстановление в модели пассивного железного нерва». Журнал общей физиологии. 7 (4): 473–507. Дои:10.1085 / jgp.7.4.473. ЧВК 2140733. PMID 19872151. Смотрите также Кейнс и Эйдли 1991, п. 78
- ^ Тасаки I (1939). «Электросальтарная передача нервного импульса и действие наркоза на нервное волокно». Am. J. Physiol. 127: 211–27. Дои:10.1152 / ajplegacy.1939.127.2.211.
- ^ Тасаки I, Такеучи Т. (1941). "Der am Ranvierschen Knoten entstehende Aktionsstrom und seine Bedeutung für die Erregungsleitung". Pflügers Archiv für die gesamte Physiologie. 244 (6): 696–711. Дои:10.1007 / BF01755414. S2CID 8628858.
* Тасаки I, Такеучи Т. (1942). "Weitere Studien über den Aktionsstrom der markhaltigen Nervenfaser und über die elektrosaltatorische Übertragung des nervenimpulses". Pflügers Archiv für die gesamte Physiologie. 245 (5): 764–82. Дои:10.1007 / BF01755237. S2CID 44315437. - ^ Хаксли А.Ф., Stämpfli R (май 1949 г.). «Доказательства скачкообразной проводимости в периферических миелинизированных нервных волокнах». Журнал физиологии. 108 (3): 315–39. Дои:10.1113 / jphysiol.1949.sp004335. ЧВК 1392492. PMID 16991863.
* Хаксли А.Ф., Stampfli R (февраль 1951 г.). «Прямое определение мембранного потенциала покоя и потенциала действия в одиночных миелинизированных нервных волокнах». Журнал физиологии. 112 (3–4): 476–95. Дои:10.1113 / jphysiol.1951.sp004545. ЧВК 1393015. PMID 14825228. - ^ Раштон, Вашингтон (Сентябрь 1951 г.). «Теория влияния размера волокна в мозговом нерве». Журнал физиологии. 115 (1): 101–22. Дои:10.1113 / jphysiol.1951.sp004655. ЧВК 1392008. PMID 14889433.
- ^ а б Хартлайн Д.К., Колман Д.Р. (январь 2007 г.). «Быстрое проведение и эволюция гигантских аксонов и миелинизированных волокон». Текущая биология. 17 (1): Р29-35. Дои:10.1016 / j.cub.2006.11.042. PMID 17208176. S2CID 10033356.
- ^ Миллер Р. Х., Ми С. (ноябрь 2007 г.). «Расслаивающая демиелинизация». Природа Неврология. 10 (11): 1351–4. Дои:10.1038 / nn1995. PMID 17965654. S2CID 12441377.
- ^ Кельвин WT (1855). «К теории электрического телеграфа». Труды Королевского общества. 7: 382–99. Дои:10.1098 / rspl.1854.0093. S2CID 178547827.
- ^ Ходжкин А.Л., Раштон, Вашингтон (декабрь 1946 г.). «Электрические константы нервного волокна ракообразных». Труды Королевского медицинского общества. 134 (873): 444–79. Bibcode:1946RSPSB.133..444H. Дои:10.1098 / rspb.1946.0024. PMID 20281590.
- ^ Süudhof TC (2008). «Выпуск нейротрансмиттера». Фармакология высвобождения нейротрансмиттера. Справочник по экспериментальной фармакологии. 184. С. 1–21. Дои:10.1007/978-3-540-74805-2_1. ISBN 978-3-540-74804-5. PMID 18064409.
- ^ Русаков Д.А. (август 2006 г.). «Са2 + -зависимые механизмы пресинаптического контроля в центральных синапсах». Нейробиолог. 12 (4): 317–26. Дои:10.1177/1073858405284672. ЧВК 2684670. PMID 16840708.
- ^ Юмо И., Дуссо Ф, Грант Нью-Джерси, Пулен Б. (май 2000 г.). «Как нейротоксины ботулина и столбняка блокируют высвобождение нейромедиаторов». Биохимия. 82 (5): 427–46. Дои:10.1016 / S0300-9084 (00) 00216-9. PMID 10865130.
- ^ Zoidl G, Dermietzel R (ноябрь 2002 г.). «О поисках электрического синапса: взгляд в будущее». Исследования клеток и тканей. 310 (2): 137–42. Дои:10.1007 / s00441-002-0632-х. PMID 12397368. S2CID 22414506.
- ^ Brink PR, Cronin K, Ramanan SV (август 1996 г.). «Щелевые соединения в возбудимых клетках». Журнал биоэнергетики и биомембран. 28 (4): 351–8. Дои:10.1007 / BF02110111. PMID 8844332. S2CID 46371790.
- ^ Хирш Н.П. (июль 2007 г.). «Нервно-мышечный переход в здоровье и болезни». Британский журнал анестезии. 99 (1): 132–8. Дои:10.1093 / bja / aem144. PMID 17573397. В архиве из оригинала 16 июля 2012 г.
- ^ Хьюз Б.В., Куснер Л.Л., Камински Х.Дж. (апрель 2006 г.). «Молекулярная архитектура нервно-мышечного соединения». Мышцы и нервы. 33 (4): 445–61. Дои:10.1002 / mus.20440. PMID 16228970. S2CID 1888352.
- ^ а б Ньюмарк Дж. (Январь 2007 г.). «Нервно-паралитические агенты». Невролог. 13 (1): 20–32. Дои:10.1097 / 01.nrl.0000252923.04894.53. PMID 17215724. S2CID 211234081.
- ^ Costa LG (апрель 2006 г.). «Актуальные вопросы токсикологии фосфорорганических соединений». Clinica Chimica Acta; Международный журнал клинической химии. 366 (1–2): 1–13. Дои:10.1016 / j.cca.2005.10.008. PMID 16337171.
- ^ а б c Kléber AG, Руди Y (апрель 2004 г.). «Основные механизмы распространения сердечного импульса и связанные с ним аритмии». Физиологические обзоры. 84 (2): 431–88. Дои:10.1152 / физрев.00025.2003. PMID 15044680. S2CID 21823003.
- ^ Тамарго Дж., Кабальеро Р., Дельпон Е. (январь 2004 г.). «Фармакологические подходы в лечении фибрилляции предсердий». Современная лекарственная химия. 11 (1): 13–28. Дои:10.2174/0929867043456241. PMID 14754423.
- ^ Слейман К.Л., Лонг В.С., Градманн Д. (апрель 1976 г.). ""Потенциалы действия «в Neurospora crassa, мицелиальном грибе». Biochimica et Biophysica Acta (BBA) - Биомембраны. 426 (4): 732–44. Дои:10.1016/0005-2736(76)90138-3. PMID 130926.
- ^ Маммерт Х., Градманн Д. (декабрь 1991 г.). «Потенциалы действия в Acetabularia: измерение и моделирование потоков, управляемых напряжением». Журнал мембранной биологии. 124 (3): 265–73. Дои:10.1007 / BF01994359. PMID 1664861. S2CID 22063907.
- ^ Градманн Д. (2001). «Модели колебаний растений». Aust. J. Plant Physiol. 28 (7): 577–590. Дои:10.1071 / pp01017.
- ^ Бейлби MJ (2007). Потенциал действия у харофитов. Международный обзор цитологии. 257. С. 43–82. Дои:10.1016 / S0074-7696 (07) 57002-6. ISBN 978-0-12-373701-4. PMID 17280895.
- ^ Gradmann D, Hoffstadt J (ноябрь 1998 г.). «Электросвязь переносчиков ионов в растениях: взаимодействие с внутренними концентрациями ионов». Журнал мембранной биологии. 166 (1): 51–9. Дои:10.1007 / s002329900446. PMID 9784585. S2CID 24190001.
- ^ Фромм Дж., Лотнер С. (март 2007 г.). «Электрические сигналы и их физиологическое значение в растениях». Растения, клетки и окружающая среда. 30 (3): 249–257. Дои:10.1111 / j.1365-3040.2006.01614.x. PMID 17263772.
- ^ Leys SP, Mackie GO, Meech RW (май 1999 г.). «Проведение импульса в губке». Журнал экспериментальной биологии. 202 (Pt 9) (9): 1139–50. PMID 10101111.
- ^ Кейнс RD (1989). «Роль гигантских аксонов в исследованиях нервного импульса». BioEssays. 10 (2–3): 90–3. Дои:10.1002 / bies.950100213. PMID 2541698.
- ^ Менье С, Сегев I (ноябрь 2002 г.). «Игра в адвоката дьявола: полезна ли модель Ходжкина-Хаксли?». Тенденции в неврологии. 25 (11): 558–63. Дои:10.1016 / S0166-2236 (02) 02278-6. PMID 12392930. S2CID 1355280.
- ^ Коул К.С. (1949). «Динамические электрические характеристики мембраны аксона кальмара». Arch. Sci. Физиол. 3: 253–8.
- ^ Линг Джи, Джерард Р.В. (декабрь 1949 г.). «Нормальный мембранный потенциал волокон портняжника лягушки». Журнал клеточной и сравнительной физиологии. 34 (3): 383–96. Дои:10.1002 / jcp.1030340304. PMID 15410483.
- ^ Настук В. Л., Ходжкин А. (1950). «Электрическая активность отдельных мышечных волокон». Журнал клеточной и сравнительной физиологии. 35: 39–73. Дои:10.1002 / jcp.1030350105.
- ^ Брок Л.Г., Кумбс Дж. С., Экклс Дж. К. (август 1952 г.). «Регистрация потенциалов мотонейронов с помощью внутриклеточного электрода». Журнал физиологии. 117 (4): 431–60. Дои:10.1113 / jphysiol.1952.sp004759. ЧВК 1392415. PMID 12991232.
- ^ Росс В. Н., Зальцберг Б. М., Коэн Л. Б., Давила Н. В. (декабрь 1974 г.). «Большое изменение поглощения красителя во время действия потенциала действия». Биофизический журнал. 14 (12): 983–6. Bibcode:1974BpJ .... 14..983R. Дои:10.1016 / S0006-3495 (74) 85963-1. ЧВК 1334592. PMID 4429774.
* Grynkiewicz G, Poenie M, Tsien RY (март 1985). «Новое поколение индикаторов Ca2 + со значительно улучшенными флуоресцентными свойствами». Журнал биологической химии. 260 (6): 3440–50. PMID 3838314. - ^ Бу Г, Адамс Х, Бербари Э. Дж., Рубарт М (март 2009 г.). «Равномерная реполяризация потенциала действия в сарколемме кардиомиоцитов желудочков in situ». Биофизический журнал. 96 (6): 2532–46. Bibcode:2009BpJ .... 96.2532B. Дои:10.1016 / j.bpj.2008.12.3896. ЧВК 2907679. PMID 19289075.
- ^ Миллиган СП, Эдвардс К. (июль 1965 г.). «Некоторые факторы, влияющие на продолжительность восстановления способности контрактуры после калиевой контрактуры в поперечно-полосатой мышце лягушки». Журнал общей физиологии. 48 (6): 975–83. Дои:10.1085 / jgp.48.6.975. ЧВК 2195447. PMID 5855511.
* Ричи JM, Rogart RB (1977). «Связывание сакситоксина и тетродотоксина с возбудимой тканью». Обзоры по физиологии, биохимии и фармакологии, том 79. Обзоры физиологии, биохимии и фармакологии. 79. С. 1–50. Дои:10.1007 / BFb0037088. ISBN 0-387-08326-X. PMID 335473.
* Кейнс Р.Д., Ричи Дж. М. (август 1984 г.). «О связывании меченого сакситоксина с гигантским аксоном кальмара». Труды Лондонского королевского общества. Серия B, Биологические науки. 222 (1227): 147–53. Bibcode:1984RSPSB.222..147K. Дои:10.1098 / rspb.1984.0055. PMID 6148754. S2CID 11465181. - ^ Piccolino M (октябрь 1997 г.). «Луиджи Гальвани и животное электричество: два века спустя после основания электрофизиологии». Тенденции в неврологии. 20 (10): 443–8. Дои:10.1016 / S0166-2236 (97) 01101-6. PMID 9347609. S2CID 23394494.
- ^ Piccolino M (апрель 2000 г.). «Двухсотлетие Вольтовской батареи (1800–2000 гг.): Искусственный электрический орган». Тенденции в неврологии. 23 (4): 147–51. Дои:10.1016 / S0166-2236 (99) 01544-1. PMID 10717671. S2CID 393323.
- ^ Бернштейн Дж. (1902). "Untersuchungen zur Thermodynamik der bioelektrischen Ströme". Pflügers Archiv für die gesamte Physiologie. 92 (10–12): 521–562. Дои:10.1007 / BF01790181. S2CID 33229139.
- ^ Коул К.С., Кертис HJ (май 1939 г.). "Электрический импеданс аксона гигантского кальмара во время активности". Журнал общей физиологии. 22 (5): 649–70. Дои:10.1085 / jgp.22.5.649. ЧВК 2142006. PMID 19873125.
- ^ Лапик Л. (1907). «Изучение количественных показателей при электрическом возбуждении с учетом одинаковой поляризации». J. Physiol. Патол. Gen. 9: 620–635.
- ^ Ходжкин А.Л., Кац Б (Март 1949 г.). «Влияние ионов натрия на электрическую активность гигантского аксона кальмара». Журнал физиологии. 108 (1): 37–77. Дои:10.1113 / jphysiol.1949.sp004310. ЧВК 1392331. PMID 18128147.
- ^ Neher E, Сакманн Б. (апрель 1976 г.). «Одноканальные токи, записанные с мембраны денервированных мышечных волокон лягушки». Природа. 260 (5554): 799–802. Bibcode:1976Натура.260..799Н. Дои:10.1038 / 260799a0. PMID 1083489. S2CID 4204985.
* Хэмилл О.П., Марти А., Нехер Э., Сакманн Б., Сигворт Ф.Дж. (август 1981 г.). «Усовершенствованные методы фиксации патч-зажима для записи тока с высоким разрешением от клеток и бесклеточных мембранных участков». Архив Пфлюгерс. 391 (2): 85–100. Дои:10.1007 / BF00656997. PMID 6270629. S2CID 12014433.
* Neher E, Сакманн Б. (март 1992 г.). «Техника патч-кламп». Scientific American. 266 (3): 44–51. Bibcode:1992SciAm.266c..44N. Дои:10.1038 / scientificamerican0392-44. PMID 1374932. - ^ Йеллен Дж. (Сентябрь 2002 г.). «Напряжения калиевые каналы и их родственники». Природа. 419 (6902): 35–42. Bibcode:2002Натура.419 ... 35л. Дои:10.1038 / природа00978. PMID 12214225. S2CID 4420877.
- ^ Дойл Д.А., Мораис Кабрал Дж., Пфуэцнер Р.А., Куо А., Гулбис Дж. М., Коэн С. Л. и др. (Апрель 1998 г.). «Структура калиевого канала: молекулярные основы K + проводимости и селективности». Наука. 280 (5360): 69–77. Bibcode:1998 Наука ... 280 ... 69D. Дои:10.1126 / science.280.5360.69. PMID 9525859.
* Чжоу Ю., Мораис-Кабрал Дж. Х., Кауфман А., Маккиннон Р. (ноябрь 2001 г.). «Химия ионной координации и гидратации, выявленная комплексом K + канал-Fab при разрешении 2,0 A». Природа. 414 (6859): 43–8. Bibcode:2001Натура 414 ... 43Z. Дои:10.1038/35102009. PMID 11689936. S2CID 205022645.
* Цзян Ю., Ли А., Чен Дж., Рута В., Каден М., Чайт Б. Т., Маккиннон Р. (май 2003 г.). «Рентгеновская структура зависимого от напряжения K + канала». Природа. 423 (6935): 33–41. Bibcode:2003Натура 423 ... 33J. Дои:10.1038 / природа01580. PMID 12721618. S2CID 4347957. - ^ Ча А., Снайдер Г.Е., Селвин П.Р., Безанилья Ф. (декабрь 1999 г.). «Движение в атомном масштабе в области измерения напряжения в калиевом канале, измеренное с помощью спектроскопии». Природа. 402 (6763): 809–13. Bibcode:1999Натура 402..809C. Дои:10.1038/45552. PMID 10617201. S2CID 4353978.
* Глаунер К.С., Маннуццу Л.М., Ганди К.С., Исакофф Е.Ю. (декабрь 1999 г.). «Спектроскопическое картирование движения датчика напряжения в калиевом канале шейкер». Природа. 402 (6763): 813–7. Bibcode:1999Натура.402..813Г. Дои:10.1038/45561. PMID 10617202. S2CID 4417476.
* Безанилла Ф (апрель 2000 г.). «Датчик напряжения в ионных каналах, зависимых от напряжения». Физиологические обзоры. 80 (2): 555–92. Дои:10.1152 / Physrev.2000.80.2.555. PMID 10747201. - ^ Catterall WA (февраль 2001 г.). «Трехмерный вид натриевых каналов». Природа. 409 (6823): 988–9, 991. Bibcode:2001Натура.409..988C. Дои:10.1038/35059188. PMID 11234048. S2CID 4371677.
* Сато К., Уэно Ю., Асаи К., Такахаши К., Сато М., Энгель А., Фудзиёси И. (февраль 2001 г.). «Чувствительный к напряжению натриевый канал представляет собой молекулу в форме колокола с несколькими полостями». Природа. 409 (6823): 1047–51. Bibcode:2001Натура.409.1047S. Дои:10.1038/35059098. PMID 11234014. S2CID 4430165. - ^ Skou JC (февраль 1957 г.). «Влияние некоторых катионов на аденозинтрифосфатазу периферических нервов». Biochimica et Biophysica Acta. 23 (2): 394–401. Дои:10.1016/0006-3002(57)90343-8. PMID 13412736.
- ^ Ходжкин А.Л., Кейнс Р.Д. (апрель 1955 г.). «Активный транспорт катионов в гигантских аксонах от Сепии и Лолиго». Журнал физиологии. 128 (1): 28–60. Дои:10.1113 / jphysiol.1955.sp005290. ЧВК 1365754. PMID 14368574.
- ^ Колдуэлл П.С., Ходжкин А.Л., Кейнс Р.Д., Шоу Т.Л. (июль 1960 г.). «Влияние инъекций« богатых энергией »фосфатных соединений на активный транспорт ионов в гигантских аксонах Лолиго». Журнал физиологии. 152 (3): 561–90. Дои:10.1113 / jphysiol.1960.sp006509. ЧВК 1363339. PMID 13806926.
- ^ Caldwell PC, Keynes RD (июнь 1957 г.). «Использование энергии фосфатной связи для экструзии натрия из гигантских аксонов». Журнал физиологии. 137 (1): 12–3С. Дои:10.1113 / jphysiol.1957.sp005830. PMID 13439598. S2CID 222188054.
- ^ Morth JP, Pedersen BP, Toustrup-Jensen MS, Sørensen TL, Petersen J, Andersen JP и др. (Декабрь 2007 г.). «Кристаллическая структура натриево-калиевого насоса». Природа. 450 (7172): 1043–9. Bibcode:2007Натура.450.1043М. Дои:10.1038 / природа06419. PMID 18075585. S2CID 4344526.
- ^ Lee AG, East JM (июнь 2001 г.). «Что структура кальциевого насоса говорит нам о его механизме». Биохимический журнал. 356 (Pt 3): 665–83. Дои:10.1042/0264-6021:3560665. ЧВК 1221895. PMID 11389676.
- ^ * Фитцхью Р. (май 1960 г.). «Пороги и плато в уравнениях нервов Ходжкина-Хаксли». Журнал общей физиологии. 43 (5): 867–96. Дои:10.1085 / jgp.43.5.867. ЧВК 2195039. PMID 13823315.
* Кеплер ТБ, Эбботт Л.Ф., Мардер Э. (1992). «Редукция моделей нейронов на основе проводимости». Биологическая кибернетика. 66 (5): 381–7. Дои:10.1007 / BF00197717. PMID 1562643. S2CID 6789007. - ^ Моррис Ч., Лекар Х (июль 1981 г.). «Колебания напряжения в мышечном волокне усоногих гигантских». Биофизический журнал. 35 (1): 193–213. Bibcode:1981BpJ .... 35..193M. Дои:10.1016 / S0006-3495 (81) 84782-0. ЧВК 1327511. PMID 7260316.
- ^ Фитцхью Р. (июль 1961 г.). «Импульсы и физиологические состояния в теоретических моделях нервной мембраны». Биофизический журнал. 1 (6): 445–66. Bibcode:1961BpJ ..... 1..445F. Дои:10.1016 / S0006-3495 (61) 86902-6. ЧВК 1366333. PMID 19431309.
* Нагумо Дж., Аримото С., Йошизава С. (1962). «Активная линия передачи импульсов, имитирующая аксон нерва». Труды IRE. 50 (10): 2061–2070. Дои:10.1109 / JRPROC.1962.288235. S2CID 51648050. - ^ Бонхёффер К.Ф. (сентябрь 1948 г.). «Активация пассивного железа как модель нервного возбуждения». Журнал общей физиологии. 32 (1): 69–91. Дои:10.1085 / jgp.32.1.69. ЧВК 2213747. PMID 18885679.
* Бонхёффер К.Ф. (1953). "Modelle der Nervenerregung". Naturwissenschaften. 40 (11): 301–311. Bibcode:1953NW ..... 40..301B. Дои:10.1007 / BF00632438. S2CID 19149460.
* ван дер Поль Б (1926). «О релаксационных колебаниях». Философский журнал. 2: 977–992.
* ван дер Поль Б, ван дер Марк Дж (1928). «Сердцебиение рассматривается как расслабляющее колебание и электрическая модель сердца». Философский журнал. 6: 763–775. Дои:10.1080/14786441108564652.
* ван дер Поль Б, ван дер Марк Дж (1929). «Сердцебиение рассматривается как расслабляющее колебание и электрическая модель сердца». Arch. Neerl. Физиол. 14: 418–443. - ^ Эванс Дж. В. (1972). «Уравнения нервного аксона. I. Линейные приближения». Indiana Univ. Математика. J. 21 (9): 877–885. Дои:10.1512 / iumj.1972.21.21071.
* Эванс Дж. У., Феро Дж. (1977). «Теория локальной устойчивости нервного импульса». Математика. Biosci. 37: 23–50. Дои:10.1016/0025-5564(77)90076-1. - ^ Кинер JP (1983). «Аналоговая схема для уравнений Ван дер Поля и ФитцХью-Нагумо». IEEE Transactions по системам, человеку и кибернетике. 13 (5): 1010–1014. Дои:10.1109 / TSMC.1983.6313098. S2CID 20077648.
- ^ Hooper SL (март 2000 г.). «Генераторы центральных паттернов». Текущая биология. 10 (5): R176 – R179. CiteSeerX 10.1.1.133.3378. Дои:10.1016 / S0960-9822 (00) 00367-5. PMID 10713861. S2CID 11388348.
Книги
- Андерсон Дж., Розенфельд Э, ред. (1988). Нейрокомпьютеры: основы исследований. Кембридж, Массачусетс: MIT Press. ISBN 978-0-262-01097-9. LCCN 87003022. OCLC 15860311.
- Бернштейн Дж. (1912). Elektrobiologie, die Lehre von den elektrischen Vorgängen im Organismus auf moderner Grundlage dargestellt [Электробиология, изучение электрических процессов в организме, представленное на современной основе.]. Брауншвейг: Vieweg und Sohn. LCCN 12027986. OCLC 11358569.
- Бауэр Дж. М., Биман Д. (1995). Книга GENESIS: Изучение реалистичных нейронных моделей с помощью общей системы нейронной симуляции. Санта-Клара, Калифорния: TELOS. ISBN 978-0-387-94019-9. LCCN 94017624. OCLC 30518469.
- Бразье М.А. (1961). История электрической активности мозга. Лондон: Питман. LCCN 62001407. OCLC 556863.
- Баллок TH, Хорридж Г.А. (1965). Строение и функции нервной системы беспозвоночных. Серия книг по биологии. Сан-Франциско: В. Х. Фриман. LCCN 65007965. OCLC 558128.
- Баллок TH, Орканд Р., Гриннелл А. (1977). Введение в нервные системы. Серия книг по биологии. Сан-Франциско: В. Х. Фриман. ISBN 978-0-7167-0030-2. LCCN 76003735. OCLC 2048177.
- Поле J, изд. (1959). Справочник по физиологии: критическое, всестороннее изложение физиологических знаний и концепций: Раздел 1: Нейрофизиология. 1. Вашингтон, округ Колумбия: Американское физиологическое общество. LCCN 60004587. OCLC 830755894.
- Ганонг, ВФ (1991). Обзор медицинской физиологии. Обзор медицинской физиологии Ганонга (15-е изд.). Норуолк, Коннектикут: Аплтон и Ланге. ISBN 978-0-8385-8418-7. ISSN 0892-1253. LCCN 87642343. OCLC 23761261.
- Guckenheimer J, Holmes P, ред. (1986). Нелинейные колебания, динамические системы и бифуркации векторных полей.. Прикладные математические науки. 42 (2-е изд.). Нью-Йорк: Springer Verlag. ISBN 978-0-387-90819-9. OCLC 751129941.
- Хоппенстедт (1986). Введение в математику нейронов. Кембриджские исследования по математической биологии. 6. Кембридж: Издательство Кембриджского университета. ISBN 978-0-521-31574-6. LCCN 85011013. OCLC 12052275.
- Юнге Д. (1981). Нервное и мышечное возбуждение (2-е изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0-87893-410-2. LCCN 80018158. OCLC 6486925.
- Кеттенманн Х., Грантин Р., ред. (1992). Практические электрофизиологические методы: руководство по исследованиям in vitro в нейробиологии позвоночных. Нью-Йорк: Вили. ISBN 978-0-471-56200-9. LCCN 92000179. OCLC 25204689.
- Кейнс Р.Д., Эйдли DJ (1991). Нервы и мышцы (2-е изд.). Кембридж: Издательство Кембриджского университета. ISBN 978-0-521-41042-7. LCCN 90015167. OCLC 25204483.
- Кох С, Сегев I, ред. (1989). Методы нейронного моделирования: от синапсов к сетям. Кембридж, Массачусетс: MIT Press. ISBN 978-0-262-11133-1. LCCN 88008279. OCLC 18384545.
- Lavallée M, Schanne OF, Hébert NC, eds. (1969). Стеклянные микроэлектроды. Нью-Йорк: Вили. ISBN 978-0-471-51885-3. LCCN 68009252. OCLC 686.
- Маккаллох WS (1988). Воплощения разума. Кембридж, Массачусетс: MIT Press. ISBN 978-0-262-63114-3. LCCN 88002987. OCLC 237280.
- McHenry LC, Garrison FH (1969). История неврологии Гарнизона. Спрингфилд, штат Иллинойс: Чарльз С. Томас. OCLC 429733931.
- Silverthorn DU (2010). Физиология человека: комплексный подход (5-е изд.). Сан-Франциско: Пирсон. ISBN 978-0-321-55980-7. LCCN 2008050369. OCLC 268788623.
- Spanswick RM, Lucas WJ, Dainty J, ред. (1980). Мембранный транспорт растений: актуальные концептуальные вопросы. Разработки в биологии растений. 4. Амстердам: Elsevier Biomedical Press. ISBN 978-0-444-80192-0. LCCN 79025719. OCLC 5799924.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, Williams SM (2001). «Освобождение передатчиков из синаптических пузырьков». Неврология (2-е изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0-87893-742-4. LCCN 00059496. OCLC 806472664.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, White LE (2008). Неврология (4-е изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0-87893-697-7. LCCN 2007024950. OCLC 144771764.
- Рике Г. Н., Познански Р. Р., Спорнс О., Розенберг Дж. Р., Линдси К. А., ред. (2005). Моделирование в нейронауках: от биологических систем до нейромиметической робототехники. Бока-Ратон, Флорида: Тейлор и Фрэнсис. ISBN 978-0-415-32868-5. LCCN 2005298022. OCLC 489024131.
- Шмидт-Нильсен К (1997). Физиология животных: адаптация и окружающая среда (5-е изд.). Кембридж: Издательство Кембриджского университета. ISBN 978-0-521-57098-5. LCCN 96039295. OCLC 35744403.
- Шванн HP, изд. (1969). Биологическая инженерия. Межвузовская серия электроники. 9. Нью-Йорк: Макгроу-Хилл. ISBN 978-0-07-055734-5. LCCN 68027513. OCLC 51993.
- Стивенс CF (1966). Нейрофизиология: учебник. Нью-Йорк: Джон Уайли и сыновья. LCCN 66015872. OCLC 1175605.
- Ваксман С.Г., изд. (2007). Молекулярная неврология. Берлингтон, Массачусетс: Elsevier Academic Press. ISBN 978-0-12-369509-3. LCCN 2008357317. OCLC 154760295.
- Worden FG, Swazey JP, Adelman G, ред. (1975). Неврология, Пути открытий. Кембридж, Массачусетс: MIT Press. ISBN 978-0-262-23072-8. LCCN 75016379. OCLC 1500233.
веб-страница
- ^ Фитцхью Р., Ижикевич Э. (2006). «Модель ФитцХью-Нагумо». Scholarpedia. 1 (9): 1349. Bibcode:2006SchpJ ... 1.1349I. Дои:10.4249 / scholarpedia.1349.
- ^ "Нобелевская премия по физиологии и медицине 1963 г." (Пресс-релиз). Шведская королевская академия наук. 1963 г. В архиве из оригинала 16 июля 2007 г.. Получено 21 февраля 2010.
- ^ "Нобелевская премия по физиологии и медицине 1991 г." (Пресс-релиз). Шведская королевская академия наук. 1991 г. В архиве из оригинала 24 марта 2010 г.. Получено 21 февраля 2010.
- ^ "Нобелевская премия по физиологии и медицине 1906 г." (Пресс-релиз). Шведская королевская академия наук. 1906 г. В архиве из оригинала от 4 декабря 2008 г.. Получено 21 февраля 2010.
- ^ Warlow C (июнь 2007 г.). «Недавняя эволюция симбиотического ионного канала в семействе бобовых, изменила ионную проводимость и улучшила функцию передачи сигналов кальция». Практическая неврология. Издательская группа BMJ. 7 (3): 192–197. В архиве из оригинала 14 марта 2012 г.. Получено 23 марта 2013.
- ^ "Нобелевская премия по химии 1997 г." (Пресс-релиз). Шведская королевская академия наук. 1997 г. В архиве из оригинала 23 октября 2009 г.. Получено 21 февраля 2010.
дальнейшее чтение
- Эйдли DJ, Stanfield PR (1996). Ионные каналы: молекулы в действии. Кембридж: Издательство Кембриджского университета. ISBN 978-0-521-49882-1.
- Медведь М.Ф., Коннорс Б.В., Парадизо, Массачусетс (2001). Неврология: изучение мозга. Балтимор: Липпинкотт. ISBN 0-7817-3944-6.
- Клэй JR (май 2005 г.). «Возвращение к аксональной возбудимости». Прогресс в биофизике и молекулярной биологии. 88 (1): 59–90. Дои:10.1016 / j.pbiomolbio.2003.12.004. PMID 15561301.
- Deutsch S, Мишели-Цанаку Э (1987). Нейроэлектрические системы. Нью-Йорк: Издательство Нью-Йоркского университета. ISBN 0-8147-1782-9.
- Hille B (2001). Ионные каналы возбудимых мембран. (3-е изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0-87893-321-1.
- Джонстон Д., Ву С.М. (1995). Основы клеточной нейрофизиологии. Кембридж, Массачусетс: Книга Брэдфорда, MIT Press. ISBN 0-262-10053-3.
- Кандел ER, Шварц Дж. Х., Джессел Т. М. (2000). Принципы нейронологии (4-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 0-8385-7701-6.
- Миллер C (1987). «Как работают белки ионных каналов». В Kaczmarek LK, Levitan IB (ред.). Нейромодуляция: биохимический контроль возбудимости нейронов. Нью-Йорк: Издательство Оксфордского университета. С. 39–63. ISBN 978-0-19-504097-5.
- Нельсон Д.Л., Кокс М.М. (2008). Принципы биохимии Ленингера (5-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 978-0-7167-7108-1.
внешние ссылки
- Ионный поток в потенциалах действия в Blackwell Publishing
- Распространение потенциала действия в миелинизированных и немиелинизированных аксонах в Blackwell Publishing
- Генерация АД в клетках сердца и генерация AP в нейронных клетках
- Мембранный потенциал покоя от Жизнь: Наука биологии, WK Purves, D Sadava, GH Orians и HC Heller, 8-е издание, Нью-Йорк: WH Freeman, ISBN 978-0-7167-7671-0.
- Ионное движение и напряжение Гольдмана для произвольных концентраций ионов в Университет Аризоны
- Мультфильм, иллюстрирующий потенциал действия
- Распространение потенциала действия
- Создание потенциала действия: моделирование ограничения тока и напряжения[постоянная мертвая ссылка ]
- Программное обеспечение с открытым исходным кодом для моделирования нейрональных и сердечных потенциалов действия в SourceForge.net
- Введение в потенциал действия, Неврология онлайн (Электронный учебник по неврологии Медицинской школы UT в Хьюстоне)
- Khan Academy: Электротоника и потенциал действия




