Цитрат кальция - Calcium citrate
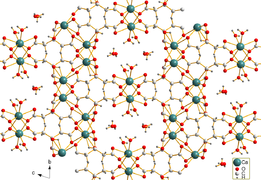
 2D структура цитрата кальция | |
 Тетрагидрат цитрата кальция[1] | |
| Имена | |
|---|---|
| Название ИЮПАК Кальциевая соль 2-гидрокси-1,2,3-пропантрикарбоновой кислоты (2: 3) | |
| Другие имена E333, трикальций дицитрат | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.011.265 |
| Номер ЕС |
|
| Номер E | E333 (антиоксиданты, ...) |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| Ca3(C6ЧАС5О7)2 | |
| Молярная масса | 498,4334 г / моль (безводный) 570,4945 г / моль (тетрагидрат) |
| Внешность | белый порошок |
| Запах | без запаха |
| Плотность | 1,63 г / см3 (безводный) 2,00 г / см3 (тетрагидрат)[1] |
| Температура плавления | Разлагается |
| Точка кипения | Разлагается |
| 0,85 г / л (18 ° С) 0,95 г / л (25 ° С) | |
| Растворимость | не растворим в алкоголь |
| Структура | |
| Триклиник (тетрагидрат) | |
| п1, №2 | |
а = 0,59466 (4) нм, б = 1.02247 (8) нм, c = 1,66496 (13) нм α = 72,213 (7) °, β = 79,718 (7) °, γ = 89,791 (6) °[1] | |
| Опасности | |
| Основной опасности | Раздражающий |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другой катионы | Цитрат натрия |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Цитрат кальция это кальциевая соль из лимонная кислота. Обычно используется как пищевая добавка (E333 ), обычно как консервант, но иногда для аромат. В этом смысле он похож на цитрат натрия. Цитрат кальция также содержится в некоторых пищевых добавках с кальцием (например, Citracal). Кальций составляет 24,1% цитрата кальция (безводного) и 21,1% цитрата кальция (тетрагидрата) по массе. Тетрагидрат встречается в природе как минерал. Эрландит.
Химические свойства
Цитрат кальция плохо растворяется в воде. Игольчатые кристаллы тетрагидрата дицитрата трикальция [Ca3(C6ЧАС5О7)2(ЧАС2O)2] · 2H2O были получены гидротермальным синтезом. Кристаллическая структура представляет собой трехмерную сеть, в которой восьмикратно координированный Ca2+ катионы связаны цитрат-анионами и водородными связями между двумя некоординирующими молекулами кристаллической воды и двумя координирующими молекулами воды.[1]
Производство
Цитрат кальция является промежуточным продуктом при выделении лимонная кислота от ферментация процесс промышленного производства лимонной кислоты.[2] Лимонная кислота в бульонном растворе нейтрализуется гидроксид кальция, осаждая нерастворимый цитрат кальция. Затем его отфильтровывают от остальной части бульона и промывают, чтобы получить чистый цитрат кальция.
- 3 Са (ОН)2 (с) + 2 С6ЧАС8О7 (л) → Ca3(C6ЧАС5О7)2 (с) + 6 часов2О(l)
Полученный таким образом цитрат кальция можно продавать как есть, или он может быть преобразован в лимонную кислоту с использованием разбавленной серной кислоты.
Биологическая роль
У многих людей биодоступность цитрата кальция равен более дешевому карбонат кальция.[3] Однако изменения в пищеварительном тракте могут изменить способ переваривания и всасывания кальция. В отличие от карбоната кальция, который является основным и нейтрализует желудочную кислоту, цитрат кальция не влияет на желудочную кислоту.[4] Карбонат кальция усваивается труднее, чем цитрат кальция,[4] а карбонат кальция несет в себе риск «отскока кислоты» (желудок чрезмерно компенсирует это за счет производства большего количества кислоты),[4] поэтому люди, чувствительные к антацидам или имеющие трудности с выработкой достаточного количества желудочного сока, могут предпочесть цитрат кальция карбонату кальция в качестве добавок. Согласно недавнему исследованию абсорбции кальция после операции обходного желудочного анастомоза,[5] Цитрат кальция может иметь улучшенную биодоступность по сравнению с карбонатом кальция у пациентов с обходным желудочным анастомозом по Roux-en-Y, которые принимают цитрат кальция в качестве пищевая добавка после операции. В основном это связано с изменениями, связанными с тем, где происходит всасывание кальция в пищеварительном тракте этих людей.
использованная литература
- ^ а б c d Хердтвек, Эберхардт; Корнпробст, Тобиас; Зибер, Роланд; Стрейвер, Лео; Планка, Иоганн (2011). «Кристаллическая структура, синтез и свойства тетрагидрата дицитрата трикальция [Ca3(C6ЧАС5О7)2(ЧАС2O)2] · 2H2О ". Zeitschrift für anorganische und allgemeine Chemie. 637 (6): 655–659. Дои:10.1002 / zaac.201100088.
- ^ «Использование извести в химической промышленности». Национальная ассоциация извести. Архивировано из оригинал 29 сентября 2006 г.. Получено 2006-11-25.
- ^ Хини Р.П., Доуэлл М.С., Бирман Дж., Хейл Калифорния, Бендич А. (2001). «Всасываемость и экономическая эффективность при добавлении кальция». Журнал Американского колледжа питания. 20 (3): 239–46. Дои:10.1080/07315724.2001.10719038. PMID 11444420. S2CID 206488.
- ^ а б c «Что нужно знать о кальции». Публикации Гарварда по вопросам здравоохранения. Получено 4 августа 2014.
- ^ Тондапу П., Провост Д., Адамс-Хуэт Б., Симс Т., Чанг С., Сахаи К. (июнь 2009 г.). «Сравнение абсорбции карбоната кальция и цитрата кальция после желудочного обходного анастомоза Roux-en-Y». Хирургия ожирения. 19 (9): 1256–1261. Дои:10.1007 / s11695-009-9850-6. ЧВК 4469176. PMID 19437082.

