Бисульфат калия - Potassium bisulfate
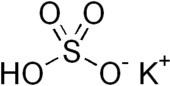 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гидросульфат калия | |
| Другие имена Сульфат калия кислоты | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.722 |
| Номер ЕС |
|
| Номер E | E515 (ii) (регуляторы кислотности, ...) |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2509 |
| |
| |
| Характеристики | |
| ХСО4 | |
| Молярная масса | 136,169 г / моль |
| Внешность | бесцветное твердое вещество |
| Запах | без запаха |
| Плотность | 2,245 г / см3 |
| Температура плавления | 197 ° С (387 ° F, 470 К) |
| Точка кипения | 300 ° С (572 ° F, 573 К) (разлагается) |
| 36,6 г / 100 мл (0 ° С) 49 г / 100 мл (20 ° С) 121,6 г / 100 мл (100 ° С) | |
| Растворимость | растворим в ацетон, этиловый спирт. |
| −49.8·10−6 см3/ моль | |
| Термохимия | |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -1163,3 кДж / моль |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
Классификация ЕС (DSD) (устарело) | Едкий (C) |
| R-фразы (устарело) | R34, R36, R37, R38 |
| S-фразы (устарело) | (S1 / 2), S26, S36 / 37/39, S45 |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 2340 мг * кг−1 |
| Родственные соединения | |
Родственные соединения | Сульфат калия Бисульфат натрия |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бисульфат калия является неорганическое соединение с химическая формула ХСО4 и это калий кислотная соль из серная кислота. Это белое водорастворимое твердое вещество.
Подготовка
В 1985 г. было произведено более 1 млн. Тонн продукции на начальном этапе производства. Мангеймский процесс для получения сульфата калия. Соответствующим преобразованием является экзотермическая реакция хлорида калия и серной кислоты:[1][2]
- KCl + H2ТАК4 → HCl + KHSO4
Бисульфат калия является побочным продуктом при производстве азотная кислота из азотнокислый калий и серная кислота:[3]
- KNO3 + H2ТАК4 → ХСО4 + HNO3
Химические свойства
Термическое разложение форм бисульфата калия пиросульфат калия:[1]
- 2 ХСО4 → K2S2О7 + H2О
При температуре выше 600 ° C пиросульфат калия превращается в сульфат калия и триоксид серы:[4]
- K2S2О7 → K2ТАК4 + ТАК3
Использует
Бисульфат калия обычно используется для приготовления битартрат калия за виноделие.[5] Бисульфат калия также используется как дезинтегрирующий агент в аналитическая химия или как предшественник подготовить персульфат калия, мощный окислитель.[6]
Вхождение
Меркаллит, то минералогический форма бисульфата калия, встречается очень редко.[7] Мисенит еще одна более сложная форма бисульфата калия с формулой K8ЧАС6(ТАК4)7.
Рекомендации
- ^ а б Вашингтон Вили, Харви (1895). Принципы и практика сельскохозяйственного анализа: удобрения. Истон, Пенсильвания: Chemical Publishing Co., стр.218. Получено 31 декабря 2015.
Дисульфат калия.
- ^ Х. Шульц, Г. Бауэр, Э. Шахль, Ф. Хагедорн, П. Шмиттингер (2005). «Соединения калия». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a22_039. ISBN 978-3527306732.CS1 maint: использует параметр авторов (связь)
- ^ Прадёт, Патнаик (2003). Справочник неорганических химикатов. Нью-Йорк: Макгроу-Хилл. п. 636. ISBN 978-0070494398.
- ^ Иредель Диллард Хиндс, Джон (1908). Неорганическая химия: с элементами физической и теоретической химии. Нью-Йорк: Джон Вили и сыновья. п.547. Получено 31 декабря 2015.
Дисульфат калия.
- ^ Вайсблатт, Джейн; Монтни, Чарльз Б. (2006). Химические соединения. ISBN 978-1-4144-0453-0.
- ^ Брауэр, Георг (1963). Справочник по препаративной неорганической химии Vol. 1, 2-е изд.. Нью-Йорк: Academic Press. п. 392. ISBN 978-0121266011.
- ^ «Меркаллит: информация о минералах, данные и местонахождение». mindat.org. Получено 2019-05-08.
| Этот неорганический сложный –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
