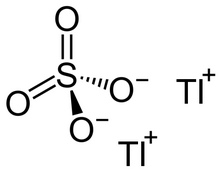
Сульфат таллия (I) - Thallium(I) sulfate
 | |
| Имена | |
|---|---|
| Другие имена Сульфат таллия, сульфат таллия | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.365 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| Tl2ТАК4 | |
| Молярная масса | 504,83 г / моль |
| Внешность | белые призмы или густой белый порошок |
| Запах | без запаха |
| Плотность | 6,77 г / см3 |
| Температура плавления | 632 ° С (1170 ° F, 905 К) |
| 2,70 г / 100 мл (0 ° С) 4,87 г / 100 мл (20 ° С) 18,45 г / 100 мл (100 ° С) | |
| −112.6·10−6 см3/ моль | |
| 1.860 | |
| Структура | |
| ромбовидный | |
| Опасности | |
Классификация ЕС (DSD) (устарело) | |
| R-фразы (устарело) | R28, R38, R48 / 25, R51 / 53 |
| S-фразы (устарело) | (S1 / 2), S13, S36 / 37, S45, S61 |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 16 мг / кг (крыса, перорально) 23,5 мг / кг (мышь, перорально)[1] |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сульфат таллия (I) (Tl2ТАК4) или же талловый сульфат это сульфат соль таллий в обычной степени окисления +1, что обозначено римской цифрой I. Его часто называют просто сульфатом таллия.[2]
Использует
В течение последних двух столетий Tl2ТАК4 использовались для различных медицинских процедур, но были заброшены. В конце 1900-х годов он нашел применение в основном для родентициды.[3] Эти приложения были запрещены в 1975 году в США из-за неселективной природы его токсичности. Сульфат таллия (I) подавляет рост растений, предотвращая прорастание. Tl2ТАК4 в основном используется сегодня как источник Tl+ в исследовательской лаборатории. Это предшественник сульфид таллия (I) (Tl2S), который демонстрирует высокую электропроводность при воздействии инфракрасный свет.
Подготовка
Сульфат таллия (I) получают в результате реакции металлического таллия с серная кислота с последующим кристаллизация.
Структура
Tl2ТАК4 принимает ту же структуру, что и K2ТАК4. В водном растворе таллий (I) катионы и сульфат анионы разделены и очень растворенный. Кристаллы сульфата таллия (I) имеют C2 симметрия.
Токсичность
Сульфат таллия (I) растворим в воде, и его токсическое действие обусловлено катионом таллия (I). Средняя смертельная доза сульфата таллия (I) для взрослого составляет около 1 грамма. Поскольку сульфат таллия (I) представляет собой простой порошок с неотличимыми свойствами, его можно легко принять за более безвредные химические вещества. Он может попасть в организм при проглатывании, вдыхании или при контакте с кожей. Катион таллия (I) очень похож на калий и натрий катионы, необходимые для жизни. После того, как ион таллия попадает в клетку, многие процессы, которые транспорт калия и натрия нарушены. Из-за его ядовитой природы многие западные страны запретили использование сульфата таллия (I) в продуктах для домашнего использования, и многие компании также прекратили использование этого соединения.
Дозировка более 500 мг считается смертельной. Сульфат таллия (I) после попадания в организм концентрируется в почках, печени, головном мозге и других тканях организма.
Сульфат таллия (I) использовался в Израиль контролировать популяцию грызунов; есть подозрение, что в 1950-х годах это привело к исчезновению коричневая рыба сова.[4]
Источники
Рекомендации
- ^ «Таллий (растворимые соединения, как Tl)». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Мик, Генрих; Вольф, Ханс Уве (2000). «Таллий и соединения таллия». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a26_607.
- ^ Лист данных Всемирной организации здравоохранения по пестицидам № 10 (1975)
- ^ Мендельсон, Х. Экологические последствия химической борьбы с грызунами и шакалами в Израиле в LPO Mission Rapaces
внешняя ссылка
- Международная карта химической безопасности 0336
- Карманный справочник NIOSH по химической опасности
- Паспорт пестицидов (ВОЗ /ФАО )
- Каунасский технологический университет
- Химический факультет Университета Висконсин-Мэдисон
- Смитсоновский национальный зоологический парк
- ИГИЛ проводит испытания химического оружия на живых жертвах

