Карнитин пальмитоилтрансфераза I - Carnitine palmitoyltransferase I
Карнитин пальмитоилтрансфераза I (CPT1) также известный как карнитинацилтрансфераза I, CPTI, CAT1, КоА: карнитинацилтрансфераза (CCAT), или же пальмитоилСоА трансфераза I, это митохондриальный фермент ответственны за образование ацилкарнитинов, катализируя перенос ацильной группы длинноцепочечного жирного ацил-КоА от кофермента А к l-карнитин. Товар часто Пальмитоилкарнитин (отсюда и название), но другие жирные кислоты также могут быть субстратами.[5][6] Он является частью семейства ферментов, называемых карнитинацилтрансферазами.[7] Этот «препарат» позволяет последующее перемещение ацилкарнитина из цитозоль в межмембранное пространство митохондрий.
Три изоформы из CPT1 в настоящее время известны: CPT1A, CPT1B и CPT1C. CPT1 связан с внешняя митохондриальная мембрана. Этот фермент может подавляться малонил-КоА, первый промежуточный промежуточный продукт, образующийся в процессе синтеза жирных кислот. Его роль в метаболизм жирных кислот делает CPT1 важным при многих метаболических нарушениях, таких как сахарный диабет. С его Кристальная структура не известно, его точный механизм действия еще предстоит определить.
Структура

CPT1 - это интегральный мембранный белок который связан с внешней мембраной митохондрий через трансмембранные области в пептид цепь. И N-, и C-терминал домены подвержены цитозольный сторона мембраны.[8]
В тканях млекопитающих существуют три изоформы CPT1. Изоформа печени (CPT1A или CPTI-L) находится по всему телу в митохондриях всех клеток, кроме клеток скелетных мышц и коричневые жировые клетки.[9][10] Изоформа мышц (CPT1B или CPTI-M) высоко экспрессируется в клетках сердца и скелетных мышц, а также в коричневых жировых клетках.[8][9][10] Третья изоформа, изоформа мозга (CPT1C), была выделена в 2002 году. Она экспрессируется преимущественно в головном мозге и семенниках. Мало что известно о CPT1C.[11][12]
Точная структура любой из изоформ CPT1 еще не определена, хотя множество in silico модели для CPT1 были созданы на основе близкородственных карнитинацилтрансфераз, таких как карнитинацетилтрансфераза (CRAT).[13]
Важное структурное различие между CPT1 и CPT2, CRAT и карнитиноктаноилтрансфераза (COT) состоит в том, что CPT1 содержит дополнительный домен на своем N-концевой состоящий примерно из 160 аминокислот. Было определено, что этот дополнительный N-концевой домен важен для ключевой ингибиторной молекулы CPT1, малонил-КоА.[14]
Два разных участок связывания были предложены для использования в CPT1A и CPT1B. «Сайт А» или «сайт КоА», по-видимому, связывает как малонил-КоА, так и пальмитоил-КоА, а также другие молекулы, содержащие кофермент А, предполагая, что фермент связывает эти молекулы посредством взаимодействия с фрагментом кофермента А. Было высказано предположение, что малонил-КоА может вести себя как конкурентный ингибитор CPT1A на этом сайте. Второй «O-сайт» был предложен для более прочного связывания малонил-КоА, чем для A-сайта. В отличие от сайта A, сайт O связывается с малонил-КоА через дикарбонильную группу малонатный фрагмент малонил-КоА. Связывание малонил-КоА с сайтами A и O ингибирует действие CPT1A, исключая связывание карнитина с CPT1A.[15] Поскольку кристаллическая структура CPT1A еще не была выделена и отображена, ее точная структура еще предстоит выяснить.
Функция
Ферментный механизм
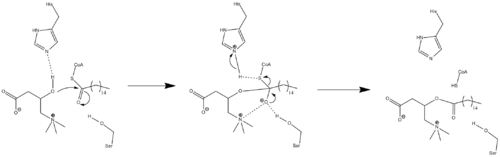
Поскольку данные о кристаллической структуре в настоящее время недоступны, точный механизм CPT1 в настоящее время не известен. Было постулировано несколько различных возможных механизмов для CPT1, оба из которых включают гистидин остаток 473 как ключевой каталитический остаток. Один из таких механизмов, основанный на модели карнитинацетилтрансферазы, показан ниже, в котором His 473 депротонирует карнитин, в то время как соседний серин остаток стабилизирует тетраэдрический оксианион средний.[7]
Был предложен другой механизм, предполагающий, что каталитическая триада состоящий из остатков Cys-305, His-473 и Asp-454, выполняет стадию переноса ацила катализ.[16] Этот каталитический механизм включает образование тиоацил-фермента. ковалентный промежуточное звено с Cys-305.
Биологическая функция
Система карнитин-пальмитоилтрансферазы является важным этапом в бета-окисление из длинноцепочечные жирные кислоты. Эта система переноса необходима, потому что, пока жирные кислоты активируются (в виде тиоэфир связь с коферментом А) на внешней митохондриальной мембране, активированные жирные кислоты должны окисляться внутри митохондриальный матрикс. Длинноцепочечные жирные кислоты, такие как пальмитоил-КоА, в отличие от коротко- и среднецепочечных жирных кислот, не могут свободно размытый сквозь митохондриальная внутренняя мембрана, и требуют, чтобы система шаттла была доставлена в митохондриальный матрикс.[17]

Карнитин пальмитоилтрансфераза I является первым компонентом и ограничивающий шаг карнитин-пальмитоилтрансферазной системы, катализирующей перенос ацильной группы от кофермента А к карнитину с образованием пальмитоилкарнитин. А транслоказа затем переносит ацилкарнитин через внутреннюю митохондриальную мембрану, где он снова превращается в пальмитоил-КоА.
Действуя как акцептор ацильной группы, карнитин может также играть роль регулятора внутриклеточного соотношения КоА: ацил-КоА.[18]
Регулирование
CPT1 ингибируется малонил-КоА, хотя точный механизм ингибирования остается неизвестным. Было показано, что изоформа скелетных мышц и сердца CPT1, CPT1B, в 30–100 раз более чувствительна к ингибированию малонил-КоА, чем CPT1A. Это ингибирование является хорошей мишенью для будущих попыток регулировать CPT1 для лечения метаболических нарушений.[19]
Ацетил-КоА карбоксилаза (АСС), фермент, который катализирует образование малонил-КоА из ацетил-КоА, важен для регуляции метаболизма жирных кислот. Ученые продемонстрировали, что ACC2 нокаутные мыши имеют меньше жира и веса по сравнению с дикого типа мышей. Это результат снижения активности АСС, что вызывает последующее снижение концентрации малонил-КоА. Эти пониженные уровни малонил-КоА, в свою очередь, предотвращают ингибирование СРТ1, вызывая окончательное увеличение окисления жирных кислот.[20] Поскольку клетки сердца и скелетных мышц обладают низкой способностью к синтезу жирных кислот, АСС может действовать в этих клетках исключительно как регуляторный фермент.
Клиническое значение
Форма "CPT1A" связана с дефицит карнитин-пальмитоилтрансферазы I.[21] Это редкое заболевание связано с риском печеночная энцефалопатия, гипокетотическая гипогликемия, судороги и внезапная неожиданная смерть в младенчестве.[22]
CPT1 связан с диабет 2 типа и резистентность к инсулину. Такие заболевания, наряду со многими другими проблемами со здоровьем, приводят к повышению уровня свободных жирных кислот (СЖК) у людей, накоплению жира в скелетных мышцах и снижению способности мышц окислять жирные кислоты. CPT1 участвует в возникновении этих симптомов. Повышенный уровень малонил-КоА, вызванный гипергликемия и гиперинсулинемия подавляют СРТ1, что вызывает последующее снижение транспорта длинноцепочечных жирных кислот в митохондрии мышц и сердца, уменьшая окисление жирных кислот в таких клетках. Шунтирование LCFAs от митохондрий приводит к наблюдаемому увеличению уровней FFA и накоплению жира в скелетных мышцах.[23][24]
Его важность в метаболизме жирных кислот делает CPT1 потенциально полезным ферментом, на котором следует сосредоточиться при разработке методов лечения многих других метаболических нарушений.[25]
Взаимодействия
Известно, что CPT1 взаимодействует со многими белками, включая белки семейства NDUF, PKC1 и ENO1.[26]
В ВИЧ Vpr усиливает экспрессию мРНК карнитинпальмитоилтрансферазы I (CPT1), индуцированную PPARbeta / дельта PDK4 в клетках.[27] Нокдаун CPT1A путем скрининга библиотеки shRNA ингибирует репликацию ВИЧ-1 в культивируемых Т-клетках Jurkat.[28]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000110090 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000024900 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ ван дер Лей Ф. Р., Хёйкман Н. С., Бумсма С., Койперс Дж. Р., Бартельд Б. (2000). «Геномика генов карнитинацилтрансферазы человека». Молекулярная генетика и метаболизм. 71 (1–2): 139–53. Дои:10.1006 / мг.2000.3055. PMID 11001805.
- ^ Боннефонт Дж. П., Джуади Ф., Прип-Буус С., Гобин С., Мюнхен А., Бастин Дж. (2004). «Карнитин пальмитоилтрансферазы 1 и 2: биохимические, молекулярные и медицинские аспекты». Молекулярные аспекты медицины. 25 (5–6): 495–520. Дои:10.1016 / j.mam.2004.06.004. PMID 15363638.
- ^ а б Jogl G, Tong L (январь 2003 г.). «Кристаллическая структура карнитинацетилтрансферазы и значение для каталитического механизма и транспорта жирных кислот». Клетка. 112 (1): 113–22. Дои:10.1016 / S0092-8674 (02) 01228-X. PMID 12526798. S2CID 18633987.
- ^ а б Ямазаки Н., Яманака Ю., Хашимото Ю., Шинохара Ю., Шима А., Терада Х (июнь 1997 г.). «Структурные особенности гена, кодирующего карнитин пальмитоилтрансферазу I мышечного типа человека». Письма FEBS. 409 (3): 401–406. Дои:10.1016 / S0014-5793 (97) 00561-9. PMID 9224698. S2CID 39046724.
- ^ а б Браун Н.Ф., Хилл Дж. К., Эссер В., Киркланд Дж. Л., Корки Б. Е., Фостер Д. В., МакГарри Д. Д. (октябрь 1997 г.). «Белые адипоциты мыши и клетки 3T3-L1 демонстрируют аномальный паттерн экспрессии изоформы карнитин-пальмитоилтрансферазы (CPT) I во время дифференцировки. Межтканевая и межвидовая экспрессия ферментов CPT I и CPT II». Биохимический журнал. 327 (1): 225–31. Дои:10.1042 / bj3270225. ЧВК 1218784. PMID 9355756.
- ^ а б Ли Дж., Эллис Дж. М., Вольфганг М. Дж. (Январь 2015 г.). «Окисление жирных кислот жировой ткани необходимо для термогенеза и потенцирует воспаление, вызванное окислительным стрессом». Отчеты по ячейкам. 10 (2): 266–279. Дои:10.1016 / j.celrep.2014.12.023. ЧВК 4359063. PMID 25578732.
- ^ Price N, van der Leij F, Jackson V, Corstorphine C, Thomson R, Sorensen A, Zammit V (октябрь 2002 г.). «Новый белок, экспрессируемый мозгом, родственный карнитин-пальмитоилтрансферазе I». Геномика. 80 (4): 433–442. Дои:10.1006 / geno.2002.6845. PMID 12376098.
- ^ Лаврентьев Е.Н., Матта С.Г., Кук Г.А. (февраль 2004 г.). «Экспрессия трех изоформ карнитинпальмитоилтрансферазы-I в 10 областях мозга крыс во время кормления, голодания и диабета». Сообщения о биохимических и биофизических исследованиях. 315 (1): 174–178. Дои:10.1016 / j.bbrc.2004.01.040. PMID 15013442.
- ^ Морильяс М., Лопес-Виньяс Е., Валенсия А., Серра Д., Гомес-Пуэртас П., Хегардт Ф. Г., Асинс Г. (май 2004 г.). «Структурная модель карнитин пальмитоилтрансферазы I на основе кристалла карнитинацетилтрансферазы». Биохимический журнал. 379 (Pt 3): 777–784. Дои:10.1042 / BJ20031373. ЧВК 1224103. PMID 14711372.
- ^ Woldegiorgis G, Dai J, Arvidson D (2005). "Структурно-функциональные исследования митохондриальных карнитин-пальмитоилтрансфераз I и II". Monatshefte für Chemie. 136 (8): 1325–1340. Дои:10.1007 / s00706-005-0334-7. S2CID 84170080.
- ^ Лопес-Виньяс Е., Бентебибель А., Гурунатан С., Морильяс М., де Арриага Д., Серра Д., Асинс Г., Хегардт Ф. Г., Гомес-Пуэртас П. (июнь 2007 г.). «Определение с помощью функционального и структурного анализа двух сайтов малонил-КоА в карнитин пальмитоилтрансферазе 1А». Журнал биологической химии. 282 (25): 18212–24. Дои:10.1074 / jbc.M700885200. PMID 17452323.
- ^ Лю Х., Чжэн Дж., Требер М., Дай Дж., Вольдегиоргис Дж. (Февраль 2005 г.). «Сканирующий цистеин мутагенез карнитин-пальмитоилтрансферазы I в мышцах показывает, что единственный остаток цистеина (Cys-305) важен для катализа». Журнал биологической химии. 280 (6): 4524–4531. Дои:10.1074 / jbc.M400893200. PMID 15579906.
- ^ Берг Дж. М., Тимочо Дж. Л., Страйер Л., «Биохимия», 6-е издание 2007 г.
- ^ Джогл Г., Сяо Ю.С., Тонг Л. (ноябрь 2004 г.). «Структура и функции карнитин-ацилтрансфераз». Летопись Нью-Йоркской академии наук. 1033 (1): 17–29. Дои:10.1196 / анналы.1320.002. PMID 15591000. S2CID 24466239.
- ^ Ши Дж., Чжу Х., Арвидсон Д. Н., Вольдегиоргис Дж. (Февраль 2000 г.). «Первые 28 N-концевых аминокислотных остатков карнитин-пальмитоилтрансферазы I сердечной мышцы человека необходимы для чувствительности к малонил-КоА и связывания с высоким сродством». Биохимия. 39 (4): 712–717. Дои:10.1021 / bi9918700. PMID 10651636.
- ^ Абу-Эльхейга Л., О В., Кордари П., Вакил С.Дж. (сентябрь 2003 г.). «Мыши с мутантной ацетил-КоА-карбоксилазой 2 защищены от ожирения и диабета, вызванного диетами с высоким содержанием жиров и углеводов». Труды Национальной академии наук Соединенных Штатов Америки. 100 (18): 10207–10212. Дои:10.1073 / pnas.1733877100. ЧВК 193540. PMID 12920182.
- ^ Огава Е., Канадзава М., Ямамото С., Оцука С., Огава А., Отаке А., Такаянаги М., Коно Ю. (2002). «Анализ экспрессии двух мутаций при дефиците карнитин-пальмитоилтрансферазы IA». Журнал генетики человека. 47 (7): 342–7. Дои:10.1007 / с100380200047. PMID 12111367.
- ^ Коллинз С.А., Синклер Дж., Макинтош С., Бамфорт Ф., Томпсон Р., Соболь И., Осборн Дж., Корриво А., Сантос М., Хэнли Б., Гринберг С. Р., Валланс Х, Арбор Л. (2010). «Распространенность карнитин-пальмитоилтрансферазы 1A (CPT1A) P479L у живых новорожденных в Юконе, Северо-Западных территориях и Нунавуте». Молекулярная генетика и метаболизм. 101 (2–3): 200–204. Дои:10.1016 / j.ymgme.2010.07.013. PMID 20696606.
- ^ Расмуссен BB, Holmbäck UC, Volpi E, Morio-Liondore B, Paddon-Jones D, Wolfe RR (декабрь 2002 г.). «Малонил-кофермент А и регулирование функциональной активности карнитинпальмитоилтрансферазы-1 и окисления жиров в скелетных мышцах человека». Журнал клинических исследований. 110 (11): 1687–93. Дои:10.1172 / JCI15715. ЧВК 151631. PMID 12464674.
- ^ McGarry JD, Mills SE, Long CS, Foster DW (июль 1983 г.). «Наблюдения за сродством к карнитину и чувствительностью к малонил-КоА карнитин-пальмитоилтрансферазы I в тканях животных и человека. Демонстрация присутствия малонил-КоА в непеченочных тканях крысы». Биохимический журнал. 214 (1): 21–8. Дои:10.1042 / bj2140021. ЧВК 1152205. PMID 6615466.
- ^ Schreurs M, Kuipers F, van der Leij FR (2010). «Регулирующие ферменты бета-окисления митохондрий как мишени для лечения метаболического синдрома». Обзоры ожирения. 11 (5): 380–8. Дои:10.1111 / j.1467-789X.2009.00642.x. PMID 19694967. S2CID 24954036.
- ^ Havugimana PC, Hart GT, Nepusz T, Yang H, Turinsky AL, Li Z, Wang PI, Boutz DR, Fong V, Phanse S, Babu M, Craig SA, Hu P, Wan C, Vlasblom J, Dar VU, Bezginov A , Кларк GW, Wu GC, Wodak SJ, Tillier ER, Paccanaro A, Marcotte EM, Emili A (август 2012 г.). «Перепись человеческих растворимых белковых комплексов». Клетка. 150 (5): 1068–81. Дои:10.1016 / j.cell.2012.08.011. ЧВК 3477804. PMID 22939629.
- ^ Шривастав С., Чжан Л., Окамото К., Ли Х., Лагранья С., Абэ Й., Баласубраманьям А., Лопащук Г. Д., Кино Т., Копп Дж. Б. (сентябрь 2013 г.). «ВИЧ-1 Vpr усиливает опосредованную PPARβ / δ транскрипцию, увеличивает экспрессию PDK4 и снижает активность PDC». Молекулярная эндокринология. 27 (9): 1564–76. Дои:10.1210 / me.2012-1370. ЧВК 3753422. PMID 23842279.
- ^ Йунг М.Л., Хузет Л., Йедавалли В.С., Джанг К.Т. (июль 2009 г.). «Скрининг короткой шпилечной РНК по всему геному Т-клеток jurkat на предмет белков человека, способствующих продуктивной репликации ВИЧ-1». Журнал биологической химии. 284 (29): 19463–73. Дои:10.1074 / jbc.M109.010033. ЧВК 2740572. PMID 19460752.




