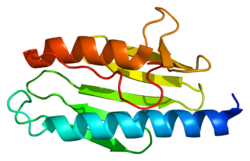
Фратаксин - Frataxin
Фратаксин это белок что у человека кодируется FXN ген.[5][6]
Он расположен в митохондрии, и мРНК фратаксина в основном экспрессируется в тканях с высокой скоростью метаболизма. Функция фратаксина не ясна, но он участвует в сборке железо-серных кластеров. Было предложено действовать как шаперон железа или как запасной белок. Пониженная экспрессия фратаксина является причиной атаксии Фридрейха.
Структура
Рентгеновская кристаллография показал, что человеческий фратаксин состоит из β-лист который поддерживает пару параллельных α-спирали, образуя компактный бутерброд αβ.[7] Фратаксин гомологи у других видов похожи, разделяя ту же основную структуру. Однако последовательности хвоста фратаксина, отходящие от конца одной спирали, расходятся по последовательности и различаются по длине. Фратаксин человека имеет более длинную хвостовую последовательность, чем фратаксин, обнаруженный в бактериях или дрожжах. Предполагается, что цель хвоста - стабилизировать белок.[7]
Как большинство митохондриальные белки, фратаксин синтезируется в цитоплазматическом рибосомы в виде больших молекул-предшественников с последовательностями, нацеленными на митохондрии. При входе в митохондрии молекулы разрушаются протеолитический реакция на получение зрелого фратаксина.[8]
Функция
Фратаксин локализуется в митохондрия. Функция фратаксина не совсем ясна, но, похоже, он участвует в сборке железо-серные кластеры. Было предложено действовать как утюг сопровождающий или белок хранения железа.[9]
Фратаксин мРНК преимущественно выразил в ткани с высоким метаболический ставка (включая печень, почки, бурый жир и сердце). Мышь и дрожжи фратаксин гомологи содержат потенциальную N-концевую целевую последовательность митохондрий, и человек Было обнаружено, что фратаксин совместно локализуется с митохондриальным белком. Кроме того, нарушение дрожжи было показано, что ген приводит к дисфункции митохондрий. Атаксия Фридрейха считается митохондриальным болезнь вызвано мутация в ядерном геноме (в частности, расширение интронного триплетного повтора GAA в гене FXN, который кодирует белок фратаксин).[5][10][11]
Клиническое значение
Пониженная экспрессия фратаксина является причиной Атаксия Фридрейха (FRDA), а нейродегенеративный болезнь. Снижение экспрессии гена фратаксина может быть связано либо с подавлением транскрипции гена фратаксина из-за эпигенетический модификации в хромосомной сущности[12] или от неспособности сращивание расширенный GAA повторяется в первом интрон пре-мРНК, наблюдаемой у бактерий[13] и клетки человека[14] или оба. Расширение интронных тринуклеотидных повторов GAA приводит к атаксии Фридрейха.[15] Этот расширенный повтор вызывает R-петля формирование, и с помощью повторного нацеливания олигонуклеотид нарушение R-петли может реактивировать экспрессию фратаксина.[16]
96% пациентов с FRDA имеют ГАА экспансия тринуклеотидного повтора в интроне 1 обоих аллели их гена FXN.[17] В целом это приводит к снижению фратаксина. мРНК синтез и снижение (но не отсутствие) белка фратаксина у людей с FRDA. (Подмножество пациентов с FRDA имеет расширение GAA в одной хромосоме и точечная мутация в экзоне FXN в другой хромосоме.) В типичном случае длина аллеля с более коротким расширением GAA обратно коррелирует с уровнями фратаксина. Периферические ткани пациентов с FRDA обычно имеют менее 10% уровней фратаксина, характерных для здоровых людей.[17] Более низкий уровень фратаксина приводит к более раннему началу заболевания и более быстрому прогрессированию.
FRDA характеризуется атаксией, потерей чувствительности и кардиомиопатией. Причина возникновения этих симптомов из-за дефицита фратаксина не совсем ясна. На клеточном уровне это связано с накоплением железа в митохондриях и повышенной чувствительностью к окислителям. По причинам, которые до конца не изучены, это в первую очередь влияет на ткань ганглии задних корешков, мозжечок, и сердечная мышца.[8]
Исследования на животных
У мышей полная инактивация гена FXN летальна на ранней эмбриональной стадии.[18] Хотя почти все организмы экспрессируют гомолог фратаксина, повторение GAA в интроне 1 существует только у людей и других приматы, поэтому мутация, вызывающая FDRA, не может возникать естественным образом у других животных. Ученые разработали несколько вариантов моделирования этого заболевания на мышах. Один из подходов - подавить экспрессию фратаксина только в одном конкретном интересующем типе ткани: сердце (модифицированные таким образом мыши называются MCK), все нейроны (NSE) или только спинной мозг и мозжечок (PRP).[19] Другой подход включает вставку расширения GAA в первый интрон гена FXN мыши, который должен ингибировать продукцию фратаксина, как и у людей. Мышей, гомозиготных по этому модифицированному гену, называют KIKI (knock-in knock-in), а сложные гетерозиготы образованный путем скрещивания мышей KIKI с фратаксином нокаутные мыши называются KIKO (нокаут-нокаут). Однако даже мыши KIKO экспрессируют 25-36% нормального уровня фратаксина и проявляют очень легкие симптомы. Последний подход предполагает создание трансгенный мышей с расширенной GAA версией гена фратаксина человека. Этих мышей называют YG22R (одна последовательность GAA из 190 повторов) и YG22R (две последовательности GAA из 90 и 190 повторов). Эти мыши проявляют симптомы, сходные с симптомами пациентов-людей.[19]
Сверхэкспрессия фратаксина в Дрозофила показал повышение антиоксидантной способности, устойчивости к окислительному стрессу и долголетия,[20] поддерживая теорию о том, что роль фратаксина заключается в защите митохондрий от окислительного стресса и последующего повреждения клеток.
Фибробласты из мышиной модели фибробластов пациентов FRDA и FRDA показывают повышенные уровни ДНК двухниточные разрывы.[21] А система доставки гена лентивируса был использован для доставки гена фратаксина в модель мыши FRDA и клетки пациента-человека, и это привело к долгосрочному восстановлению экспрессии фратаксина. мРНК и белок фратаксин. Это восстановление экспрессии гена фратаксина сопровождалось значительным уменьшением количества двухцепочечных разрывов ДНК.[21] Нарушение фратаксина в клетках FRDA, по-видимому, вызывает снижение способности к восстановлению Повреждение ДНК и это может способствовать нейродегенерация.[21]
Взаимодействия
Было показано, что фратаксин биологически взаимодействовать с ферментом PMPCB.[22]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000165060 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000059363 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б Campuzano V, Montermini L, Moltò MD, Pianese L, Cossée M, Cavalcanti F, Monros E, Rodius F, Duclos F, Monticelli A, Zara F, Cañizares J, Koutnikova H, Bidichandani SI, Gellera C, Brice A, Trouillas P , Де Микеле Дж., Филла А., Де Фрутос Р., Палау Ф, Патель П. И., Ди Донато С., Мандель Дж. Л., Кокоцца С., Кениг М., Пандольфо М. (март 1996 г.). «Атаксия Фридрейха: аутосомно-рецессивное заболевание, вызванное интронной экспансией триплетных повторов GAA». Наука. 271 (5254): 1423–7. Bibcode:1996 Наука ... 271.1423C. Дои:10.1126 / science.271.5254.1423. PMID 8596916. S2CID 20303793.
- ^ Карвахал Дж. Дж., Пок М. А., дос Сантос М., Дудни К., Хиллерманн Р., Миноуг С., Уильямсон Р., Сюань Дж. Дж., Чемберлен С. (октябрь 1996 г.). «Ген атаксии Фридрейха кодирует новую фосфатидилинозитол-4-фосфат-5-киназу». Природа Генетика. 14 (2): 157–62. Дои:10.1038 / ng1096-157. PMID 8841185. S2CID 6324358.
- ^ а б Де-Паганон С., Шигета Р., Чи И. И., Ристоу М., Шоелсон С. Е. (октябрь 2000 г.). «Кристаллическая структура фратаксина человека». Журнал биологической химии. 275 (40): 30753–6. Дои:10.1074 / jbc.C000407200. PMID 10900192.
- ^ а б Стеммлер Т.Л., Lesuisse E, Pain, Dancis (август 2010 г.). "Фратаксин и кластерный биогенез митохондрий FeS". Журнал биологической химии. 285 (35): 26737–26743. Дои:10.1074 / jbc.R110.118679. ЧВК 2930671. PMID 20522547.
- ^ Adinolfi S, Iannuzzi C, Prischi F, Pastore C, Iametti S, Martin SR, Bonomi F, Pastore A (апрель 2009 г.). «Бактериальный фратаксин CyaY является привратником образования железо-серных кластеров, катализируемого IscS». Структурная и молекулярная биология природы. 16 (4): 390–6. Дои:10.1038 / nsmb.1579. PMID 19305405. S2CID 205522816.
- ^ Dürr A, Cossee M, Agid Y, Campuzano V, Mignard C, Penet C, Mandel JL, Brice A, Koenig M (октябрь 1996 г.). «Клинические и генетические аномалии у пациентов с атаксией Фридрейха». Медицинский журнал Новой Англии. 335 (16): 1169–75. Дои:10.1056 / NEJM199610173351601. PMID 8815938.
- ^ Кутникова Х., Кампузано В., Фори Ф., Долле П., Кацзалини О., Кениг М. (август 1997 г.). «Исследования гомологов человека, мышей и дрожжей указывают на митохондриальную функцию фратаксина». Природа Генетика. 16 (4): 345–51. Дои:10.1038 / ng0897-345. PMID 9241270. S2CID 5883249.
- ^ Ким Э., Напьерала М., Дент С.Ю. (октябрь 2011 г.). «Гиперэкспансия повторов GAA влияет на пост-инициацию этапов транскрипции FXN при атаксии Фридрейха». Исследования нуклеиновых кислот. 39 (19): 8366–77. Дои:10.1093 / nar / gkr542. ЧВК 3201871. PMID 21745819.
- ^ Pan X, Ding Y, Shi L (ноябрь 2009 г.). «Роли SbcCD и RNaseE в транскрипции повторов GAA x TTC в Escherichia coli». Ремонт ДНК. 8 (11): 1321–7. Дои:10.1016 / j.dnarep.2009.08.001. PMID 19733517.
- ^ Баралле М., Пастор Т., Буссани Э., Пагани Ф. (июль 2008 г.). «Влияние экспансий некодирующих повторов GAA при атаксии Фридрейха на процессинг пре-мРНК». Американский журнал генетики человека. 83 (1): 77–88. Дои:10.1016 / j.ajhg.2008.06.018. ЧВК 2443835. PMID 18597733.
- ^ "Entrez Gene: FXN frataxin".
- ^ Ли Л., Мацуи М., Кори Д.Р. (01.01.2016). «Активация экспрессии фратаксина с помощью повторяющихся нуклеиновых кислот». Nature Communications. 7: 10606. Bibcode:2016НатКо ... 710606L. Дои:10.1038 / ncomms10606. ЧВК 4742999. PMID 26842135.
- ^ а б Кларк Э., Джонсон Дж., Донг Ю.Н., Меркадо-Айон, Уоррен Н., Чжай М., Макмиллан Э., Саловин А., Линь Х., Линч Д.Р. (ноябрь 2018 г.). «Роль дефицита белка фратаксина и метаболической дисфункции в атаксии Фридрейха, аутосомно-рецессивном митохондриальном заболевании». Нейронная передача сигналов. 2 (4): NS20180060. Дои:10.1042 / NS20180060. ЧВК 7373238. PMID 32714592.
- ^ Cossée M, Puccio H, Gansmuller A, Koutnikova H, Dierich A, LeMeur M, Fischbeck K, Dollé P, Kœnig M (май 2000 г.). «Инактивация гена мышиной атаксии Фридрейха приводит к ранней эмбриональной летальности без накопления железа». Молекулярная генетика человека. 9 (8): 1219–1226. Дои:10.1093 / hmg / 9.8.1219. PMID 10767347. В архиве из оригинала 2 июня 2018 г.. Получено 5 апреля 2019.
- ^ а б Perdomini M, Hick A, Puccio H (17 июля 2013 г.). «Животные и клеточные модели атаксии Фридрейха». Журнал нейрохимии. 126: 65–79. Дои:10.1111 / jnc.12219. PMID 23859342. S2CID 1427817.
- ^ Рунко А.П., Грисволд А.Дж., Мин К.Т. (март 2008 г.). «Избыточная экспрессия фратаксина в митохондриях увеличивает устойчивость к окислительному стрессу и увеличивает продолжительность жизни у дрозофилы». Письма FEBS. 582 (5): 715–9. Дои:10.1016 / j.febslet.2008.01.046. PMID 18258192. S2CID 207603250.
- ^ а б c Хонсари Х., Шнайдер М., Аль-Махдави С., Кьянеа Ю.Г., Фемида М., Пэррис С., Пок М.А., Фемида М. (декабрь 2016 г.). «Доставка гена фратаксина, опосредованная лентивирусом, устраняет нестабильность генома у пациентов с атаксией Фридрейха и фибробластов на мышиной модели». Джин Тер. 23 (12): 846–856. Дои:10.1038 / gt.2016.61. ЧВК 5143368. PMID 27518705.
- ^ Кутникова Х, Кампузано В, Кениг М (сентябрь 1998 г.). «Созревание дикого типа и мутировавшего фратаксина с помощью митохондриальной процессинговой пептидазы». Молекулярная генетика человека. 7 (9): 1485–9. Дои:10.1093 / hmg / 7.9.1485. PMID 9700204.
дальнейшее чтение
- Thierbach R, Drewes G, Fusser M, Voigt A, Kuhlow D, Blume U, Schulz TJ, Reiche C, Glatt H, Epe B, Steinberg P, Ristow M (ноябрь 2010 г.). «Фратаксиновый белок атаксии Фридрейха модулирует эксцизионную репарацию оснований ДНК у прокариот и млекопитающих». Биохимический журнал. 432 (1): 165–72. Дои:10.1042 / BJ20101116. ЧВК 2976068. PMID 20819074.
- Montermini L, Rodius F, Pianese L, Moltò MD, Cossée M, Campuzano V, Cavalcanti F, Monticelli A, Palau F, Gyapay G (ноябрь 1995 г.). "Критическая область атаксии Фридрейха охватывает интервал 150 т.п.н. на хромосоме 9q13". Американский журнал генетики человека. 57 (5): 1061–7. ЧВК 1801369. PMID 7485155.
- Бидичандани С.И., Ашизава Т., Патель П.И. (май 1997 г.). «Атипичная атаксия Фридрейха, вызванная сложной гетерозиготностью новой миссенс-мутации и экспансии триплетных повторов GAA». Американский журнал генетики человека. 60 (5): 1251–6. ЧВК 1712428. PMID 9150176.
- Бэбкок М., де Сильва Д., Оукс Р., Дэвис-Каплан С., Джиралерспонг С., Монтермини Л., Пандольфо М., Каплан Дж. (Июнь 1997 г.). «Регулирование накопления митохондриального железа с помощью Yfh1p, предполагаемого гомолога фратаксина». Наука. 276 (5319): 1709–12. Дои:10.1126 / science.276.5319.1709. PMID 9180083.
- Кутникова Х., Кампузано В., Фори Ф., Долле П., Кацзалини О., Кениг М. (август 1997 г.). «Исследования гомологов человека, мышей и дрожжей указывают на митохондриальную функцию фратаксина». Природа Генетика. 16 (4): 345–51. Дои:10.1038 / ng0897-345. PMID 9241270. S2CID 5883249.
- Уилсон РБ, Roof DM (август 1997 г.). «Дыхательная недостаточность из-за потери митохондриальной ДНК в дрожжах, лишенных гомолога фратаксина». Природа Генетика. 16 (4): 352–7. Дои:10.1038 / ng0897-352. PMID 9241271. S2CID 22652291.
- Campuzano V, Montermini L, Lutz Y, Cova L, Hindelang C, Jiralerspong S, Trottier Y, Kish SJ, Faucheux B, Trouillas P, Authier FJ, Dürr A, Mandel JL, Vescovi A, Pandolfo M, Koenig M (октябрь 1997 г. ). «Фратаксин снижен у пациентов с атаксией Фридрейха и связан с митохондриальными мембранами». Молекулярная генетика человека. 6 (11): 1771–80. Дои:10.1093 / hmg / 6.11.1771. PMID 9302253.
- Рётиг А., де Лонле П., Кретьен Д., Фори Ф., Кениг М., Сиди Д., Мюнхен А., Растин П. (октябрь 1997 г.). «Аконитаза и дефицит митохондриального белка железа-серы при атаксии Фридрейха». Природа Генетика. 17 (2): 215–7. Дои:10.1038 / ng1097-215. PMID 9326946. S2CID 23151137.
- Джиралерспонг С., Лю Ю., Монтермини Л., Стифани С., Пандольфо М. (1997). «Фратаксин демонстрирует регулируемую тканеспецифичную экспрессию в эмбрионе мыши». Нейробиология болезней. 4 (2): 103–13. Дои:10.1006 / nbdi.1997.0139. PMID 9331900. S2CID 6520439.
- Кутникова Х, Кампузано В, Кениг М (сентябрь 1998 г.). «Созревание дикого типа и мутированного фратаксина с помощью митохондриальной процессинговой пептидазы». Молекулярная генетика человека. 7 (9): 1485–9. Дои:10.1093 / hmg / 7.9.1485. PMID 9700204.
- Zühlke C, Laccone F, Cossée M, Kohlschütter A, Koenig M, Schwinger E (июль 1998 г.). «Мутация стартового кодона в гене FRDA1: анализ сцепления трех родословных с трансверсией ATG в ATT указывает на уникального общего предка». Генетика человека. 103 (1): 102–5. Дои:10.1007 / s004390050791. PMID 9737785. S2CID 26999143.
- Бартоло С., Менделл-младший, Приор Т.В. (октябрь 1998 г.). «Идентификация миссенс-мутации у пациента с атаксией Фридрейха: значение для диагностики и исследований носителей». Американский журнал медицинской генетики. 79 (5): 396–9. Дои:10.1002 / (SICI) 1096-8628 (19981012) 79: 5 <396 :: AID-AJMG13> 3.0.CO; 2-M. PMID 9779809.
- Cossée M, Dürr A, Schmitt M, Dahl N, Trouillas P, Allinson P, Kostrzewa M, Nivelon-Chevallier A, Gustavson KH, Kohlschütter A, Müller U, Mandel JL, Brice A, Koenig M, Cavalcanti F, Tammaro A, Де Микеле Дж., Филла А., Кокоцца С., Лабуда М., Монтермини Л., Пуарье Дж., Пандольфо М. (февраль 1999 г.). «Атаксия Фридрейха: точечные мутации и клинические проявления сложных гетерозигот». Анналы неврологии. 45 (2): 200–6. Дои:10.1002 / 1531-8249 (199902) 45: 2 <200 :: AID-ANA10> 3.0.CO; 2-U. PMID 9989622.
- Коппола Дж., Де Микеле Дж., Кавальканти Ф, Пианез Л, Перретти А, Санторо Л, Вита Дж., Тоскано А, Амбони М, Гримальди Дж., Сальваторе Е, Карузо Дж., Филла А (май 1999 г.). «Почему у некоторых пациентов с атаксией Фридрейха сохраняются сухожильные рефлексы? Клиническое, нейрофизиологическое и молекулярное исследование». Журнал неврологии. 246 (5): 353–7. Дои:10.1007 / s004150050362. PMID 10399865. S2CID 7367457.
- Бранда С.С., Кавадини П., Адамек Дж., Калоусек Ф., Тарони Ф., Исая Дж. (Август 1999 г.). «Дрожжи и человеческий фратаксин перерабатываются в зрелую форму в два последовательных этапа митохондриальной процессинговой пептидазой». Журнал биологической химии. 274 (32): 22763–9. Дои:10.1074 / jbc.274.32.22763. PMID 10428860.
- Гордон Д.М., Ши К., Дансис А., Пейн Д. (ноябрь 1999 г.). «Созревание фратаксина в митохондриях млекопитающих и дрожжей: одностадийная обработка пептидазой матричной обработки». Молекулярная генетика человека. 8 (12): 2255–62. Дои:10.1093 / hmg / 8.12.2255. PMID 10545606.
- Форрест С.М., Найт М., Делатицки М.Б., Пэрис Д., Уильямсон Р., Кинг Дж., Йунг Л., Нассиф Н., Николсон Г.А. (август 1998 г.). «Корреляция клинического фенотипа при атаксии Фридрейха с местом точечной мутации в гене FRDA». Нейрогенетика. 1 (4): 253–7. Дои:10.1007 / с100480050037. PMID 10732799. S2CID 7463903.
- Аль-Махдави С., Пок М., Чемберлен С. (июль 2000 г.). «Новая миссенс-мутация (L198R) в гене атаксии Фридрейха». Человеческая мутация. 16 (1): 95. Дои:10.1002 / 1098-1004 (200007) 16: 1 <95 :: AID-HUMU29> 3.0.CO; 2-E. PMID 10874325.
внешняя ссылка
- GeneReviews / NCBI / NIH / UW запись об атаксии Фридрейха
- фратаксин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: Q16595 (Фратаксин, митохондриальный) на PDBe-KB.