Аминотрансфераза аминокислот с разветвленной цепью - Branched-chain amino acid aminotransferase
| Аминотрансфераза аминокислот с разветвленной цепью | |||||||
|---|---|---|---|---|---|---|---|
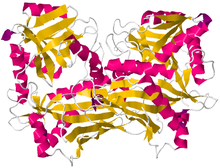 Кристаллографическая структура аминотрансферазы с разветвленной цепью из Микобактерии смегматис[1] | |||||||
| Идентификаторы | |||||||
| Символ | BCAT | ||||||
| Альт. символы | BCT | ||||||
| Ген NCBI | 587 | ||||||
| HGNC | 977 | ||||||
| OMIM | 113530 | ||||||
| RefSeq | NM_001190 | ||||||
| UniProt | O15382 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 2.6.1.42 | ||||||
| Locus | Chr. 19 q13 | ||||||
| |||||||
Аминотрансфераза аминокислот с разветвленной цепью (BCAT), также известный как трансаминаза аминокислот с разветвленной цепью, является аминотрансфераза фермент (EC 2.6.1.42 ) который действует на аминокислоты с разветвленной цепью (BCAA). Он закодирован BCAT2 ген в людях. Фермент BCAT катализирует превращение BCAA и α-кетоглутарат в разветвленную цепь α-кетокислоты и глутамат.
Структура справа аминотрансферазы аминокислот с разветвленной цепью была найдена с использованием дифракция рентгеновских лучей с разрешением 2,20 Å. Аминотрансфераза с разветвленной цепью, обнаруженная на этом изображении, была выделена из микобактерии. Этот белок состоит из двух одинаковых полипептидные цепи, всего 372 остатка.[2]
Биологическая функция аминотрансфераз аминокислот с разветвленной цепью состоит в том, чтобы катализировать синтез или разложение аминокислоты с разветвленной цепью лейцин, изолейцин, и валин.[3] У человека аминокислоты с разветвленной цепью существенный и ухудшаются из-за BCAT.
Структура и функции
У людей BCAT гомодимеры состоит из двух доменов, небольшой субъединицы (остатки 1–170) и большой субъединицы (остатки 182–365). Эти субъединицы соединены короткой петлевой соединительной областью (остатки 171–181).[4] Оба подразделения состоят из четырех альфа-спирали и бета-гофрированный лист.[5] Структурные исследования аминотрансфераз аминокислот с разветвленной цепью человека (hBCAT) показали, что все пептидные связи в обеих изоформах транс за исключением связи между остатками Gly338-Pro339.[5] В активный сайт фермента находится на границе раздела между двумя доменами.[5] Как и другие ферменты трансаминаз (а также многие ферменты других классов), BCAT требует кофактора. пиридоксаль-5'-фосфат (PLP) за активность. Было обнаружено, что PLP изменяет конформацию ферментов аминотрансфераз, блокируя конформацию фермента через База Шиффа (иминная) связь в реакции между остатком лизина фермента и карбонильной группой кофактора.[6] Это конформационное изменение позволяет субстратам связываться с карманом активного сайта ферментов.
Активный сайт
В дополнение к связи основания Шиффа, PLP прикрепляется к активному сайту фермента посредством водородной связи на остатках Tyr 207 и Glu237. Кроме того, атомы кислорода фосфата на молекуле PLP взаимодействуют с остатками Arg99, Val269, Val270 и Thr310.[5] BCAT млекопитающих демонстрируют уникальный структурный мотив CXXC (Cys315 и Cys318), чувствительный к окислителям.[7] и модулируется S-нитрозированием,[8] посттрансляционная модификация, регулирующая передачу сигналов клетки.[9] Было обнаружено, что модификация этих двух остатков цистеина путем окисления (in vivo / vitro) или титрования (in vitro) ингибирует активность фермента,[4] это указывает на то, что мотив CXXC имеет решающее значение для оптимального фолдинга и функции белка.[10] Чувствительность обоих изоферментов к окисление сделать их потенциальными биомаркерами для редокс среда внутри клетки.[11] Хотя мотив CXXC присутствует только в BCAT млекопитающих, было обнаружено, что окружающие аминокислотные остатки являются высококонсервативными как в прокариотических, так и в эукариотических клетках.[12] Конвей, Йенавар и др. обнаружили, что активный центр млекопитающих содержит три поверхности: поверхность A (Phe75, Tyr207 и Thr240), поверхность B (Phe30, Tyr141 и Ala314) и поверхность C (Tyr70, Leu153 и Val155, расположенные в противоположном домене), которые связываются с субстрат во взаимодействии типа Ван-дер-Ваальса с разветвленными боковыми цепями аминокислотных субстратов.[12]
Изоформы
Млекопитающее
BCAT у млекопитающих катализируют первую стадию метаболизма аминокислот с разветвленной цепью, обратимое трансаминирование с последующим окислительным декарбоксилированием продуктов трансаминирования α-кетоизокапроата, α-кето-β-метилвалерата и α-кетоизовалерата до изовалерил-КоА, 3- метилбутирил-КоА и изобутирил-КоА соответственно.[13] Эта реакция регулирует метаболизм аминокислот и является решающим шагом в транспортировке азота по всему телу.[14] Аминокислоты с разветвленной цепью (BCAA) повсеместно встречаются во многих организмах, составляя 35% всех белков и 40% аминокислот, необходимых для всех млекопитающих.[13] BCAT млекопитающих бывают двух изоформ: цитозольной (BCATc) и митохондриальной (BCATm). Изоформы имеют 58% гомологии,[15] но различаются по расположению и каталитической эффективности.
BCATc
Цитозольные аминокислотные аминотрансферазы с разветвленной цепью являются менее распространенными из двух изоформ, обнаруживаемых в цитоплазме клеток млекопитающих почти исключительно во всей нервной системе.[15] Несмотря на то что BCATc экспрессируются только в нескольких взрослых тканях, они экспрессируются на высоком уровне во время эмбриогенеза.[16] Цитозольная изоформа имеет более высокую скорость обновления, примерно в 2-5 раз быстрее, чем митохондриальная изоформа.[17] Было обнаружено, что BCATc более стабилен, чем BCATm, и имеются данные, свидетельствующие о наличии 2 сульфидных связей. Цитозольный изофермент не демонстрирует потери активности при титровании одной тиоловой группы.[17] hBCATc демонстрирует более низкий окислительно-восстановительный потенциал (примерно 30 мВ), чем hBCATm.[11]
BCATm
Митохондриальные аминокислотные аминотрансферазы с разветвленной цепью являются наиболее распространенными из двух изоформ, присутствующих во всех тканях митохондрий клетки.[8] Было обнаружено, что ацинарная ткань поджелудочной железы несет самый высокий уровень BCATm в организме.[18] Кроме того, были обнаружены два гомолога нормальному BCATm. Один гомолог обнаружен в ткани плаценты, а другой ко-репрессирует ядерные рецепторы тироидных гормонов.[16][19] BCATm более чувствителен к окислительно-восстановительной среде клетки и может подавляться ионами никеля, даже если среда восстанавливается. Было обнаружено, что BCATm не образует дисульфидных связей, а титрование двух групп -SH 5,5'-дитиобис (2-нитробензойной кислотой) полностью устраняет активность фермента в случае изофермента BCATm.[17]
Изоформы растений
BCAT растений также были идентифицированы, но они различаются между видами с точки зрения количества и последовательности. В исследованияхArabidopsis thaliana (кресс-салат), было идентифицировано шесть изоформ BCAT, которые имеют 47,5-84,1% гомологии друг с другом. Эти изоформы также имеют примерно 30% гомологию последовательностей с человеческой и дрожжевой (Saccharomyces cerevisiae) изоформы.[20] BCAT1 находится в митохондриях, BCAT2, 3 и 5 - в хлоропластах, а BCAT4 и 6 - в цитоплазме A. thaliana.[21] Однако исследования BCAT в Solanum tuberosum (картофель) выявили две изоформы длиной 683 (BCAT1) и 746 (BCAT2) п.н., локализованные преимущественно в хлоропластах.[22]
Бактериальные изоформы
У бактерий есть только одна изоформа фермента BCAT. Однако структура фермента у разных организмов разная. В кишечная палочка, фермент представляет собой гексамер, содержащий шесть идентичных субъединиц. Каждая субъединица имеет молекулярную массу 34 кДа и состоит из 308 аминокислот.[23] В отличие, Lactococcus lactis BCAT представляет собой гомодимер, подобный изоформам млекопитающих. Каждое подразделение L. lactis BCAT состоит из 340 аминокислот с молекулярной массой 38 кДа.[24]
Физиологические роли
Люди
Поскольку аминокислоты с разветвленной цепью имеют решающее значение в образовании и функционировании многих белков, BCAT несут множество функций в физиологии млекопитающих. Было обнаружено, что BCAT взаимодействуют с протеин-дисульфидными изомеразами, классом ферментов, регулирующих восстановление клеток и правильную укладку белков.[10] Второй этап метаболизма аминокислот с разветвленной цепью (окислительное карбоксилирование с помощью дегидрогеназы кетокислоты с разветвленной цепью) стимулирует секрецию инсулина. Потеря BCATm коррелирует с потерей стимулированной BCKD секреции инсулина, но не связана с потерей секреции инсулина другими метаболическими путями.[18] BCATc регулирует пути передачи сигналов mTORC1 и TCR-индуцированного гликолитического метаболизма во время CD4.+ Активация Т-клеток.[25] В головном мозге BCATc регулирует количество продукции глутамата для использования в качестве нейромедиатора или для будущего синтеза γ-аминомасляной кислоты (ГАМК).[26]
Растения
BCAT также играют роль в физиологии видов растений, но они не были изучены так широко, как BCAT млекопитающих. В Cucumis melo (дыня), было обнаружено, что BCAT играют роль в создании летучих ароматических соединений, которые придают дыням их особый запах и вкус.[27] В Solanum lycopersicum (помидоры), BCAT играют роль в синтезе аминокислот с разветвленной цепью, которые действуют как доноры электронов в цепи переноса электронов. В целом, растительные ВСАТ выполняют катаболические и анаболические регуляторные функции.[28]
Бактерии
В бактериальной физиологии BCAT выполняют обе реакции, образуя как α-кетокислоты, так и аминокислоты с разветвленной цепью. Бактерии, растущие на среде с недостаточным для роста соотношением аминокислот, должны быть способны синтезировать аминокислоты с разветвленной цепью, чтобы размножаться.[29] В Streptococcus mutans, грамположительные бактерии, которые живут в полости рта человека и отвечают за разрушение зубов, было обнаружено, что биосинтез / разложение аминокислот регулирует гликолиз и поддерживает внутренний pH клетки. Это позволяет бактериям выживать в кислых условиях ротовой полости человека за счет расщепления углеводов.[30]
Использует
Синтетическая органическая химия
ВСАТ используются в синтезе некоторых фармацевтических препаратов в качестве альтернативы катализаторам на основе тяжелых металлов, которые могут быть дорогими / экологически вредными. Аминотрансферазы (трансаминазы) в целом использовались для создания неприродных аминокислот, важных строительных блоков для пептидомиметических препаратов и сельскохозяйственных продуктов. BCAT из Кишечная палочка обычно разрабатывается для сверхэкспрессии и извлечения из целых клеток для использования в химическом синтезе.[31] Аминотрансферазы используются, потому что они могут выполнять типичную многостадийную реакцию за одну стадию, могут проводить реакции на широком диапазоне субстратов и обладают высокой региоселективностью и энантиоселективностью.[32] В синтетической органической химии BCAT обычно используются для превращения L-лейцина в 2-кетоглутарат.
Цель лекарства
Противосудорожное средство габапентин [Нейронтин; 1- (аминометил) циклогексануксусная кислота] - препарат, часто используемый для лечения пациентов с невропатической болью.[33][34][35] Эта невропатическая боль может быть вызвана множеством причин, включая диабетическую невропатию и постгерпетическую невралгию.[36] Габапентин представляет собой аминокислотный препарат, структурно подобный двум нейротрансмиттерам - глутамату (синтезированному BCAT) и ГАМК. Препарат конкурентно ингибирует обе изоформы BCAT в головном мозге, замедляя выработку глутамата.[37] Габапентин также ингибирует ГАМК-аминотрансферазу (ГАМК-Т) и глутаматдегидрогеназу (ГДГ), два других фермента метаболического пути глутамата и ГАМК.
Производство вяленого мяса и сыра
Бактерии L. lactis является основными бактериями, ответственными за созревание сыров, а ферменты, входящие в состав бактерий, играют ключевую роль в формировании вкуса, текстуры и аромата.[38] Аминотрансферазы аминокислот с разветвленной цепью помогают производить такие соединения, как изовалериановая кислота, изомасляная кислота, 2- и 3-метилбутан (ал) (ол) и 2-метилпропан (ал) (ол), которые придают фруктовый или солодовый аромат в зависимости от количества. присутствующего соединения.[39] Наряду с ароматическими аминотрансферазами (AraT), BCAT в L. lactis помогают развить аромат / вкус, обусловленный летучими соединениями серы, образующимися во время ферментации.
Бактерии Стафилококк карнозный и Enterococcus faecalis являются часто используется в тандеме с другими молочнокислыми бактериями, чтобы начать процесс ферментации мяса. BCAT в этих двух бактериях осуществляют трансаминирование во время ферментации мяса, производя соответствующие α-кетокислоты из аминокислот. По мере ферментации эти α-кетокислоты распадаются на класс соединений, известных как летучие соединения с метильными разветвлениями, которые включают альдегиды, спирты и карбоновые кислоты, все из которых вносят свой вклад в отчетливые ароматы и вкус вяленого мяса.[40]
Идеальные условия
Исследование BCAT от Lactococcus lactis Ивон, Шамбеллон и др. нашли следующие идеальные условия для бактериального изофермента:
- pH: ~ 7,5
- Температура: ~ 35-40 ° C (хранение при 6 ° C сохраняет стабильность фермента в течение ~ 1 недели)
- Отсутствие карбонила, сульфгидрила или Cu2+ или Co2+ реагенты / соединения
- Фермент лучше всего катализирует реакцию с аминокислотами с разветвленной цепью (в порядке от наибольшей активности к наименьшей: изолейцин, лейцин, валин)
- Фермент также проявляет минимальную активность с метионином, цистеином и аланином.[24]
Рекомендации
- ^ «Резюме структуры для 3DTF - Структурный анализ микобактериальной аминотрансферазы с разветвленной цепью - значение для разработки ингибитора». Банк данных белков RCSB.
- ^ «Банк данных белка RCSB - Резюме структуры для 3DTF - Структурный анализ микобактериальной аминотрансферазы с разветвленной цепью - значение для разработки ингибитора».
- ^ Хатсон С (2001). «Структура и функции аминотрансфераз с разветвленной цепью». Прогресс в исследованиях нуклеиновых кислот и молекулярной биологии. 70: 175–206. Дои:10.1016 / s0079-6603 (01) 70017-7. ISBN 9780125400701. PMID 11642362.
- ^ а б Конвей М.Э., Йеннавар Н., Валлин Р., Пул Л. Б., Хатсон С. М. (июль 2002 г.). «Идентификация пероксид-чувствительного редокс-переключателя в мотиве CXXC в митохондриальной аминотрансферазе с разветвленной цепью». Биохимия. 41 (29): 9070–8. Дои:10.1021 / bi020200i. PMID 12119021.
- ^ а б c d Йеннавар Н., Данбар Дж., Конвей М., Хатсон С., Фарбер Г. (апрель 2001 г.). «Структура митохондриальной аминотрансферазы с разветвленной цепью человека». Acta Crystallographica Раздел D. 57 (Pt 4): 506–15. Дои:10.1107 / s0907444901001925. PMID 11264579.
- ^ Тони MD (ноябрь 2011 г.). «Энзимология пиридоксальфосфатов». Biochimica et Biophysica Acta (BBA) - Белки и протеомика. Энзимология пиридоксальфосфата. 1814 (11): 1405–6. Дои:10.1016 / j.bbapap.2011.08.007. PMID 21871586.
- ^ Йеннавар Н.Х., Ислам М.М., Конвей М., Валлин Р., Хатсон С.М. (декабрь 2006 г.). «Изофермент митохондриальной аминотрансферазы с разветвленной цепью человека: структурная роль центра CXXC в катализе». Журнал биологической химии. 281 (51): 39660–71. Дои:10.1074 / jbc.M607552200. PMID 17050531.
- ^ а б Халл Дж., Хинди М.Э., Кехо П.Г., Чалмерс К., Лав С., Конвей М.Э. (декабрь 2012 г.). «Распределение белков аминотрансфераз с разветвленной цепью в мозге человека и их роль в регуляции глутамата». Журнал нейрохимии. 123 (6): 997–1009. Дои:10.1111 / jnc.12044. PMID 23043456. S2CID 206088992.
- ^ Thomas DD, Jourd'heuil D (октябрь 2012 г.). «S-нитрозирование: современные концепции и новые разработки». Антиоксиданты и редокс-сигналы. 17 (7): 934–6. Дои:10.1089 / ars.2012.4669. ЧВК 3411337. PMID 22530975.
- ^ а б Эль Хинди М., Хезвани М., Корри Д., Халл Дж., Эль Амрауи Ф., Харрис М., Ли С., Форшоу Т., Уилсон А., Мэнсбридж А., Хасслер М., Патель В. Б., Кехо П. Г., Лав С., Конвей М. Э. (июнь 2014 г.) . «Белки аминотрансферазы с разветвленной цепью: новые окислительно-восстановительные шапероны для протеин-дисульфид-изомеразы - значение при болезни Альцгеймера». Антиоксиданты и редокс-сигналы. 20 (16): 2497–513. Дои:10.1089 / ars.2012.4869. ЧВК 4026213. PMID 24094038.
- ^ а б Коулз SJ, Хэнкок JT, Конвей ME (февраль 2012 г.). «Дифференциальный окислительно-восстановительный потенциал между цитозольной и митохондриальной аминотрансферазой с разветвленной цепью». Acta Biochimica et Biophysica Sinica. 44 (2): 172–6. Дои:10.1093 / abbs / gmr103. PMID 22107788.
- ^ а б Конвей М.Э., Йеннавар Н., Валлин Р., Пул Л. Б., Хатсон С. М. (апрель 2003 г.). «Человеческая митохондриальная аминотрансфераза с разветвленной цепью: структурная основа для субстратной специфичности и роли окислительно-восстановительных активных цистеинов». Biochimica et Biophysica Acta (BBA) - Белки и протеомика. 3-й Международный симпозиум по витамину B6, PQQ, карбонильному катализу и хинопротеинам. 1647 (1–2): 61–5. Дои:10.1016 / S1570-9639 (03) 00051-7. PMID 12686109.
- ^ а б Харпер А.Е., Миллер Р.Х., Блок КП (1984-01-01). «Обмен аминокислот с разветвленной цепью». Ежегодный обзор питания. 4 (1): 409–54. Дои:10.1146 / annurev.nu.04.070184.002205. PMID 6380539.
- ^ Биксель М., Шимомура Ю., Хатсон С., Хампрехт Б. (март 2001 г.). «Распределение ключевых ферментов метаболизма аминокислот с разветвленной цепью в глиальных и нейрональных клетках в культуре». Журнал гистохимии и цитохимии. 49 (3): 407–18. Дои:10.1177/002215540104900314. PMID 11181743.
- ^ а б Д'Мелло JP (2012). Аминокислоты в питании и здоровье человека. КАБИ. ISBN 978-1-84593-901-4.
- ^ а б Линь Х.М., Канешиге М., Чжао Л., Чжан Х, Ганновер Д.А., Ченг С.Ю. (декабрь 2001 г.). «Изоформа аминотрансферазы с разветвленной цепью - новый корепрессор ядерных рецепторов тироидных гормонов». Журнал биологической химии. 276 (51): 48196–205. Дои:10.1074 / jbc.M104320200. PMID 11574535.
- ^ а б c Давуди Дж., Утопление П.М., Бледсо Р.К., Валлин Р., Рейнхарт Г.Д., Хатсон С.М. (февраль 1998 г.). «Сверхэкспрессия и характеристика митохондриальных и цитозольных аминотрансфераз с разветвленной цепью человека». Журнал биологической химии. 273 (9): 4982–9. Дои:10.1074 / jbc.273.9.4982. PMID 9478945.
- ^ а б Чжоу Ю., Джеттон Т.Л., Гошорн С., Линч С.Дж., Ши П. (октябрь 2010 г.). «Для стимуляции секреции инсулина требуется трансаминирование альфа-кетоизокапроата, но не лейцина». Журнал биологической химии. 285 (44): 33718–26. Дои:10.1074 / jbc.M110.136846. ЧВК 2962470. PMID 20736162.
- ^ Than NG, Sümegi B, Than GN, Bellyei S, Bohn H (2001). «Молекулярное клонирование и характеристика белка 18 плацентарной ткани (PP18a) / митохондриальной аминотрансферазы с разветвленной цепью (BCATm) и его нового альтернативно сплайсированного варианта PP18b». Плацента. 22 (2–3): 235–43. Дои:10.1053 / plac.2000.0603. PMID 11170829.
- ^ Diebold R, Schuster J, Däschner K, Binder S (июнь 2002 г.). «Семейство генов трансаминаз аминокислот с разветвленной цепью у Arabidopsis кодирует пластидные и митохондриальные белки». Физиология растений. 129 (2): 540–50. Дои:10.1104 / стр.001602. ЧВК 161671. PMID 12068099.
- ^ Биндер С., Книл Т., Шустер Дж. (Ноябрь 2006 г.). «Метаболизм аминокислот с разветвленной цепью у высших растений». Physiologia Plantarum. 129 (1): 68–78. Дои:10.1111 / j.1399-3054.2006.00800.x.
- ^ Кэмпбелл М.А., Патель Дж. К., Мейерс Дж. Л., Майрик Л. К., Гастин Дж. Л. (октябрь 2001 г.). «Гены, кодирующие аминотрансферазу с разветвленной цепью, по-разному экспрессируются в растениях». Физиология и биохимия растений. 39 (10): 855–860. Дои:10.1016 / S0981-9428 (01) 01306-7.
- ^ Окада К., Хироцу К., Сато М., Хаяси Х., Кагамияма Х. (апрель 1997 г.). «Трехмерная структура аминотрансферазы аминокислот с разветвленной цепью Escherichia coli при разрешении 2,5 A». Журнал биохимии. 121 (4): 637–41. Дои:10.1093 / oxfordjournals.jbchem.a021633. PMID 9163511.
- ^ а б Ивон М., Шамбеллон Э, Болотин А., Рудо-Альгарон Ф (февраль 2000 г.). «Характеристика и роль аминотрансферазы с разветвленной цепью (BcaT), выделенной из Lactococcus lactis subsp. Cremoris NCDO 763». Прикладная и экологическая микробиология. 66 (2): 571–7. Дои:10.1128 / AEM.66.2.571-577.2000. ЧВК 91865. PMID 10653720.
- ^ Ананьева Э.А., Патель Ч., Дрейк Ч., Пауэлл Дж. Д., Хатсон С. М. (июль 2014 г.). «Цитозольная аминотрансфераза с разветвленной цепью (BCATc) регулирует передачу сигналов mTORC1 и гликолитический метаболизм в CD4 + Т-клетках». Журнал биологической химии. 289 (27): 18793–804. Дои:10.1074 / jbc.M114.554113. ЧВК 4081922. PMID 24847056.
- ^ Свитт А.Дж., Гарсия-Эспиноса М.А., Валлин Р., Хатсон С.М. (сентябрь 2004 г.). «Аминокислоты с разветвленной цепью и метаболизм нейротрансмиттеров: экспрессия цитозольной аминотрансферазы с разветвленной цепью (BCATc) в мозжечке и гиппокампе». Журнал сравнительной неврологии. 477 (4): 360–70. Дои:10.1002 / cne.20200. PMID 15329886. S2CID 18780804.
- ^ Гонда I, Бар E, Портной В., Лев С., Бургер Дж., Шаффер А.А., Тадмор Ю., Гепштейн С., Джованнони Дж. Дж., Кацир Н., Левинсон Э. (февраль 2010 г.). «Катаболизм ароматических аминокислот с разветвленной цепью в летучие ароматические вещества в плодах Cucumis melo L.». Журнал экспериментальной ботаники. 61 (4): 1111–23. Дои:10.1093 / jxb / erp390. ЧВК 2826658. PMID 20065117.
- ^ Мэлони Г.С., Кочевенко А., Тиман Д.М., Тогге Т., Кригер Ю., Замир Д., Тейлор М.Г., Ферни А.Р., Клее Х.Д. (июль 2010 г.). «Характеристика семейства ферментов аминотрансфераз с разветвленной цепью в томатах». Физиология растений. 153 (3): 925–36. Дои:10.1104 / стр.110.154922. ЧВК 2899903. PMID 20435740.
- ^ Энгельс В.Дж., Альтинг А.С., Арнц М.М., Gruppen H, Voragen AG, Смит Г., Виссер С. (август 2000 г.). «Частичная очистка и характеристика двух аминотрансфераз из Lactococcus lactis subsp. Cremoris B78, участвующих в катаболизме метионина и аминокислот с разветвленной цепью». Международный молочный журнал. 10 (7): 443–452. Дои:10.1016 / S0958-6946 (00) 00068-6.
- ^ Сантьяго Б., МакГилврей М., Фаустоферри Р.С., Куиви Р.Г. (апрель 2012 г.). «Аминотрансфераза аминокислот с разветвленной цепью, кодируемая ilvE, участвует в устойчивости к кислоте у Streptococcus mutans». Журнал бактериологии. 194 (8): 2010–9. Дои:10.1128 / JB.06737-11. ЧВК 3318461. PMID 22328677.
- ^ Тейлор П.П., Панталеоне Д.П., Сенкпейл РФ, Фотерингем И.Г. (октябрь 1998 г.). «Новые биосинтетические подходы к производству неприродных аминокислот с использованием трансаминаз». Тенденции в биотехнологии. 16 (10): 412–8. Дои:10.1016 / S0167-7799 (98) 01240-2. PMID 9807838.
- ^ Хван Би, Чо Би, Юн Х, Котешвар К., Ким Би (декабрь 2005 г.). «Пересмотр аминотрансферазы в эпоху генома и ее применение в биокатализе». Журнал молекулярного катализа B: Ферментативный. 37 (1–6): 47–55. Дои:10.1016 / j.molcatb.2005.09.004.
- ^ Виффен, Филип Дж .; Дерри, Шина; Белл, Рэй Ф .; Райс, Эндрю С. С.; Тёлле, Томас Рудольф; Филлипс, Тюдор; Мур, Р. Эндрю (2017-06-09). «Габапентин от хронической невропатической боли у взрослых». Кокрановская база данных систематических обзоров. 6: CD007938. Дои:10.1002 / 14651858.CD007938.pub4. ISSN 1469-493X. ЧВК 6452908. PMID 28597471.
- ^ Габапентин для взрослых с невропатической болью: обзор клинических данных и рекомендаций [Интернет]. Оттава: Канадское агентство по лекарствам и технологиям в области здравоохранения. 26 сентября 2014 г. PMID 25411680.
- ^ Габапентин для взрослых с невропатической болью: обзор клинической эффективности и безопасности [Интернет]. Оттава: Канадское агентство по лекарствам и технологиям в области здравоохранения. 14 апреля 2015 г. PMID 26180879.
- ^ Баконья М., Гланцман Р.Л. (январь 2003 г.). «Дозирование габапентина при невропатической боли: данные рандомизированных плацебо-контролируемых клинических испытаний». Клиническая терапия. 25 (1): 81–104. Дои:10.1016 / s0149-2918 (03) 90011-7. PMID 12637113.
- ^ Goldlust A, Su TZ, Welty DF, Taylor CP, Oxender DL (сентябрь 1995 г.). «Влияние противосудорожного препарата габапентин на ферменты метаболических путей глутамата и ГАМК». Исследования эпилепсии. 22 (1): 1–11. Дои:10.1016/0920-1211(95)00028-9. PMID 8565962. S2CID 22622907.
- ^ Гарсия-Каюэла Т., Гомес де Кадиньянос Л.П., Пелаес С., Рекена Т. (октябрь 2012 г.). «Экспрессия в Lactococcus lactis функциональных генов, связанных с катаболизмом аминокислот и образованием сырного аромата, находится под влиянием аминокислот с разветвленной цепью». Международный журнал пищевой микробиологии. 159 (3): 207–13. Дои:10.1016 / j.ijfoodmicro.2012.09.002. PMID 23107499.
- ^ Райнен Л., Ивон М., ван Краненбург Р., Куртин П., Верхойл А., Шамбеллон Е., Смит Г. (01.01.2003). «Лактококковые аминотрансферазы AraT и BcaT являются ключевыми ферментами для образования ароматических соединений из аминокислот в сыре». Международный молочный журнал. 13 (10): 805–812. Дои:10.1016 / S0958-6946 (03) 00102-X.
- ^ Фрайдинг С., Эрманн М.А., Фогель РФ (апрель 2012 г.). «Сравнение различных аминотрансфераз IlvE в Lactobacillus sakei и исследование их вклада в формирование аромата из аминокислот с разветвленной цепью». Пищевая микробиология. Ферментированное мясо 29 (2): 205–14. Дои:10.1016 / j.fm.2011.07.008. PMID 22202874.
