Щавелевоуксусная кислота - Oxaloacetic acid
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC 2-оксобутандиовая кислота | |
| Другие имена Щавелевоуксусная кислота Щавелевоуксусная кислота 2-оксоянтарная кислота Кетоянтарная кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.005.755 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C4ЧАС4О5 | |
| Молярная масса | 132,07 г / моль |
| Плотность | 0,18 г / см3 |
| Температура плавления | 161 ° С (322 ° F, 434 К) |
| Термохимия | |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -943,21 кДж / моль |
Станд. Энтальпия горение (ΔcЧАС⦵298) | -1205,58 кДж / моль |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Щавелевоуксусная кислота (также известен как щавелевоуксусная кислота или же OAA) является кристаллическим органическое соединение с химическая формула HO2CC (O) CH2CO2H. Щавелевоуксусная кислота в форме ее сопряженное основание оксалоацетат, является промежуточным звеном метаболизма во многих процессах, происходящих у животных. Принимает участие в глюконеогенез, то цикл мочевины, то глиоксилатный цикл, синтез аминокислот, синтез жирных кислот и цикл лимонной кислоты.[1]
Характеристики
Щавелевоуксусная кислота подвергается последовательному депротонированию с образованием дианиона:
- HO2CC (O) CH2CO2H ⇌ −О2CC (O) CH2CO2H + H+ pKа = 2.22
- −О2CC (O) CH2CO2H ⇌ −О2CC (O) CH2CO2− + H+, pKа = 3.89
При высоком pH енолизируемый протон ионизируется:
- −О2CC (O) CH2CO2− ⇌ −О2CC (O−) CHCO2− + H+, pKа = 13.03
В энол формы щавелевоуксусной кислоты особенно стабильны, так что две таутомеры имеют разную температуру плавления (152 ° C для СНГ изоформы и 184 ° C для транс изоформа).
Биосинтез
Оксалоацетат образуется в природе несколькими способами. Главный маршрут находится на окисление из L-малат, катализируемый малатдегидрогеназа, в цикле лимонной кислоты. Малат также окисляется сукцинатдегидрогеназа в медленной реакции с исходным продуктом енолоксалоацетат.[2]
Это также возникает из-за конденсации пируват с угольной кислотой, за счет гидролиза АТФ:
- CH3C (O) CO2− + HCO3− + АТФ → −О2CCH2C (O) CO2− + ADP + Pi
Происходит в мезофилл растений этот процесс протекает через фосфоенолпируват, катализируемый фосфоенолпируваткарбоксилаза.
Оксалоацетат также может образовываться из транс- или разоблачение аспарагиновая кислота.
Биохимические функции
Оксалоацетат является промежуточным продуктом цикл лимонной кислоты, где он реагирует с ацетил-КоА формировать цитрат, катализируемый цитрат-синтаза. Он также участвует в глюконеогенез, то цикл мочевины, то глиоксилатный цикл, синтез аминокислот, и синтез жирных кислот. Оксалоацетат также является мощным ингибитором комплекс II.
Глюконеогенез
Глюконеогенез[1] представляет собой метаболический путь, состоящий из серии из одиннадцати катализируемых ферментами реакций, приводящих к образованию глюкоза из неуглеводных субстратов. Начало этого процесса происходит в митохондриальном матриксе, где пируват молекулы найдены. Молекула пирувата карбоксилируется пируваткарбоксилаза фермент, активируемый молекулой каждого из АТФ и вода. Эта реакция приводит к образованию оксалоацетата. НАДН восстанавливает оксалоацетат до малат. Это преобразование необходимо для транспортировки молекулы из митохондрии. Однажды в цитозоль, малат снова окисляется до оксалоацетата с помощью НАД +. Тогда оксалоацетат остается в цитозоле, где и будут проходить остальные реакции. Оксалоацетат позже декарбоксилируется и фосфорилируется фосфоенолпируваткарбоксикиназа и становится 2-фосфоенолпируват с помощью гуанозинтрифосфат (GTP) в качестве источника фосфата. Глюкоза получается после дальнейшей переработки.
Цикл мочевины
В цикл мочевины это метаболический путь, который приводит к образованию мочевина с использованием двух молекул аммония и одной молекулы бикарбоната.[1] Этот маршрут обычно встречается в гепатоциты. Реакции, связанные с циклом мочевины, производят НАДН ), а НАДН можно получить двумя разными способами. Одно из этих применений оксалоацетат. В цитозоле есть фумарат молекулы. Фумарат может быть преобразован в малат действием фермента фумаразы. Малат подвергается действию малатдегидрогеназы, превращаясь в оксалоацетат с образованием молекулы НАДН. После этого оксалоацетат будет переработан в аспартат, поскольку трансаминазы предпочитают эти кетокислоты другим. Эта переработка поддерживает поток азот в камеру.

Глиоксилатный цикл
В глиоксилатный цикл представляет собой вариант цикла лимонной кислоты.[3] Это анаболический путь, происходящий в растения и бактерии используя ферменты изоцитратлиаза и малатсинтаза. Некоторые промежуточные стадии цикла немного отличаются от цикла лимонной кислоты; тем не менее оксалоацетат выполняет одинаковую функцию в обоих процессах.[1] Это означает, что оксалоацетат в этом цикле также действует как первичный реагент и конечный продукт. Фактически оксалоацетат является чистым продуктом глиоксилатный цикл потому что его петля цикла включает две молекулы ацетил-КоА.
Синтез жирных кислот
На предыдущих этапах ацетил-КоА переносится из митохондрий в цитоплазму, где синтаза жирных кислот проживает. Ацетил-КоА транспортируется в виде цитрата, который ранее был образован в матриксе митохондрий из ацетил-КоА и оксалоацетата. Эта реакция обычно запускает цикл лимонной кислоты, но когда нет потребности в энергии, она транспортируется в цитоплазму, где расщепляется на цитоплазматический ацетил-КоА и оксалоацетат.
Другая часть цикла требует НАДФН для синтеза жирных кислот.[4] Часть этой восстанавливающей способности генерируется, когда цитозольный оксалоацетат возвращается в митохондрии до тех пор, пока внутренний митохондриальный слой не проницаем для оксалоацетата. Сначала оксалоацетат восстанавливается до малата с помощью НАДН. Затем малат декарбоксилируется до пирувата. Теперь этот пируват может легко попасть в митохондрии, где он снова карбоксилируется до оксалоацетата под действием пируваткарбоксилазы. Таким образом, перенос ацетил-КоА из митохондрий в цитоплазму приводит к образованию молекулы НАДН. Общую реакцию, которая носит спонтанный характер, можно резюмировать следующим образом:
- HCO3– + АТФ + ацетил-КоА → АДФ + Ря + малонил-КоА
Синтез аминокислот
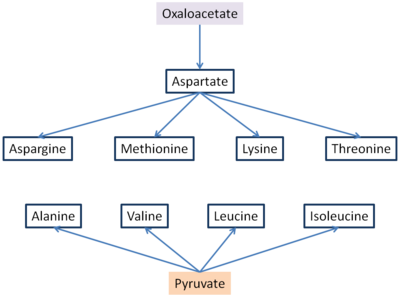
Шесть незаменимых аминокислот и три заменимых синтезируются из оксалоацетат и пируват.[5] Аспартат и аланин образуются из оксалоацетата и пирувата, соответственно, путем трансаминирования из глутамата. Аспарагин, метионин, лизин и треонин синтезируются аспартатом, поэтому, учитывая важность оксалоацетата, без него не будет образовываться аспартат и не будут производиться следующие другие аминокислоты.
Биосинтез оксалатов
Оксалоацетат производит оксалат путем гидролиза.[6]
- оксалоацетат + H2O ⇌ оксалат + ацетат
Этот процесс катализируется фермент оксалоацетаза. Этот фермент присутствует в растениях, но не известен в животном мире. [7]
Интерактивная карта проезда
| Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.[§ 1] Гликолиз и глюконеогенез редактировать
| Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи. [§ 1] Цикл TCA редактировать
|
Смотрите также
Рекомендации
- ^ а б c d Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 0-7167-4339-6.
- ^ М.В. Панченко; Виноградов А.Д. (1991). «Прямая демонстрация енол-оксалоацетата как непосредственного продукта окисления малата сукцинатдегидрогеназой млекопитающих». Письма FEBS. 286 (1–2): 76–78. Дои:10.1016 / 0014-5793 (91) 80944-X.
- ^ "Добро пожаловать в место химии". www.pearsonhighered.com. Получено 5 апреля 2018.
- ^ «синтез жирных кислот». http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb2/part1/fasynthesis.htm. Внешняя ссылка в
| publisher =(помощь); Отсутствует или пусто| url =(помощь) - ^ "http://faculty.ksu.edu.sa/69436/Documents/lecture-15-aa_from_oxaloacetate_and_pyruvate.pptx". Архивировано из оригинал в 2013-10-21. Получено 2013-10-21. Внешняя ссылка в
| название =(помощь) - ^ Гэдд, Джеффри М. "Грибковое производство лимонной и щавелевой кислоты: важность в составе металлов, физиологии и биогеохимических процессах", Успехи в физиологии микробов (1999), 41, 47-92.
- ^ Сюй, Хуа-Вэй. «Накопление оксалатов и регуляция не зависят от гликолатоксидазы в листьях риса» Journal of Experimental Botany, Vol 57, No. 9 pp. 1899-1908, 2006
| + ЧАС 2О | НАДН + Н+ НАД+ ЧАС2О FADH2 FAD КоА + АТФ (ГТФ) пя + ADP (ВВП) | ||
| НАДН + Н+ + CO 2 | |||
| CoA | НАД+ | ||












