Клеточное дыхание - Cellular respiration
эта статья нужны дополнительные цитаты для проверка. (Сентябрь 2014 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

Клеточное дыхание это набор метаболический реакции и процессы, происходящие в клетки из организмы преобразовать химическая энергия от кислород молекулы[1] или питательные вещества в аденозинтрифосфат (АТФ), а затем выпускают отходы.[2] Реакции, связанные с дыханием: катаболические реакции, которые разбивают большие молекулы на более мелкие, высвобождая энергию из-за слабых высокоэнергетических связей, в частности, в молекулярном кислороде,[3] заменяются более прочными связями в продуктах. Дыхание - один из ключевых способов высвобождения химической энергии клеткой для подпитки клеточной активности. Общая реакция происходит в виде серии биохимических стадий, некоторые из которых являются окислительно-восстановительными реакциями. Хотя клеточное дыхание технически реакция горения, он явно не похож на тот, который возникает в живой клетке, из-за медленного контролируемого высвобождения энергии в результате ряда реакций.
Питательные вещества, которые обычно используются клетками животных и растений при дыхании, включают: сахар, аминокислоты и жирные кислоты, а наиболее распространенные окислитель обеспечивает большую часть химической энергии молекулярной кислород (O2).[1] Химическая энергия, запасенная в АТФ (связь его третьей фосфатной группы с остальной частью молекулы может быть разорвана, позволяя формировать более стабильные продукты, тем самым высвобождая энергию для использования клеткой), затем может использоваться для управления процессами, требующими энергии, включая биосинтез, движение или перенос молекул через клеточные мембраны.
Аэробного дыхания
Аэробного дыхания требует кислород (O2) для создания АТФ. Несмотря на то что углеводы, жиры, и белки расходуются в качестве реагентов, аэробное дыхание является предпочтительным методом пируват распад в гликолиз, и требует пирувата для митохондрии чтобы полностью окислиться цикл лимонной кислоты. Продуктами этого процесса являются углекислый газ и вода, а передаваемая энергия используется для разрыва связей в АДФ, чтобы добавить третью фосфатную группу с образованием АТФ (аденозинтрифосфат ), от фосфорилирование на уровне субстрата, НАДН и FADH2
| Упрощенная реакция: | C6ЧАС12О6 (s) + 6 O2 (г) → 6 СО2 (г) + 6 часов2O (л) + тепло |
| ΔG = −2880 кДж на моль C6ЧАС12О6 |
Отрицательное значение ΔG указывает на то, что реакция может происходить самопроизвольно.
Потенциал НАДН и ФАДН2 преобразуется в большее количество АТФ через электронная транспортная цепь с кислородом и протонами (водородом) в качестве «концевых акцепторов электронов».[1] Большая часть АТФ, производимого аэробным клеточным дыханием, производится окислительного фосфорилирования. Энергия O2 [1] Release используется для создания хемиосмотический потенциал накачивая протоны через мембрану. Затем этот потенциал используется для управления АТФ-синтазой и производства АТФ из ADP и фосфатная группа. В учебниках биологии часто говорится, что 38 молекул АТФ могут образовываться на одну окисленную молекулу глюкозы во время клеточного дыхания (2 из гликолиза, 2 из цикла Кребса и около 34 из системы транспорта электронов).[4] Однако этот максимальный выход никогда не достигается полностью из-за потерь из-за протекающих мембран, а также из-за затрат на перемещение пирувата и АДФ в митохондриальный матрикс, и текущие оценки колеблются от 29 до 30 АТФ на глюкозу.[4]
Аэробный метаболизм до 15 раз более эффективен, чем анаэробный метаболизм (который дает 2 молекулы АТФ на 1 молекулу глюкозы), потому что двойная связь в O2 имеет более высокую энергию, чем другие двойные связи или пары одинарных связей в других распространенных молекулах биосферы.[3] Однако некоторые анаэробные организмы, такие как метаногены могут продолжить анаэробное дыхание, производя больше АТФ за счет использования других неорганических молекул (не кислорода) с высокой энергией в качестве конечных акцепторов электронов в цепи переноса электронов. Они разделяют первоначальный путь гликолиз но аэробный метаболизм продолжается с циклом Кребса и окислительным фосфорилированием. Постгликолитические реакции происходят в митохондриях в эукариотические клетки, а в цитоплазма в прокариотические клетки.
Гликолиз
Гликолиз - это метаболический путь что происходит в цитозоль клеток всех живых организмов. Гликолиз можно дословно перевести как «расщепление сахара»,[5] и происходит в присутствии кислорода или без него. В аэробных условиях процесс превращает одну молекулу глюкоза на две молекулы пируват (пировиноградная кислота), генерирующая энергию в виде двух чистых молекул АТФ. Фактически производятся четыре молекулы АТФ на глюкозу, однако две из них потребляются как часть подготовительный этап. Начальный фосфорилирование глюкозы требуется для увеличения реакционной способности (снижения ее стабильности), чтобы молекула расщепилась на две части. пируват молекулы фермента альдолаза. В течение фаза выплаты гликолиза, четыре фосфат группы передаются в ADP фосфорилирование на уровне субстрата чтобы произвести четыре АТФ и два НАДН, когда пируват окисляется. Общую реакцию можно выразить так:
- Глюкоза + 2 НАД+ + 2 Пя + 2 ADP → 2 пируват + 2 часа+ + 2 НАДН + 2 АТФ + 2 Н+ + 2 часа2O + энергия
Начиная с глюкозы, 1 АТФ используется для передачи фосфата глюкозе для производства глюкозо-6-фосфата. Гликоген может быть преобразован в глюкозо-6-фосфат также с помощью гликогенфосфорилазы. Во время энергетического обмена глюкозо-6-фосфат становится фруктозо-6-фосфатом. Дополнительный АТФ используется для фосфорилирования фруктозо-6-фосфата в фруктозо-1,6-бисфосфат с помощью фосфофруктокиназы. Затем 1,6-бифосфат фруктозы расщепляется на две фосфорилированные молекулы с тремя углеродными цепями, которые позже распадаются на пируват.
Окислительное декарбоксилирование пирувата
Пируват окисляется до ацетил-КоА и СО.2 посредством пируватдегидрогеназный комплекс (PDC). PDC содержит несколько копий трех ферментов и расположен в митохондрии эукариотических клеток и в цитозоле прокариот. При превращении пирувата в ацетил-КоА одна молекула НАДН и одна молекула СО2 сформирован.
Цикл лимонной кислоты
Это также называется Цикл Кребса или цикл трикарбоновых кислот. Когда присутствует кислород, ацетил-КоА производится из молекул пирувата, созданных в результате гликолиза. однажды ацетил-КоА может возникнуть аэробное или анаэробное дыхание.[6] Когда присутствует кислород, митохондрии подвергаются аэробному дыханию, которое приводит к циклу Кребса. Однако, если кислорода нет, происходит ферментация молекулы пирувата. В присутствии кислорода, когда образуется ацетил-КоА, молекула затем попадает в цикл лимонной кислоты (Цикл Кребса) внутри митохондриального матрикса и окисляется до CO2 в то же время уменьшая НАД к НАДН. НАДН может использоваться электронная транспортная цепь создавать дальше АТФ как часть окислительного фосфорилирования. Чтобы полностью окислить эквивалент одной молекулы глюкозы, два ацетил-КоА должны метаболизироваться в цикле Кребса. Два низкоэнергетических отходы, H2O и CO2, создаются во время этого цикла.
Цикл лимонной кислоты - это 8-этапный процесс, в котором участвуют 18 различных ферментов и коферментов.[6] Во время цикла ацетил-КоА (2 атома углерода) + оксалоацетат (4 атома углерода) дает цитрат (6 атомов углерода), который превращается в более реактивную форму, называемую изоцитратом (6 атомов углерода). Изоцитрат модифицируется в α-кетоглутарат (5 атомов углерода), сукцинил-КоА, сукцинат, фумарат, малат и, наконец, оксалоацетат.
Чистая прибыль от одного цикла составляет 3 НАДН и 1 ФАДН.2 в виде соединений, переносящих водород (протоны плюс электрон), и 1 высокоэнергетический GTP, который впоследствии может быть использован для производства АТФ. Таким образом, общий выход из 1 молекулы глюкозы (2 молекул пирувата) составляет 6 НАДН, 2 ФАДН.2, и 2 АТФ.
Окислительного фосфорилирования
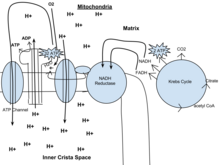
У эукариот окислительное фосфорилирование происходит в митохондриях. кристы. Он включает в себя цепь переноса электронов, которая устанавливает протонный градиент (хемиосмотический потенциал) через границу внутренней мембраны за счет окисления НАДН, образующегося в цикле Кребса. АТФ синтезируется ферментом АТФ-синтаза, когда хемиосмотический градиент используется для управления фосфорилированием АДФ. Перенос электронов осуществляется за счет химической энергии экзогенного кислорода.[1] а при добавлении двух протонов образуется вода.
Эффективность производства АТФ
В таблице ниже описаны реакции, происходящие при полном окислении одной молекулы глюкозы до диоксида углерода. Предполагается, что все уменьшенный коферменты окисляются цепью переноса электронов и используются для окислительного фосфорилирования.
| Шаг | выход кофермента | Выход АТФ | Источник АТФ |
|---|---|---|---|
| Подготовительный этап гликолиза | −2 | Фосфорилирование глюкозы и фруктозо-6-фосфата использует два АТФ из цитоплазмы. | |
| Окупаемость гликолиза | 4 | Фосфорилирование на уровне субстрата | |
| 2 НАДН | 3 или 5 | Окислительное фосфорилирование: каждый НАДН производит чистое 1,5 АТФ (вместо обычных 2,5) за счет транспорта НАДН через митохондриальную мембрану. | |
| Окислительное декарбоксилирование пирувата | 2 НАДН | 5 | Окислительного фосфорилирования |
| Цикл Кребса | 2 | Фосфорилирование на уровне субстрата | |
| 6 НАДН | 15 | Окислительного фосфорилирования | |
| 2 FADH2 | 3 | Окислительного фосфорилирования | |
| Общая доходность | 30 или 32 АТФ | От полного окисления одной молекулы глюкозы до двуокиси углерода и окисления всех восстановленных коферментов. | |
Хотя существует теоретический выход 38 молекул АТФ на глюкозу во время клеточного дыхания, такие условия обычно не реализуются из-за потерь, таких как затраты на перемещение пирувата (из гликолиза), фосфата и АДФ (субстратов для синтеза АТФ) в митохондрии. . Все они активно транспортируются с помощью носителей, которые используют запасенную энергию протона. электрохимический градиент.
- Пируват поглощается специфическим транспортером с низким Km, чтобы доставить его в митохондриальный матрикс для окисления пируватдегидрогеназным комплексом.
- В фосфатный носитель (PiC) опосредует электронейтральный обмен (антипорт ) фосфата (H2PO4−; пя) для OH− или Симпорт фосфата и протонов (H+) через внутреннюю мембрану, а движущей силой перемещения ионов фосфата в митохондрии является движущая сила протона.
- В АТФ-АДФ транслоказа (также называется адениннуклеотидтранслоказа, ANT ) является антипортер и обменивает ADP и ATP через внутренняя мембрана. Движущая сила возникает из-за того, что АТФ (-4) имеет более отрицательный заряд, чем АДФ (-3), и, таким образом, он рассеивает часть электрического компонента протонного электрохимического градиента.
Результатом этих транспортных процессов с использованием протонного электрохимического градиента является то, что более 3 H+ необходимы для производства 1 АТФ. Очевидно, это снижает теоретическую эффективность всего процесса, и вероятный максимум находится ближе к 28–30 молекулам АТФ.[4] На практике эффективность может быть даже ниже, потому что внутренняя мембрана митохондрий слегка пропускает протоны.[7] Другие факторы также могут рассеивать протонный градиент, создавая явно протекающие митохондрии. Несвязывающий белок, известный как термогенин экспрессируется в некоторых типах клеток и является каналом, по которому могут переноситься протоны. Когда этот белок активен во внутренней мембране, он замыкает связь между электронная транспортная цепь и Синтез АТФ. Потенциальная энергия протонного градиента не используется для производства АТФ, но генерирует тепло. Это особенно важно в бурый жир термогенез новорожденных и спящих млекопитающих.
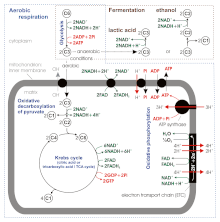
Согласно некоторым более новым источникам, выход АТФ во время аэробного дыхания составляет не 36–38, а всего около 30–32 молекул АТФ на 1 молекулу глюкозы. [8], потому что:
- АТФ: НАДН + Н+ и ATP: FADH2 соотношения во время окислительного фосфорилирования оказываются не 3 и 2, а 2,5 и 1,5 соответственно. В отличие от фосфорилирование на уровне субстрата, стехиометрию здесь установить сложно.
- АТФ-синтаза производит 1 АТФ / 3 H+. Однако обмен матричного АТФ на цитозольный АДФ и Pi (антипорт с ОН− или symport с H+) при посредничестве АТФ-АДФ транслоказа и фосфатный носитель потребляет 1 ч+ / 1 АТФ в результате регенерации трансмембранного потенциала изменился во время этого переноса, поэтому чистое соотношение составляет 1 АТФ: 4 H+.
- Митохондриальный электронная транспортная цепь протонный насос переносится через внутреннюю мембрану 10 H+ / 1 НАДН + Н+ (4 + 2 + 4) или 6 H+ / 1 FADH2 (2 + 4).
- Итак, окончательная стехиометрия
- 1 НАДН + Н+ : 10 часов+ : 10/4 АТФ = 1 НАДН + Н+ : 2,5 АТФ
- 1 FADH2 : 6 часов+ : 6/4 АТФ = 1 FADH2 : 1,5 АТФ
- АТФ: НАДН + Н+ коэффициент гликолиза при окислительном фосфорилировании составляет
- 1.5, как для FADH2, если атомы водорода (2H++ 2e−) переносятся из цитозольного NADH + H+ митохондриальному ФАД глицеринфосфатный челнок расположен во внутренней митохондриальной мембране.
- 2,5 в случае малат-аспартатный челнок перенос атомов водорода из цитозольного НАДН + Н+ к митохондриальному НАД+
Итак, наконец, на молекулу глюкозы
- Фосфорилирование на уровне субстрата: 2 АТФ от гликолиз + 2 АТФ (напрямую GTP) от Цикл Кребса
- Окислительного фосфорилирования
- 2 НАДН + Н+ от гликолиза: 2 × 1,5 АТФ (если челнок глицеринфосфата переносит атомы водорода) или 2 × 2,5 АТФ (челнок малат-аспартат)
- 2 НАДН + Н+ от окислительное декарбоксилирование пирувата и 6 из цикла Кребса: 8 × 2,5 АТФ
- 2 FADH2 из цикла Кребса: 2 × 1,5 АТФ
В сумме это дает 4 + 3 (или 5) + 20 + 3 = 30 (или 32) АТФ на молекулу глюкозы.
Эти цифры могут потребовать дальнейшей настройки по мере появления новых деталей конструкции. Приведенное выше значение 3 H + / ATP для синтазы предполагает, что синтаза перемещает 9 протонов и производит 3 ATP за один оборот. Число протонов зависит от количества субъединиц c в Fo c-кольцо, а теперь известно, что это 10 в дрожжах Fo[9] и 8 для позвоночных.[10] Включая один H + для транспортных реакций, это означает, что для синтеза одного АТФ требуется 1 + 10/3 = 4,33 протона у дрожжей и 1 + 8/3 = 3,67 у позвоночных. Это означало бы, что в митохондриях человека 10 протонов от окисления НАДН будут производить 2,72 АТФ (вместо 2,5), а 6 протонов от окисления сукцината или убихинола будут производить 1,64 АТФ (вместо 1,5). Это согласуется с экспериментальными результатами в пределах погрешности, описанными в недавнем обзоре.[11]
Общий выход АТФ в этаноле или молочной кислоте ферментация только 2 молекулы происходят из гликолиз, поскольку пируват не переносится в митохондрия и, наконец, окисляется до диоксида углерода (CO2), но сводится к этиловый спирт или молочная кислота в цитоплазма.[8]
Ферментация
Без кислорода пируват (пировиноградная кислота ) не метаболизируется посредством клеточного дыхания, но подвергается процессу ферментации. Пируват не транспортируется в митохондрии, но остается в цитоплазме, где превращается в отходы который может быть удален из камеры. Это служит цели окисления переносчиков электронов, чтобы они могли снова выполнять гликолиз и удалять избыток пирувата. Ферментация окисляет НАДН до НАД+ поэтому его можно повторно использовать при гликолизе. В отсутствие кислорода ферментация предотвращает накопление НАДН в цитоплазме и обеспечивает НАД+ для гликолиза. Эти отходы различаются в зависимости от организма. В скелетных мышцах отходы молочная кислота. Этот вид брожения называется молочнокислое брожение. При напряженных упражнениях, когда потребность в энергии превышает запас энергии, дыхательная цепь не может обработать все атомы водорода, к которым присоединен NADH. Во время анаэробного гликолиза НАД+ восстанавливается, когда пары водорода соединяются с пируватом с образованием лактата. Образование лактата катализируется лактатдегидрогеназой в обратимой реакции. Лактат также может использоваться в качестве косвенного предшественника гликогена печени. Во время восстановления, когда становится доступным кислород, НАД+ присоединяется к водороду из лактата с образованием АТФ. В дрожжах отходы этиловый спирт и углекислый газ. Этот тип ферментации известен как алкогольный или ферментация этанола. АТФ, генерируемый в этом процессе, производится фосфорилирование на уровне субстрата, не требующий кислорода.
Ферментация менее эффективно использует энергию глюкозы: на глюкозу вырабатывается только 2 АТФ, по сравнению с 38 АТФ на глюкозу, которые номинально производятся аэробным дыханием. Это потому, что большая часть энергии аэробного дыхания происходит от O2 с его относительно слабой высокоэнергетической двойной связью.[3][1] Однако гликолитический АТФ создается быстрее. Чтобы прокариоты продолжали быстро расти, когда они переходят из аэробной среды в анаэробную, они должны увеличивать скорость гликолитических реакций. Для многоклеточных организмов во время коротких всплесков напряженной активности мышечные клетки используют ферментацию, чтобы дополнить выработку АТФ из-за более медленного аэробного дыхания, поэтому ферментация может использоваться клеткой даже до того, как уровень кислорода истощится, как это имеет место в спорте. не требовать от спортсменов темпов, например спринт.
Анаэробное дыхание
Клеточное дыхание - это процесс, при котором биологическое топливо окисляется в присутствии высокоэнергетического неорганического акцептора электронов (такого как кислород[1]) для производства большого количества энергии, чтобы стимулировать массовое производство АТФ.
Анаэробное дыхание используется некоторыми микроорганизмами, у которых ни кислород (аэробное дыхание), ни производные пирувата (ферментация) не являются конечными акцепторами электронов с высокой энергией. Скорее неорганический акцептор, такой как сульфат (SO42-), нитрат (NO3–), или сера (S) используется.[12]Такие организмы обычно встречаются в необычных местах, таких как подводные пещеры или поблизости от них. гидротермальные источники на дне океана.
В июле 2019 года было проведено научное исследование Кидд Майн в Канаде обнаружил серодышащие организмы которые живут на глубине 7900 футов под поверхностью и дышат серой, чтобы выжить. Эти организмы также примечательны тем, что потребляют такие минералы, как пирит в качестве источника пищи. [13][14][15]
Смотрите также
- Поддерживающее дыхание: поддержание как функциональный компонент клеточного дыхания
- Микрофизиометрия
- Точка Пастера
- Респирометрия: инструмент для исследования клеточного дыхания
- Тетразолия хлорид: индикатор клеточного дыхания
- Комплекс 1: НАДН: убихинон оксидоредукты
использованная литература
- ^ а б c d е ж г Шмидт-Рор, К. (2020). «Кислород - это высокоэнергетическая молекула, питающая сложную многоклеточную жизнь: фундаментальные поправки к традиционной биоэнергетике» СКУД Омега 5: 2221-2233. http://dx.doi.org/10.1021/acsomega.9b03352
- ^ Бейли, Регина. "Клеточное дыхание". В архиве из оригинала от 05.05.2012.
- ^ а б c Шмидт-Рор, К. (2015). «Почему процессы сгорания всегда экзотермичны, давая около 418 кДж на моль O2", J. Chem. Educ. 92: 2094-2099. http://dx.doi.org/10.1021/acs.jchemed.5b00333
- ^ а б c Рич, П. Р. (2003). «Молекулярный аппарат дыхательной цепи Кейлина». Сделки Биохимического Общества. 31 (Pt 6): 1095–1105. Дои:10.1042 / BST0311095. PMID 14641005.
- ^ Рис1 Урри2 Каин3 Вассерман4 Минорски5 Джексон6, Джейн1 Лиза2 Майкл3 Стивен4 Питер5 Роберт6 (2010). Кэмпбелл Биология Девятое издание. Pearson Education, Inc. стр. 168.
- ^ а б "Клеточное дыхание" (PDF). В архиве (PDF) из оригинала от 10.05.2017.
- ^ Porter, R .; Бранд, М. (1 сентября 1995 г.). «Митохондриальная протонная проводимость и соотношение H + / O не зависят от скорости переноса электронов в изолированных гепатоцитах». Биохимический журнал (Бесплатный полный текст). 310 (Pt 2): 379–382. Дои:10.1042 / bj3100379. ISSN 0264-6021. ЧВК 1135905. PMID 7654171.
- ^ а б c Страйер, Люберт (1995). Биохимия (четвертое изд.). Нью-Йорк - Бейзингсток: В. Х. Фриман и компания. ISBN 978-0716720096.
- ^ Stock D, Leslie AG, Walker JE (1999). «Молекулярная архитектура вращающегося двигателя в АТФ-синтазе». Наука. 286 (5445): 1700–5. Дои:10.1126 / science.286.5445.1700. PMID 10576729.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Ватт И.Н., Монтгомери М.Г., Рансвик М.Дж., Лесли А.Г.У., Уокер Дж. Э. (2010). «Биоэнергетические затраты на создание молекулы аденозинтрифосфата в митохондриях животных». Proc. Natl. Акад. Sci. Соединенные Штаты Америки. 107 (39): 16823–16827. Дои:10.1073 / pnas.1011099107. ЧВК 2947889. PMID 20847295.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ П.Хинкль (2005). «Соотношения P / O митохондриального окислительного фосфорилирования». Biochimica et Biophysica Acta (BBA) - Биоэнергетика. 1706 (1–2): 1–11. Дои:10.1016 / j.bbabio.2004.09.004. PMID 15620362.
- ^ Lumen Boundless Microbiology. «Анаэробное дыхание - доноры и акцепторы электронов в анаэробном дыхании». course.lumenlearning.org. Boundless.com. Получено 19 ноября, 2020.
Анаэробное дыхание - это образование АТФ без кислорода. Этот метод по-прежнему включает дыхательную цепь переноса электронов, но без использования кислорода в качестве конечного акцептора электронов. Вместо этого в качестве акцепторов электронов используются такие молекулы, как сульфат (SO42-), нитрат (NO3–) или сера (S).
- ^ Lollar, Garnet S .; Уорр, Оливер; Рассказывая, Джон; Osburn, Magdalena R .; Шервуд Лоллар, Барбара (2019). "'«Следуй за водой»: гидрогеохимические ограничения на микробиологические исследования. 2,4 км под поверхностью в обсерватории глубинных флюидов и глубинной жизни Кидд-Крик ». Журнал геомикробиологии. 36: 859–872. Дои:10.1080/01490451.2019.1641770. S2CID 199636268.
- ^ Самые старые подземные воды в мире поддерживают жизнь благодаря химическому составу воды и горных пород В архиве 2019-09-10 в Wayback Machine, 29 июля 2019 г., deepcarbon.net.
- ^ Странные формы жизни, найденные глубоко в шахте, указывают на огромные `` подземные Галапагосы '' В архиве 2019-09-09 в Wayback Machine, Кори С. Пауэлл, 7 сентября 2019 г., nbcnews.com.
внешние ссылки
- Подробное описание дыхания и брожения
- Интернет-ресурс Кимбалла по клеточному дыханию
- Клеточное дыхание и ферментация в Clermont College
| Библиотечные ресурсы около Клеточное дыхание |

