Haemophilus influenzae - Haemophilus influenzae
| Haemophilus influenzae | |
|---|---|
 | |
| H. influenzae на Шоколадный агар пластина. | |
| Научная классификация | |
| Домен: | |
| Королевство: | |
| Тип: | |
| Учебный класс: | |
| Заказ: | |
| Семья: | |
| Род: | |
| Разновидность: | H. influenzae |
| Биномиальное имя | |
| Haemophilus influenzae (Леманн и Нойман, 1896 г.) Уинслоу и другие. 1917 | |
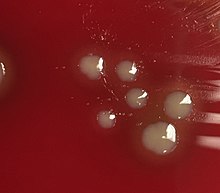
Haemophilus influenzae (ранее назывался Бацилла Пфайффера или же Bacillus influenzae) это Грамотрицательный, коккобациллярный, факультативно анаэробный капнофильный патогенная бактерия семьи Pasteurellaceae. H. influenzae был впервые описан в 1892 г. Ричард Пфайффер во время грипп пандемия.[1]
Некоторые утверждали, что бактерия является причиной грипп[2] до 1933 г., когда вирусная природа грипп был твердо установлен, и инфекции до сих пор в просторечии известны как бактериальный грипп. H. influenzae отвечает за широкий спектр локализованных и инвазивных инфекций.
Этот вид был первым свободноживущим организмом, который полностью геном последовательность.[3]
Серотипы
В 1930 году две основные категории H. influenzae были определены: неинкапсулированные штаммы и инкапсулированные штаммы. Инкапсулированные штаммы были классифицированы на основе их отдельных капсульных антигенов. Шесть общепризнанных типов инкапсулированных H. influenzae являются: a, b, c, d, e и f.[4]Генетическое разнообразие среди неинкапсулированных штаммов больше, чем внутри инкапсулированной группы. Неинкапсулированные штаммы называют нетипируемыми (NTHi), потому что у них отсутствуют капсульные серотипы; однако их можно классифицировать по мультилокусному типированию последовательностей. В патогенез из H. influenzae инфекции до конца не изучены, хотя наличие капсулы в инкапсулированном типе b (Hib), серотипе, вызывающем такие состояния, как эпиглоттит, как известно, является основным фактором вирулентности. Их капсула позволяет им сопротивляться фагоцитоз и дополнять -опосредованный лизис у неиммунного хозяина. Неинкапсулированные штаммы почти всегда менее инвазивны; однако они могут вызывать воспалительную реакцию у людей, которая может приводить ко многим симптомам. Вакцинация Конъюгированная вакцина против Hib эффективно предотвращает инфицирование Hib, но не предотвращает заражение штаммами NTHi.[5]
Болезни
| Haemophilus influenzae инфекционное заболевание | |
|---|---|
| Специальность | Инфекционное заболевание |
Большинство штаммов H. influenzae являются условно-патогенными микроорганизмами; то есть они обычно живут в своем хозяине, не вызывая болезни, но вызывают проблемы только тогда, когда другие факторы (такие как вирусная инфекция, снижение иммунной функции или хроническое воспаление тканей, например, из-за аллергии) создают возможность. Они заражают хозяина, прилипая к клетке-хозяину, используя адгезины тримерного автотранспорта.
Естественно приобретенное заболевание, вызванное H. influenzae кажется, происходит только у людей. У младенцев и детей младшего возраста H. influenzae тип b (Hib) причины бактериемия, пневмония, эпиглоттит и острые бактериальные менингит. Иногда это вызывает целлюлит, остеомиелит, и инфекционный артрит. Это одна из причин неонатальная инфекция.[6]
Благодаря регулярному использованию конъюгированной вакцины Hib в США с 1990 года заболеваемость инвазивной Hib-инфекцией снизилась до 1,3 на 100 000 у детей. Однако Hib остается основной причиной инфекций нижних дыхательных путей у младенцев и детей в развивающихся странах, где вакцина не используется широко. Неинкапсулированный H. influenzae штаммы не подвержены действию вакцины Hib и вызывают ушные инфекции (средний отит ), глазные инфекции (конъюнктивит ), и синусит у детей и связаны с пневмония.
Диагностика



Клинические признаки могут включать начальные симптомы Инфекция верхних дыхательных путей имитирующую вирусную инфекцию, обычно связанную с лихорадкой, часто субфебрильной. Это может прогрессировать в нижние дыхательные пути в течение нескольких дней с признаками, часто напоминающими хрипный бронхит. Мокрота отхаркивается с трудом, часто бывает серого или кремового цвета. Кашель может сохраняться в течение нескольких недель без соответствующего лечения. Многие случаи диагностируются после инфекций грудной клетки, которые не реагируют на пенициллины или цефалоспорины первого поколения. А рентгенограмма грудной клетки можно определить альвеолярное уплотнение.[7]
Клинический диагноз H. influenzae обычно выполняется бактериальная культура или агглютинации латексных частиц. Диагноз считается подтвержденным, когда организм изолирован от стерильного участка тела. В этом отношении, H. influenzae посев из полости носоглотки или мокроты не указывает на H. influenzae болезнь, потому что эти участки колонизируются у здоровых людей.[8] Тем не мение, H. influenzae выделенный из спинномозговой жидкости или крови может указывать на H. influenzae инфекционное заболевание.
Культура
Бактериальная культура H. influenzae выполняется на чашках с агаром, предпочтительнее шоколадный агар, с добавлением X (гемин ) и V (никотинамид аденин динуклеотид ) факторов при 37 ° C в CO2-обогащенный инкубатор.[9] Рост кровяного агара достигается только как явление-спутник вокруг других бактерий. Колонии H. influenzae выглядят как выпуклые, гладкие, бледные, серые или прозрачные колонии.
Окрашено по Граму и микроскопическое наблюдение образца H. influenzae покажет грамотрицательные коккобациллы. Культивированный организм можно дополнительно охарактеризовать с помощью каталаза и оксидаза тесты, оба из которых должны быть положительными. Необходимо дальнейшее серологическое тестирование, чтобы отличить капсульный полисахарид и различать H. influenzae б и неинкапсулированные виды.
Несмотря на высокую специфичность, бактериальная культура H. influenzae не хватает чувствительности. Использование антибиотиков перед взятием образцов значительно снижает уровень изоляции, убивая бактерии до того, как станет возможной идентификация.[10] За этим, H. influenzae является привередливой бактерией к культивированию, и любое изменение процедур культивирования может значительно снизить уровень изоляции. Низкое качество лабораторий в развивающихся странах привело к низким показателям изоляции H. influenzae.
H. influenzae будет расти в гемолитической зоне Золотистый стафилококк на пластинах с кровяным агаром; гемолиз клеток S. aureus высвобождает фактор V, необходимый для его роста. H. influenzae не будет расти за пределами гемолитической зоны S. aureus из-за нехватки питательных веществ, таких как фактор V, в этих областях. Лучше всего изолировать агар Файлдеса. В среде Левинталя капсулированные штаммы демонстрируют характерные переливчатость.
Латексная агглютинация частиц
В тест на агглютинацию латексных частиц (LAT) - более чувствительный метод обнаружения H. influenzae чем культура.[11] Поскольку метод основан на антигене, а не на жизнеспособных бактериях, предыдущее применение антибиотиков не влияет на результаты. Он также имеет дополнительное преимущество в том, что он намного быстрее, чем методы культивирования. Однако тестирование чувствительности к антибиотикам невозможно с одним LAT, поэтому необходим параллельный посев.
Молекулярные методы
Полимеразной цепной реакции (ПЦР) было доказано, что они более чувствительны, чем LAT или культуральные тесты, и обладают высокой специфичностью.[11] Однако ПЦР-анализы еще не стали обычным явлением в клинических условиях. Противоточный иммуноэлектрофорез оказался эффективным диагностическим методом исследования, но его в значительной степени вытеснили ПЦР.
Взаимодействие с Пневмококк
Обе H. influenzae и S. pneumoniae можно найти в верхних дыхательных путях человека. В in vitro изучение конкуренции, S. pneumoniae всегда побежден H. influenzae нападая на него пероксид водорода и удаляя поверхностные молекулы H. influenzae потребности для выживания.[12]
Когда обе бактерии помещаются вместе в полость носа, в течение 2 недель только H. influenzae выживает. Когда любой из них помещается отдельно в носовую полость, каждый выживает. При исследовании тканей верхних дыхательных путей мышей, подвергшихся воздействию обоих видов бактерий, чрезвычайно большое количество нейтрофилы (иммунные клетки). У мышей, подвергшихся воздействию только одного вида, нейтрофилы отсутствовали.
Лабораторные тесты показали, что нейтрофилы подвергаются воздействию мертвых H. influenzae были более агрессивны в атаке S. pneumoniae чем неэкспонированные нейтрофилы. Воздействие на мертвых H. influenzae не повлиял на жизнь H. influenzae.
Этот ответ может быть вызван двумя сценариями:
- Когда H. influenzae атакован S. pneumoniae, он сигнализирует иммунной системе атаковать S. pneumoniae
- Комбинация двух видов вызывает ответ иммунной системы, который не вызывается ни одним из видов по отдельности.
Непонятно почему H. influenzae не зависит от иммунного ответа.[13]
Болезнь
Haemophilus influenzae может вызывать инфекции дыхательных путей, включая пневмонию, средний отит, эпиглоттит (отек в горле), инфекции глаз и инфекции кровотока, менингит. Он также может вызывать целлюлит (кожную инфекцию) и инфекционный артрит (воспаление сустава).[14]
Уход
Haemophilus influenzae производит бета-лактамазы, а также может изменять свои пенициллин-связывающие белки, поэтому он приобрел устойчивость к антибиотикам семейства пенициллина. цефотаксим и цефтриаксон доставляются непосредственно в кровоток избранные антибиотики, а для менее тяжелых случаев - ассоциация ампициллин и сульбактам, цефалоспорины второго и третьего поколения, или фторхинолоны являются предпочтительными. (Устойчивый к фторхинолонам Haemophilus influenzae наблюдались.)[15]
Макролидные антибиотики (например, кларитромицин ) может применяться у пациентов с аллергией на бета-лактамные антибиотики в анамнезе.[нужна цитата ] Макролид также наблюдается сопротивление.[16]
Серьезные осложнения
Серьезными осложнениями HiB являются повреждение головного мозга, потеря слуха, и даже смерть.[17]
Профилактика

Эффективный вакцины для Haemophilus influenzae Тип B был доступен с начала 1990-х годов и рекомендован для детей в возрасте до 5 лет и пациентов с аспелезией. В Всемирная организация здоровья рекомендует пентавалентная вакцина, комбинируя вакцины против дифтерия, столбняк, коклюш, гепатит Б и Hib. Пока нет достаточных доказательств того, насколько эффективна эта пентавалентная вакцина по сравнению с отдельными вакцинами.[18]
Стоимость вакцин против Hib примерно в семь раз превышает общую стоимость вакцин против кори, полиомиелита, туберкулеза, дифтерии, столбняка и коклюша. Следовательно, в то время как 92% населения развитых стран были вакцинированы против Hib по состоянию на 2003 г., охват вакцинацией составил 42% для развивающихся стран и только 8% для наименее развитых стран.[19]
Вакцины Hib не обеспечивают перекрестной защиты с другими вакцинами. Haemophilus influenzae серотипы, такие как Hia, Hic, Hid, Hie или Hif.[20]
Оральная вакцинация была разработана для нетипируемых Haemophilus influenzae (NTHi) для пациентов с хронический бронхит но он не показал свою эффективность в снижении количества и серьезности ХОБЛ обострения.[21]
Последовательность действий
H. influenzae был первым свободноживущим организмом, весь геном которого был секвенирован. Завершено Крейгом Вентером и его командой в Институт геномных исследований - один из институтов, который сейчас входит в состав Института Дж. Крейга Вентера. Гемофильный был выбран потому, что один из руководителей проекта, лауреат Нобелевской премии Гамильтон Смит, работал над этим десятилетиями и смог предоставить высококачественные библиотеки ДНК. Геном штамма Rd KW20 состоит из 1830 138 пар оснований ДНК в одной кольцевой хромосоме, содержащей 1604 гена, кодирующего белок, 117 псевдогенов, 57 генов тРНК и 23 других гена РНК.[22] Используемый метод секвенирования был полногеномное ружье, который был завершен и опубликован в Наука в 1995 г.[23]
Вероятная защитная роль трансформации
Неинкапсулированный H. influenzae часто наблюдается в дыхательных путях пациентов с хронической обструктивной болезнью легких (ХОБЛ). Нейтрофилы также в большом количестве обнаруживаются в мокроте пациентов с ХОБЛ. Фагоцитируются нейтрофилы H. influenzae, тем самым активируя окислительный респираторный взрыв.[24] Однако вместо того, чтобы убивать бактерии, нейтрофилы сами убивают (хотя такой окислительный взрыв, вероятно, вызывает повреждение ДНК в H. influenzae ячеек). Отсутствие уничтожения бактерий, по-видимому, объясняет сохранение инфекции при ХОБЛ.[24]
H. influenzae мутанты, дефектные в rec1 ген (гомолог recA ) очень чувствительны к гибели окислителем перекисью водорода.[25] Это открытие предполагает, что rec1 выражение важно для H. influenzae выживание в условиях окислительного стресса. Поскольку это гомолог recA, rec1 вероятно, играет ключевую роль в рекомбинационной репарации повреждений ДНК. Таким образом H. influenzae может защитить свой геном от активных форм кислорода, продуцируемых фагоцитарными клетками хозяина, посредством рекомбинационной репарации окислительных повреждений ДНК.[26] Рекомбинационная репарация поврежденного участка хромосомы требует, помимо rec1, вторая гомологичная неповрежденная молекула ДНК. Индивидуальный H. influenzae клетки способны принимать гомологичную ДНК из других клеток в процессе трансформация. Преобразование в H. influenzae включает не менее 15 генных продуктов,[23] и, вероятно, адаптация для восстановления повреждений ДНК в резидентной хромосоме.
Вакцины, нацеленные на неинкапсулированные H. influenzae серотипы находятся в стадии разработки.[27]
Смотрите также
Рекомендации
- ^ Kuhnert, P; Christensen, H, eds. (2008). Pasteurellaceae: биология, геномика и молекулярные аспекты. Caister Academic Press. ISBN 978-1-904455-34-9.
- ^ Сопер, Г. А. (1919-05-30). "УРОКИ ПАНДЕМИИ". Наука. 49 (1274): 501–506. Дои:10.1126 / science.49.1274.501. ISSN 0036-8075.
- ^ [1] Об Институте Дж. Крейга Вентера, веб-сайт института Дж. Крейга Вентера, получено 21 ноября 2015 г.
- ^ Райан, KJ; Рэй, CG, ред. (2004). Шеррис Медицинская микробиология (4-е изд.). Макгроу Хилл. С. 396–401. ISBN 978-0-8385-8529-0.
- ^ Slack, МП; и другие. (1998). "Усиленное наблюдение за инвазивными Haemophilus influenzae болезнь в Англии, 1990–1996 годы: влияние конъюгированных вакцин ». Педиатр Infect Dis J. 17 (9 доп.): S204–7. Дои:10.1097/00006454-199809001-00026. PMID 9781764.
- ^ Baucells, B.J .; Mercadal Hally, M .; Álvarez Sánchez, A.T .; Фигерас Алой, Дж. (2015). "Проблемные препараты для профилактики некрозного энтероколита и позднего восстановления сепсиса и смертной казни неонатального ребенка в течение 1,500 г: una revisión sistemática". Anales de Pediatría. 85 (5): 247–255. Дои:10.1016 / j.anpedi.2015.07.038. ISSN 1695-4033. PMID 26611880.
- ^ «Измерение воздействия конъюгированной вакцинации против Streptococcus pneumoniae и Haemophilus influenzae типа b» (PDF). Всемирная организация здоровья. Сентябрь 2012 г.
- ^ Puri J; Талвар V; Juneja M; Agarwal KN; и другие. (1999). «Распространенность устойчивости к противомикробным препаратам среди респираторных изолятов Haemophilus influenzae". Индийский педиатр. 36 (10): 1029–32. PMID 10745313.
- ^ Levine OS; Schuchat A; Schwartz B; Венгер JD; Elliott J; Центры по контролю за заболеваниями (1997). "Общий протокол для популяционного наблюдения за Haemophilus influenzae тип B " (PDF). Всемирная организация здоровья. WHO / VRD / GEN / 95.05.
- ^ Джон TJ; Cherian T; Steinhoff MC; Simoes EA; и другие. (1991). «Этиология острых респираторных инфекций у детей в тропической южной Индии». Rev Infect Dis. 13: Дополнение 6: S463–9. Дои:10.1093 / Clinids / 13.supplement_6.s463. PMID 1862277.
- ^ а б Кеннеди В.А., Чанг С.Дж., Пурди К., Л.Е. Т. и др. (2007). «Заболеваемость бактериальным менингитом в Азии с использованием расширенного тестирования спинномозговой жидкости: полимеразная цепная реакция, латексная агглютинация и посевы». Эпидемиол Инфекция. 135 (7): 1217–26. Дои:10.1017 / S0950268806007734. ЧВК 2870670. PMID 17274856.
- ^ Периконе, Кристофер Д.; Овервег, Карин; Hermans, Peter W. M .; Вайзер, Джеффри Н. (2000). «Ингибирующие и бактерицидные эффекты производства перекиси водорода Streptococcus pneumoniae на других жителей верхних дыхательных путей». Заразить иммунную. 68 (7): 3990–3997. Дои:10.1128 / IAI.68.7.3990-3997.2000. ЧВК 101678. PMID 10858213.
- ^ Лысенко Е; Ратнер А; Нельсон А; Вайзер Дж. (2005). «Роль врожденных иммунных ответов в исходе межвидовой конкуренции за колонизацию поверхностей слизистых оболочек». PLoS Pathog. 1 (1): e1. Дои:10.1371 / journal.ppat.0010001. ЧВК 1238736. PMID 16201010.
- ^ "Признаки и симптомы". Центры по контролю и профилактике заболеваний (CDC). 2019-01-24.
- ^ Чанг СМ; Lauderdale TL; Ли ХК; и другие. (Август 2010 г.). «Колонизация фторхинолон-резистентных Haemophilus influenzae среди жителей домов престарелых на юге Тайваня ". J. Hosp. Заразить. 75 (4): 304–8. Дои:10.1016 / j.jhin.2009.12.020. PMID 20356651.
- ^ Робертс MC; Soge OO; Нет БД (январь 2011 г.). «Характеристика генов устойчивости к макролидам в Haemophilus influenzae изолирован от детей с муковисцидозом ». J. Antimicrob. Chemother. 66 (1): 100–4. Дои:10.1093 / jac / dkq425. PMID 21081549.
- ^ "Серьезные осложнения - сайт CDC". www.cdc.gov.
- ^ Bar-On ES; Гольдберг Э; Hellmann S; Лейбовичи Л. (2012). «Комбинированная вакцина АКДС-ВГВ-HIB по сравнению с отдельно вводимыми вакцинами АКДС-ВГВ и HIB для первичной профилактики дифтерии, столбняка, коклюша, гепатита В и Haemophilus influenzae B (HIB) ". Кокрановская база данных Syst Rev. 4 (4): CD005530. Дои:10.1002 / 14651858.CD005530.pub3. PMID 22513932.
- ^ "Haemophilus influenzae тип B (HiB) ". Темы о здоровье от А до Я. Получено 2011-03-29.
- ^ Джин З., Ромеро-Штайнер С., Карлоне GM, Роббинс Дж. Б., Шнеерсон Р. (2007). «Инфекция Haemophilus influenzae типа А и ее профилактика». Заразить. Иммунная. 75 (6): 2650–4. Дои:10.1128 / IAI.01774-06. ЧВК 1932902. PMID 17353280.
- ^ Тео, Эдвард; Локхарт, Кэтлин; Пурчури, Саи Навья; Пушпараджа, Дженнифер; Криппс, Аллан В .; ван Дриэль, Мике Л. (19 июня 2017 г.). «Оральная вакцинация против Haemophilus influenzae для предотвращения обострений хронического бронхита и хронической обструктивной болезни легких». Кокрановская база данных систематических обзоров. 6: CD010010. Дои:10.1002 / 14651858.CD010010.pub3. ISSN 1469-493X. ЧВК 6481520. PMID 28626902.
- ^ «Haemophilus influenzae Rd KW20, полная последовательность». 2020-04-04. Цитировать журнал требует
| журнал =(помощь) - ^ а б Fleischmann R; Адамс М; Белый O; Clayton R; и другие. (1995). "Полногеномное случайное секвенирование и сборка Haemophilus influenzae Rd ». Наука. 269 (5223): 496–512. Bibcode:1995Научный ... 269..496F. Дои:10.1126 / science.7542800. PMID 7542800.
- ^ а б Нейлор Э.Дж.; Бакстад Д; Biffen M; и другие. (Август 2007 г.). "Haemophilus influenzae вызывает некроз нейтрофилов: роль в хронической обструктивной болезни легких? ». Являюсь. J. Respir. Cell Mol. Биол. 37 (2): 135–43. Дои:10.1165 / rcmb.2006-0375OC. PMID 17363778.
- ^ Санчес-Ринкон Д.А.; Кабрера-Хуарес Э. (октябрь 1991 г.). «Смертельное и мутагенное действие перекиси водорода на Haemophilus influenzae". J. Bacteriol. 173 (20): 6632–4. Дои:10.1128 / jb.173.20.6632-6634.1991. ЧВК 209002. PMID 1917884.
- ^ Michod RE; Bernstein H; Недельку AM (май 2008 г.). «Адаптивное значение секса у микробных патогенов». Заразить. Genet. Evol. 8 (3): 267–85. Дои:10.1016 / j.meegid.2008.01.002. PMID 18295550.} В качестве PDF
- ^ «Исследование для оценки безопасности, реактогенности и иммуногенности исследуемой вакцины GlaxoSmithkline (GSK) Biologicals 'GSK2838504A при введении пациентам с хронической обструктивной болезнью легких (ХОБЛ) с постоянной обструкцией дыхательных путей». ClinicalTrials.gov. 2014-02-27. Получено 2016-09-20.
внешняя ссылка
- Информация о Hib на Всемирная организация здоровья (ВОЗ) сайт.
- Информационный бюллетень на Центры по контролю и профилактике заболеваний (CDC) сайт.
- Инициатива Hib -из Университет Джона Хопкинса, Лондонская школа гигиены и тропической медицины, CDC & ВОЗ
- 2 ноября: Веб-сайт Всемирного дня пневмонии
- Центры по контролю и профилактике заболеваний (2012 г.). «Глава 7: Haemophilus influenzae». В Аткинсоне W; Wolfe S; Хамборский Дж (ред.). Эпидемиология и профилактика заболеваний, предупреждаемых с помощью вакцин (12-е изд.). Вашингтон, округ Колумбия: Фонд общественного здравоохранения. С. 87–100. Архивировано из оригинал на 2017-03-10.
- "Haemophilus influenzae". Браузер таксономии NCBI. 727.
- Типовой штамм Haemophilus influenzae в BacНырять - База метаданных по бактериальному разнообразию
| Классификация | |
|---|---|
| Внешние ресурсы |

