Нейроэндокринная опухоль поджелудочной железы - Pancreatic neuroendocrine tumor
| Нейроэндокринная опухоль поджелудочной железы | |
|---|---|
 | |
| Специальность | Онкология |
| Уход | лучевая терапия, химиотерапия |
| Прогноз | Пятилетняя выживаемость ~ 61% |
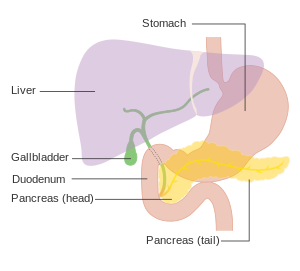
Нейроэндокринные опухоли поджелудочной железы (ПанНЕТ, Домашние питомцы, или же PNET), часто называемые «опухолями островковых клеток»,[1][2] или «эндокринные опухоли поджелудочной железы»[3][4] находятся нейроэндокринный новообразования которые возникают из клетки из эндокринный (гормональный ) и нервная система в пределах поджелудочная железа.
PanNET - это разновидность нейроэндокринная опухоль, что составляет около одной трети гастроэнтеропанкреатические нейроэндокринные опухоли (GEP-NET). Многие сети PanNET доброкачественный, а некоторые злокачественный. Агрессивные опухоли PanNET традиционно называются «островково-клеточной карциномой».
PanNET сильно отличаются от обычной формы панкреатический рак, большинство из которых аденокарциномы, возникающий в экзокринной части поджелудочной железы. Только 1 или 2% клинически значимых новообразований поджелудочной железы являются PanNET.
Типы
Большинство сетей PanNET доброкачественный, а некоторые злокачественный. Схема классификации Всемирной организации здравоохранения (ВОЗ) разделяет нейроэндокринные опухоли на три основные категории, в которых подчеркивается: степень опухоли а не анатомическое происхождение.[3] На практике те опухоли, которые называются хорошо или промежуточно дифференцированный Сети PanNET в схеме ВОЗ иногда называют "островковая клетка опухоли ». Подтип высокой степени злокачественности, называемый нейроэндокринным раком (НЭК) в схеме ВОЗ, является синонимом« карциномы островковых клеток ».
| Тип | Относительная заболеваемость | Типичное расположение опухоли[5] | Биомаркеры[5] | Симптомы[6] |
|---|---|---|---|---|
| Инсулинома | 35-40%[6] | Голова, тело, хвост поджелудочной железы | инсулин, проинсулин, С-пептид | Гипогликемия |
| Гастринома | 16-30%[6] | Гастриномный треугольник | гастрин, ПП |
|
| VIPoma | <10%[6] | Дистальный отдел поджелудочной железы (тело и хвост) | VIP |
|
| Соматостатинома | <5%[6] | Панкреатодуоденальная борозда, ампулярная, периампулярная | соматостатин | |
| PPoma | Голова или поджелудочная железа | панкреатический полипептид | ||
| Глюкагонома | 1%[7] | Тело и хвост поджелудочной железы | глюкагон, глицентин |
Относительная частота дается как процент от всех функциональных нейроэндокринных опухолей поджелудочной железы.
Признаки и симптомы
Некоторые сети PanNET не вызывают никаких симптомов, и в этом случае они могут быть случайно обнаружены при компьютерной томографии, выполненной с другой целью.[8]:43–44 Такие симптомы, как боль или давление в животе или спине, диарея, несварение желудка или пожелтение кожи и белков глаз, могут возникать в результате воздействия более крупной опухоли PanNET либо локально, либо метастаз.[9][требуется медицинская цитата ] Около 40%[требуется медицинская цитата ] PanNETS имеют симптомы, связанные с чрезмерной секрецией гормоны или активный полипептиды и соответственно помечены как «функциональные»; симптомы отражают тип выделяемого гормона, как обсуждается ниже. До 60%[требуется медицинская цитата ] сетей PanNET не являются секретными или нефункциональными, в которых нет секреции, или количества или типа продуктов, таких как панкреатический полипептид (PPoma), хромогранин А и нейротензин, не вызывают клинического синдрома, хотя уровни в крови могут быть повышены.[10] В общей сложности 85% PanNET имеют повышенный маркер крови.[2]
Функциональные опухоли часто классифицируют по гормону, который секретируется сильнее всего, например:
- гастринома: чрезмерный гастрин причины Синдром Золлингера-Эллисона (ZES) с пептические язвы и понос
- инсулинома:[11] гипогликемия происходит с одновременным повышением инсулин, проинсулин и С пептид[12]
- глюкагонома: не все симптомы связаны с повышением уровня глюкагона,[12] и включать сыпь, боль во рту, нарушение работы кишечника, венозный тромбоз, и высокий уровень глюкозы в крови[12]
- VIPoma, производя чрезмерное вазоактивный кишечный пептид, что может вызвать глубокие хронические шатери dиарея и в результате обезвоживание, часипокалиемия, и ахлоргидрия (WDHA или синдром панкреатической холеры)
- соматостатинома: эти редкие опухоли связаны с повышенным уровнем глюкозы в крови, ахлоргидрия, желчекаменная болезнь, и понос[12]
- менее распространенные типы включают АКТОМА, CRHoma, кальцитонинома, GHRHoma, GRFoma, и паращитовидная железа гормонозависимая пептидная опухоль
В этих различных типах функциональных опухолей частота злокачественных новообразований и выживаемость прогноз были оценены по-разному, но доступно соответствующее доступное резюме.[13]
Диагностика
Поскольку симптомы неспецифичны, диагностика часто откладывается.[14]
Измерение гормонов, включая панкреатический полипептид, гастрин, проинсулин, инсулин, глюкагон, и вазоактивный кишечный пептид может определить, вызывает ли опухоль гиперсекрецию.[14][15]
Многофазная КТ и МРТ являются основными методами морфологической визуализации PNET. Хотя МРТ превосходит КТ для визуализации как первичной опухоли, так и оценки метастазов, КТ более доступна. Примечательно, что в то время как многие злокачественные образования являются гиподенсированными в исследованиях с контрастным усилением, метастазы PNET в печени являются гиперваскулярными и легко визуализируются в поздней артериальной фазе постконтрастного исследования КТ. Однако одной морфологической визуализации недостаточно для постановки точного диагноза. [14][16]
На биопсия, иммуногистохимия в целом положительно для хромогранин и синаптофизин.[17] Генетическое тестирование из них обычно видны измененные MEN1 и DAXX /ATRX.[17]
Постановка
В классификации опухолей пищеварительной системы ВОЗ 2010 г. нейроэндокринные опухоли на три категории в зависимости от степени клеточная дифференциация (от хорошо дифференцированного «NET G1» до плохо дифференцированного «NET G3»). NCCN рекомендует использовать ту же систему стадирования AJCC-UICC, что и аденокарцинома поджелудочной железы.[8]:52 При использовании этой схемы поэтапные результаты для PanNET не похожи на экзокринный рак поджелудочной железы.[18] Европейское общество нейроэндокринных опухолей предложило другую систему TNM для PanNET.[19]
- Стадия нейроэндокринной опухоли поджелудочной железы (AJCC )

Стадия Т1

Стадия Т2

Стадия Т3

Стадия Т4

Поражение близлежащих лимфатических узлов - стадия N1

Метастаз - стадия М1
Уход
В общем, лечение PanNET включает тот же набор опций, что и другие нейроэндокринные опухоли, как описано в этой основной статье. Однако есть некоторые специфические отличия, которые обсуждаются здесь.[8]
В функционирующих сетях PanNET октреотид обычно рекомендуется перед биопсией[8]:21 или операция[8]:45 но обычно избегают инсулиномы чтобы избежать глубокого гипогликемия.[8]:69
ПанНЕТ в Множественная эндокринная неоплазия 1 типа часто бывают множественными и поэтому требуют разных стратегий лечения и наблюдения.[8]
Некоторые сети PanNET более чувствительны к химиотерапия чем желудочно-кишечные карциноид опухоли. Несколько агентов проявили активность.[12] В хорошо дифференцированных PanNET химиотерапия обычно применяется, когда нет других вариантов лечения. Использовались комбинации нескольких лекарств, например: доксорубицин с стрептозоцин и фторурацил (5-ФУ)[12] и капецитабин с темозоломидом.[нужна цитата ] Хотя малоэффективен в хорошо дифференцированных ПЭТ, цисплатин с этопозид имеет некоторую активность при низкодифференцированном нейроэндокринном раке (PDNEC),[12] особенно если PDNEC имеет чрезвычайно высокий Ki-67 оценка более 50%.[8]:30
Несколько таргетная терапия агенты были одобрены в PanNETs FDA на основе улучшенных выживаемость без прогрессирования (PFS):
- эверолимус (Афинитор) предназначен для лечения прогрессирующих нейроэндокринных опухолей поджелудочной железы у пациентов с неоперабельным, местнораспространенным или метастатическим заболеванием.[20][21] Безопасность и эффективность эверолимуса при карциноидных опухолях не установлены.[20][21]
- сунитиниб (Сутент) предназначен для лечения прогрессирующих, хорошо дифференцированных нейроэндокринных опухолей поджелудочной железы у пациентов с неоперабельным местнораспространенным или метастатическим заболеванием.[22][23] Сутент также получил одобрение Европейской комиссии для лечения «неоперабельных или метастатических, хорошо дифференцированных нейроэндокринных опухолей поджелудочной железы с прогрессированием заболевания у взрослых».[24] Исследование фазы III лечения сунитинибом при хорошо дифференцированной пНЭО, состояние которой ухудшилось за последние 12 месяцев (запущенное или метастатическое заболевание), показало улучшение лечения сунитинибом выживаемость без прогрессирования (11,4 месяца против 5,5 месяца), Общая выживаемость, а уровень объективных ответов (9,3% против 0,0%) по сравнению с плацебо.[25]
Генетика
Нейроэндокринные опухоли поджелудочной железы могут возникать в контексте множественная эндокринная неоплазия 1 типа, Болезнь фон Гиппеля – Линдау, нейрофиброматоз типа 1 (NF-1) или туберозный склероз (TSC)[26][27]
Анализ соматического ДНК мутации при хорошо дифференцированных нейроэндокринных опухолях поджелудочной железы были выявлены четыре важных вывода:[28][6]
- как и ожидалось, гены мутировал в NET, MEN1, ATRX, DAXX, TSC2, PTEN и PIK3CA,[28] отличаются от мутировавших генов, ранее обнаруженных в панкреатический аденокарцинома.[29][30]
- каждая шестая хорошо дифференцированная НЭО поджелудочной железы имеет мутации в mTOR гены пути, такие как TSC2, PTEN и PIK3CA.[28] Обнаружение секвенирования может позволить выбрать, какие сети выиграют от ингибирования mTOR, например, с помощью эверолимус, но это ожидает проверки в клиническое испытание.
- мутации, влияющие на новый путь рака с участием ATRX и DAXX гены были обнаружены примерно в 40% НЭО поджелудочной железы.[28] Белки, кодируемые ATRX и DAXX, участвуют в хроматин реконструкция теломеры;[31] эти мутации связаны с теломераза -независимый механизм поддержания, называемый ALT (альтернативное удлинение теломер), который приводит к аномально длинным концам теломер хромосомы.[31]
- ATRX /DAXX и MEN1 мутации были связаны с лучшим прогноз.[28]
Рекомендации
- ^ Бернс В. Р., Эдиль Б. Х. (март 2012 г.). «Нейроэндокринные опухоли поджелудочной железы: рекомендации по ведению и обновлению». Современные варианты лечения в онкологии. 13 (1): 24–34. Дои:10.1007 / s11864-011-0172-2. PMID 22198808.
- ^ а б Лечение нейроэндокринных опухолей поджелудочной железы (опухоли островковых клеток) (PDQ) Версия для специалистов здравоохранения. Национальный институт рака. 7 марта 2014 г. [1]
- ^ а б Номинал PanNET соответствует текущему ВОЗ руководящие указания. Исторически сложилось так, что PanNETs также назывались различными терминами, и их все еще часто называют «опухолями островковых клеток» или «эндокринными опухолями поджелудочной железы». Видеть: Климстра Д.С., Модлин И.Р., Коппола Д., Ллойд Р.В., Сустер С. (август 2010 г.). «Патологическая классификация нейроэндокринных опухолей: обзор номенклатуры, классификации и систем стадий» (PDF). Поджелудочная железа. 39 (6): 707–12. Дои:10.1097 / MPA.0b013e3181ec124e. PMID 20664470.
- ^ Оберг К. (декабрь 2010 г.). «Эндокринные опухоли поджелудочной железы». Семинары по онкологии. 37 (6): 594–618. Дои:10.1053 / j.seminoncol.2010.10.014. PMID 21167379.
- ^ а б Если иное не указано в полях, ссылка: Виник А., Казеллини С., Перри Р. Р., Фелиберти Е., Винган Х (2015). «Патофизиология и лечение нейроэндокринных опухолей поджелудочной железы (PNET): новые разработки». In De Groot LJ, Chrousos G, Dungan K, Feingold KR, Grossman A, Hershman JM, Koch C, Korbonits M, McLachlan R (ред.). Эндотекст. Южный Дартмут (Массачусетс): MDText.com, Inc. PMID 25905300.
- ^ а б c d е ж Маккенна Л. Р., Эдиль Б. Х. (ноябрь 2014 г.). «Обновленная информация о нейроэндокринных опухолях поджелудочной железы». Хирургия железы. 3 (4): 258–75. Дои:10.3978 / j.issn.2227-684X.2014.06.03. ЧВК 4244504. PMID 25493258.
- ^ «Глюкагонома: основы практики, патофизиология, эпидемиология». Medscape. 2019-02-01.
- ^ а б c d е ж грамм час «Нейроэндокринные опухоли, Руководство NCCN, версия 1.2015» (PDF). Рекомендации NCCN. Национальная комплексная онкологическая сеть, Inc. 11 ноября 2014 г.. Получено 25 декабря, 2014.
- ^ Лечение нейроэндокринных опухолей поджелудочной железы (опухоли островковых клеток) (PDQ®) Национальный институт рака [2]
- ^ Дженсен Р.Т., Берна М.Дж., Бингем Д.Б., Нортон Дж.А. (октябрь 2008 г.). «Унаследованные эндокринные опухолевые синдромы поджелудочной железы: достижения в молекулярном патогенезе, диагностике, лечении и противоречиях». Рак. 113 (7 Прил.): 1807–43. Дои:10.1002 / cncr.23648. ЧВК 2574000. PMID 18798544.
- ^ Грант CS (октябрь 2005 г.). «Инсулинома». Лучшие практики и исследования. Клиническая гастроэнтерология. 19 (5): 783–98. Дои:10.1016 / j.bpg.2005.05.008. PMID 16253900.
- ^ а б c d е ж грамм Бенсон А.Б., Майерсон Р.Дж. и Сассон А.Р. Рак поджелудочной железы, нейроэндокринного желудочно-кишечного тракта и надпочечников. Лечение рака: мультидисциплинарный подход, 13-е издание, 2010 г. ISBN 978-0-615-41824-7 Текст доступен в электронном виде (но может потребоваться бесплатная регистрация) на сайте http://www.cancernetwork.com/cancer-management/pancreatic/article/10165/1802606
- ^ Рэймидж Дж. К., Дэвис А. Х., Ардилл Дж., Бакс Н., Кэплин М., Гроссман А. и др. (Июнь 2005 г.). «Рекомендации по лечению гастроэнтеропанкреатических нейроэндокринных (включая карциноидных) опухолей». Кишечник. 54. 54 Приложение 4 (Suppl_4): iv1-16. Дои:10.1136 / gut.2004.053314. ЧВК 1867801. PMID 15888809.
- ^ а б c Ро К., Чай В., Ю В. Е., Ю Р. (июнь 2013 г.). «Нейроэндокринные опухоли поджелудочной железы: биология, диагностика и лечение». Китайский журнал рака. 32 (6): 312–24. Дои:10.5732 / cjc.012.10295. ЧВК 3845620. PMID 23237225.
- ^ Виник А., Казеллини С., Перри Р. Р., Фелиберти Е., Винган Х (2015). «Патофизиология и лечение нейроэндокринных опухолей поджелудочной железы (PNET): новые разработки». Эндотекст. MDText.com, Inc.
- ^ Сундин, Андерс; Арнольд, Рудольф; Боден, Эрик; Cwikla, Jaroslaw B .; Эрикссон, Барбро; Фанти, Стефано; Фацио, Никола; Джаммариле, Франческо; Хикс, Родни Дж .; Кьяер, Андреас; Креннинг, Эрик (2017). «Консенсусное руководство ENETS по стандартам лечения нейроэндокринных опухолей: радиологическая, ядерная медицина и гибридная визуализация». Нейроэндокринология. 105 (3): 212–244. Дои:10.1159/000471879. ISSN 0028-3835.
- ^ а б Если иное не указано в полях, ссылка: Пишваян MJ, Броды JR (2017). «Терапевтическое значение молекулярного подтипирования рака поджелудочной железы». Онкология (Уиллистон-Парк). 31 (3): 159–66, 168. PMID 28299752.
- ^ Национальный институт рака. Лечение нейроэндокринных опухолей поджелудочной железы (опухоли островковых клеток) (PDQ®) Частота и смертность [3]
- ^ Öberg K, Knigge U, Kwekkeboom D, Perren A (октябрь 2012 г.). «Нейроэндокринные опухоли желудочно-кишечного тракта и поджелудочной железы: клинические рекомендации ESMO по диагностике, лечению и наблюдению». Анналы онкологии. 23 Дополнение 7: vii124-30. Дои:10.1093 / annonc / mds295. PMID 22997445. (Таблица 5 описывает предлагаемую промежуточную систему TNM для сетей PanNET.)
- ^ а б Эверолимус одобрен для лечения нейроэндокринных опухолей поджелудочной железы. Почта ASCO. 15 мая 2011 г., Том 2, Выпуск 8 «Архивная копия». Архивировано из оригинал на 2013-01-17. Получено 2014-12-25.CS1 maint: заархивированная копия как заголовок (связь)
- ^ а б http://www.pharma.us.novartis.com/product/pi/pdf/afinitor.pdf
- ^ Национальный институт рака. Информация о лекарствах от рака. Одобрение FDA для сунитиниба малата. Нейроэндокринные опухоли поджелудочной железы http://www.cancer.gov/cancertopics/druginfo/fda-sunitinib-malate
- ^ http://labeling.pfizer.com/ShowLabeling.aspx?id=607
- ^ «Pfizer получает новое одобрение Sutent в Европе». 2 декабря 2010 г.
- ^ Raymond E, Dahan L, Raoul JL, Bang YJ, Borbath I, Lombard-Bohas C, et al. (Февраль 2011 г.). «Сунитиниб малат для лечения нейроэндокринных опухолей поджелудочной железы». Медицинский журнал Новой Англии. 364 (6): 501–13. Дои:10.1056 / NEJMoa1003825. PMID 21306237.
- ^ Ро К., Чай В., Ю В. Е., Ю Р. (июнь 2013 г.). «Нейроэндокринные опухоли поджелудочной железы: биология, диагностика и лечение». Китайский журнал рака. 32 (6): 312–24. Дои:10.5732 / cjc.012.10295. ЧВК 3845620. PMID 23237225.
- ^ Бакман С., Бьёрклунд П. (2017). Диагностическая и терапевтическая ядерная медицина при нейроэндокринных опухолях. Современная эндокринология. Humana Press, Cham. С. 127–140. Дои:10.1007/978-3-319-46038-3_6. ISBN 9783319460369.
- ^ а б c d е Цзяо Ю., Ши С., Эдиль Б. Х., де Вильде Р. Ф., Климстра Д. С., Майтра А. и др. (Март 2011 г.). «Гены пути DAXX / ATRX, MEN1 и mTOR часто изменяются в нейроэндокринных опухолях поджелудочной железы». Наука. 331 (6021): 1199–203. Дои:10.1126 / science.1200609. ЧВК 3144496. PMID 21252315.
- ^ Jones S, Zhang X, Parsons DW, Lin JC, Leary RJ, Angenendt P и др. (Сентябрь 2008 г.). «Основные сигнальные пути при раке поджелудочной железы человека, выявленные глобальным геномным анализом». Наука. 321 (5897): 1801–6. Дои:10.1126 / science.1164368. ЧВК 2848990. PMID 18772397.
- ^ Харада Т., Челала С., Црногорак-Юрчевич Т., Лемуан Н.Р. (2009). «Полногеномный анализ рака поджелудочной железы с использованием методов на основе микрочипов». Панкреатология. 9 (1–2): 13–24. Дои:10.1159/000178871. PMID 19077451.
- ^ а б Heaphy CM, de Wilde RF, Jiao Y, Klein AP, Edil BH, Shi C, et al. (Июль 2011 г.). «Измененные теломеры в опухолях с мутациями ATRX и DAXX». Наука. 333 (6041): 425. Дои:10.1126 / science.1207313. ЧВК 3174141. PMID 21719641.
внешняя ссылка
| Классификация |
|---|






