Холангиокарцинома - Cholangiocarcinoma
| Холангиокарцинома | |
|---|---|
| Другие имена | Рак желчного протока, рак желчного протока[1] |
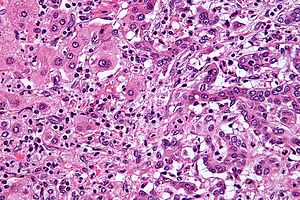 | |
| Микрофотография внутрипеченочной холангиокарциномы (справа на изображении) рядом с нормальным клетки печени (слева от изображения). H&E пятно. | |
| Произношение |
|
| Специальность | Онкология |
| Симптомы | Боль в животе, желтоватая кожа, потеря веса, генерализованный зуд, высокая температура[1] |
| Обычное начало | 70 лет[3] |
| Типы | Внутрипеченочный, перихилярный, дистальный[3] |
| Факторы риска | Первичный склерозирующий холангит, язвенный колит, заражение определенными печеночные двуустки, некоторые врожденные пороки развития печени[1] |
| Диагностический метод | Подтверждено исследованием опухоли под микроскоп[4] |
| Уход | Хирургическая резекция, химиотерапия, радиационная терапия, стентирование процедуры, трансплантация печени[1] |
| Прогноз | В целом плохой[5] |
| Частота | 1–2 человека на 100 000 в год (западный мир)[6] |
Холангиокарцинома, также известный как рак желчного протока, это тип рак что формируется в желчные протоки.[2] Симптомы холангиокарциномы могут включать: боль в животе, желтоватая кожа, потеря веса, генерализованный зуд, и лихорадка.[1] Светлый табурет или темно моча также может произойти.[4] Другой желчные пути раковые образования включают рак желчного пузыря и рак ампула Фатера.[7]
Факторы риска холангиокарциномы включают: первичный склерозирующий холангит (воспалительное заболевание желчных протоков), язвенный колит, цирроз, гепатит С, гепатит Б, заражение определенными печеночные двуустки, и некоторые врожденные пороки развития печени.[1][3][8] Однако у большинства людей нет идентифицируемых факторов риска.[3] Диагноз подозревается на основании комбинации анализы крови, медицинская визуализация, эндоскопия, а иногда и хирургическое обследование.[4] Заболевание подтверждается исследованием клеток опухоли под микроскоп.[4] Обычно это аденокарцинома (рак, который образует железы или секреты муцин ).[3]
Холангиокарцинома обычно неизлечима при постановке диагноза.[1] В этих случаях паллиативное лечение может включать хирургическая резекция, химиотерапия, радиационная терапия, и стентирование процедуры.[1] Примерно в трети случаев, связанных с общий желчный проток реже в других местах опухоль может быть полностью удалена хирургическим путем, что дает шанс на излечение.[1] Даже если хирургическое удаление прошло успешно, обычно рекомендуется химиотерапия и лучевая терапия.[1] В некоторых случаях операция может включать трансплантация печени.[3] Даже если операция прошла успешно 5-летняя выживаемость обычно меньше 50%.[6]
Холангиокарцинома редко встречается в западный мир, по оценкам 0,5–2 человека на 100 000 в год.[1][6] Ставки выше в Юго-Восточная Азия где распространены печеночные двуустки.[5] Ставки по частям Таиланд 60 на 100 000 в год.[5] Обычно это происходит у людей в возрасте 70 лет; однако у людей с первичным склерозирующим холангитом он часто возникает в возрасте 40 лет.[3] Частота холангиокарциномы в печени в западном мире увеличилась.[6]
Признаки и симптомы

Наиболее частыми физическими признаками холангиокарциномы являются отклонения от нормы. функциональные пробы печени, желтуха (пожелтение глаз и кожи, возникающее при закупорке опухолью желчных протоков), боль в животе (30–50%), генерализованный зуд (66%), потеря веса (30–50%), лихорадка (до 20%) и изменение цвета табурет или же моча.[9][10] В некоторой степени симптомы зависят от местоположения опухоли: люди с холангиокарциномой во внепеченочных желчных протоках (за пределами печени) чаще страдают желтухой, тогда как пациенты с опухолями желчных протоков в печени чаще испытывают боль без желтуха.[11]
Анализы крови функции печени у людей с холангиокарциномой часто выявляют так называемую «обструктивную картину» с повышенным билирубин, щелочная фосфатаза, и гамма-глутамилтрансфераза уровни и относительно нормальные трансаминаза уровни. Такие лабораторные данные предполагают обструкцию желчных протоков, а не воспаление или инфекция печени паренхима, как первопричина желтухи.[12]
Факторы риска

Хотя у большинства людей отсутствуют какие-либо очевидные факторы риска, ряд факторы риска для развития холангиокарциномы. В западном мире наиболее распространенным из них является первичный склерозирующий холангит (PSC), воспалительное заболевание желчных протоков, которые тесно связаны с язвенный колит (UC).[13] Эпидемиологические исследования показали, что пожизненный риск развития холангиокарциномы для человека с ПСХ составляет порядка 10-15%,[14] хотя серия аутопсий показала, что в этой популяции частота достигает 30%.[15]
Определенный паразитарные заболевания печени также могут быть факторами риска. Колонизация с печеночные двуустки Описторхис виверрини (встречается в Таиланде, Лаосской Народно-Демократической Республике и Вьетнаме)[16][17][18] или же Clonorchis sinensis (встречается в Китае, Тайване, восточной части России, Корее и Вьетнаме)[19][20] был связан с развитием холангиокарциномы. Контрольные программы направленные на ограничение потребления сырых и недоваренных продуктов, в некоторых странах позволили снизить заболеваемость холангиокарциномой.[21] Людям с хроническим заболеванием печени, будь то вирусный гепатит (например, гепатит Б или же гепатит С ),[22][23][24] алкогольная болезнь печени, или же цирроз печени по другим причинам, имеют значительно повышенный риск холангиокарциномы.[25][26] ВИЧ-инфекция был также идентифицирован в одном исследовании как потенциальный фактор риска холангиокарциномы, хотя было неясно, ВИЧ само по себе или другие коррелированные и смешанные факторы (например, инфекция гепатита С) были ответственны за ассоциацию.[25]
Заражение бактериями Helicobacter bilis и Helicobacter hepaticus виды могут вызвать рак желчных путей.[27]
Врожденный аномалии печени, такие как Синдром Кароли (конкретный тип из пяти признанных кисты холедоха ), были связаны с примерно 15% пожизненным риском развития холангиокарциномы.[28][29] Редкие наследственные заболевания Синдром Линча II и билиарный папилломатоз также связаны с холангиокарциномой.[30][31] Наличие камней в желчном пузыре (желчекаменная болезнь ) явно не связан с холангиокарциномой. Однако внутрипеченочные камни (называемые гепатолитиаз ), которые редки на Западе, но распространены в некоторых частях Азии, были тесно связаны с холангиокарциномой.[32][33][34] Воздействие на Торотраст, форма диоксид тория который использовался как радиологический контраст, был связан с развитием холангиокарциномы уже через 30-40 лет после заражения; Торотраст был запрещен в США в 1950-х годах из-за его канцерогенность.[35][36][37]
Патофизиология

Холангиокарцинома может поражать любую область желчных протоков внутри или за пределами печени. Опухоли, возникающие в желчных протоках в печени, называются внутрипеченочныйте, которые возникают в протоках вне печени, являются внепеченочный, и опухоли, возникающие в месте выхода желчных протоков из печени, могут называться перихилярный. Холангиокарцинома, возникающая на стыке левого и правого печеночных протоков, образуя общий печеночный проток можно отнести к одноименно как Опухоль Клацкина.[38]
Хотя известно, что холангиокарцинома имеет гистологические и молекулярные особенности аденокарцинома эпителиальных клеток, выстилающих желчные пути, фактическое происхождение клетки неизвестно. Недавние данные свидетельствуют о том, что исходная трансформированная клетка, которая генерирует первичную опухоль, может возникнуть из плюрипотентный печеночный стволовая клетка.[39][40][41] Считается, что холангиокарцинома проходит несколько стадий - от раннего гиперплазия и метаплазия, через дисплазия, к развитию откровенного карцинома - в процессе, аналогичном тому, который наблюдается при разработке рак толстой кишки.[42] Хроническое воспаление считается, что обструкция желчных протоков и, как следствие, нарушение оттока желчи, играют роль в этом прогрессировании.[42][43][44]
Гистологически, холангиокарциномы могут варьироваться от от недифференцированного до хорошо дифференцированного. Их часто окружает бойкая фиброзный или же десмопластический тканевый ответ; при наличии обширного фиброза бывает трудно отличить хорошо дифференцированную холангиокарциному от нормальной реактивной эпителий. Нет полностью конкретного иммуногистохимический пятно, которое можно различить злокачественный из доброкачественный ткань желчных протоков, хотя окрашивание на цитокератины, карциноэмбриональный антиген, и муцины может помочь в диагностике.[45] Большинство опухолей (> 90%) аденокарциномы.[46]
Диагностика

Анализы крови
Нет конкретных анализы крови которые могут сами диагностировать холангиокарциному. Уровни сыворотки карциноэмбриональный антиген (CEA) и CA19-9 часто приподняты, но не чувствительный или же специфический достаточно, чтобы использоваться в качестве генерала скрининг инструмент. Однако они могут быть полезны в сочетании с методы визуализации в поддержку предполагаемого диагноза холангиокарциномы.[47]
Визуализация брюшной полости

УЗИ из печень и желчное дерево часто используется в качестве начального метода визуализации у людей с подозрением на механическую желтуху.[48][49] Ультразвук может выявить обструкцию и расширение протоков, а в некоторых случаях может быть достаточным для диагностики холангиокарциномы.[50] Компьютерная томография (КТ) сканирование также может играть важную роль в диагностике холангиокарциномы.[51][52][53]
Визуализация желчного дерева

В то время как визуализация брюшной полости может быть полезна при диагностике холангиокарциномы, прямая визуализация желчные протоки часто бывает необходимо. Эндоскопическая ретроградная холангиопанкреатография (ERCP), эндоскопический процедура, выполняемая гастроэнтеролог или специально обученного хирурга, широко использовались для этой цели. Хотя ЭРХПГ является инвазивной процедурой с сопутствующими рисками, ее преимущества включают возможность биопсия и разместить стенты или выполнить другие вмешательства для снятия обструкции желчных путей.[12] Эндоскопическое УЗИ также может выполняться во время ERCP и может повысить точность биопсии и дать информацию о лимфатический узел вторжение и работоспособность.[54] В качестве альтернативы ERCP, чрескожная чреспеченочная холангиография (PTC) могут быть использованы. Магнитно-резонансная холангиопанкреатография (MRCP) - это неинвазивный альтернатива ERCP.[55][56][57] Некоторые авторы предположили, что MRCP должен заменять ERCP в диагностике рака желчных путей, поскольку он может более точно определять опухоль и избегать рисков ERCP.[58][59][60]
Хирургия
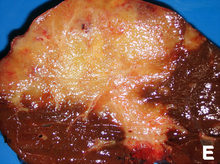
Хирургическое исследование может потребоваться для получения подходящего биопсия и точно сцена человек с холангиокарциномой. Лапароскопия могут использоваться в целях постановки и могут избежать необходимости в более инвазивных хирургических процедурах, таких как лапаротомия, у некоторых людей.[61][62]
Патология
Гистологически холангиокарциномы классически хорошо или умеренно дифференцированы. аденокарциномы. Иммуногистохимия полезен при диагностике и может использоваться для дифференциации холангиокарциномы от гепатоцеллюлярная карцинома и метастазирование других опухолей желудочно-кишечного тракта.[63] Цитологические соскобы часто недиагностика,[64] поскольку эти опухоли обычно имеют десмопластический стромы и, следовательно, не выделяют диагностические опухолевые клетки со соскобами.
Постановка
Хотя есть как минимум три системы постановки для холангиокарциномы (например, висмута, Блюмгарта и Американский объединенный комитет по раку ), ни один из них не оказался полезным для прогнозирования выживаемости.[65] Наиболее важным вопросом стадии является то, может ли опухоль быть хирургически удален, или слишком ли она развита для успешного хирургического лечения. Часто это определение можно сделать только во время операции.[12]
Общие рекомендации по работоспособности включают:[66][67]
- Отсутствие лимфатический узел или же печень метастазы
- Отсутствие вовлечения воротная вена
- Отсутствие прямого вторжения в соседние органы
- Отсутствие широко распространенного метастатического заболевания
Уход
Холангиокарцинома считается неизлечимой и быстро смертельной болезнью, если все опухоли не могут быть полностью удалены. резецированный (вырезано хирургическим путем). Поскольку в большинстве случаев работоспособность опухоли можно оценить только во время операции,[68] Большинство людей подвергаются диагностической хирургии, если уже нет четких указаний на то, что опухоль неоперабельна.[12] Тем не менее, клиника Мэйо сообщила о значительных успехах в лечении рака желчных протоков на ранних стадиях с помощью трансплантации печени с использованием протоколированного подхода и строгих критериев отбора.[69]
Адъювантная терапия с последующей трансплантация печени может сыграть роль в лечении некоторых неоперабельных случаев.[70] Локорегиональные методы лечения, включая трансартериальную химиоэмболизацию (TACE), трансартериальную радиоэмболизацию (TARE) и абляционную терапию, играют роль во внутрипеченочных вариантах холангиокарциномы, обеспечивая паллиативное или возможное излечение у людей, которые не являются кандидатами на хирургическое вмешательство.[71]
Адъювантная химиотерапия и лучевая терапия
Если опухоль удаляется хирургическим путем, люди могут получить адъювант химиотерапия или же радиационная терапия после операции, чтобы улучшить шансы на выздоровление. Если края ткани отрицательные (т.е. опухоль полностью исчезла) вырезанный ), адъювантная терапия не имеет определенного преимущества. Оба положительных[72][73] и отрицательный[11][74][75] сообщалось о результатах адъювантной лучевой терапии в этих условиях, и никаких перспективных рандомизированные контролируемые испытания были проведены по состоянию на март 2007 года. Адъювантная химиотерапия оказалась неэффективной у людей с полностью удаленными опухолями.[76] Роль комбинированной химиолучевой терапии в этой ситуации неясна. Однако, если границы опухолевой ткани положительные, что указывает на то, что опухоль не была полностью удалена хирургическим путем, то на основании имеющихся данных обычно рекомендуется адъювантная терапия с лучевой и, возможно, химиотерапией.[77]
Лечение запущенной болезни
В большинстве случаев холангиокарцинома протекает как неоперабельное (неоперабельное) заболевание.[78] в этом случае людей обычно лечат паллиативный химиотерапия, с или без лучевая терапия. Химиотерапия была показана в рандомизированное контролируемое исследование улучшить качество жизни и увеличить выживаемость у людей с неоперабельной холангиокарциномой.[79] Не существует единой схемы химиотерапии, которая используется повсеместно, и клинические испытания часто рекомендуется, когда это возможно.[77] Химиотерапевтические агенты, используемые для лечения холангиокарциномы, включают: 5-фторурацил с лейковорин,[80] гемцитабин как единый агент,[81] или гемцитабин плюс цисплатин,[82] иринотекан,[83] или же капецитабин.[84] Небольшое пилотное исследование показало возможную пользу от тирозинкиназа ингибитор эрлотиниб у людей с запущенной холангиокарциномой.[85]Лучевая терапия, по-видимому, продлевает выживаемость у людей с удаленной внепеченочной холангиокарциномой.[86] и несколько сообщений о его применении при неоперабельной холангиокарциноме, по-видимому, показывают улучшение выживаемости, но их количество невелико.[87]
Прогноз
Хирургическая резекция - единственный потенциальный шанс на излечение холангиокарциномы. Для неоперабельных случаев 5-летняя выживаемость составляет 0%, если болезнь неоперабельна, поскольку в дистальных лимфатических узлах обнаруживаются метастазы.[88] и менее 5% в целом.[89] Общая средняя продолжительность выживания у людей с метастазами составляет менее 6 месяцев.[90]
В хирургических случаях шансы на излечение варьируются в зависимости от локализации опухоли и от того, можно ли удалить опухоль полностью или только частично. Дистальные холангиокарциномы (возникающие из общий желчный проток ) обычно лечат хирургическим путем с Процедура Уиппла; долгосрочная выживаемость составляет 15-25%, хотя в одной серии сообщалось о пятилетняя выживаемость 54% для людей без участия лимфатический узел.[91] Внутрипеченочные холангиокарциномы (возникающие из желчных протоков внутри печень ) обычно лечатся частичная гепатэктомия. В различных сериях сообщалось об оценке выживаемости после операции в диапазоне от 22 до 66%; результат может зависеть от поражения лимфатических узлов и полноты операции.[92] Перихилярные холангиокарциномы (возникающие рядом с выходом желчных протоков из печени) с наименьшей вероятностью поддаются операции. Когда возможно хирургическое вмешательство, к ним обычно относятся агрессивно, часто включая: удаление желчного пузыря и потенциально часть печени. У пациентов с операбельными перихилярными опухолями 5-летняя выживаемость варьируется от 20 до 50%.[93]
В прогноз может быть хуже для людей с первичным склерозирующим холангитом, у которых развивается холангиокарцинома, вероятно, потому, что рак не обнаруживается, пока он не продвинулся.[15][94] Некоторые данные свидетельствуют о том, что результаты могут улучшаться при более агрессивных хирургических подходах и адъювантная терапия.[95]
Эпидемиология
| Страна | IC (мужчины / женщины) | ЭК (мужчины / женщины) |
|---|---|---|
| СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. | 0.60/0.43 | 0.70/0.87 |
| Япония | 0.23/0.10 | 5.87/5.20 |
| Австралия | 0.70/0.53 | 0.90/1.23 |
| Англия / Уэльс | 0.83/0.63 | 0.43/0.60 |
| Шотландия | 1.17/1.00 | 0.60/0.73 |
| Франция | 0.27/0.20 | 1.20/1.37 |
| Италия | 0.13/0.13 | 2.10/2.60 |

Холангиокарцинома - относительно редкая форма рака; ежегодно в Соединенных Штатах диагностируется примерно от 2000 до 3000 новых случаев, что означает ежегодный заболеваемость 1-2 случая на 100 000 человек.[98] Вскрытие серия сообщила о распространенность от 0,01% до 0,46%.[78][99] В Азии более высокая распространенность холангиокарциномы, которую связывают с эндемическим хроническим паразитарным заражением. Заболеваемость холангиокарциномой увеличивается с возрастом, и заболевание несколько чаще встречается у мужчин, чем у женщин (возможно, из-за более высокой частоты первичный склерозирующий холангит, основной фактор риска у мужчин).[46] По данным аутопсических исследований, распространенность холангиокарциномы у людей с первичным склерозирующим холангитом может достигать 30%.[15]
Множественные исследования документально подтвердили устойчивый рост заболеваемости внутрипеченочной холангиокарциномой за последние несколько десятилетий; рост был замечен в Северной Америке, Европе, Азии и Австралии.[100] Причины учащения холангиокарциномы неясны; Отчасти это может быть связано с улучшенными диагностическими методами, но распространенность потенциальных факторов риска холангиокарциномы, таких как ВИЧ-инфекция, также увеличилась в течение этого периода времени.[25]
Примечания
- ^ а б c d е ж грамм час я j k «Лечение рака желчных протоков (холангиокарциномы) (PDQ®) - версия для специалистов в области здравоохранения». Национальный институт рака. 14 марта 2018 г.. Получено 21 января 2019.
- ^ а б "Словарь терминов по раку NCI". Национальный институт рака. 2 февраля 2011 г.. Получено 21 января 2019.
- ^ а б c d е ж грамм Разумилава Н., Горес Г.Дж. (июнь 2014 г.). «Холангиокарцинома». Ланцет. 383 (9935): 2168–79. Дои:10.1016 / S0140-6736 (13) 61903-0. ЧВК 4069226. PMID 24581682.
- ^ а б c d «Симптомы, анализы, прогнозы и стадии рака желчных протоков (холангиокарциномы)». Национальный институт рака. 5 июля 2018 г.. Получено 21 января 2019.
- ^ а б c Босман, Фрэнк Т. (2014). «Глава 5.6: Рак печени». У Стюарта, Бернарда У .; Уайлд, Кристофер П. (ред.). Всемирный доклад о раке. Международное агентство по изучению рака Всемирной организации здравоохранения. С. Глава 5.6. ISBN 978-92-832-0443-5.

- ^ а б c d Бриджуотер Дж. А., Гудман К. А., Калян А., Малкахи М. Ф. (2016). «Рак желчных путей: эпидемиология, лучевая терапия и молекулярное профилирование». Учебное пособие Американского общества клинической онкологии. Американское общество клинической онкологии. Ежегодное собрание. 35 (36): e194-203. Дои:10.1200 / EDBK_160831. PMID 27249723.
- ^ Бенавидес М., Антон А., Гальего Дж., Гомес М.А., Хименес-Гордо А., Ла Каста А. и др. (Декабрь 2015 г.). «Рак желчных путей: клинические рекомендации SEOM». Клиническая и трансляционная онкология. 17 (12): 982–7. Дои:10.1007 / s12094-015-1436-2. ЧВК 4689747. PMID 26607930.
- ^ Стил Дж. А., Рихтер С. К., Эчаубард П., Саенна П., Стаут В., Сититхаворн П., Уилкокс Б. А. (май 2018 г.). «Не ограничиваясь Opisthorchis viverrini риска холангиокарциномы в регионе нижнего Меконга: систематический обзор и метаанализ». Инфекционные болезни бедности. 7 (1): 44. Дои:10.1186 / s40249-018-0434-3. ЧВК 5956617. PMID 29769113.
- ^ Нагорни Д.М., Донохью Дж. Х., Фарнелл М.Б., Шлек CD, Ilstrup DM (Август 1993 г.). «Результаты после лечебных резекций холангиокарциномы». Архив хирургии. 128 (8): 871–7, обсуждение 877–9. Дои:10.1001 / archsurg.1993.01420200045008. PMID 8393652.
- ^ Рак желчных протоков: причина и лечение
- ^ а б Накиб А., Питт Х.А., Сон Т.А., Коулман Дж., Абрамс Р.А., Пиантадози С., Хрубан Р.Х., Лиллемо К.Д., Йео С.Дж., Кэмерон Дж.Л. (октябрь 1996 г.). «Холангиокарцинома. Спектр внутрипеченочных, перихилярных и дистальных опухолей». Анналы хирургии. 224 (4): 463–73, обсуждение 473–5. Дои:10.1097/00000658-199610000-00005. ЧВК 1235406. PMID 8857851.
- ^ а б c d Марк Фельдман; Лоуренс С. Фридман; Лоуренс Дж. Брандт, ред. (21 июля 2006 г.). Заболевания желудочно-кишечного тракта и печени Слейзенгера и Фордтрана (8-е изд.). Сондерс. стр.1493–6. ISBN 978-1-4160-0245-1.
- ^ Чепмен Р.В. (1999). «Факторы риска канцерогенеза желчевыводящих путей». Анналы онкологии. 10 Дополнение 4 (Suppl 4): 308–11. Дои:10.1023 / А: 1008313809752. PMID 10436847.
- ^ Эпидемиологические исследования, которые изучали заболеваемость холангиокарциномой у людей с первичным склерозирующим холангитом, включают следующее:
- Бергквист А., Экбом А., Олссон Р., Корнфельдт Д., Лёф Л., Даниэльссон А., Хульткранц Р., Линдгрен С., Приц Х., Сандберг-Герцен Х., Альмер С., Гранат Ф., Бруме У. (март 2002 г.). «Печеночные и внепеченочные злокачественные новообразования при первичном склерозирующем холангите». Журнал гепатологии. 36 (3): 321–7. Дои:10.1016 / S0168-8278 (01) 00288-4. PMID 11867174.
- Бергквист А., Глауманн Х., Перссон Б., Бруме У. (февраль 1998 г.). «Факторы риска и клинические проявления гепатобилиарной карциномы у пациентов с первичным склерозирующим холангитом: исследование случай-контроль». Гепатология. 27 (2): 311–6. Дои:10.1002 / hep.510270201. PMID 9462625.
- Бурак К., Ангуло П., Паша Т.М., Иган К., Петц Дж., Линдор К.Д. (март 2004 г.). «Заболеваемость и факторы риска холангиокарциномы при первичном склерозирующем холангите». Американский журнал гастроэнтерологии. 99 (3): 523–6. PMID 15056096.
- ^ а б c Rosen CB, Nagorney DM, Wiesner RH, Coffey RJ, LaRusso NF (январь 1991 г.). «Холангиокарцинома, осложняющая первичный склерозирующий холангит». Анналы хирургии. 213 (1): 21–5. Дои:10.1097/00000658-199101000-00004. ЧВК 1358305. PMID 1845927.
- ^ Ватанапа П., Ватанапа ВБ (август 2002 г.). «Холангиокарцинома, связанная с двуусткой печени». Британский журнал хирургии. 89 (8): 962–70. Дои:10.1046 / j.1365-2168.2002.02143.x. PMID 12153620.
- ^ Шрипа Б., Кеукес С., Сититаворн П., Майианг Э, Лаха Т., Смаут М., Пайроджкул С., Бхудхисавасди В., Тесана С., Thinkamrop Б., Бетони Дж. М., Лукас А., Бриндли П.Дж. (июль 2007 г.). «Печеночная двуустка вызывает холангиокарциному». PLOS Медицина. 4 (7): e201. Дои:10.1371 / journal.pmed.0040201. ЧВК 1913093. PMID 17622191.
- ^ Срипа Б., Кеукес С., Интапан П.М., Малеевонг В., Бриндли П.Дж. (2010). Пищевые трематодозы в Юго-Восточной Азии эпидемиология, патология, клинические проявления и борьба. Достижения в паразитологии. 72. С. 305–50. Дои:10.1016 / S0065-308X (10) 72011-X. ISBN 9780123815132. PMID 20624536.
- ^ Рустаги Т., Дасану ЦА (июнь 2012 г.). «Факторы риска рака желчного пузыря и холангиокарциномы: сходства, различия и обновления». Журнал рака желудочно-кишечного тракта. 43 (2): 137–47. Дои:10.1007 / s12029-011-9284-у. PMID 21597894.
- ^ Hong ST, Fang Y (март 2012 г.). «Clonorchis sinensis и клонорхоз, обновление». Parasitology International. 61 (1): 17–24. Дои:10.1016 / j.parint.2011.06.007. PMID 21741496.
- ^ Шрипа Б., Тангкаваттана С., Сангникул Т. (август 2017 г.). «Модель Лава: устойчивая комплексная программа борьбы с описторхозом с использованием подхода EcoHealth в районе озера Лава в Таиланде». Parasitology International. 66 (4): 346–354. Дои:10.1016 / j.parint.2016.11.013. ЧВК 5443708. PMID 27890720.
- ^ Кобаяси М., Икеда К., Сайто С., Сузуки Ф., Цубота А., Сузуки Ю., Арасе Ю., Мурашима Н., Чаяма К., Кумада Х (июнь 2000 г.). «Заболеваемость первичной холангиоцеллюлярной карциномой печени у японских пациентов с циррозом, связанным с вирусом гепатита С». Рак. 88 (11): 2471–7. Дои:10.1002 / 1097-0142 (20000601) 88:11 <2471 :: AID-CNCR7> 3.0.CO; 2-T. PMID 10861422.
- ^ Ямамото С., Кубо С., Хай С., Уениши Т., Ямамото Т., Шуто Т., Такемура С., Танака Н., Ямадзаки О., Хирохаши К., Танака Т. (июль 2004 г.). «Инфекция вирусом гепатита С как вероятная этиология внутрипеченочной холангиокарциномы». Наука о раке. 95 (7): 592–5. Дои:10.1111 / j.1349-7006.2004.tb02492.x. PMID 15245596.
- ^ Лу Х, Е М.К., Тхунг С.Н., Даш С., Гербер М.А. (декабрь 2000 г.). «Обнаружение последовательностей РНК вируса гепатита С в холангиокарциномах у китайских и американских пациентов». Китайский медицинский журнал. 113 (12): 1138–41. PMID 11776153.
- ^ а б c Шаиб Я. Х., Эль-Сераг Х. Б., Давила Дж. А., Морган Р., МакГлинн К. А. (март 2005 г.). «Факторы риска внутрипеченочной холангиокарциномы в Соединенных Штатах: исследование случай-контроль». Гастроэнтерология. 128 (3): 620–6. Дои:10.1053 / j.gastro.2004.12.048. PMID 15765398.
- ^ Соренсен Х.Т., Фриис С., Олсен Дж. Х., Тюльструп А.М., Меллемкьяер Л., Лайнет М., Трихопулос Д., Вилструп Х., Олсен Дж. (Октябрь 1998 г.). «Риск развития рака печени и других типов рака у пациентов с циррозом: общенациональное когортное исследование в Дании». Гепатология. 28 (4): 921–5. Дои:10.1002 / hep.510280404. PMID 9755226.
- ^ Чанг А.Х., Парсоннет Дж. (Октябрь 2010 г.). «Роль бактерий в онкогенезе». Обзоры клинической микробиологии. 23 (4): 837–57. Дои:10.1128 / CMR.00012-10. ЧВК 2952975. PMID 20930075.
- ^ Lipsett PA, Pitt HA, Colombani PM, Boitnott JK, Cameron JL (ноябрь 1994 г.). «Заболевание кисты холедоха. Меняющаяся картина проявления». Анналы хирургии. 220 (5): 644–52. Дои:10.1097/00000658-199411000-00007. ЧВК 1234452. PMID 7979612.
- ^ Dayton MT, Longmire WP, Tompkins RK (январь 1983 г.). «Болезнь Кароли: предраковое состояние?». Американский журнал хирургии. 145 (1): 41–8. Дои:10.1016/0002-9610(83)90164-2. PMID 6295196.
- ^ Mecklin JP, Järvinen HJ, Virolainen M (март 1992). «Связь между холангиокарциномой и наследственной неполипозной колоректальной карциномой». Рак. 69 (5): 1112–4. Дои:10.1002 / cncr.2820690508. PMID 1310886.
- ^ Lee SS, Kim MH, Lee SK, Jang SJ, Song MH, Kim KP, Kim HJ, Seo DW, Song DE, Yu E, Lee SG, Min YI (февраль 2004 г.). «Клинико-патологический обзор 58 больных билиарным папилломатозом». Рак. 100 (4): 783–93. Дои:10.1002 / cncr.20031. PMID 14770435.
- ^ Ли CC, Wu CY, Chen GH (сентябрь 2002 г.). «Как влияет сосуществование гепатолитиаза на холангиокарциному?». Журнал гастроэнтерологии и гепатологии. 17 (9): 1015–20. Дои:10.1046 / j.1440-1746.2002.02779.x. PMID 12167124.
- ^ Су CH, Shyr YM, Lui WY, P'Eng FK (июль 1997 г.). «Гепатолитиаз, связанный с холангиокарциномой». Британский журнал хирургии. 84 (7): 969–73. Дои:10.1002 / bjs.1800840717. PMID 9240138.
- ^ Донато Ф., Гелатти Ю., Таггер А., Фаврет М., Риберо М. Л., Каллеа Ф, Мартелли С., Савио А., Тревизи П., Нарди Дж. (Декабрь 2001 г.). «Внутрипеченочная холангиокарцинома и вирусная инфекция гепатита C и B, употребление алкоголя и гепатолитиаз: исследование случай-контроль в Италии». Причины рака и борьба с ними. 12 (10): 959–64. Дои:10.1023 / А: 1013747228572. PMID 11808716.
- ^ Сахани Д., Прасад С.Р., Таннабе К.К., Хан П.Ф., Мюллер П.Р., Шайни С. (2003). «Холангиокарцинома, вызванная торотрастом: клинический случай». Визуализация брюшной полости. 28 (1): 72–4. Дои:10.1007 / s00261-001-0148-y. PMID 12483389.
- ^ Чжу AX, Lauwers GY, Tanabe KK (2004). «Холангиокарцинома, связанная с воздействием Торотраста». Журнал гепато-билиарной-панкреатической хирургии. 11 (6): 430–3. Дои:10.1007 / s00534-004-0924-5. PMID 15619021.
- ^ Липшуц Г.С., Бреннан ТВ, Уоррен Р.С. (ноябрь 2002 г.). "Неоплазия печени, вызванная торотрастом: коллективный обзор". Журнал Американского колледжа хирургов. 195 (5): 713–8. Дои:10.1016 / S1072-7515 (02) 01287-5. PMID 12437262.
- ^ Клацкин Г (февраль 1965 г.). «Аденокарцинома печеночного протока при его бифуркации в воротах печени. Необычная опухоль с отличительными клиническими и патологическими особенностями». Американский журнал медицины. 38 (2): 241–56. Дои:10.1016/0002-9343(65)90178-6. PMID 14256720.
- ^ Роскамс Т (июнь 2006 г.). «Стволовые клетки печени и их значение в гепатоцеллюлярной и холангиокарциноме». Онкоген. 25 (27): 3818–22. Дои:10.1038 / sj.onc.1209558. PMID 16799623.
- ^ Лю Ц., Ван Дж., Оу Кью (ноябрь 2004 г.). «Возможное происхождение холангиокарциномы человека из стволовых клеток». Всемирный журнал гастроэнтерологии. 10 (22): 3374–6. Дои:10.3748 / wjg.v10.i22.3374. ЧВК 4572317. PMID 15484322.
- ^ Продайте S, Дансфорд HA (июнь 1989 г.). "Доказательства происхождения гепатоцеллюлярной карциномы и холангиокарциномы стволовыми клетками". Американский журнал патологии. 134 (6): 1347–63. ЧВК 1879951. PMID 2474256.
- ^ а б Sirica AE (январь 2005 г.). «Холангиокарцинома: стратегии молекулярного таргетинга для химиопрофилактики и терапии». Гепатология. 41 (1): 5–15. Дои:10.1002 / hep.20537. PMID 15690474.
- ^ Holzinger F, Z'graggen K, Büchler MW (1999). «Механизмы канцерогенеза желчных путей: патогенетический многоступенчатый каскад к холангиокарциноме». Анналы онкологии. 10 Дополнение 4 (Suppl 4): 122–6. Дои:10.1023 / А: 1008321710719. PMID 10436802.
- ^ Горс Г.Дж. (май 2003 г.). «Холангиокарцинома: современные концепции и идеи». Гепатология. 37 (5): 961–9. Дои:10.1053 / jhep.2003.50200. PMID 12717374.
- ^ de Groen PC, Gores GJ, LaRusso NF, Gunderson LL, Nagorney DM (октябрь 1999 г.). «Рак желчных путей». Медицинский журнал Новой Англии. 341 (18): 1368–78. Дои:10.1056 / NEJM199910283411807. PMID 10536130.
- ^ а б Henson DE, Albores-Saavedra J, Corle D (сентябрь 1992 г.). «Карцинома внепеченочных желчных протоков. Гистологические типы, стадия заболевания, степень и выживаемость». Рак. 70 (6): 1498–501. Дои:10.1002 / 1097-0142 (19920915) 70: 6 <1498 :: AID-CNCR2820700609> 3.0.CO; 2-C. PMID 1516001.
- ^ Исследования эффективности сывороточных маркеров холангиокарциномы (таких как карциноэмбриональный антиген и CA19-9) у пациентов с первичным склерозирующим холангитом и без него включают следующее:
- Нелс О., Грегор М., Кламп Б. (май 2004 г.). «Сывороточные и желчные маркеры холангиокарциномы». Семинары по заболеванию печени. 24 (2): 139–54. Дои:10.1055 / с-2004-828891. PMID 15192787.
- Siqueira E, Schoen RE, Silverman W, Martin J, Rabinovitz M, Weissfeld JL, Abu-Elmaagd K, Madariaga JR, Slivka A, Martini J (июль 2002 г.). «Выявление холангиокарциномы у больных первичным склерозирующим холангитом». Эндоскопия желудочно-кишечного тракта. 56 (1): 40–7. Дои:10.1067 / mge.2002.125105. PMID 12085033.
- Леви К., Лимп Дж., Ангуло П., Горс Дж. Дж., Ларуссо Н., Линдор К. Д. (сентябрь 2005 г.). «Значение сывороточного CA 19-9 в прогнозировании холангиокарцином у пациентов с первичным склерозирующим холангитом». Пищеварительные заболевания и науки. 50 (9): 1734–40. Дои:10.1007 / s10620-005-2927-8. PMID 16133981.
- Патель А.Х., Харнуа Д.М., Клее Г.Г., ЛаРуссо Н.Ф., Горс Г.Дж. (январь 2000 г.). «Полезность CA 19-9 в диагностике холангиокарциномы у пациентов без первичного склерозирующего холангита». Американский журнал гастроэнтерологии. 95 (1): 204–7. PMID 10638584.
- ^ Сайни С. (июнь 1997 г.). «Визуализация гепатобилиарного тракта». Медицинский журнал Новой Англии. 336 (26): 1889–94. Дои:10.1056 / NEJM199706263362607. PMID 9197218.
- ^ Шарма MP, Ахуджа V (1999). «Этиологический спектр механической желтухи и диагностические возможности ультразвукового исследования: взгляд клинициста». Тропическая гастроэнтерология. 20 (4): 167–9. PMID 10769604.
- ^ Блум С.М., Лангер Б., Уилсон С.Р. (1999). «Роль УЗИ в обнаружении, характеристике и постановке холангиокарциномы». Радиография. 19 (5): 1199–218. Дои:10.1148 / радиография.19.5.g99se081199. PMID 10489176.
- ^ Valls C, Gumà A, Puig I, Sanchez A, Andía E, Serrano T, Figueras J (2000). «Внутрипеченочная периферическая холангиокарцинома: оценка КТ». Визуализация брюшной полости. 25 (5): 490–6. Дои:10.1007 / s002610000079. PMID 10931983.
- ^ Тиллих М., Мишингер Х. Дж., Прайсеггер К. Х., Рабл Х., Солар Д. Х. (сентябрь 1998 г.) «Многофазная спиральная компьютерная томография в диагностике и стадировании внутригрудной холангиокарциномы». AJR. Американский журнал рентгенологии. 171 (3): 651–8. Дои:10.2214 / ajr.171.3.9725291. PMID 9725291.
- ^ Чжан Ю., Учида М., Абэ Т., Нисимура Н., Хаябучи Н., Накашима Ю. (1999). «Внутрипеченочная периферическая холангиокарцинома: сравнение динамической КТ и динамической МРТ». Журнал компьютерной томографии. 23 (5): 670–7. Дои:10.1097/00004728-199909000-00004. PMID 10524843.
- ^ Сугияма М, Хаги Х, Атоми Y, Сайто М (1997). «Диагностика инвазии воротной вены панкреатобилиарной карциномой: значение эндоскопической ультрасонографии». Визуализация брюшной полости. 22 (4): 434–8. Дои:10.1007 / s002619900227. PMID 9157867.
- ^ Schwartz LH, Coakley FV, Sun Y, Blumgart LH, Fong Y, Panicek DM (июнь 1998 г.). «Неопластическая обструкция панкреатобилиарного протока: оценка с помощью МР-холангиопанкреатографии с задержкой дыхания». AJR. Американский журнал рентгенологии. 170 (6): 1491–5. Дои:10.2214 / ajr.170.6.9609160. PMID 9609160.
- ^ Zidi SH, Prat F, Le Guen O, Rondeau Y, Pelletier G (январь 2000 г.). «Характеристики эффективности магнитно-резонансной холангиографии при стадировании злокачественных стриктур корней легких». Кишечник. 46 (1): 103–6. Дои:10.1136 / гут.46.1.103. ЧВК 1727781. PMID 10601064.
- ^ Ли М.Г., Пак КБ, Шин Ю.М., Юн Х.К., Сун КБ, Ким М.Х., Ли С.Г., Кан Э.М. (март 2003 г.). «Предоперационная оценка холангиокарциномы корня грудной клетки с помощью трехмерной быстрой визуализации с контрастированием и стационарной прецессионной магнитно-резонансной ангиографии: сравнение с внутриартериальной цифровой субтракционной ангиографией». Всемирный журнал хирургии. 27 (3): 278–83. Дои:10.1007 / s00268-002-6701-1. PMID 12607051.
- ^ Йе Т.С., Ян Й.Й., Ценг Дж.Х., Чиу К.Т., Чен Т.С., Хван Т.Л., Чен М.Ф. (февраль 2000 г.). «Злокачественная перихилярная билиарная непроходимость: результаты магнитно-резонансной холангиопанкреатографии». Американский журнал гастроэнтерологии. 95 (2): 432–40. PMID 10685746.
- ^ Фриман М.Л., Зилафф Т.Д. (2003). «Современный подход к лечению злокачественной обструкции прикорневых желчных путей». Отзывы в Гастроэнтерологические расстройства. 3 (4): 187–201. PMID 14668691.
- ^ Szklaruk J, Tamm E, Charnsangavej C (октябрь 2002 г.). «Предоперационная визуализация рака желчных путей». Клиники хирургической онкологии Северной Америки. 11 (4): 865–76. Дои:10.1016 / S1055-3207 (02) 00032-7. PMID 12607576.
- ^ Вебер С.М., ДеМаттео Р.П., Фонг Й., Блюмгарт Л.Х., Ярнагин В.Р. (март 2002 г.). «Стадирование лапароскопии у больных внепеченочной билиарной карциномой. Анализ 100 пациентов». Анналы хирургии. 235 (3): 392–9. Дои:10.1097/00000658-200203000-00011. ЧВК 1422445. PMID 11882761.
- ^ Callery MP, Strasberg SM, Doherty GM, Soper NJ, Norton JA (июль 1997 г.). «Стадия лапароскопии с лапароскопической ультрасонографией: оптимизация резектабельности при злокачественных опухолях гепатобилиарной и поджелудочной железы». Журнал Американского колледжа хирургов. 185 (1): 33–9. Дои:10.1016 / с 1072-7515 (97) 00003-3. PMID 9208958.
- ^ Länger F, von Wasielewski R, Kreipe HH (июль 2006 г.). «[Важность иммуногистохимии для диагностики холангиокарциномы]». Der Pathologe (на немецком). 27 (4): 244–50. Дои:10.1007 / s00292-006-0836-z. PMID 16758167.
- ^ Дарвин PE, Кеннеди А. Холангиокарцинома в eMedicine
- ^ Зервос Е.Е., Осборн Д., Голдин С.Б., Вилладолид Д.В., Томец Д.П., Дуркин А., Кэри Л.С., Rosemurgy AS (ноябрь 2005 г.). «Стадия не позволяет прогнозировать выживаемость после резекции холангиокарциномы корня зуба, что способствует агрессивному оперативному вмешательству». Американский журнал хирургии. 190 (5): 810–5. Дои:10.1016 / j.amjsurg.2005.07.025. PMID 16226963.
- ^ Цао Джи, Нимура Й., Камия Дж., Хаякава Н., Кондо С., Нагино М., Миячи М., Канаи М., Уэсака К., Ода К., Росси Р. Л., Брааш Дж. В., Дуган Дж. М. (август 2000 г.). «Лечение внутригрудной холангиокарциномы: сравнение опыта американцев и японцев». Анналы хирургии. 232 (2): 166–74. Дои:10.1097/00000658-200008000-00003. ЧВК 1421125. PMID 10903592.
- ^ Раджагопалан В., Дайнес В.П., Гроссбард М.Л., Козуч П. (июнь 2004 г.). «Карцинома желчного пузыря и желчных путей: подробное обновление, часть 1». Онкология. 18 (7): 889–96. PMID 15255172.
- ^ Su CH, Tsay SH, Wu CC, Shyr YM, King KL, Lee CH, Lui WY, Liu TJ, P'eng FK (апрель 1996 г.). «Факторы, влияющие на послеоперационную заболеваемость, смертность и выживаемость после резекции по поводу внутригрудной холангиокарциномы». Анналы хирургии. 223 (4): 384–94. Дои:10.1097/00000658-199604000-00007. ЧВК 1235134. PMID 8633917.
- ^ Розен CB, Heimbach JK, Gores GJ (2008). «Хирургия холангиокарциномы: роль трансплантации печени». Е.П.Б.. 10 (3): 186–9. Дои:10.1080/13651820801992542. ЧВК 2504373. PMID 18773052.
- ^ Heimbach JK, Gores GJ, Haddock MG, Alberts SR, Pedersen R, Kremers W., Nyberg SL, Ishitani MB, Rosen CB (декабрь 2006 г.). «Предикторы рецидива заболевания после неоадъювантной химиолучевой терапии и трансплантации печени по поводу неоперабельной перихилярной холангиокарциномы». Трансплантация. 82 (12): 1703–7. Дои:10.1097 / 01.tp.0000253551.43583.d1. PMID 17198263.
- ^ Kuhlmann JB, Blum HE (май 2013 г.). «Локорегиональная терапия холангиокарциномы». Текущее мнение в гастроэнтерологии. 29 (3): 324–8. Дои:10.1097 / MOG.0b013e32835d9dea. PMID 23337933.
- ^ Тодороки Т., Охара К., Кавамото Т., Коике Н., Йошида С., Касиваги Х., Оцука М., Фукао К. (февраль 2000 г.). «Преимущества адъювантной лучевой терапии после радикальной резекции местнораспространенной карциномы магистрального протока печени». Международный журнал радиационной онкологии, биологии, физики. 46 (3): 581–7. Дои:10.1016 / S0360-3016 (99) 00472-1. PMID 10701737.
- ^ Олден М.Э., Мохиуддин М. (март 1994 г.). «Влияние дозы облучения при комбинированной дистанционной лучевой и внутрипросветной брахитерапии Ir-192 при раке желчных протоков». Международный журнал радиационной онкологии, биологии, физики. 28 (4): 945–51. Дои:10.1016/0360-3016(94)90115-5. PMID 8138448.
- ^ Гонсалес Гонсалес Д., Гума Д. Д., Раус Е. А., ван Гулик Т. М., Босма А., Коедудер С. (1999). «Роль лучевой терапии, в частности внутрипросветной брахитерапии, в лечении рака проксимального желчного протока». Анналы онкологии. 10 Дополнение 4 (Suppl 4): 215–20. Дои:10.1023 / А: 1008339709327. PMID 10436826.
- ^ Питт Х.А., Накиб А., Абрамс Р.А., Коулман Дж., Пиантадози С., Йео С.Дж., Лиллемор К.Д., Кэмерон Дж. Л. (июнь 1995 г.). «Перихилярная холангиокарцинома. Послеоперационная лучевая терапия не улучшает выживаемость». Анналы хирургии. 221 (6): 788–97, обсуждение 797–8. Дои:10.1097/00000658-199506000-00017. ЧВК 1234714. PMID 7794082.
- ^ Такада Т, Амано Х, Ясуда Х, Нимура Й, Мацусиро Т, Като Х, Нагакава Т, Накаяма Т (октябрь 2002 г.). «Полезна ли послеоперационная адъювантная химиотерапия при карциноме желчного пузыря? Многоцентровое проспективное рандомизированное контролируемое исследование III фазы у пациентов с резекцией панкреатобилиарной карциномы». Рак. 95 (8): 1685–95. Дои:10.1002 / cncr.10831. PMID 12365016.
- ^ а б «Руководство Национальной комплексной онкологической сети (NCCN) по оценке и лечению злокачественных опухолей гепатобилиарной системы» (PDF). (216 КБ). Проверено 13 марта 2007 года.
- ^ а б Воти Дж. Н., Блюмгарт Л. Х. (май 1994 г.). «Последние достижения в лечении холангиокарцином». Семинары по заболеванию печени. 14 (2): 109–14. Дои:10.1055 / с-2007-1007302. PMID 8047893.
- ^ Глимелиус Б., Хоффман К., Сьёден П.О., Якобссон Г., Селлстрём Х., Энандер Л.К., Линне Т., Свенссон С. (август 1996 г.). «Химиотерапия улучшает выживаемость и качество жизни при запущенном раке поджелудочной железы и желчных путей». Анналы онкологии. 7 (6): 593–600. Дои:10.1093 / oxfordjournals.annonc.a010676. PMID 8879373.
- ^ Choi CW, Choi IK, Seo JH, Kim BS, Kim JS, Kim CD, Um SH, Kim JS, Kim YH (август 2000 г.). «Эффекты 5-фторурацила и лейковорина при лечении аденокарциномы поджелудочной железы и желчных путей». Американский журнал клинической онкологии. 23 (4): 425–8. Дои:10.1097/00000421-200008000-00023. PMID 10955877.
- ^ Park JS, Oh SY, Kim SH, Kwon HC, Kim JS, Jin-Kim H, Kim YH (февраль 2005 г.). "Single-agent gemcitabine in the treatment of advanced biliary tract cancers: a phase II study". Японский журнал клинической онкологии. 35 (2): 68–73. Дои:10.1093/jjco/hyi021. PMID 15709089.
- ^ Giuliani F, Gebbia V, Maiello E, Borsellino N, Bajardi E, Colucci G (June 2006). "Gemcitabine and cisplatin for inoperable and/or metastatic biliary tree carcinomas: a multicenter phase II study of the Gruppo Oncologico dell'Italia Meridionale (GOIM)". Анналы онкологии. 17 Suppl 7 (Suppl 7): vii73–7. Дои:10.1093/annonc/mdl956. PMID 16760299.
- ^ Bhargava P, Jani CR, Savarese DM, O'Donnell JL, Stuart KE, Rocha Lima CM (September 2003). "Gemcitabine and irinotecan in locally advanced or metastatic biliary cancer: preliminary report". Онкология. 17 (9 Suppl 8): 23–6. PMID 14569844.
- ^ Knox JJ, Hedley D, Oza A, Feld R, Siu LL, Chen E, Nematollahi M, Pond GR, Zhang J, Moore MJ (April 2005). "Combining gemcitabine and capecitabine in patients with advanced biliary cancer: a phase II trial". Журнал клинической онкологии. 23 (10): 2332–8. Дои:10.1200/JCO.2005.51.008. PMID 15800324.
- ^ Philip PA, Mahoney MR, Allmer C, Thomas J, Pitot HC, Kim G, Donehower RC, Fitch T, Picus J, Erlichman C (July 2006). "Phase II study of erlotinib in patients with advanced biliary cancer". Журнал клинической онкологии. 24 (19): 3069–74. Дои:10.1200/JCO.2005.05.3579. PMID 16809731.
- ^ Bonet Beltrán M, Allal AS, Gich I, et al. (2012). "Is adjuvant radiotherapy needed after curative resection of extrahepatic biliary tract cancers? A systematic review with a meta-analysis of observational studies". Cancer Treat Rev. 38 (2): 111–119. Дои:10.1016/j.ctrv.2011.05.003. PMID 21652148.
- ^ Bridgewater JA, Goodman KA, Kalyan A, Mulcahy MF (2016). "Biliary Tract Cancer: Epidemiology, Radiotherapy, and Molecular Profiling". Учебное пособие Американского общества клинической онкологии. 36 (36): e194–e203. Дои:10.1200/EDBK_160831. PMID 27249723.
- ^ Yamamoto M, Takasaki K, Yoshikawa T (March 1999). "Lymph node metastasis in intrahepatic cholangiocarcinoma". Японский журнал клинической онкологии. 29 (3): 147–50. Дои:10.1093/jjco/29.3.147. PMID 10225697.
- ^ Farley DR, Weaver AL, Nagorney DM (May 1995). "'Natural history' of unresected cholangiocarcinoma: patient outcome after noncurative intervention". Труды клиники Мэйо. 70 (5): 425–9. Дои:10.4065/70.5.425. PMID 7537346.
- ^ Grove MK, Hermann RE, Vogt DP, Broughan TA (April 1991). "Role of radiation after operative palliation in cancer of the proximal bile ducts". Американский журнал хирургии. 161 (4): 454–8. Дои:10.1016/0002-9610(91)91111-U. PMID 1709795.
- ^ Studies of surgical outcomes in distal cholangiocarcinoma include:
- Nakeeb A, Pitt HA, Sohn TA, Coleman J, Abrams RA, Piantadosi S, Hruban RH, Lillemoe KD, Yeo CJ, Cameron JL (October 1996). "Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors". Анналы хирургии. 224 (4): 463–73, discussion 473–5. Дои:10.1097/00000658-199610000-00005. ЧВК 1235406. PMID 8857851.
- Jang JY, Kim SW, Park DJ, Ahn YJ, Yoon YS, Choi MG, Suh KS, Lee KU, Park YH (January 2005). "Actual long-term outcome of extrahepatic bile duct cancer after surgical resection". Анналы хирургии. 241 (1): 77–84. Дои:10.1097/01.sla.0000150166.94732.88. ЧВК 1356849. PMID 15621994.
- Bortolasi L, Burgart LJ, Tsiotos GG, Luque-De León E, Sarr MG (2000). "Adenocarcinoma of the distal bile duct. A clinicopathologic outcome analysis after curative resection". Пищеварительная хирургия. 17 (1): 36–41. Дои:10.1159/000018798. PMID 10720830.
- Fong Y, Blumgart LH, Lin E, Fortner JG, Brennan MF (December 1996). "Outcome of treatment for distal bile duct cancer". British Journal of Surgery. 83 (12): 1712–5. Дои:10.1002/bjs.1800831217. PMID 9038548.
- ^ Studies of outcome in intrahepatic cholangiocarcinoma include:
- Nakeeb A, Pitt HA, Sohn TA, Coleman J, Abrams RA, Piantadosi S, Hruban RH, Lillemoe KD, Yeo CJ, Cameron JL (October 1996). "Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors". Анналы хирургии. 224 (4): 463–73, discussion 473–5. Дои:10.1097/00000658-199610000-00005. ЧВК 1235406. PMID 8857851.
- Lieser MJ, Barry MK, Rowland C, Ilstrup DM, Nagorney DM (1998). "Surgical management of intrahepatic cholangiocarcinoma: a 31-year experience". Journal of Hepato-Biliary-Pancreatic Surgery. 5 (1): 41–7. Дои:10.1007/PL00009949. PMID 9683753.
- Valverde A, Bonhomme N, Farges O, Sauvanet A, Flejou JF, Belghiti J (1999). "Resection of intrahepatic cholangiocarcinoma: a Western experience". Journal of Hepato-Biliary-Pancreatic Surgery. 6 (2): 122–7. Дои:10.1007/s005340050094. PMID 10398898.
- Nakagohri T, Asano T, Kinoshita H, Kenmochi T, Urashima T, Miura F, Ochiai T (March 2003). "Aggressive surgical resection for hilar-invasive and peripheral intrahepatic cholangiocarcinoma". World Journal of Surgery. 27 (3): 289–93. Дои:10.1007/s00268-002-6696-7. PMID 12607053.
- Weber SM, Jarnagin WR, Klimstra D, DeMatteo RP, Fong Y, Blumgart LH (October 2001). "Intrahepatic cholangiocarcinoma: resectability, recurrence pattern, and outcomes". Journal of the American College of Surgeons. 193 (4): 384–91. Дои:10.1016/S1072-7515(01)01016-X. PMID 11584966.
- ^ Estimates of survival after surgery for perihilar cholangiocarcinoma include:
- Burke EC, Jarnagin WR, Hochwald SN, Pisters PW, Fong Y, Blumgart LH (September 1998). "Hilar Cholangiocarcinoma: patterns of spread, the importance of hepatic resection for curative operation, and a presurgical clinical staging system". Анналы хирургии. 228 (3): 385–94. Дои:10.1097/00000658-199809000-00011. ЧВК 1191497. PMID 9742921.
- Tsao JI, Nimura Y, Kamiya J, Hayakawa N, Kondo S, Nagino M, Miyachi M, Kanai M, Uesaka K, Oda K, Rossi RL, Braasch JW, Dugan JM (August 2000). "Management of hilar cholangiocarcinoma: comparison of an American and a Japanese experience". Анналы хирургии. 232 (2): 166–74. Дои:10.1097/00000658-200008000-00003. ЧВК 1421125. PMID 10903592.
- Chamberlain RS, Blumgart LH (2000). "Hilar cholangiocarcinoma: a review and commentary". Анналы хирургической онкологии. 7 (1): 55–66. Дои:10.1007/s10434-000-0055-4. PMID 10674450.
- Washburn WK, Lewis WD, Jenkins RL (March 1995). "Aggressive surgical resection for cholangiocarcinoma". Архив хирургии. 130 (3): 270–6. Дои:10.1001/archsurg.1995.01430030040006. PMID 7534059.
- Nagino M, Nimura Y, Kamiya J, Kanai M, Uesaka K, Hayakawa N, Yamamoto H, Kondo S, Nishio H (1998). "Segmental liver resections for hilar cholangiocarcinoma". Hepato-Gastroenterology. 45 (19): 7–13. PMID 9496478.
- Rea DJ, Munoz-Juarez M, Farnell MB, Donohue JH, Que FG, Crownhart B, Larson D, Nagorney DM (May 2004). "Major hepatic resection for hilar cholangiocarcinoma: analysis of 46 patients". Архив хирургии. 139 (5): 514–23, discussion 523–5. Дои:10.1001/archsurg.139.5.514. PMID 15136352.
- Launois B, Reding R, Lebeau G, Buard JL (2000). "Surgery for hilar cholangiocarcinoma: French experience in a collective survey of 552 extrahepatic bile duct cancers". Journal of Hepato-Biliary-Pancreatic Surgery. 7 (2): 128–34. Дои:10.1007/s005340050166. PMID 10982604.
- ^ Kaya M, de Groen PC, Angulo P, Nagorney DM, Gunderson LL, Gores GJ, Haddock MG, Lindor KD (April 2001). "Treatment of cholangiocarcinoma complicating primary sclerosing cholangitis: the Mayo Clinic experience". Американский журнал гастроэнтерологии. 96 (4): 1164–9. PMID 11316165.
- ^ Nakeeb A, Tran KQ, Black MJ, Erickson BA, Ritch PS, Quebbeman EJ, Wilson SD, Demeure MJ, Rilling WS, Dua KS, Pitt HA (October 2002). "Improved survival in resected biliary malignancies". Хирургия. 132 (4): 555–63, discission 563–4. Дои:10.1067/msy.2002.127555. PMID 12407338.
- ^ Khan SA, Taylor-Robinson SD, Toledano MB, Beck A, Elliott P, Thomas HC (December 2002). "Changing international trends in mortality rates for liver, biliary and pancreatic tumours". Журнал гепатологии. 37 (6): 806–13. Дои:10.1016/S0168-8278(02)00297-0. PMID 12445422.
- ^ Table 37.2 в: Sternberg, Stephen (2012). Диагностическая хирургическая патология Штернберга. Place of publication not identified: LWW. ISBN 978-1-4511-5289-0. OCLC 953861627.CS1 maint: ref = harv (связь)
- ^ Landis SH, Murray T, Bolden S, Wingo PA (1998). "Cancer statistics, 1998". Ca. 48 (1): 6–29. Дои:10.3322/canjclin.48.1.6. PMID 9449931.
- ^ Cancer Statistics Home Page — National Cancer Institute
- ^ Multiple independent studies have documented a steady increase in the worldwide incidence of cholangiocarcinoma. Some relevant journal articles include:
- Patel T (May 2002). "Worldwide trends in mortality from biliary tract malignancies". BMC Cancer. 2: 10. Дои:10.1186/1471-2407-2-10. ЧВК 113759. PMID 11991810.
- Patel T (June 2001). "Increasing incidence and mortality of primary intrahepatic cholangiocarcinoma in the United States". Гепатология. 33 (6): 1353–7. Дои:10.1053/jhep.2001.25087. PMID 11391522.
- Shaib YH, Davila JA, McGlynn K, El-Serag HB (March 2004). "Rising incidence of intrahepatic cholangiocarcinoma in the United States: a true increase?". Журнал гепатологии. 40 (3): 472–7. Дои:10.1016/j.jhep.2003.11.030. PMID 15123362.
- West J, Wood H, Logan RF, Quinn M, Aithal GP (June 2006). "Trends in the incidence of primary liver and biliary tract cancers in England and Wales 1971-2001". British Journal of Cancer. 94 (11): 1751–8. Дои:10.1038/sj.bjc.6603127. ЧВК 2361300. PMID 16736026.
- Khan SA, Taylor-Robinson SD, Toledano MB, Beck A, Elliott P, Thomas HC (December 2002). "Changing international trends in mortality rates for liver, biliary and pancreatic tumours". Журнал гепатологии. 37 (6): 806–13. Дои:10.1016/S0168-8278(02)00297-0. PMID 12445422.
- Welzel TM, McGlynn KA, Hsing AW, O'Brien TR, Pfeiffer RM (June 2006). "Impact of classification of hilar cholangiocarcinomas (Klatskin tumors) on the incidence of intra- and extrahepatic cholangiocarcinoma in the United States". Журнал Национального института рака. 98 (12): 873–5. Дои:10.1093/jnci/djj234. PMID 16788161.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
| Схолия имеет тема профиль для Холангиокарцинома. |
