Цвет химикатов - Color of chemicals
В цвет химикатов это физическая собственность химических веществ, которые в большинстве случаев поступают из возбуждение электронов из-за поглощения энергии химическим веществом. Глаз видит не поглощенный цвет, а дополнительный цвет от удаления абсорбированного длины волн. Эта спектральная перспектива впервые была отмечена в атомная спектроскопия.
Изучение химической структуры посредством поглощения и высвобождения энергии обычно называют спектроскопия.
Теория
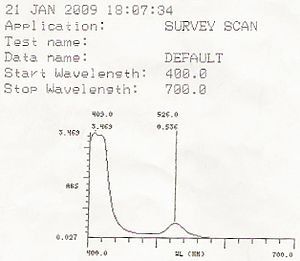
Все атомы и молекулы способны поглощать и выделять энергию в виде фотоны, сопровождающееся изменением квантового состояния. Количество поглощенной или высвобожденной энергии - это разница между энергиями двух квантовых состояний. Существуют различные типы квантовых состояний, включая, например, вращательные и колебательные состояния молекулы. Однако выделение видимой человеческим глазом энергии, обычно называемой видимым светом, охватывает длины волн приблизительно от 380 нм до 760 нм, в зависимости от человека, и фотоны в этом диапазоне обычно сопровождают изменение атомный или же молекулярная орбиталь квантовое состояние. Восприятие света регулируется тремя типами цвет рецепторы в глазу, которые чувствительны к разным диапазонам длин волн в этом диапазоне.
Связь между энергией и длиной волны определяется Соотношение Планка-Эйнштейна:
куда E это энергия квант (фотон ), ж это частота световой волны, час является Постоянная Планка, λ это длина волны и c это скорость света.
Отношения между энергиями различных квантовых состояний рассматриваются как атомная орбиталь, молекулярная орбиталь, Теория поля лигандов и Теория кристаллического поля. Если фотоны определенной длины волны поглощаются веществом, тогда, когда мы наблюдаем свет, отраженный от этого вещества или проходящий через него, мы видим дополнительный цвет, состоящий из оставшихся длин волн видимого диапазона. Например, бета-каротин имеет максимальное поглощение при 454 нм (синий свет), следовательно, то, что остается видимым светом, кажется оранжевым.
Цвета по длине волны
Ниже представлена приблизительная таблица длин волн, цветов и дополнительных цветов. Это использует научные CMY и RGB цветные колеса а не традиционный RYB цветовой круг.[1]
| Длина волны (нм) | Цвет | Дополнительный цвет | ||
|---|---|---|---|---|
| 400–424 | фиолетовый | Желтый | ||
| 424–491 | Синий | апельсин | ||
| 491–570 | Зеленый | красный | ||
| 570–585 | Желтый | фиолетовый | ||
| 585–647 | апельсин | Синий | ||
| 647–700 | красный | Зеленый | ||
Это можно использовать только в качестве очень приблизительного ориентира, например, если поглощается узкий диапазон длин волн в диапазоне 647-700, тогда синие и зеленые рецепторы будут полностью стимулироваться, делая голубой, а красный рецептор будет частично стимулироваться. , разбавляя голубой до сероватого оттенка.
По категории
Подавляющее большинство простых неорганических (например, хлорид натрия ) и органические соединения (например, этанол) бесцветны. Переходный металл соединения часто окрашиваются из-за переходов электронов между d-орбитали разной энергии. (видеть Переходный металл # Цветные соединения ). Органические соединения имеют тенденцию к окрашиванию при большом количестве спряжение, вызывая энергетический разрыв между HOMO и LUMO уменьшаться, переводя полосу поглощения из УФ в видимую область. Точно так же цвет возникает из-за энергии, поглощаемой соединением, когда электрон переходит от ВЗМО к НСМО. Ликопин является классическим примером соединения с обширной конъюгацией (11 конъюгированных двойных связей), приводящей к интенсивному красному цвету (ликопин отвечает за цвет помидоры ). Зарядно-передающие комплексы имеют тенденцию к очень насыщенным цветам по разным причинам.
Примеры
| Имя | Формула | Цвет | |
|---|---|---|---|
| Щелочноземельные металлы | M2+ | Бесцветный | |
| Скандий (III) | Sc3+ | Бесцветный | |
| Титан (III) | Ti3+ | фиолетовый | |
| Титан (IV) | Ti4+ | Бесцветный | |
| Титанил | TiO2+ | Бесцветный | |
| Ванадий (II) | V2+ | Лаванда | |
| Ванадий (III) | V3+ | Темно-серо-зеленый | |
| Ванадил (IV) | VO2+ | Синий | |
| Ванадий (IV) (ванадит ) | V 4О2− 9 | коричневый | |
| Ванадий (V) (перванадил ) | VO+ 2 | Желтый | |
| Метаванадат | VO− 3 | Бесцветный | |
| Ортованадат | VO3− 4 | Бесцветный | |
| Хром (II) | Cr2+ | Ярко-голубой | |
| Хром (III) | Cr3+ | Сине-зелено-серый | |
| Сульфат хрома (III) | CrSO4+ | Темно-зеленый | |
| Гидроксид хрома (III) | Cr (ОН)63− | желтоватый | |
| Монохромат | CrO2− 4 | Желтый | |
| Дихромат | Cr 2О2− 7 | апельсин | |
| Марганец (II) | Mn2+ | Бледно-розовый | |
| Марганец (III) | Mn3+ | малиновый цвет | |
| Манганат (V) | MnO3− 4 | Темно-синий | |
| Манганат (VI) | MnO2− 4 | Темно-зеленый | |
| Манганат (VII) (перманганат ) | MnO− 4 | Темно-фиолетовый | |
| Сульфат железа (II) | Fe2+ | Очень бледно-зеленый | |
| Оксид-гидроксид железа (III) | FeO (ОН) | Темно коричневый | |
| Тетрахлор комплекс железа (III) | FeCl− 4 | Желтый / коричневый | |
| Фторид кобальта (II) | Co2+ | Розовый | |
| Кобальт (III) амминный комплекс | Co (NH 3)3+ 6 | Желтый / оранжевый | |
| Никель (II) | Ni2+ | Светло-зеленый | |
| Никель (II) амминный комплекс | Ni (NH 3)2+ 6 | Лаванда / синий | |
| Медный (I) амминный комплекс | Cu (NH 3)+ 2 | Бесцветный | |
| Медь (II) | Cu2+ | Синий | |
| Комплекс аммина меди (II) | Cu (NH 3)2+ 4 | Индиго синий | |
| Тетрахлор комплекс меди (II) | CuCl2− 4 | Зеленый | |
| Цинк (II) | Zn2+ | Бесцветный | |
| Серебро (I) | Ag+ | Бесцветный | |
| Серебро (III) в конц. HNO3 | Ag3+ | Темно коричневый | |
Однако важно отметить, что цвета элементов будут варьироваться в зависимости от того, с чем они входят в комплекс, а также от их химического состояния. Пример с ванадием (III); VCl3 имеет характерный красноватый оттенок, тогда как V2О3 кажется черным.
Соли
Предсказать цвет соединения может быть чрезвычайно сложно. Вот некоторые примеры:
- Хлорид кобальта бывает розового или синего цвета в зависимости от степени гидратации (синий сухой, розовый от воды), поэтому он используется в качестве индикатора влажности в силикагеле.
- Оксид цинка имеет белый цвет, но при более высоких температурах становится желтым, а по мере охлаждения становится белым.
| Имя | Формула соответствующих солей | Цвет | Рисунок |
|---|---|---|---|
| Гидроксид хрома (III) | Cr (ОН)3 | Зеленый | |
| Сульфат меди (II) (безводный) | CuSO4 | белый |  |
| Пентагидрат сульфата меди (II) | CuSO4· 5H2О | Синий |  |
| Бензоат меди (II) | Cu (C7ЧАС5О2)2 | Синий |  |
| Хлорид кобальта (II) | CoCl2 | Темно-синий |  |
| Гексагидрат хлорида кобальта (II) | CoCl2· 6H2О | Темно-пурпурный |  |
| Хлорид марганца (II) тетрагидрат | MnCl2· 4H2О | Розовый |  |
| Хлорид меди (II) дигидрат | CuCl2· 2H2О | Цвет морской волны |  |
| Никель (II) хлорид гексагидрат | NiCl2· 6H2О | Зеленый |  |
| Иодид свинца (II) | PbI2 | Желтый |
Ионы в пламени
| Имя | Формула | Цвет | |
|---|---|---|---|
| Литий | Ли | красный | |
| Натрий | Na | Желтый / оранжевый | |
| Магний | Mg | Блестящий белый | |
| Калий | K | Сиреневый / фиолетовый | |
| Кальций | Ca | Красный кирпич | |
| Рубидий | Руб. | Розовый / красный | |
| Стронций | Sr | красный | |
| Цезий | CS | Светло-синий | |
| Барий | Ба | Желто-зеленый | |
| Медь | Cu | Синий / зеленый (часто с белыми вспышками) | |
| Свинец | Pb | Серый / белый | |
Газы
| Имя | Формула | Цвет | |
|---|---|---|---|
| Водород | ЧАС2 | бесцветный | |
| Кислород | О2 | бесцветный | |
| Озон | О3 | очень бледно-голубой | |
| Фтор | F2 | очень бледно-желтый / коричневый | |
| Хлор | Cl2 | зеленовато-желтый | |
| Бром | Br2 | красно-коричневый | |
| Йод | я2 | темно фиолетовый | |
| Диоксид хлора | ClO2 | интенсивно-желтый | |
| Монооксид дихлора | Cl2О | коричневый / желтый | |
| Диоксид азота | НЕТ2 | темно коричневый | |
| Трифторнитрозометан | CF3НЕТ | темно-синий | |
| Диазометан | CH2N2 | желтый | |
Бисерные тесты
При испытании шариков, которое является качественным испытанием для определения металлов, получают различные цвета, часто похожие на цвета, обнаруженные при испытании на пламя. А платиновая петля увлажняется и окунается в мелкий порошок рассматриваемого вещества и бура. Затем петлю с налипшими порошками нагревают в пламени до тех пор, пока она не расплавится, и не будет наблюдаться цвет полученного шарика.
| Металл[3] | Окислительное пламя | Уменьшение пламени |
|---|---|---|
| Алюминий | бесцветный (горячий и холодный), непрозрачный | бесцветный, непрозрачный |
| Сурьма | бесцветный, желтый или коричневый (горячий) | серый и непрозрачный |
| Барий | бесцветный | |
| Висмут | бесцветный, желтый или коричневатый (горячий) | серый и непрозрачный |
| Кадмий | бесцветный | серый и непрозрачный |
| Кальций | бесцветный | |
| Церий | красный (горячий) | бесцветный (горячий и холодный) |
| Хром | Темно-желтый (горячий), зеленый (холодный) | зеленый (горячий и холодный) |
| Кобальт | синий (горячий и холодный) | синий (горячий и холодный) |
| Медь | зеленый (горячий), синий (холодный) | красный, непрозрачный (холодный), бесцветный (горячий) |
| Золото | золотой (горячий), серебряный (холодный) | красный (горячий и холодный) |
| Утюг | желтый или коричневато-красный (горячий и холодный) | зеленый (горячий и холодный) |
| Свинец | бесцветный, желтый или коричневатый (горячий) | серый и непрозрачный |
| Магний | бесцветный | |
| Марганец | фиолетовый (горячий и холодный) | бесцветный (горячий и холодный) |
| Молибден | бесцветный | желтый или коричневый (горячий) |
| Никель | коричневый, красный (холодный) | серый и непрозрачный (холодный) |
| Кремний | бесцветный (горячий и холодный), непрозрачный | бесцветный, непрозрачный |
| Серебро | бесцветный | серый и непрозрачный |
| Стронций | бесцветный | |
| Банка | бесцветный (горячий и холодный), непрозрачный | бесцветный, непрозрачный |
| Титан | бесцветный | желтый (горячий), фиолетовый (холодный) |
| Вольфрам | бесцветный | коричневый |
| Уран | Желтый или коричневатый (горячий) | зеленый |
| Ванадий | бесцветный | зеленый |
Рекомендации
- ^ http://www.sapdesignguild.org/resources/glossary_color/index1.html
- ^ Испытания на пламя на Chemguide.co.uk
- ^ CRC Справочник по химии и физике. CRC Press. 1985 г. ISBN 0-8493-0466-0.


