Катехоламин - Catecholamine

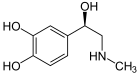
А катехоламин (/ˌkæтəˈkoʊлəмяп/; сокращенный CA) это моноаминный нейромедиатор, органическое соединение что есть катехол (бензол с двумя гидроксил боковые группы рядом друг с другом) и боковая цепь амин.[1]
Катехол может быть либо свободной молекулой, либо заместитель более крупной молекулы, где он представляет собой 1,2-дигидроксибензольную группу.
Катехоламины являются производными аминокислота тирозин, который получают из пищевых источников, а также синтезируют из фенилаланин.[2] Катехоламины водорастворимы и на 50% связаны с белками плазмы крови в кровотоке.
В число катехоламинов входят: адреналин (адреналин), норэпинефрин (норадреналин) и дофамин. Выпуск гормоны адреналин и норэпинефрин от мозговое вещество надпочечников из надпочечники является частью борьба или бегство.[3]
Тирозин создается из фенилаланина гидроксилирование ферментом фенилаланингидроксилаза. Тирозин также поступает напрямую из пищевого белка. Клетки, секретирующие катехоламин, используют несколько реакций для последовательного преобразования тирозина в L-ДОПА а затем дофамина. В зависимости от типа клеток дофамин может далее преобразовываться в норэпинефрин или даже в адреналин.[4]
Различный стимулятор наркотики (например, ряд замещенные амфетамины ) являются аналогами катехоламинов.
Структура
Катехоламины имеют отчетливую структуру бензольное кольцо с двумя гидроксил группы, промежуточный этил цепь и терминал амин группа. Фенилэтаноламины, такие как норэпинефрин, имеют гидроксильную группу в этильной цепи.
Производство и деградация
L-Фенилаланин превращается в L-тирозин гидроксилаза ароматических аминокислот (AAAH) фермент (фенилаланин-4-гидроксилаза ), с молекулярной кислород (O2) и тетрагидробиоптерин так как кофакторы. L-Тирозин превращается в L-ДОПА другим ферментом AAAH (тирозин-3-гидроксилаза ) с участием тетрагидробиоптерин, O2, и железо утюг (Fe2+) как кофакторы. L-Дофа превращается в дофамин ферментом ароматный Lдекарбоксилаза аминокислот (AADC), с участием пиридоксальфосфат в качестве кофактора. Сам дофамин также используется в качестве прекурсора при синтезе нейромедиаторов. норэпинефрин и адреналин. Дофамин превращается в норэпинефрин ферментом дофамин-β-гидроксилаза (DBH), с O2 и L-аскорбиновая кислота как кофакторы. Норэпинефрин превращается в адреналин под действием фермента фенилэтаноламин N-метилтрансфераза (PNMT) с S-аденозил-L-метионин в качестве кофактора. |
Расположение
Катехоламины производятся в основном хромаффинные клетки из мозговое вещество надпочечников и постганглионарные волокна из Симпатическая нервная система. Дофамин, который действует как нейротрансмиттер в Центральная нервная система, в основном продуцируется телами нейронных клеток в двух областях ствола мозга: вентральная тегментальная область и черная субстанция, последний из которых содержит нейромеланин -пигментированные нейроны. Аналогично нейромеланин-пигментированные клеточные тела голубое пятно производить норэпинефрин. Адреналин вырабатывается небольшими группами нейронов головного мозга человека, которые экспрессируют его синтезирующий фермент, фенилэтаноламин N-метилтрансфераза;[8] эти нейроны выступают из ядра, которое прилегает (вентролатерально) к область пострема и от ядра в дорсальной области уединенный тракт.[8]
Биосинтез
Дофамин - первый катехоламин, синтезированный из ДОФА. В свою очередь, норэпинефрин и адреналин являются производными от дальнейшей метаболической модификации дофамина. Фермент дофамин гидроксилаза требует меди в качестве кофактор (не показано на схеме) и ДОФА декарбоксилаза требует PLP (не показано на схеме). Ограничивающей скорость стадией биосинтеза катехоламинов через преобладающий метаболический путь является гидроксилирование L-тирозин к L-ДОПА.
Синтез катехоламинов ингибируется альфа-метил-п-тирозин (AMPT ), что подавляет тирозингидроксилаза.[нужна цитата ]
Аминокислоты фенилаланин и тирозин являются предшественниками катехоламинов. Обе аминокислоты содержатся в высоких концентрациях в плазма крови и мозг. У млекопитающих тирозин может образовываться из пищевого фенилаланина с помощью фермента фенилаланингидроксилаза, в больших количествах содержится в печени. Недостаточное количество фенилаланингидроксилазы приводит к фенилкетонурия, нарушение обмена веществ, которое приводит к интеллектуальному дефициту, если не лечить диетическими манипуляциями.[нужна цитата ] Считается, что синтез катехоламинов начинается с тирозина. Фермент тирозингидроксилаза (TH) превращает аминокислоту L-тирозин в 3,4-дигидроксифенилаланин (L-ДОПА). Гидроксилирование L-тирозин под действием TH приводит к образованию предшественника DA L-ДОПА, который метаболизируется ароматный Lдекарбоксилаза аминокислот (AADC; см. Cooper et al., 2002[нужна цитата ]) к передатчику дофамина. Этот шаг происходит так быстро, что трудно измерить L-DOPA в головном мозге без предварительного подавления AADC.[нужна цитата ] В нейроны которые используют DA в качестве передатчика, декарбоксилирование L-ДОПА к дофамину - заключительный шаг в формировании передатчика; однако в тех нейронах, использующих норэпинефрин (норадреналин) или адреналин (адреналин) в качестве переносчиков, фермент дофамин-β-гидроксилаза (DBH), который превращает дофамин в норэпинефрин, также присутствует. В других нейронах, в которых адреналин является медиатором, третий фермент фенилэтаноламин N-метилтрансфераза (PNMT) превращает норэпинефрин в адреналин. Таким образом, клетка, которая использует адреналин в качестве своего передатчика, содержит четыре фермента (TH, AADC, DBH и PNMT), тогда как нейроны норэпинефрина содержат только три фермента (без PNMT), а клетки дофамина только два (TH и AADC).[нужна цитата ]
Деградация
Катехоламины при циркуляции в крови имеют период полураспада в несколько минут. Они могут быть разрушены метилированием катехолО-метилтрансферазы (COMT) или путем дезаминирования моноаминоксидазы (МАО).
MAOI связываются с МАО, тем самым предотвращая расщепление катехоламинов и других моноаминов.
Катаболизм катехоламинов опосредуется двумя основными ферментами: катехоламинов.О-метилтрансфераза (COMT), которая присутствует в синаптической щели и цитозоле клетки, и моноаминоксидаза (MAO), которая находится в митохондриальной мембране. Оба фермента требуют кофакторов: COMT использует Mg2+ в качестве кофактора, в то время как МАО использует FAD. Первый этап катаболического процесса опосредуется либо МАО, либо СОМТ, что зависит от ткани и местоположения катехоламинов (например, деградация катехоламинов в синаптической щели опосредуется СОМТ, поскольку МАО является митохондриальным ферментом). Следующие катаболические шаги на этом пути включают: алкогольдегидрогеназа, альдегиддегидрогеназа и альдегидредуктаза. Конечный продукт адреналина и норэпинефрина - ванилилминдальная кислота (ВМА) который выделяется в моча. Катаболизм дофамина приводит к образованию гомованиловая кислота (HVA).[9]
Функция
Модальность
Два катехоламина, норэпинефрин и дофамин, вести себя как нейромодуляторы в Центральная нервная система и как гормоны в кровообращении. Катехоламин норэпинефрин является нейромодулятором периферической симпатической нервной системы, но также присутствует в крови (в основном через «побочный эффект» от синапсы симпатической системы).
Высокий уровень катехоламинов в крови связан с: стресс, которые могут быть вызваны психологическими реакциями или факторами окружающей среды, такими как повышенный уровень звука, интенсивный свет, или низкий уровень сахара в крови.
Чрезвычайно высокий уровень катехоламинов (также известный как токсичность катехоламинов) может возникать в Центральная нервная система травма из-за стимуляции или повреждения ядра в мозговой ствол, в частности, ядра, влияющие на Симпатическая нервная система. В неотложная медицинская помощь, это явление широко известно как «свалка катехоламинов».
Чрезвычайно высокий уровень катехоламинов также может быть вызван: нейроэндокринные опухоли в мозговое вещество надпочечников, излечимое состояние, известное как феохромоцитома.
Высокий уровень катехоламинов также может быть вызван: моноаминоксидаза А (МАО-А) дефицит, известный как Синдром Бруннера. Поскольку МАО-А является одним из ферментов, ответственных за деградацию этих нейромедиаторов, его дефицит значительно увеличивает биодоступность этих нейротрансмиттеров. Это происходит при отсутствии феохромоцитома, нейроэндокринные опухоли, и карциноидный синдром, но он похож на карциноидный синдром с такими симптомами, как покраснение лица и агрессия.[10][11]
Острый порфирия может вызвать повышенный уровень катехоламинов.[12]
Эффекты
Катехоламины вызывают общие физиологические изменения, которые подготавливают организм к физической нагрузке ( борьба или бегство ). Некоторые типичные эффекты - увеличение частота сердцебиения, артериальное давление, глюкоза в крови уровней, и общая реакция Симпатическая нервная система.[нужна цитата ] Некоторые препараты, например толкапон (центральный COMT -ингибитор), повышают уровень всех катехоламинов.
Катехоламин выделяется с мочой после расщепления, и уровень его секреции можно измерить для диагностики заболеваний, связанных с уровнем катехоламинов в организме.[13] Анализ мочи катехоламин используется для обнаружения феохромоцитома.
Функция в растениях
«Они были обнаружены у 44 семейств растений, но у них не было установлено никакой важной метаболической функции. Они являются предшественниками бензо [c] фенантридин алкалоиды, которые являются основными активными ингредиентами многих лекарственное растение экстракты. Предполагается, что CA могут играть возможную защитную роль от насекомых-хищников, травм и детоксикации азота. Было показано, что они способствуют росту тканей растений, соматических эмбриогенез от культур in vitro и цветения. КА ингибируют индол-3-уксусная кислота окисление и усиление этилен биосинтез. Также было показано, что они синергетически усиливают различные эффекты гиббереллины."[14]
Тест на катехоламины
Катехоламины секретируются клетками тканей различных систем человеческого тела, в основном нервной и эндокринной системами. Надпочечники выделяют определенные катехоламины в кровь, когда человек находится в состоянии физического или психического стресса, и это обычно является здоровой физиологической реакцией.[15] Однако острый или хронический избыток циркулирующих катехоламинов может потенциально повысить кровяное давление и частоту сердечных сокращений до очень высоких уровней и в конечном итоге спровоцировать опасные эффекты. Тесты на фракционированную плазму бесплатно метанефрины или метанефрины в моче используются для подтверждения или исключения определенных заболеваний, когда врач определяет признаки гипертония и тахикардия которые не адекватно поддаются лечению.[16][17] Каждый из тестов измеряет количество метаболитов адреналина и норадреналина, соответственно называемых метанефрин и норметанефрин.
Также проводятся анализы крови для определения количества катехоламинов, присутствующих в организме.
Тесты на катехоламины проводятся для выявления редких опухолей надпочечников или нервной системы. Тесты на катехоламины предоставляют информацию относительно опухолей, таких как феокромоцитома, параганглиома и нейробластома.[18][19]
Смотрите также
использованная литература
- ^ Фитцджеральд, П. А. (2011). «Глава 11. Медулла и параганглии надпочечников». В Gardner, D. G .; Шобак Д. (ред.). Основы и клиническая эндокринология Гринспена (9-е изд.). Нью-Йорк: Макгроу-Хилл. Получено 26 октября, 2011.
- ^ Purves, D .; Августин, Г. Дж .; Фитцпатрик, Д .; Hall, W. C .; LaMantia, A. S .; McNamara, J. O .; Уайт, Л. Э., ред. (2008). Неврология (4-е изд.). Sinauer Associates. С. 137–138. ISBN 978-0-87893-697-7.
- ^ «Катехоламины». Библиотека здоровья. Сан-Диего, Калифорния: Калифорнийский университет. Архивировано из оригинал 16 июля 2011 г.
- ^ Joh, T. H .; Хван, О. (1987). «Дофамин-бета-гидроксилаза: биохимия и молекулярная биология». Летопись Нью-Йоркской академии наук. 493: 342–350. Дои:10.1111 / j.1749-6632.1987.tb27217.x. PMID 3473965.
- ^ Бродли К.Дж. (март 2010 г.). «Сосудистые эффекты следовых аминов и амфетаминов». Фармакология и терапия. 125 (3): 363–375. Дои:10.1016 / j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (май 2005 г.). «Возрождение следовых аминов, вдохновленное новым семейством GPCR». Тенденции в фармакологических науках. 26 (5): 274–281. Дои:10.1016 / j.tips.2005.03.007. PMID 15860375.
- ^ Ван Х, Ли Дж, Донг Дж, Юэ Дж (февраль 2014 г.). «Эндогенные субстраты CYP2D мозга». Европейский журнал фармакологии. 724: 211–218. Дои:10.1016 / j.ejphar.2013.12.025. PMID 24374199.
- ^ а б Kitahama, K .; Пирсон, Дж .; Денорой, Л .; Копп, Н .; Ulrich, J .; Maeda, T .; Жуве, М. (1985). «Адренергические нейроны в головном мозге человека продемонстрированы иммуногистохимическим методом с использованием антител к фенилэтаноламину-N-метилтрансфераза (PNMT): открытие новой группы в солитарном ядре ". Письма о неврологии. 53 (3): 303–308. Дои:10.1016/0304-3940(85)90555-5. PMID 3885079. S2CID 2578817.
- ^ Eisenhofer, G .; Копин, И. Дж .; Гольдштейн, Д. С. (2004). «Метаболизм катехоламинов: современный взгляд на физиологию и медицину». Фармакологические обзоры. 3 (56): 331–349. Дои:10.1124 / пр.56.3.1. PMID 15317907. S2CID 12825309.
- ^ Усадьба, И .; Tyano, S .; Mel, E .; Eisenberg, J .; Bachner-Melman, R .; Котлер, М .; Эбштейн, Р. П. (2002). «Семейные и ассоциативные исследования моноаминоксидазы А и синдрома дефицита внимания с гиперактивностью (СДВГ): преимущественная передача длинного повтора промоторной области и его связь с ухудшением производительности в тесте непрерывной производительности (TOVA)». Молекулярная психиатрия. 7 (6): 626–632. Дои:10.1038 / sj.mp.4001037. PMID 12140786.
- ^ Бруннер, Х. Г. (1996). «Дефицит МАОА и ненормальное поведение: перспективы ассоциации». Симпозиум Фонда Ciba. Симпозиумы Фонда Новартис. 194: 155–167. Дои:10.1002 / 9780470514825.ch9. ISBN 9780470514825. PMID 8862875.
- ^ Стюарт, М. Ф .; Croft, J .; Reed, P .; Новый, Дж. П. (2006). «Острая перемежающаяся порфирия и феохромоцитома: общие черты». Журнал клинической патологии. 60 (8): 935–936. Дои:10.1136 / jcp.2005.032722. ЧВК 1994495. PMID 17660335.
- ^ «Катехоламины в моче». webmd.com. Получено 4 мая 2017.
- ^ Куклин, А. И .; Конгер, Б. В. (1995). «Катехоламины в растениях». Журнал регулирования роста растений. 14 (2): 91–97. Дои:10.1007 / BF00203119. S2CID 41493767.
- ^ «Бой или беги», Википедия, 2019-12-16, получено 2019-12-24
- ^ "Метанефрины, свободные от плазмы | Лабораторные испытания в Интернете". labtestsonline.org. Получено 2019-12-24.
- ^ «Метанефрины в моче | Лабораторные тесты онлайн». labtestsonline.org. Получено 2019-12-24.
- ^ «Анализы мочи и крови на катехоламины». WebMD. Получено 2019-10-09.
- ^ «Катехоламины». labtestsonline.org. Получено 2019-10-09.
внешние ссылки
- Катехоламины в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)



