Глюкозооксидаза - Glucose oxidase
| Глюкозооксидаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
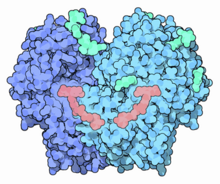 Структура димера глюкозооксидазы (темно-синий) в комплексе с FAD (лосось) и гликаны (аквамарин) из Penicillium amagasakiense.[1] | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 1.1.3.4 | ||||||||
| Количество CAS | 9001-37-0 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
В глюкозооксидаза фермент (GOx или же БОГ) также известный как нотатин (Номер ЕС 1.1.3.4) является оксидоредуктаза который катализирует окисление глюкоза к пероксид водорода и D-глюконо-δ-лактон. Этот фермент вырабатывается некоторыми видами грибов и насекомых и отображает антибактериальный активность при наличии кислорода и глюкозы.[2]

Глюкозооксидаза широко используется для определения свободной глюкозы в жидкостях организма (диагностика ), в растительном сырье и в пищевой промышленности. Он также имеет множество приложений в биотехнологии, как правило, ферментные анализы на биохимия включая биосенсоры в нанотехнологии.[3][4] Впервые он был изолирован Детлев Мюллер в 1928 г. из Aspergillus niger.[5]
Функция
Глюкозооксидаза синтезируется у нескольких видов грибов и насекомых, где она используется для производства перекиси водорода, которая, в свою очередь, убивает бактерии.[2]
Нотатин, извлеченные из антибактериальных культур Penicillium notatum, изначально назывался Пенициллин А, но был переименован во избежание путаницы с пенициллин.[6] Было показано, что Нотатин идентичен Пенициллин B и глюкозооксидаза, ферменты, извлеченные из других плесеней, кроме P. notatum;[7] теперь она известна как глюкозооксидаза.[8]
Ранние эксперименты показали, что нотатин проявляет in vitro антибактериальная активность (в присутствии глюкозы) за счет образования перекиси водорода.[6][9] В естественных условиях тесты показали, что нотатин неэффективен для защиты грызунов от Гемолитический стрептококк, Золотистый стафилококк, или же сальмонелла, и в некоторых дозах вызвал серьезное повреждение тканей.[9]
Глюкозооксидаза также вырабатывается гипофарингеальными железами пчеловоды и помещается в мед, где действует как естественный консервант. GOx на поверхности меда снижает атмосферный O2 к пероксид водорода (ЧАС2О2), который действует как противомикробный барьер.[10]
Структура

GOx - это димерный белок, трехмерная структура которого выяснена. Активный центр, где связывается глюкоза, находится в глубоком кармане. Фермент, как и многие белки, действующие вне клетки, покрыт углевод цепи.
Механизм
При pH 7 глюкоза существует в растворе в форме циклического полуацеталя в виде 63,6% β-D-глюкопиранозы и 36,4% α-D-глюкопиранозы, доля линейных и фураноза форма незначительна. Глюкозооксидаза специфически связывается с β-D-глюкопиранозой и не действует на α-D-глюкозу. Он способен окислять всю глюкозу в растворе, потому что равновесие между α и β аномерами движется в сторону β, поскольку она расходуется в реакции.[3]
Глюкозооксидаза катализирует окисление β-D-глюкозы в D-глюконо-1,5-лактон, который затем гидролизует к глюконовая кислота.
Для работы в качестве катализатора GOx требуется кофактор, флавинаденин динуклеотид (FAD). ФАД является обычным компонентом биологического окисления-восстановления (окислительно-восстановительные реакции ). Окислительно-восстановительные реакции включают приобретение или потерю электронов в молекуле. В окислительно-восстановительной реакции, катализируемой GOx, FAD работает как начальный акцептор электронов и восстанавливается до FADH.2. Тогда FADH2 окисляется конечным акцептором электронов, молекулярным кислород (O2), который может это сделать, поскольку имеет более высокий восстановительный потенциал. О2 затем сводится к пероксид водорода (ЧАС2О2).
Приложения
Мониторинг глюкозы
Глюкозооксидаза широко используется в сочетании с пероксидаза реакция, которая колориметрически визуализирует образующийся H2О2, для определения свободной глюкозы в сыворотка или же плазма крови для диагностики с использованием спектрометрических анализов вручную или с помощью автоматизированных процедур и даже для быстрых анализов в точках использования.[3][8]
Подобные анализы позволяют контролировать уровень глюкозы в ферментации, биореакторах, а также контролировать уровень глюкозы в растительном сырье и пищевых продуктах.[нужна цитата ] В анализе глюкозооксидазы глюкоза сначала окисляется, катализируемая глюкозооксидазой, с образованием глюконата и пероксида водорода. Затем перекись водорода окислительно связывается с хромоген для получения окрашенного соединения, которое можно измерить спектроскопически. Например, перекись водорода вместе с 4 амино-антипирен (4-ААР) и фенол в присутствии пероксидазы дают красный хиноэиминовый краситель, который можно измерить при 505 нм. Поглощение при 505 нм пропорционально концентрации глюкозы в образце.
Ферментативная глюкоза биосенсоры использовать электрод вместо O2 поглощать электроны, необходимые для окисления глюкозы, и производить электронный ток пропорционально концентрации глюкозы.[11] Это технология, лежащая в основе одноразовых сенсорных полосок глюкозы, используемых диабетики для контроля уровня глюкозы в сыворотке.[12]
Консервация продуктов
В производстве GOx используется в качестве добавки благодаря его окислительным свойствам: он способствует получению более прочного теста в пекарня, заменяя окислители, такие как бромат.[13] Он также используется в качестве консерванта для пищевых продуктов, чтобы помочь удалить кислород и глюкозу из пищевых продуктов, когда они упакованы, например, сухой яичный порошок, чтобы предотвратить нежелательное потемнение и нежелательный вкус.[14]
Обработка ран
В продуктах для ухода за ранами, таких как «Flaminal Hydro», используется альгинатный гидрогель, содержащий глюкозооксидазу и другие компоненты в качестве окислителя.
Клинические испытания
Назальный спрей от мешок на клапане устройство, которое смешивает глюкозооксидазу с глюкозой, подверглось клинические испытания в 2016 году для профилактики и лечения простуда.[15][16][17]
Смотрите также
Рекомендации
- ^ PDB: 1gpe; Гудселл Д. (май 2006 г.). «Молекула месяца: оксидаза глюкозы». Банк данных белков RCSB. Дои:10.2210 / rcsb_pdb / mom_2006_5.
- ^ а б Вонг CM, Вонг KH, Чен XD (апрель 2008 г.). «Глюкозооксидаза: естественное происхождение, функции, свойства и промышленное применение». Прикладная микробиология и биотехнология. 78 (6). Дои:10.1007 / s00253-008-1407-4. PMID 18330562.
- ^ а б c «Технический паспорт глюкозооксидазы» (PDF). Интерхим.[постоянная мертвая ссылка ]
- ^ Ghoshdastider U, Xu R, Trzaskowski B, Mlynarczyk K, Miszta P, Viswanathan S, Renugopalakrishnan V, Filipek S (2015). «Молекулярные эффекты инкапсуляции димера оксидазы глюкозы графеном». RSC Advances. 5: 13570–8. Дои:10.1039 / C4RA16852F.
- ^ «Детлев Мюллер открыл глюкозооксидазу». Tacomed.com. Архивировано из оригинал 18 апреля 2018 г.. Получено 13 июн 2017.
- ^ а б Култхард CE, Михаэлис R, Шорт WF, Сайкс G (1945). «Нотатин: антибактериальная глюкозо-аэродегидрогеназа из Penicillium notatum Вестлинг и Penicillium resticulosum sp. ноя ". Биохимический журнал. 39 (1): 24–36. Дои:10.1042 / bj0390024. ЧВК 1258144. PMID 16747849.
- ^ Кейлин Д., Хартри Э. Ф. (январь 1952 г.). «Специфичность глюкозооксидазы (нотатина)». Биохимический журнал. 50 (3): 331–41. Дои:10.1042 / bj0500331. ЧВК 1197657. PMID 14915954.
- ^ а б Хулио Раба Дж, Моттола HA (1995). «Глюкозооксидаза как аналитический реагент» (PDF). Критические обзоры в аналитической химии. 25 (1): 1–42. Дои:10.1080/10408349508050556.
- ^ а б Broom WA, Coulthard CE, Gurd MR, Sharpe ME (декабрь 1946 г.). «Некоторые фармакологические и химиотерапевтические свойства нотатина». Британский журнал фармакологии и химиотерапии. 1 (4): 225–233. Дои:10.1111 / j.1476-5381.1946.tb00041.x. ЧВК 1509745. PMID 19108091.
- ^ Бучекова М., Валачева И., Кохутова Л., Прочазка Е., Клаудины Дж., Майтан Дж. (Август 2014 г.). «Глюкозооксидаза медоносной пчелы - ее экспрессия у рабочих пчел и сравнительный анализ ее содержания и H2О2-опосредованная антибактериальная активность в натуральном меде ». Die Naturwissenschaften. 101 (8). Дои:10.1007 / s00114-014-1205-z. PMID 24969731.
- ^ Blanford CF (декабрь 2013 г.). «Рождение белковой электрохимии». Химические коммуникации. Королевское химическое общество. 49 (95): 11130–11132. Дои:10.1039 / C3CC46060F. PMID 24153438.
- ^ Касс А.Е., Дэвис Дж., Фрэнсис Дж. Д., Хилл Х.А., Астон У. Дж., Хиггинс И. Дж., Плоткин Е. В., Скотт Л. Д., Тернер А. П. (апрель 1984 г.). «Ферроцен-опосредованный ферментный электрод для амперометрического определения глюкозы». Аналитическая химия. Американское химическое общество. 56 (4): 667–671. Дои:10.1021 / ac00268a018. PMID 6721151.
- ^ Вонг CM, Вонг KH, Чен XD (апрель 2008 г.). «Глюкозооксидаза: естественное происхождение, функции, свойства и промышленное применение». Прикладная микробиология и биотехнология. 78 (6): 927–38. Дои:10.1007 / s00253-008-1407-4. PMID 18330562.
- ^ Дубей М.К., Зехра А., Аамир М., Мина М., Ахирвал Л., Сингх С. и др. (2017). «Стратегии усовершенствования, рентабельное производство и потенциальные применения грибковой глюкозооксидазы (GOD): текущие обновления». Границы микробиологии. 8: 1032. Дои:10.3389 / fmicb.2017.01032. ЧВК 5468390. PMID 28659876.
- ^ Номер клинического исследования NCT01883427 на «Назальный спрей с глюкозооксидазой, предотвращающий простуду у детей дошкольного возраста» в ClinicalTrials.gov
- ^ Номер клинического исследования NCT01883440 на «Глюкозооксидаза как средство от простуды» на ClinicalTrials.gov
- ^ Номер клинического исследования NCT01883453 для «Назального спрея с оксидазой глюкозы для лечения простуды» в ClinicalTrials.gov
внешняя ссылка
- «Глюкозооксидаза: широко используемый и любимый фермент в биосенсорах» в Университет Пейсли
- Глюкоза + оксидаза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
