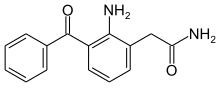
Непафенак - Nepafenac
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Неванац, Илевро, Амнак, другие |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a606007 |
| Данные лицензии | |
| Беременность категория | |
| Маршруты администрация | Глазные капли для местного применения |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.207.414 |
| Химические и физические данные | |
| Формула | C15ЧАС14N2О2 |
| Молярная масса | 254.289 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Непафенак, продается под торговой маркой Неванац среди прочего, это нестероидный противовоспалительный препарат (НПВП), обычно продается как рецепт слеза 0,1% раствор (Неванак) или 0,3% раствор (Илевро). Он используется для лечения боли и воспалений, связанных с катаракта хирургия.[2] Непафенак - это пролекарство из амфенак, ингибитор СОХ-1 и СОХ-2 Мероприятия.[3][4]
Медицинское использование
Непафенак показан для лечения боли и воспалений после операции по удалению катаракты.[2][5][6][7]
В Европейском Союзе непафенак также показан для снижения риска послеоперационного периода. макулярный отек связанные с хирургией катаракты у людей с диабетом.[7]
Фармакология
Механизм действия
Непафенак - это НПВП, который считается пролекарством амфенака после превращения гидролазами глазной ткани после проникновения через роговица.[5][6] Считается, что амфенак, как и другие НПВП, подавляет циклооксигеназа действие.[5][6]
Неблагоприятные события
Побочные эффекты включать головную боль; насморк; боль или давление в лице; тошнота; рвота; и сухие, зудящие, липкие глаза.[8] Серьезные побочные эффекты включают красные или кровавые глаза; ощущение инородного тела в глазу; чувствительность к свету; уменьшился Острота зрения; видеть пятнышки или пятна; слезящимися глазами; или выделения из глаз или корки.[8]
Нормативный
Неванац
25 февраля 2005 г. компания "Алкон" подала Заявка на новый препарат (NDA) с США Управление по контролю за продуктами и лекарствами (FDA) для Неванака 0,1%.[9] Результаты двух исследований, упомянутых в NDA (исследование фазы 2/3 C-02-53; исследование фазы 3 C-03-32), не были опубликованы.[10] Исследование C-02-53 включало 228 пациентов в 10 центрах США.[11] В исследование C-03-32 вошли 522 пациента в 22 центрах США.[11] Представленные результаты эффективности были подтверждены в исследовании, опубликованном в 2007 году.[12]
Неванак был одобрен FDA 19 августа 2005 г. под номером заявки 021–862.[13]
Илевро
NDA для Ilevro было подписано 15 декабря 2011 года.[14] В ходе исследования продолжительностью один месяц не было выявлено новых токсических эффектов в новой лекарственной форме непафенака.[15] Информация о безопасности и эффективности была получена из предыдущего применения Неванака.[15] В июне 2010 года началось подтверждающее исследование (Исследование C09055) с участием более 2000 пациентов из 49 центров США и 37 европейских центров.[16][17] Вторая фаза 3 исследования (Исследование C11003) была проведена на популяции из 1342 пациентов в 37 центрах США, которые не смогли продемонстрировать превосходство над Неванаком в измененном режиме дозирования.[16]
Ilevro был одобрен FDA 16 октября 2012 года под номером заявки 203–491.[18]
Коммерциализация
И Неванац, и Илевро производятся и продаются Alcon, Inc.[5][6] Alcon в настоящее время является подразделением Новартис International AG, базирующаяся в основном за пределами Швейцарии.[19] Alcon, Inc. также имеет представительства в Швейцарии и США.[20] Компания претерпела несколько изменений названия: от Alcon Laboratories, Inc. до Alcon Universal, Ltd., до Alcon, Inc.[20]
Nevanac вышел на рынок в 2005 году как продукт компании Alcon, в то время дочерней компании Nestlé.[21] 6 апреля 2008 года Novartis согласилась приобрести у Nestlé около 74 миллионов акций Alcon по цене 143,18 доллара за акцию.[21] 4 января 2010 года Novartis согласилась выкупить у Nestlé все оставшиеся акции Alcon, на общую сумму 156 миллионов акций или 77% акций компании.[21] Во время покупки предложение о слиянии в соответствии с законодательством Швейцарии о слияниях было передано совету директоров Alcon.[21] Слияние было согласовано 15 декабря 2010 г., в результате чего Alcon стал «вторым по величине подразделением в Novartis».[21] Слияние завершено 8 апреля 2011 года.[22]
Ilevro был запущен компанией Alcon 21 января 2013 года.[23] В 2014 и 2015 годах чистые продажи Alcon выросли, отчасти благодаря увеличению объема продаж Ilevro.[24][25][26] В том финансовом году Novartis сообщила, что общий финансовый долг составляет 18 миллиардов долларов.[24] С тех пор эта цифра неуклонно росла. В 2016 году Novartis сообщила об общем долге в 23,8 миллиарда долларов.[27] по сравнению с 21,9 млрд долларов в 2015 г. [26] и 20,4 млрд долларов, о которых сообщалось в 2014 году.[25] По состоянию на май 2017 года стоимость Novartis оценивается в 193,2 миллиарда долларов.[28]
27 января 2016 г. компания Alcon была переведена в подразделение инновационных лекарственных средств Novartis.[27] В начале 2016 года Alcon заключила соглашения с TrueVision и PowerVision и приобрела Transcend Medical.[27] По состоянию на январь 2017 года Novartis взвешивает варианты для Alcon в структуре бизнеса.[27]
Расходы
По состоянию на 2015 год примерно 266 751 пациенту Medicare Part D был назначен препарат Илевро в рамках их терапевтического режима по поводу операции по удалению катаракты, что принесло компании Novartis примерно 95,2 миллиона долларов в 2015 году из 411 000 заявок, поданных на лекарство.[29] Средняя годовая стоимость пациента программы Medicare Part D для Ilevro составляет 94 доллара.[29] Ориентировочная цена за единицу Неванака в США составляет 88,93 доллара.[30] Для Ilevro цена за единицу бутылки на 1,7 мл в среднем составляет 156,89 долларов, а цена за единицу для бутылки на 3 мл в среднем составляет 88,91 долларов.[31] Средняя цена на оба препарата близка.[30][31]
Дженерики для обоих препаратов пока недоступны.[30][31]
Коммерческие риски
В 2016 году компания Alcon столкнулась с падением роста, столкнувшись с проблемами в разработке и маркетинге новых продуктов.[27]
Маркетинг
Novartis имеет отдел детализации, ориентированный на специалистов в области здравоохранения, состоящий из более чем 3000 сотрудников в США и еще 21000 сотрудников по всему миру.[27] Novartis также стремится расширить прямую рекламу потребителям и выйти на рынки специальных товаров.[27] Novartis также отмечает влияние позиции и предпочтений на формуляры центров Medicare и Medicaid США в увеличении их рыночной стоимости.[27]
Непафенак, Неванац и Илевро отсутствуют в годовом отчете компании Novartis за 2016 год.[27]
Интеллектуальная собственность
В настоящее время есть[когда? ] семь зарегистрированных патентов США, которые напрямую связаны с модернизированными составами непафенака, все получены от Novartis.[32] Есть три патента, связанных с Неванац, которые все еще[когда? ] активный[33] и четыре связаны с Илевро.[34] Самый ранний патент, связанный с современными формами непафенака, был одобрен 11 июня 2002 года после подачи заявки в 1999 году Бахрамом Асгаряном.[35] Патент был подан Уорреном Вонгом, связанным с Alcon, Inc., базирующейся в Форт-Уэрт, Техас от 2 декабря 2005 г. для водных суспензий непафенака.[36] Другой патент на лекарство на основе непафенака был подан 8 мая 2006 года Джеффри Оуэном, Эми Брукс и Густавом Граффом.[37] Патент был подан Масудом А. Чоуханом и Хуаган Чен 9 февраля 2007 г. и утвержден 24 мая 2011 г.[38] Затем последовал патент, поданный Уорреном Вонгом 23 сентября 2010 г. и утвержденный 6 декабря 2011 г.[39] Масуд А. Чоухан, Малай Гош, Бахрам Асгарян и Уэсли Вехсин Хан подали еще один патент 1 декабря 2010 г. и одобрили его 30 декабря 2014 г.[40] Самый последний[когда? ] Патент был подан Масудом А. Чоуханом, Малай Гхошем, Бахрамом Асгарян и Уэсли Вешином Ханом 12 ноября 2014 г. и утвержден 30 мая 2017 г.[41] Эти патенты действительны до дат с 17 июля 2018 г. по 31 марта 2032 г.[34]
Новартис также имеет патенты на непафенак в 26 странах за пределами США.[42]
Вызовы
Этот раздел должен быть обновлено. (Июль 2020) |
4 марта 2016 г. компания Alcon подала иск против Watson Laboratories в Делавэре за производство непатентованной версии 0,3% рецептуры непафенака Ilevro.[43] Изменения в жалобу внесены 14 июня 2017 г.[44]
Рекомендации
- ^ а б «Применение непафенака в офтальмологии во время беременности». Drugs.com. 6 июн 2019. Получено 13 сентября 2020.
- ^ а б Непафенак Монография
- ^ Банк наркотиков: Непафенак
- ^ Занетти Ф., Фулько Е. А., Чавес Ф. Р., да Коста Пинто А. П., Ариета CE, Лира РП (июль 2012 г.) «Влияние предоперационного использования местного преднизолона ацетата, кеторолака трометамина, непафенака и плацебо на поддержание интраоперационного мидриаза во время операции по удалению катаракты: рандомизированное исследование». Индийский журнал офтальмологии. 60 (4): 277–81. Дои:10.4103/0301-4738.98705. ЧВК 3442462. PMID 22824596.
- ^ а б c d «Неванак- непафенак суспензия / капли». DailyMed. 9 сентября 2019 г.. Получено 6 июля 2020.
- ^ а б c d «Илевро-непафенак суспензия». DailyMed. 9 сентября 2019 г.. Получено 6 июля 2020.
- ^ а б «Неванац EPAR». Европейское агентство по лекарствам (EMA). Получено 6 июля 2020.
- ^ а б «Непафенак офтальмологический». MedlinePlus. Национальная медицинская библиотека США. Получено 31 октября, 2017.
- ^ «Пакет одобрения Неванац» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 31 октября, 2017.
- ^ Гейнс Б.И., Оньеквулудже А. (июнь 2008 г.). «Актуальные офтальмологические НПВП: обсуждение с упором на офтальмологическую суспензию непафенака». Клиническая офтальмология. 2 (2): 355–68. Дои:10.2147 / opth.s1067. ЧВК 2693998. PMID 19668727.
- ^ а б «Статистический обзор Неванаца» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 31 октября, 2017.
- ^ Lane SS, Modi SS, Lehmann RP, Holland EJ (январь 2007 г.). «Офтальмологическая суспензия непафенака 0,1% для профилактики и лечения глазного воспаления, связанного с хирургией катаракты». Журнал катарактальной и рефракционной хирургии. 33 (1): 53–8. Дои:10.1016 / j.jcrs.2006.08.043. PMID 17189793. S2CID 38881826.
- ^ «Пакет одобрения лекарственных средств: офтальмологическая суспензия Неванак (Непафенак) NDA № 021862». НАС. Управление по контролю за продуктами и лекарствами (FDA). 6 января 2005 г.. Получено 27 октября, 2017.
- ^ «Пакет одобрения Илевро» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 31 октября, 2017.
- ^ а б "Обзор фармакологии 203491" (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 31 октября, 2017.
- ^ а б «Статистическое обозрение Илевро» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 31 октября, 2017.
- ^ «Подтверждающее исследование Непафенак 0,3%». ClinicalTrials.gov. Национальная медицинская библиотека США. Получено 31 октября, 2017.
- ^ «Пакет одобрения лекарственного средства: офтальмологическая суспензия непафенака, 0,3% NDA № 203491». НАС. Управление по контролю за продуктами и лекарствами (FDA). 8 апреля 2013 г.. Получено 27 октября, 2017.
- ^ "О нас". Новартис. Получено 27 октября, 2017.
- ^ а б «Административные документы и корреспонденция Неванаца» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 27 октября, 2017.
- ^ а б c d е «Годовой отчет Алкон 2010» (PDF). ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 30 октября, 2017.
- ^ «Алкон Форма 15». ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 30 октября, 2017.
- ^ «Alcon запускает ILEVRO ™ (офтальмологическая суспензия непафенака) 0,3%, новый нестероидный противовоспалительный препарат для лечения боли и воспаления, связанных с хирургией катаракты». Alcon. Получено 30 октября, 2017.
- ^ а б «Форма 20-F». ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 30 октября, 2017.
- ^ а б «Форма 20-F». ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 30 октября, 2017.
- ^ а б «Форма 20F». ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 30 октября, 2017.
- ^ а б c d е ж грамм час я «Форма 20-F». ТРЦ Эдгар. Комиссия по ценным бумагам и биржам США. Получено 31 октября, 2017.
- ^ «Novartis в списке лучших международных исполнителей Forbes». Forbes. Получено 31 октября, 2017.
- ^ а б "Осмотр врача: Илевро". Медицинский осмотр. ProPublica. Получено 30 октября, 2017.
- ^ а б c «Цены, купоны и программы помощи пациентам Неванац». Drugs.com. Получено 31 октября, 2017.
- ^ а б c «Цены, купоны и программы помощи пациентам Ilevro». Drugs.com. Получено 31 октября, 2017.
- ^ «Непафенак». Патенты США. ФармаКомпас. Получено 30 октября, 2017.
- ^ «Доступность универсального Неванака». Drugs.com. Получено 31 октября, 2017.
- ^ а б «Общая доступность Ilevro». Drugs.com. Получено 31 октября, 2017.
- ^ «Заявка на патент США: 6403609». Ведомство США по патентам и товарным знакам. Получено 31 октября, 2017.
- ^ "Заявка на патент США: 0060122277". Ведомство США по патентам и товарным знакам. Получено 30 октября, 2017.
- ^ "Заявка на патент США: 0060257487". Ведомство США по патентам и товарным знакам. Получено 27 октября, 2017.
- ^ «Патент США: 7947295». Ведомство США по патентам и товарным знакам. Получено 31 октября, 2017.
- ^ «Патент США: 8071648». Ведомство США по патентам и товарным знакам. Получено 31 октября, 2017.
- ^ "Патент США: 8921337". Ведомство США по патентам и товарным знакам. Получено 31 октября, 2017.
- ^ «Патент США: 9662398». Ведомство США по патентам и товарным знакам. Получено 31 октября, 2017.
- ^ "Непафенак - Общие сведения о лекарстве". ПрепаратПатентСмотреть. thinkBiotech LLC. Получено 31 октября, 2017.
- ^ "Жалоба". RPX Insight. Получено 31 октября, 2017.
- ^ «Жалоба с поправками». RPX Insight. Получено 31 октября, 2017.
внешняя ссылка
- «Непафенак». Портал информации о наркотиках. Национальная медицинская библиотека США.
