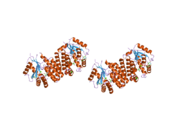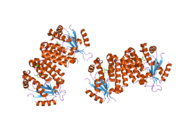Дезоксицитидин киназа - Deoxycytidine kinase
Дезоксицитидин киназа (dCK) является фермент который кодируется ДВК ген в люди.[5] dCK преимущественно фосфорилирует дезоксицитидин (dC) и преобразует dC в дезоксицитидин монофосфат. dCK катализирует один из начальных этапов спасение нуклеозидов путь[6] и имеет потенциал фосфорилирования других предварительно образованных нуклеозидов, в частности дезоксиаденозин (dA) и дезоксигуанозин (dG) и превращают их в монофосфатные формы.[7] В последнее время проявился интерес биомедицинских исследований к изучению потенциала dCK в качестве терапевтической мишени для различных типов рак.[6][7][8]
Структура

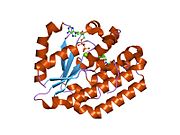
dCK - это гомодимер где каждая мономерная субъединица состоит из нескольких альфа спирали окружающий бета-лист основной.[9][7][10] Каждая субъединица включает сайт связывания донора нуклеотидов, сайт связывания акцептора нуклеозидов, сенсорную петлю нуклеотидного основания (240–254 остатка), область вставки (12–15 остатков), которая соединяет спирали 2 и 3.[9][10] dCK имеет несколько различных конформаций белков, но их конформация зависит от нуклеозида или нуклеотида, с которым он связывается. dCK может связываться с ADP, ATP, UDP или UTP (донорами фосфорильных групп), но связывание UDP / UTP изменяет конформацию фермента, перестраивая петлю, чувствительную к нуклеотидным основаниям, по сравнению с конформацией dCK при связывании с АТФ. Это изменение конформации, когда конкретный донор фосфорила связывается в сайте связывания нуклеотида, определяет, какой нуклеозид может связываться в сайте связывания нуклеозида.[9][10] Например, было замечено, что когда dCK связывается с ADP, dCK принимает «закрытую» конформацию или более компактный сайт связывания нуклеозидов, где глютаминовая кислота 53 (Glu53) находится ближе к нему, чтобы напрямую взаимодействовать с 5'-гидроксильной группой нуклеозида.[9][10]
- Одна из гипотез функциональности «открытой» конформации заключается в том, что «открытая» конформация может способствовать начальному связыванию нуклеозидов и высвобождению монофосфатного продукта.[9]
Функция
Дезоксицитидинкиназа (dCK) фосфорилирует несколько дезоксирибонуклеозидов и их аналоги нуклеозидов (нуклеозид с сахаром и другим заместителем или аналогом основания нуклеиновой кислоты, который имеет уникальные свойства при модификации) с использованием фосфатных групп из АТФ и UTP.[9][10] Более конкретно, dCK добавляет первую фосфорильную группу к предварительно сформированным нуклеозидам и обычно является ферментом, ограничивающим скорость всего процесса превращения нуклеозидов в их дезоксинуклеозидтрифосфатную форму, или нуклеотид в пути спасения нуклеозидов.[10] Ниже представлен упрощенный путь, который показывает роль dCK в синтезе нуклеотидов с использованием пути спасения нуклеозидов.[8][11]

Glu53 выполняет базовый катализ депротонировать гидроксильную группу, что позволяет теперь нуклеофильному кислороду из 5'-гидроксильной группы нуклеозида атаковать конец фосфатной цепи (гамма-фосфат) на доноре фосфорила (например, АТФ или УТФ). Это рассматривает «закрытую» конформацию как каталитически активную конформацию, поскольку она катализирует перенос фосфорила между донорами фосфорила и получением нуклеозидов.[9] Точно так же «открытую» конформацию обычно называют каталитически неактивной формой, поскольку Glu53 не находится в непосредственной близости от 5'-гидроксильной группы нуклеозида и не будет катализировать перенос фосфорила.[9]
Регулирование
Одним из методов регулирования как каталитической активности, так и субстратной специфичности является посттрансляционная модификация серина 74, остатка в области вставки на каждой из индивидуальных субъединиц dCK.[9] Хотя серин 74 находится далеко от активного центра dCK, фосфорилирование серина 74 (Ser74) на dCK вызывает изменение конформации фермента и влияет на кинетику фермента. Более конкретно, фосфорилирование Ser74 способствует тому, что dCK принимает свою открытую (неактивную) конформацию и позволяет dCK становиться более компетентным в связывании и высвобождении нуклеозидов, но ограничивает передачу фосфорильных групп dCK. Закрытая (активная) конформация dCK позволяет dCK переносить фосфорильные группы, но не связывать или высвобождать нуклеозиды. «Открытое» и «закрытое» состояния относятся к сайту связывания нуклеозида на dCK.[9]
Биосинтез нуклеотидов
dCK является ключевым ферментом в пути спасения нуклеозидов (NSP). Более конкретно, этот путь рециркулирует предварительно образованные нуклеозиды из расщепляющихся молекул ДНК для синтеза dNTP для клетки. Путь спасения нуклеозидов может выступать в качестве альтернативного пути производства нуклеотидов (dNTP) в случае de novo подавление пути.[6] То есть путь спасения (и, следовательно, dCK) активируется, когда путь de novo подавляется или ингибируется, чтобы компенсировать потерю продукции нуклеотидов. Оба de novo путь (DNP) и путь спасения нуклеозидов (NSP) являются анаболическими путями, которые производят дезоксирибонуклеотидтрифосфаты (dNTP) или нуклеотиды, мономеры которые составляют ДНК.
Терапевтическое значение
Дефицит dCK связан с устойчивостью к противовирусным и противоопухолевым химиотерапевтическим средствам. Напротив, повышенная активность дезоксицитидинкиназы связана с повышенной активацией этих агентов к цитотоксическим нуклеозидтрифосфатным производным. dCK имеет клиническое значение из-за его связи с лекарственной устойчивостью и чувствительностью.[5] Было показано, что манипулирование ферментативной активностью dCK имеет сильную корреляцию в повышении чувствительности клеток к действию других лекарств (например, ингибиторов RNR,[6] гемцитабин) или лечения (например, ионизирующего излучения)[11] и так больше комбинированная терапия в настоящее время изучаются для снижения механизмов биологической устойчивости и переносимость лекарств у пациентов.[6][11][12]
Например, гемцитабин является одобренным FDA аналогом пиримидиновых нуклеозидов и основывается на активности dCK пролекарство который использовался для лечения рака поджелудочной железы, груди, мочевого пузыря и немелкоклеточного рака легких.[8][11] Механически dCK, который поглощает предварительно образованные нуклеозиды, добавляет первую фосфорильную группу к dFdC (исходная форма гемцитабина как аналог дезоксицитидина), чтобы преобразовать его в dFdCMP, его монофосфатную форму.[8][11] Цитидилаткиназа или киназа UMP-CMP затем добавляет вторую фосфорильную группу с образованием dFdCDP (гемцитабиндифосфатная форма), которая может ингибировать рибонуклеотидредуктаза. Нуклеозид-дифосфаткиназа или же нуклеозидкиназа А добавляет третью фосфорильную группу с образованием dFdCTP (гемцитабинтрифосфатная форма), которая является активной формой гемцитабина, которая ингибирует оба дезоксицитидилат дезаминаза и ДНК-полимераза.[8] Хотя гемцитабин широко используется для лечения солидных опухолей более десяти лет, пациенты, принимающие только гемцитабин (монотерапия ) наблюдалось развитие химиорезистент к препарату.[8][11]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000156136 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000029366 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б «Entrez Gene: DCK дезоксицитидинкиназа».
- ^ а б c d е Натансон Д.А., Армийо А.Л., Том М., Ли З., Димитрова Э., Остин В.Р., Номм Дж., Кэмпбелл Д.О., Та Л., Ле TM, Ли Дж. Т., Дарвиш Р., Гордин А., Вей Л., Ляо Хай, Уилкс М., Мартин К. , Садеги С., Мерфи Дж. М., Булос Н., Фелпс М. Е., Фаулл К. Ф., Хершман Х. Р., Юнг М. Е., Чернин Дж., Лави А., Раду К. Г. (март 2014 г.). «Совместное нацеливание на конвергентные пути биосинтеза нуклеотидов для искоренения лейкемии». Журнал экспериментальной медицины. 211 (3): 473–86. Дои:10.1084 / jem.20131738. ЧВК 3949575. PMID 24567448.
- ^ а б c Сабини Е., Орт С., Моннерьян С., Конрад М., Лави А. (июль 2003 г.). «Структура dCK человека предлагает стратегии для улучшения противоопухолевой и противовирусной терапии». Структурная биология природы. 10 (7): 513–9. Дои:10.1038 / nsb942. HDL:11858 / 00-001M-0000-0012-F0B9-8. PMID 12808445. S2CID 6212685.
- ^ а б c d е ж де Соуза Кавальканте Л., Монтейро Г. (октябрь 2014 г.). «Гемцитабин: метаболизм и молекулярные механизмы действия, чувствительность и химиорезистентность при раке поджелудочной железы». Европейский журнал фармакологии. 741: 8–16. Дои:10.1016 / j.ejphar.2014.07.041. PMID 25084222.
- ^ а б c d е ж грамм час я j Хазра С., Шевчак А., Орт С., Конрад М., Лави А. (апрель 2011 г.). «Посттрансляционное фосфорилирование серина 74 дезоксицитидинкиназы человека способствует принятию ферментом открытой конформации, что делает его компетентным для связывания и высвобождения нуклеозидов». Биохимия. 50 (14): 2870–80. Дои:10.1021 / bi2001032. ЧВК 3071448. PMID 21351740.
- ^ а б c d е ж Сабини Е., Хазра С., Конрад М., Лави А. (июль 2008 г.). «Выяснение различных способов связывания пуриновых нуклеозидов с дезоксицитидинкиназой человека». Журнал медицинской химии. 51 (14): 4219–25. Дои:10.1021 / jm800134t. ЧВК 2636677. PMID 18570408.
- ^ а б c d е ж Грегуар В., Розье Дж. Ф., Де Баст М., Брюнио М., Де Костер Б., Октав-Приньо М., Скаллиет П. (июнь 2002 г.). «Роль активности дезоксицитидинкиназы (dCK) в радиоусилении гемцитабина у мышей и клеточных линий человека in vitro». Лучевая терапия и онкология. 63 (3): 329–38. Дои:10.1016 / s0167-8140 (02) 00106-8. PMID 12142097.
- ^ Bozic I, Reiter JG, Allen B., Antal T, Chatterjee K, Shah P, Moon YS, Yaqubie A, Kelly N, Le DT, Lipson EJ, Chapman PB, Diaz LA, Vogelstein B., Nowak MA (июнь 2013 г.). «Эволюционная динамика рака в ответ на таргетную комбинированную терапию». eLife. 2: e00747. Дои:10.7554 / eLife.00747. ЧВК 3691570. PMID 23805382.
дальнейшее чтение
- Хазра С., Шевчак А., Орт С., Конрад М., Лави А. (апрель 2011 г.). «Посттрансляционное фосфорилирование серина 74 дезоксицитидинкиназы человека способствует принятию ферментом открытой конформации, что делает его компетентным для связывания и высвобождения нуклеозидов». Биохимия. 50 (14): 2870–80. Дои:10.1021 / bi2001032. ЧВК 3071448. PMID 21351740.
- Хазра С., Конрад М., Лави А. (август 2010 г.). «Сахарное кольцо нуклеозида необходимо для позиционирования продуктивного субстрата в активном центре дезоксицитидинкиназы человека (dCK): значение для разработки dCK-активированных ациклических аналогов гуанина». Журнал медицинской химии. 53 (15): 5792–800. Дои:10.1021 / jm1005379. ЧВК 2936711. PMID 20684612.
- Хазра С., Орт С., Конрад М., Лави А. (август 2010 г.). «Структурная и кинетическая характеристика вариантов дезоксицитидинкиназы человека, способных фосфорилировать 5-замещенные аналоги дезоксицитидина и тимидина». Биохимия. 49 (31): 6784–90. Дои:10.1021 / bi100839e. ЧВК 2925221. PMID 20614893.
- Хазра С., Сабини Э, Орт С., Конрад М., Лави А. (февраль 2009 г.). «Расширение активности тимидинкиназы на каталитический репертуар дезоксицитидинкиназы человека». Биохимия. 48 (6): 1256–63. Дои:10.1021 / bi802062w. ЧВК 2701478. PMID 19159229.
- Сабини Е., Хазра С., Конрад М., Лави А. (июль 2008 г.). «Выяснение различных способов связывания пуриновых нуклеозидов с дезоксицитидинкиназой человека». Журнал медицинской химии. 51 (14): 4219–25. Дои:10.1021 / jm800134t. ЧВК 2636677. PMID 18570408.
- Сабини Е., Хазра С., Орт С., Конрад М., Лави А. (май 2008 г.). «Структурная основа субстратной неразборчивости dCK». Журнал молекулярной биологии. 378 (3): 607–21. Дои:10.1016 / j.jmb.2008.02.061. ЧВК 2426910. PMID 18377927.
- МакСорли Т., Орт С., Хазра С., Лави А., Конрад М. (март 2008 г.). «Имитируя фосфорилирование Ser-74 на дезоксицитидинкиназу человека, селективно увеличивает каталитическую активность для аналогов dC и dC». Письма FEBS. 582 (5): 720–4. Дои:10.1016 / j.febslet.2008.01.048. ЧВК 2636680. PMID 18258203.
- Сабини Е., Хазра С., Конрад М., Лави А. (июнь 2007 г.). «Неэнантиоселективность дезоксицитидинкиназы человека объясняется структурами фермента в комплексе с L- и D-нуклеозидами». Журнал медицинской химии. 50 (13): 3004–14. Дои:10.1021 / jm0700215. ЧВК 2586175. PMID 17530837.
- Сабини Э, Хазра С, Конрад М, Берли С.К., Лави А (2007). «Структурная основа активации терапевтических аналогов L-нуклеозидов 3ТС и троксацитабина дезоксицитидинкиназой человека». Исследования нуклеиновых кислот. 35 (1): 186–92. Дои:10.1093 / нар / gkl1038. ЧВК 1802566. PMID 17158155.
- Арнер Э.С., Эрикссон С. (1996). «Дезоксирибонуклеозидкиназы млекопитающих». Фармакология и терапия. 67 (2): 155–86. Дои:10.1016/0163-7258(95)00015-9. PMID 7494863.
- Chottiner EG, Shewach DS, Datta NS, Ashcraft E, Gribbin D, Ginsburg D, Fox IH, Mitchell BS (февраль 1991). «Клонирование и экспрессия кДНК дезоксицитидинкиназы человека». Труды Национальной академии наук Соединенных Штатов Америки. 88 (4): 1531–5. Дои:10.1073 / pnas.88.4.1531. ЧВК 51053. PMID 1996353.
- Эрикссон С., Седерлунд Э, Бергман Т., Йорнвалл Х., Бохман С. (март 1991 г.). «Характеристика дезоксицитидинкиназы человека. Корреляция с последовательностями кДНК». Письма FEBS. 280 (2): 363–6. Дои:10.1016 / 0014-5793 (91) 80332-В. PMID 2013338. S2CID 26841109.
- Ямада Ю., Гото Х., Огасавара Н. (ноябрь 1983 г.). «Пуриновые нуклеозидкиназы в Т- и В-лимфобластах человека». Biochimica et Biophysica Acta (BBA) - Общие предметы. 761 (1): 34–40. Дои:10.1016/0304-4165(83)90359-8. PMID 6315069.
- Херли М.С., Палелла TD, Fox IH (декабрь 1983 г.). «Фосфорилирующая активность дезоксиаденозина и дезоксигуанозина в плаценте человека». Журнал биологической химии. 258 (24): 15021–7. PMID 6317685.
- Спасокоукоцкая Т., Арнер Э.С., Бросйо О., Гунвен П., Джулиуссон Дж., Лилиемарк Дж., Эрикссон С. (1995). «Экспрессия дезоксицитидинкиназы и фосфорилирования 2-хлордезоксиаденозина в нормальных и опухолевых клетках и тканях человека». Европейский журнал рака. 31A (2): 202–8. Дои:10.1016/0959-8049(94)00435-8. PMID 7718326.
- Стегманн А.П., Хондерс М.В., Болк М.В., Весселс Дж., Виллемзе Р., Ландеджент Дж. Э. (август 1993 г.). «Отнесение гена дезоксицитидинкиназы человека (DCK) к полосе хромосомы 4 q13.3-q21.1». Геномика. 17 (2): 528–9. Дои:10.1006 / geno.1993.1365. PMID 8406512.
- Сонг Дж. Дж., Уокер С., Чен Е., Джонсон Е. Е., Спайчала Дж., Гриббин Т., Митчелл Б. С. (январь 1993 г.). «Геномная структура и хромосомная локализация гена дезоксицитидинкиназы человека». Труды Национальной академии наук Соединенных Штатов Америки. 90 (2): 431–4. Дои:10.1073 / пнас.90.2.431. ЧВК 45676. PMID 8421671.
- Йоханссон М., Брисмар С., Карлссон А. (октябрь 1997 г.). «Дезоксицитидинкиназа человека находится в ядре клетки». Труды Национальной академии наук Соединенных Штатов Америки. 94 (22): 11941–5. Дои:10.1073 / пнас.94.22.11941. ЧВК 23663. PMID 9342341.
- Хатзис П., Аль-Мадхун А.С., Джуллиг М., Петракис Т.Г., Эрикссон С., Талианидис I. (ноябрь 1998 г.). «Внутриклеточная локализация дезоксицитидинкиназы». Журнал биологической химии. 273 (46): 30239–43. Дои:10.1074 / jbc.273.46.30239. PMID 9804782.
- Саада А., Шааг А., Мандель Х, Нево Й, Эрикссон С., Эльпелег О. (ноябрь 2001 г.). «Мутантная митохондриальная тимидинкиназа в миопатии истощения митохондриальной ДНК». Природа Генетика. 29 (3): 342–4. Дои:10,1038 / ng751. PMID 11687801. S2CID 3045143.
- Веугер М.Дж., Хеемскерк М.Х., Хондерс М.В., Виллемзе Р., Баржа Р.М. (февраль 2002 г.). «Функциональная роль альтернативно сплайсированной дезоксицитидинкиназы в чувствительности к цитарабину клеток острого миелоидного лейкоза». Кровь. 99 (4): 1373–80. Дои:10.1182 / blood.V99.4.1373. PMID 11830489.
- Инносета А., Галлуцци Л., Руццо А., Андреони Ф., Кьярантини Л., Маньяни М. (февраль 2002 г.). «Молекулярная основа 2 ', 3'-дидезоксицитидин-индуцированной лекарственной устойчивости в клетках человека». Молекулярная и клеточная биохимия. 231 (1–2): 173–7. Дои:10.1023 / А: 1014441209108. PMID 11952160. S2CID 11289854.
- Krawiec K, Kierdaszuk B, Shugar D (январь 2003 г.). «Неорганический триполифосфат (PPP (i)) как донор фосфата для дезоксирибонуклеозидкиназ человека». Сообщения о биохимических и биофизических исследованиях. 301 (1): 192–7. Дои:10.1016 / S0006-291X (02) 03007-3. PMID 12535661.
- ван дер Вильт К.Л., Кроэп-младший, Лавс В.Дж., Ротс М.Г., Ван Грёнинген С.Дж., Касперс Г.Дж., Петерс Дж.Дж. (март 2003 г.). «Экспрессия дезоксицитидинкиназы в лейкозных клетках по сравнению с линиями солидных опухолевых клеток, метастазами в печень и нормальной печенью». Европейский журнал рака. 39 (5): 691–7. Дои:10.1016 / S0959-8049 (02) 00813-4. PMID 12628850.
- Дж. Й., Дженсен Т. Л., Мазерли Л. Х., Тауб Дж. В. (декабрь 2003 г.). «Физические и функциональные взаимодействия между белками USF и Sp1 регулируют активность промотора дезоксицитидинкиназы человека». Журнал биологической химии. 278 (50): 49901–10. Дои:10.1074 / jbc.M305085200. PMID 14514691.
- Усова Е., Мальцева Т., Фёльдези А., Чаттопадхаяя Дж., Эрикссон С. (декабрь 2004 г.). «Дезоксицитидинкиназа человека как дезоксирибонуклеозидфосфорилаза». Журнал молекулярной биологии. 344 (5): 1347–58. Дои:10.1016 / j.jmb.2004.10.016. PMID 15561147.
- Мани Р.С., Усова Е.В., Эрикссон С., Касс С.Е. (октябрь 2004 г.). «Флуоресцентные исследования связывания субстрата с рекомбинантной дезоксицитидин киназой человека». Нуклеозиды, нуклеотиды и нуклеиновые кислоты. 23 (8–9): 1343–6. Дои:10.1081 / NCN-200027609. PMID 15571255. S2CID 20686075.
внешняя ссылка
- Дезоксицитидин + киназа в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)