ДНК-связывающий белок - DNA-binding protein

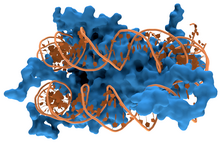


ДНК-связывающие белки находятся белки который имеет ДНК-связывающие домены и, таким образом, имеют конкретную или общую близость к одно- или двухцепочечная ДНК.[3][4][5] Последовательно-специфические ДНК-связывающие белки обычно взаимодействуют с большая канавка из B-ДНК, потому что он раскрывает больше функциональные группы которые определяют базовая пара. Однако есть некоторые известные малая бороздка ДНК-связывающие лиганды, такие как нетропсин,[6] дистамицин, Hoechst 33258, пентамидин, DAPI и другие.[7]
Примеры
Связывание с ДНК белки включают факторы транскрипции который модулировать процесс транскрипции, различные полимеразы, нуклеазы которые расщепляют молекулы ДНК, и гистоны которые участвуют в хромосома упаковка и транскрипция в ядро клетки. ДНК-связывающие белки могут включать такие домены, как цинковый палец, то спираль-поворот-спираль, а лейциновая молния (среди многих других), которые облегчают связывание с нуклеиновой кислотой. Есть и более необычные примеры, такие как активатор транскрипции, такой как эффекторы.
Неспецифические ДНК-белковые взаимодействия
Структурные белки, связывающие ДНК, являются хорошо изученными примерами неспецифических ДНК-белковых взаимодействий. Внутри хромосом ДНК находится в комплексах со структурными белками. Эти белки организуют ДНК в компактную структуру, называемую хроматин. В эукариоты, эта структура включает связывание ДНК с комплексом небольших основных белков, называемых гистоны. В прокариоты, задействованы несколько типов белков.[8][9] Гистоны образуют дискообразный комплекс, называемый нуклеосома, который содержит два полных витка двухцепочечной ДНК, обернутой вокруг своей поверхности. Эти неспецифические взаимодействия формируются за счет основных остатков в гистонах, образующих ионные связи к кислому сахарно-фосфатному остову ДНК и поэтому в значительной степени не зависят от последовательности оснований.[10] Химическая модификации этих основных аминокислота остатки включают метилирование, фосфорилирование и ацетилирование.[11] Эти химические изменения изменяют силу взаимодействия между ДНК и гистонами, делая ДНК более или менее доступной для факторы транскрипции и изменение скорости транскрипции.[12] Другие неспецифические ДНК-связывающие белки в хроматине включают белки группы высокой подвижности (HMG), которые связываются с изогнутой или искаженной ДНК.[13] Биофизические исследования показывают, что эти архитектурные белки HMG связывают, изгибают и петляют ДНК для выполнения своих биологических функций.[14][15] Эти белки важны для изгиба массивов нуклеосом и их упорядочения в более крупные структуры, образующие хромосомы.[16]
Белки, специфически связывающие одноцепочечную ДНК
Отдельной группой ДНК-связывающих белков являются ДНК-связывающие белки, которые специфически связывают одноцепочечную ДНК. В людях, репликационный белок А является наиболее изученным представителем этого семейства и используется в процессах разделения двойной спирали, включая репликацию ДНК, рекомбинацию и репарацию ДНК.[17] Эти связывающие белки, по-видимому, стабилизируют одноцепочечную ДНК и защищают ее от образования стебель-петли или быть униженным нуклеазы.
Связывание с конкретными последовательностями ДНК
Напротив, другие белки эволюционировали, чтобы связываться с конкретными последовательностями ДНК. Наиболее интенсивно изучаются различные факторы транскрипции, которые являются белками, регулирующими транскрипцию. Каждый фактор транскрипции связывается с одним конкретным набором последовательностей ДНК и активирует или ингибирует транскрипцию генов, которые имеют эти последовательности рядом с их промоторами. Факторы транскрипции делают это двумя способами. Во-первых, они могут связываться с РНК-полимеразой, ответственной за транскрипцию, либо напрямую, либо через другие белки-медиаторы; это определяет местонахождение полимеразы на промоторе и позволяет ей начать транскрипцию.[18] Альтернативно, факторы транскрипции могут связывать ферменты которые модифицируют гистоны на промоторе. Это изменяет доступность матрицы ДНК для полимеразы.[19]
Эти ДНК-мишени могут встречаться по всему геному организма. Таким образом, изменение активности одного типа факторов транскрипции может повлиять на тысячи генов.[20] Таким образом, эти белки часто являются мишенями для преобразование сигнала процессы, которые контролируют реакцию на изменения окружающей среды или клеточная дифференциация и развитие. Специфичность взаимодействия этих факторов транскрипции с ДНК обусловлена множественными контактами белков с краями оснований ДНК, что позволяет им взаимодействовать друг с другом. читать последовательность ДНК. Большинство взаимодействий с основанием происходит в большой бороздке, где основания наиболее доступны.[21] Математические описания связывания белок-ДНК с учетом специфичности последовательности, а также конкурентного и кооперативного связывания белков разных типов обычно выполняются с помощью решетчатые модели.[22] Были предложены вычислительные методы для определения специфичности ДНК-связывающей последовательности, чтобы эффективно использовать многочисленные данные о последовательностях в постгеномную эру.[23]
Взаимодействие белок-ДНК
Взаимодействие белок-ДНК происходит, когда белок связывает молекулу ДНК, часто для регулирования биологическая функция ДНК, обычно выражение из ген. Среди белков, которые связываются с ДНК, есть факторы транскрипции которые активируют или подавляют экспрессию генов путем связывания с мотивами ДНК и гистоны которые составляют часть структуры ДНК и менее специфично с ней связываются. Также белки, которые восстановить ДНК такие как урацил-ДНК гликозилаза тесно взаимодействовать с ним.
Как правило, белки связываются с ДНК в большая канавка; однако бывают исключения.[24] Взаимодействие белок-ДНК бывает в основном двух типов: либо специфическое взаимодействие, либо неспецифическое взаимодействие. Недавние эксперименты с одной молекулой показали, что ДНК-связывающие белки подвергаются быстрому повторному связыванию, чтобы связываться в правильной ориентации для распознавания целевого сайта.[25]
дизайн
Создание ДНК-связывающих белков, которые имеют определенный ДНК-связывающий сайт, было важной целью биотехнологии. Цинковый палец белки были разработаны для связывания с определенными последовательностями ДНК, и это является основой нуклеазы цинковых пальцев. Недавно эффекторные нуклеазы, подобные активаторам транскрипции (ТАЛЕНЫ) созданы на основе натуральных белки секретно Ксантомонады бактерии через их система секреции типа III когда они заражают различные завод виды.[26]
Методы обнаружения
Есть много in vitro и in vivo методы, которые полезны для обнаружения взаимодействий ДНК-белок. Ниже перечислены некоторые используемые в настоящее время методы:[27] Анализ сдвига электрофоретической подвижности (EMSA) - это широко распространенный качественный метод исследования белок-ДНК-взаимодействий известных ДНК-связывающих белков.[28][29] ДНК-белок-взаимодействие - иммуноферментный анализ (DPI-ELISA) позволяет качественный и количественный анализ предпочтений связывания ДНК известных белков in vitro.[30][31] Этот метод позволяет анализировать белковые комплексы, которые связываются с ДНК (DPI-Recruitment-ELISA), или подходит для автоматического скрининга нескольких нуклеотидных зондов благодаря стандартному формиату для планшетов ELISA.[32] [33].Анализ следа ДНКазы может быть использован для идентификации конкретных сайтов связывания белка с ДНК при разрешении пар оснований.[34] Иммунопреципитация хроматина используется для определения in vivo Целевые области ДНК известного фактора транскрипции. Этот метод в сочетании с высокопроизводительным секвенированием известен как ChIP-Seq и в сочетании с микрочипы это известно как ЧИП-чип. Одногибридная дрожжевая система (Y1H) используется для определения того, какой белок связывается с конкретным фрагментом ДНК. Бактериальная одногибридная система (B1H) используется для определения того, какой белок связывается с конкретным фрагментом ДНК. Определение структуры с использованием Рентгеновская кристаллография был использован для получения высокодетального атомарного представления взаимодействий белок-ДНК. Помимо этих методов, другие методы, такие как SELEX, PBM (микроматрицы связывания белков), микроматрицы ДНК, DamID, FAIRE или, с недавних пор, используются в DAP-seq. лаборатория для изучения взаимодействия ДНК-белок in vivo и in vitro.
Управление взаимодействиями
Взаимодействия белок-ДНК можно модулировать с помощью таких стимулов, как ионная сила буфера, макромолекулярное скопление,[35] температура, pH и электрическое поле. Это может привести к обратимой диссоциации / ассоциации комплекса белок-ДНК.[36][37]
Смотрите также
- bZIP домен
- ЧИП-экзо
- Сравнение программного обеспечения для моделирования нуклеиновых кислот
- ДНК-связывающий домен
- Спираль-петля-спираль
- Спираль-поворот-спираль
- HMG-коробка
- Лейциновая молния
- Лекситропсин (полусинтетический ДНК-связывающий лиганд)
- Дезоксирибонуклеопротеин
- Программное обеспечение для прогнозирования сайтов взаимодействия белков с ДНК
- РНК-связывающий белок
- Одноцепочечный связывающий белок
- Цинковый палец
использованная литература
- ^ Создано из PDB 1LMB
- ^ Создано из PDB 1RVA
- ^ Трэверс, А. А. (1993). ДНК-белковые взаимодействия. Лондон: Спрингер. ISBN 978-0-412-25990-6.
- ^ Пабо CO, Зауэр RT (1984). «Узнавание белка-ДНК». Анну. Преподобный Biochem. 53 (1): 293–321. Дои:10.1146 / annurev.bi.53.070184.001453. PMID 6236744.
- ^ Дикерсон Р. (1983). «Спираль ДНК и как ее читают». Sci Am. 249 (6): 94–111. Bibcode:1983SciAm.249f..94D. Дои:10.1038 / scientificamerican1283-94.
- ^ Циммер С., Венерт У. (1986). «Неинтеркалирующие ДНК-связывающие лиганды: специфичность взаимодействия и их использование в качестве инструментов в биофизических, биохимических и биологических исследованиях генетического материала». Прог. Биофиз. Мол. Биол. 47 (1): 31–112. Дои:10.1016/0079-6107(86)90005-2. PMID 2422697.
- ^ Дерван ПБ (апрель 1986 г.). «Дизайн последовательности-специфичных ДНК-связывающих молекул». Наука. 232 (4749): 464–71. Bibcode:1986Научный ... 232..464D. Дои:10.1126 / science.2421408. PMID 2421408.
- ^ Sandman K, Pereira S, Reeve J (1998). «Разнообразие прокариотических хромосомных белков и происхождение нуклеосом». Cell Mol Life Sci. 54 (12): 1350–64. Дои:10.1007 / с000180050259. PMID 9893710. S2CID 21101836.
- ^ Дама RT (2005). «Роль нуклеоид-ассоциированных белков в организации и уплотнении бактериального хроматина». Мол. Микробиол. 56 (4): 858–70. Дои:10.1111 / j.1365-2958.2005.04598.x. PMID 15853876.
- ^ Люгер К., Мэдер А., Ричмонд Р., Сарджент Д., Ричмонд Т. (1997). «Кристаллическая структура ядерной частицы нуклеосомы при разрешении 2,8 A». Природа. 389 (6648): 251–60. Bibcode:1997Натура.389..251Л. Дои:10.1038/38444. PMID 9305837. S2CID 4328827.
- ^ Jenuwein T, Allis C (2001). «Перевод гистонового кода». Наука. 293 (5532): 1074–80. CiteSeerX 10.1.1.453.900. Дои:10.1126 / science.1063127. PMID 11498575. S2CID 1883924.
- ^ Ито Т (2003). «Сборка и ремоделирование нуклеосом». Сборка и ремоделирование нуклеосом. Curr Top Microbiol Immunol. Актуальные темы микробиологии и иммунологии. 274. С. 1–22. Дои:10.1007/978-3-642-55747-7_1. ISBN 978-3-642-62909-9. PMID 12596902.
- ^ Томас Дж (2001). «HMG1 и 2: архитектурные ДНК-связывающие белки». Biochem Soc Trans. 29 (Pt 4): 395–401. Дои:10.1042 / BST0290395. PMID 11497996.
- ^ Муругесапиллай, Дивакаран; Макколи, Мика Дж .; Хо, Ран; Нельсон Холт, Молли Х .; Степанянц, Армен; Махер, Л. Джеймс; Israeloff, Nathan E .; Уильямс, Марк К. (2014). «Соединение ДНК и образование петель посредством HMO1 обеспечивает механизм стабилизации хроматина, свободного от нуклеосом». Исследования нуклеиновых кислот. 42 (14): 8996–9004. Дои:10.1093 / нар / gku635. ЧВК 4132745. PMID 25063301.
- ^ Муругесапиллай, Дивакаран; Макколи, Мика Дж .; Махер, Л. Джеймс; Уильямс, Марк К. (2017). «Одномолекулярные исследования белков, изгибающих архитектурную ДНК группы B с высокой подвижностью». Биофизические обзоры. 9 (1): 17–40. Дои:10.1007 / s12551-016-0236-4. ЧВК 5331113. PMID 28303166.
- ^ Гроссчедл Р., Гизе К., Пагель Дж. (1994). «Белки домена HMG: архитектурные элементы сборки нуклеопротеиновых структур». Тенденции Genet. 10 (3): 94–100. Дои:10.1016/0168-9525(94)90232-1. PMID 8178371.
- ^ Iftode C, Даниэли Y, Боровец J (1999). «Репликационный белок А (RPA): эукариотический SSB». Crit Rev Biochem Mol Biol. 34 (3): 141–80. Дои:10.1080/10409239991209255. PMID 10473346.
- ^ Майерс Л., Корнберг Р. (2000). «Медиатор регуляции транскрипции». Анну Рев Биохим. 69 (1): 729–49. Дои:10.1146 / annurev.biochem.69.1.729. PMID 10966474.
- ^ Шпигельман Б, Генрих Р (2004). «Биологический контроль с помощью регулируемых транскрипционных коактиваторов». Ячейка. 119 (2): 157–67. Дои:10.1016 / j.cell.2004.09.037. PMID 15479634. S2CID 14668705.
- ^ Ли З, Ван Калькар С., Ку К., Кавени В., Чжан М., Рен Б. (2003). «Глобальная регуляторная роль транскрипции c-Myc в клетках лимфомы Беркитта». Proc Natl Acad Sci USA. 100 (14): 8164–9. Bibcode:2003ПНАС..100.8164Л. Дои:10.1073 / pnas.1332764100. ЧВК 166200. PMID 12808131.
- ^ Пабо С., Зауэр Р. (1984). «Узнавание белка-ДНК». Анну Рев Биохим. 53 (1): 293–321. Дои:10.1146 / annurev.bi.53.070184.001453. PMID 6236744.
- ^ Тейф В.Б .; Риппе К. (2010). «Статистико-механические решетчатые модели связывания белок-ДНК в хроматине». Журнал физики: конденсированное вещество. 22 (41): 414105. arXiv:1004.5514. Bibcode:2010JPCM ... 22O4105T. Дои:10.1088/0953-8984/22/41/414105. PMID 21386588. S2CID 103345.
- ^ Вонг KC, Чан TM, Пэн C, Ли Y, Zhang Z (2013). «Выявление мотивов ДНК с помощью распространения убеждений». Исследования нуклеиновых кислот. 41 (16): e153. Дои:10.1093 / nar / gkt574. ЧВК 3763557. PMID 23814189.
- ^ Бьюли CA, Гроненборн AM, Clore GM (1998). «Архитектурные белки, связывающие малые бороздки: структура, функция и распознавание ДНК». Annu Rev Biophys Biomol Struct. 27: 105–31. Дои:10.1146 / annurev.biophys.27.1.105. ЧВК 4781445. PMID 9646864.
- ^ Ганджи, Махипал; Доктер, Маргрит; Ле Грис, Стюарт Ф. Дж .; Аббонданциери, Элио А. (30 сентября 2016 г.). «ДНК-связывающие белки исследуют множественные локальные конфигурации во время стыковки посредством быстрого повторного связывания». Исследования нуклеиновых кислот. 44 (17): 8376–8384. Дои:10.1093 / нар / gkw666. ISSN 0305-1048. ЧВК 5041478. PMID 27471033.
- ^ Кларк К.Дж., Войтас Д.Ф., Эккер СК (сентябрь 2011 г.). «СКАЗКА о двух нуклеазах: нацеливание гена на массы?». Данио. 8 (3): 147–9. Дои:10.1089 / zeb.2011.9993. ЧВК 3174730. PMID 21929364.
- ^ Цай Й.Х., Хуан Х. (июль 2012 г.). «Достижения в изучении взаимодействия белок-ДНК». Аминокислоты. 43 (3): 1141–6. Дои:10.1007 / s00726-012-1377-9. PMID 22842750. S2CID 310256.
- ^ Фрид М., Кротерс Д.М. (1981). «Равновесия и кинетика взаимодействий lac-репрессор-оператор при электрофорезе в полиакриламидном геле». Нуклеиновые кислоты Res. 9 (23). Дои:10.1093 / nar / 9.23.6505. PMID 6275366.
- ^ Гарнер М.М., Ревзин А (1981). «Метод гель-электрофореза для количественной оценки связывания белков с конкретными участками ДНК: применение к компонентам системы регуляции лактозного оперона Escherichia coli». Нуклеиновые кислоты Res. 9 (13). Дои:10.1093 / nar / 9.13.3047. PMID 6269071.
- ^ Бренд LH, Кирхлер Т., Хаммель С., Чабан С., Ванке Д. (2010). «DPI-ELISA: быстрый и универсальный метод определения связывания факторов транскрипции растений с ДНК in vitro». Растительные методы. 25 (6). Дои:10.1186/1746-4811-6-25. PMID 21108821.
- ^ Фишер С.М., Бёзер А., Хирш Дж. П., Ванке Д. (2016). «Количественный анализ взаимодействия белок-ДНК с помощью qDPI-ELISA». Методы Мол биол. (1482): 49–66. Дои:10.1007/978-1-4939-6396-6_4. PMID 27557760.
- ^ Хеккер А., Бренд LH, Питер С., Симончелло Н., Килиан Дж., Хартер К., Годен В., Ванке Д. (2015). «GAGA-связывающий фактор Arabidopsis BASIC PENTACYSTEINE6 привлекает компонент POLYCOMB-REPRESSIVE COMPLEX1, КАК ГЕТЕРОХРОМАТИН БЕЛК1, к мотивам ДНК GAGA». Физиология растений. 163 (3): 1013–1024. Дои:10.1104 / стр.15.00409. PMID 26025051.
- ^ Brand LH, Henneges C, Schüssler A, Kolukisaoglu HÜ, Koch G, Wallmeroth N, Hecker A, Thurow K, Zell A, Harter K, Wanke D (2013). «Скрининг взаимодействий белок-ДНК с помощью автоматизированного ELISA взаимодействия ДНК-белок». PLoS One. 8 (10). Дои:10.1371 / journal.pone.0075177. PMID 24146751.
- ^ Галас DJ, Шмитц А. (1978). «ДНК-следы: простой метод определения специфичности связывания белок-ДНК». Нуклеиновые кислоты Res. 5 (9): 3157–3170. Дои:10.1093 / nar / 5.9.3157. PMID 212715.
- ^ Ганджи, Махипал; Доктер, Маргрит; Грайс, Стюарт Ф.Дж. Ле; Аббонданциери, Элио А. (30 сентября 2016 г.). «ДНК-связывающие белки исследуют множественные локальные конфигурации во время стыковки посредством быстрого повторного связывания». Исследования нуклеиновых кислот. 44 (17): 8376–8384. Дои:10.1093 / нар / gkw666. ISSN 0305-1048. ЧВК 5041478. PMID 27471033.
- ^ Хианик Т., Ван Дж. (2009). «Электрохимические аптасенсоры - последние достижения и перспективы». Электроанализ. 21 (11): 1223–1235. Дои:10.1002 / elan.200904566.
- ^ Госай А. и др. (2016). «Связывание / расцепление комплекса тромбин-аптамер человека, контролируемое электрическим стимулом». Sci. Представитель. 6: 37449. Bibcode:2016НатСР ... 637449Г. Дои:10.1038 / srep37449. ЧВК 5118750. PMID 27874042.
внешние ссылки
- Связывание белок-ДНК: данные, инструменты и модели (аннотированный список, постоянно обновляемый)
- Морское ушко инструмент для моделирования взаимодействий ДНК-лиганд.
- DBD база данных предсказанных факторов транскрипции Использует тщательно подобранный набор ДНК-связывающих доменов для прогнозирования факторов транскрипции во всех полностью секвенированных геномах.
- Связывание с ДНК + белки в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
