Мифамуртид - Mifamurtide
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Mepact |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | внутривенный липосомальный настой более одного часа |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Биодоступность | Нет данных |
| Устранение период полураспада | минут (в плазме) 18 часов (терминал) |
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| Химические и физические данные | |
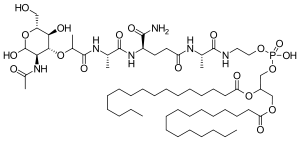
| Формула | C59ЧАС109N6О19п |
| Молярная масса | 1237.518 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Мифамуртид (торговое наименование Mepact, проданный Такеда ) является лекарством против остеосаркома, своего рода кость рак в основном поражает детей и молодых людей, что более чем в половине случаев приводит к летальному исходу. Препарат был одобрен в Европе в марте 2009 года.
Медицинское использование
Мифамуртид показан для лечения тяжелых, неметастазирующий, операбельный остеосаркома после полного хирургического удаления у детей, подростков и молодых людей в возрасте от 2 до 30 лет.[1][2][3] Остеосаркома диагностируется примерно у 1000 человек в Европе и США в год, в основном в возрасте до 30 лет.[4] Препарат применяют в комбинации с послеоперационным, мультиагентным химиотерапия убить оставшиеся раковые клетки и повысить шансы пациента на выживание.[2]
В фазе III клиническое испытание примерно у 800 пациентов с впервые диагностированной остеосаркомой мифамуртид комбинировали с химиотерапевтическими средствами. доксорубицин и метотрексат, с или без цисплатин и ифосфамид. В смертность можно снизить на 30% по сравнению с химиотерапией плюс плацебо. Через шесть лет после лечения 78% пациентов были живы. Это равняется абсолютному снижению риска на 8%.[1]
Побочные эффекты
В клиническом исследовании мифамуртид давали 332 пациентам (половина из которых были в возрасте до 16 лет), и было обнаружено, что большинство побочных эффектов имеют характер от легкой до умеренной степени. У большинства пациентов при последующем введении наблюдается меньше побочных эффектов.[5][6] Общие побочные эффекты включают: высокая температура (около 90%), рвота, усталость и тахикардия (около 50%), инфекции, анемия, анорексия, Головная боль, понос и запор (>10%).[1][7]
Взаимодействия
- Теоретические соображения подсказывают ингибиторы кальциневрина подобно циклоспорин и такролимус могут взаимодействовать с мифамуртидом из-за их воздействия на макрофаги.
- Высокая доза НПВП заблокировать механизм мифамуртида in vitro.
Следовательно, сочетание мифамуртида с этими видами препаратов противопоказано. Однако мифамуртид можно назначать одновременно с низкими дозами НПВП. Нет доказательств того, что мифамуртид взаимодействует с изучаемыми химиотерапевтическими средствами или с цитохром P450 система.[8]
Фармакология
Механизм действия
Мифамуртид - это полностью синтетическое производное мурамиловый дипептид (MDP), наименьший природный иммуностимулирующий компонент клеточных стенок из Микобактерии разновидность. Он обладает иммуностимулирующим действием, аналогичным натуральному MDP, с преимуществом более длительного периода полужизни в плазме.
NOD2 это рецептор распознавания образов который встречается в нескольких видах белые кровяные клетки, в основном моноциты и макрофаги. Он распознает мурамилдипептид, компонент клеточной стенки бактерии. Мифамуртид имитирует бактериальную инфекцию, связываясь с NOD2, активируя лейкоциты. Это приводит к увеличению производства TNF-α, интерлейкин 1, интерлейкин 6, интерлейкин 8, интерлейкин 12, и другие цитокины, а также ICAM-1. Активированные белые клетки атакуют раковые клетки, но не, по крайней мере, in vitro, другие ячейки.[9]
Фармакокинетика
После применения липосомальный инфузии, препарат выводится из плазмы в течение минут и концентрируется в легких, печени, селезенка, носоглотка, и щитовидная железа. Период полувыведения составляет 18 часов. У пациентов, получавших второй курс лечения через 11–12 недель, эффектов накопления не наблюдалось.[10]
Химия

Мифамуртид представляет собой мурамилтрипептид фосфатидилэтаноламин (MTP-PE), синтетический аналог мурамилдипептида. Боковые цепи молекулы придают ей более длинный период полувыведения чем натуральное вещество. Вещество применяется в капсулах. липосомы (L-MTP-PE). Быть фосфолипид, он накапливается в липидный бислой липосом в настое.[11]
Синтез
Один из методов синтеза (показанный первым) основан на N, N '-дициклогексилкарбодиимид (DCC) помогли этерификация из N-ацетилмурамил-L-аланил-D-изоглутаминил -L-аланин с N-гидроксисукцинимид с последующей конденсацией с 2-аминоэтил-2,3-дипальмитоил глицерилфосфорная кислота в триэтиламин (Et3N).[12] Другой подход (показан вторым) использует N-ацетилмурамил-L-аланил-D-изоглутамин, гидроксисукцинимид и аланил-2-аминоэтил-2,3-дипальмитоилглицерилфосфорная кислота;[13] то есть аланин вводится на втором этапе вместо первого.
 |  |
История
Препарат был изобретен Ciba-Geigy (сейчас же Новартис ) в начале 1980-х и продал Дженнер Биотерапия в 1990-е гг. В 2003 г. IDM Pharma купил права и развил дальше.[1] IDM Pharma была приобретена Takeda вместе с мифамуртидом в июне 2009 года.[14]
Мифамуртид уже был предоставлен орфанный препарат статус по Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в 2001 г., а Европейское агентство по лекарствам (EMA) последовала в 2004 году. Она была одобрена в 27 Евросоюз Государства-члены, а также Исландия, Лихтенштейн и Норвегия - централизованной регистрационной лицензией в марте 2009 года. В 2007 году FDA отказало в одобрении препарата.[15][16] Мифамуртид имеет лицензию EMA с марта 2009 года.[17]
Рекомендации
- ^ а б c d «Мифамуртид: CGP 19835, CGP 19835A, L-MTP-PE, липосомальный MTP-PE, MLV 19835A, MTP-PE, мурамилтрипептид фосфатидилэтаноламин». Лекарства в исследованиях и разработках. 9 (2): 131–5. 2008. Дои:10.2165/00126839-200809020-00007. PMID 18298131.
- ^ а б EMA (06.03.2009). «Mepact: Информация о продукте. Приложение I: Обзор характеристик продукта» (PDF). п. 2. Получено 2009-11-12.
- ^ EMA (06.05.2009). «Mepact: Отчет об оценке общественности в Европе. Резюме для общественности» (PDF). п. 1. Получено 2016-10-06.
- ^ Мейерс PA (август 2009 г.). «Мурамилтрипептид (мифамуртид) для лечения остеосаркомы». Экспертный обзор противоопухолевой терапии. 9 (8): 1035–49. Дои:10.1586 / эра.09.69. PMID 19671023. S2CID 29512704.
- ^ Meyers PA, Schwartz CL, Krailo MD, Healey JH, Bernstein ML, Betcher D, et al. (Февраль 2008 г.). «Остеосаркома: добавление мурамилтрипептида к химиотерапии улучшает общую выживаемость - отчет Детской онкологической группы». Журнал клинической онкологии. 26 (4): 633–8. Дои:10.1200 / JCO.2008.14.0095. PMID 18235123.
- ^ Meyers PA, Schwartz CL, Krailo M, Kleinerman ES, Betcher D, Bernstein ML, et al. (Март 2005 г.). «Остеосаркома: рандомизированное проспективное исследование добавления ифосфамида и / или мурамилтрипептида к цисплатину, доксорубицину и метотрексату в высоких дозах». Журнал клинической онкологии. 23 (9): 2004–11. Дои:10.1200 / JCO.2005.06.031. PMID 15774791.
- ^ (EMA 2009, стр. 5–7)
- ^ (EMA 2009, п. 4)
- ^ (EMA 2009, стр. 7–8)
- ^ (EMA 2009, п. 8)
- ^ Фидлер И.Дж., Сон С., Фоглер В.Е., Смит Д., Браун Д.Г., Тарксай Л., Гислер Р.Х., Шройт А.Дж. (1982). «Эффективность липосом, содержащих липофильное производное мурамилдипептида, для активации опухолевых свойств альвеолярных макрофагов in vivo». Журнал иммунотерапии. 1 (1): 43–55.
- ^ Проус Дж, Кастанер Дж (1989). «ЭНВ 2-3 / МТП-ПЭ». Наркотики Fut. 14 (3): 220. Дои:10.1358 / dof.1989.014.03.85085.
- ^ Брандиш Д.Е., Уэйд Р. (1985). «Синтез N- [2-3H] ацетил-D-мурамил-L-аланил-D-изо-глутамил-L-аланил-2- (1 ', 2'-дипальмитоил-sn-глицеро-3'-фосфорила) этиламид с высокой удельной радиоактивностью ». J Label Compd Radiopharm. 22 (1): 29–35. Дои:10.1002 / jlcr.2580220105.
- ^ «Первое лечение, улучшающее выживаемость за 20 лет, теперь доступно для пациентов с остеосаркомой (раком костей)». Такеда. Ноябрь 2009 г.. Получено 23 марта 2010.
- ^ "MEPACT (Мифамуртид, L-MTP-PE) IDM Pharma получает одобрение в Европе для лечения пациентов с неметастатической резектабельной остеосаркомой". PR Newswire. 2009-03-09. Получено 2009-11-12.
- ^ «IDM Pharma получила письмо об отказе в одобрении Мифамуртида для лечения остеосаркомы». Медицинские новости. 2007-08-28. Получено 2009-11-12.
- ^ Mepact для профессионалов здравоохранения, получено 2009-11-12
