Медицинский прибор - Medical device



А медицинский прибор любое устройство, предназначенное для использования в медицинских целях. Медицинские устройства приносят пользу пациентам, помогая поставщикам медицинских услуг диагностировать и лечить пациентов и помогать пациентам преодолевать болезни или недомогания, улучшая их качество жизни. Значительный потенциал для опасности присущи при использовании устройства в медицинских целях, и, следовательно, медицинские устройства должны быть подтверждены безопасностью и эффективностью с разумной гарантией, прежде чем регулирующие органы разрешат продажу устройства в своей стране. Как правило, по мере увеличения риска, связанного с устройством, количество тестов, необходимых для установления безопасности и эффективности, также увеличивается. Кроме того, по мере увеличения связанного риска потенциальная польза для пациента также должна увеличиваться.
Открытие того, что считалось бы медицинским устройством по современным стандартам, датируется ок. 7000 г. до н.э. в Белуджистан где неолитические дантисты использовали кремневые сверла и тетивы.[1] Изучение археологии и римской медицинской литературы также указывает на то, что многие типы медицинских устройств широко использовались во времена Древнего Рима.[2] В Соединенных Штатах медицинские устройства регулировались только после принятия Федерального закона о пищевых продуктах, лекарствах и косметических средствах (FD&C Act) в 1938 году. Позже, в 1976 году, Поправки о медицинских устройствах к Закону о FD&C установили регулирование и надзор за медицинскими устройствами, которые мы знаем сегодня в Соединенных Штатах.[3] Регулирование медицинских устройств в Европе в том виде, в каком мы его знаем сегодня, вступило в силу в 1993 году в соответствии с тем, что вместе известно как Директива по медицинскому оборудованию (MDD). 26 мая 2017 г. Регулирование медицинского оборудования (MDR) заменил MDD.
Медицинские устройства различаются как по назначению, так и по показаниям. Примеры варьируются от простых устройств с низким уровнем риска, таких как депрессоры языка, медицинские термометры, одноразовые перчатки, и совки к сложным устройствам с высоким риском, которые имплантируются и поддерживают жизнь. Одним из примеров устройств высокого риска являются устройства с встроенное программное обеспечение таких как кардиостимуляторы, и которые помогают в проведении медицинское обследование, имплантаты, и протезы. Такие сложные изделия, как корпуса для кохлеарных имплантатов, производятся с помощью процессов глубокой вытяжки и мелкой вытяжки. Дизайн медицинских устройств составляет основной сегмент в области биомедицинская инженерия.
В 2006 году мировой рынок медицинского оборудования достиг примерно 209 миллиардов долларов США.[4] и оценивалась в размере от 220 до 250 миллиардов долларов США в 2013 году.[5] США контролируют около 40% мирового рынка, за ними следуют Европа (25%), Япония (15%) и остальной мир (20%). Хотя в совокупности Европа имеет большую долю, Япония занимает вторую по величине долю рынка страны. Наибольшие доли рынка в Европе (в порядке размера доли рынка) принадлежат Германии, Италии, Франции и Великобритании. Остальной мир состоит из таких регионов, как (в произвольном порядке) Австралия, Канада, Китай, Индия и Иран. В этой статье обсуждается, что представляет собой медицинское устройство в этих различных регионах, и на протяжении всей статьи эти регионы будут обсуждаться в порядке их доли на мировом рынке.
История

Определение
Трудно дать глобальное определение медицинского устройства, поскольку существует множество регулирующих органов по всему миру, контролирующих маркетинг медицинских устройств. Хотя эти органы часто сотрудничают и обсуждают определение в целом, есть тонкие различия в формулировках, которые не позволяют глобальная гармонизация определения медицинского устройства, поэтому соответствующее определение медицинского устройства зависит от региона. Часто часть определения медицинского устройства предназначена для различения медицинских устройств и наркотики, так как нормативные требования у них разные. Определения также часто признают Диагностика in vitro в качестве подкласса медицинских изделий, а аксессуары как медицинское оборудование.
Определения по регионам
США (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов)
Раздел 201 (h) Федерального закона о пищевых продуктах, лекарствах и косметических средствах (FD&C)[6] определяет устройство как «инструмент, устройство, приспособление, машину, приспособление, имплант, реагент in vitro или другой аналогичный или связанный предмет, включая составную часть или аксессуар, который:
- признанный в официальном Национальный формуляр, или Фармакопея США, или любое дополнение к ним
- Предназначен для использования при диагностике заболеваний или других состояний, или для лечения, смягчения, лечения или предотвращения заболеваний у человека или других животных, или же
- Предназначен для воздействия на структуру или любую функцию тела человека или других животных, и
который не достигает своих основных предполагаемых целей за счет химического воздействия внутри или на теле человека или других животных и который не зависит от метаболизма для достижения своих основных предполагаемых целей. Термин «устройство» не включает программные функции, исключенные в соответствии с разделом 520 (o) ».
Евросоюз
Согласно статье 1 Директивы Совета 93/42 / EEC,[7] «медицинское устройство» означает любой «инструмент, аппарат, приспособление, программное обеспечение, материал или другое изделие, используемое по отдельности или в комбинации, включая программное обеспечение, предназначенное его производителем для использования специально для диагностических и / или терапевтических целей и необходимое для его надлежащего использования. приложение, предназначенное производителем для использования людьми с целью:
- диагностика, профилактика, мониторинг, лечение или облегчение заболевания,
- диагностика, мониторинг, лечение, облегчение или компенсация травмы или инвалидности,
- исследование, замена или изменение анатомии или физиологического процесса,
- контроль зачатия,
и которое не достигает своего основного предполагаемого действия в организме человека или на нем фармакологическими, иммунологическими или метаболическими средствами, но которое может поддерживаться в его функции такими средствами »;
Правовые рамки
На основе Новый подход, правила, касающиеся безопасности и характеристик медицинских устройств, были согласованы в ЕС в 1990-х годах. В Новый подход, как определено в резолюции Европейского совета от мая 1985 г.,[8] представляет собой инновационный способ технической гармонизации. Он направлен на устранение технических барьеров в торговле и устранение связанной с этим неопределенности для экономических операторов, чтобы облегчить свободное перемещение товаров внутри ЕС.
Основная правовая база состоит из трех директив:
- Директива 90/385 / EEC относительно активных имплантируемых медицинских устройств
- Директива 93/42 / EEC о медицинских устройствах
- Директива 98/79 / EC относительно in vitro диагностические медицинские устройства (до 2022 года Регламент по диагностике in vitro (IVDR) заменит действующую Директиву ЕС по диагностике in vitro (98/79 / EC)).
Они нацелены на обеспечение высокого уровня защиты здоровья и безопасности человека и надлежащего функционирования Единого рынка. Эти три основные директивы со временем были дополнены несколькими модифицирующими и имплементирующими директивами, включая последний технический пересмотр, внесенный Директивой 2007/47 EC.[9]
Правительство каждого государства-члена должно назначить компетентный орган отвечает за медицинские устройства. В компетентный орган (CA) - это орган, уполномоченный действовать от имени государства-члена, чтобы гарантировать, что правительство государства-члена транспонирует требования директив по медицинскому оборудованию в национальное законодательство и применяет их. СА подчиняется министру здравоохранения государства-члена. СА в одном государстве-члене не имеет юрисдикции в другом государстве-члене, но обменивается информацией и пытается достичь общих позиций.
В Великобритании, например, Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA) действует как центр сертификации. В Италии это Ministero Salute (Министерство здравоохранения). Медицинское оборудование не следует путать с лекарственные средства. В ЕС все медицинские устройства должны иметь маркировку Знак CE. Соответствие медицинского изделия среднего или высокого риска применимым нормам также оценивается внешней организацией, Уполномоченный орган, прежде чем его можно будет разместить на рынке.
В сентябре 2012 года Европейская комиссия предложила новое законодательство, направленное на повышение безопасности, отслеживаемости и прозрачности.[10] Постановление было принято в 2017 году.
Будущая основная нормативно-правовая база состоит из двух положений:
- В Регулирование медицинского оборудования (MDR (ЕС) 2017/745)
- Положение о медицинских изделиях для диагностики in vitro (IVDR (ЕС) 2017/746)
Япония
Пункт 4 статьи 2 Закон о фармацевтических делах (PAL)[11] определяет медицинские устройства как «инструменты и устройства, предназначенные для использования в диагностике, лечении или профилактике заболеваний человека или других животных; предназначенные для воздействия на структуру или функции тела человека или других животных».
Остальной мир
Канада

Термин «медицинское устройство», как он определен в Закон о пищевых продуктах и лекарствах, представляет собой «любое изделие, инструмент, устройство или приспособление, включая любой их компонент, часть или аксессуар, произведенное, проданное или представленное для использования в: диагностике, лечении, смягчении или предотвращении заболевания, расстройства или ненормального физического состояния или его симптомы у человека; восстановление, исправление или изменение функций организма или структуры тела человека; диагностика беременности у человека; или уход за человеком во время беременности, а также во время и после родов ребенка, включая уход за ребенком. Он также включает противозачаточное устройство, но не включает лекарство ".[12]
Термин охватывает широкий спектр медицинских или медицинских инструментов, используемых для лечения, смягчения, диагностики или предотвращения заболевания или ненормального физического состояния. Министерство здравоохранения Канады проверяет медицинские устройства, чтобы оценить их безопасность, эффективность и качество, прежде чем разрешить их продажу в Канаде.[13] Согласно Закону, медицинское устройство не включает устройства, предназначенные для использования с животными ».[14]
Регулирование и надзор
Классификация рисков
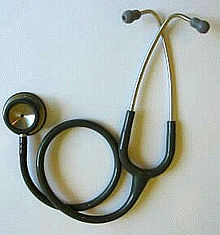
Регулирующие органы признают различные классы медицинских изделий в зависимости от их потенциального вреда при неправильном использовании, сложности конструкции и характеристик их использования. Каждая страна или регион определяет эти категории по-разному. Власти также признают, что некоторые устройства предоставляются в сочетании с лекарствами, и регулирование этих комбинированные продукты учитывает этот фактор.
Классификация медицинских устройств на основе их риска необходима для обеспечения безопасности пациентов и персонала, одновременно облегчая маркетинг медицинских продуктов. Установив разные классификации рисков, устройства с более низким уровнем риска, например стетоскоп или депрессор языка, не должны проходить тот же уровень тестирования, что и устройства с более высоким уровнем риска, такие как искусственные кардиостимуляторы. Установление иерархии классификации рисков позволяет регулирующим органам обеспечивать гибкость при проверке медицинских изделий.
Классификация по регионам
Соединенные Штаты
Эта секция дубликаты объем других статей, конкретно, Производство медицинского оборудования. (Март 2019 г.) |
Под Закон о пищевых продуктах, лекарствах и косметических средствах, Соединенные штаты. Управление по контролю за продуктами и лекарствами распознает три класса медицинских изделий в зависимости от уровня контроля, необходимого для обеспечения безопасности и эффективности.[15]
- I класс
- II класс
- III класс
Процедуры классификации описаны в Свод федеральных правил, Раздел 21, часть 860 (обычно известный как 21 CFR 860).[16]
Устройства класса I подлежат наименьшему нормативному контролю и не предназначены для поддержки или поддержания жизни или играют существенную роль в предотвращении ухудшения здоровья человека и могут не представлять необоснованного риска заболевания или травмы.[17] Примеры устройств класса I включают эластичные повязки, смотровые перчатки и ручные хирургические инструменты.[18]
На устройства класса II распространяются особые требования к маркировке, обязательные стандарты производительности и постмаркетинговое наблюдение.[18] Примеры устройств класса II включают иглы для акупунктуры, инвалидные коляски с электроприводом, инфузионные насосы, очистители воздуха, хирургические простыни, стереотаксические навигационные системы и хирургических роботов.[15][18][19][20][21]
К устройствам класса III обычно относятся те, которые поддерживают или поддерживают жизнь человека, имеют существенное значение для предотвращения ухудшения здоровья человека или представляют потенциальный, необоснованный риск заболевания или травмы и требуют предварительное одобрение.[18][15] Примеры устройств класса III включают имплантируемый кардиостимулятор, генераторы импульсов, диагностические тесты на ВИЧ, автоматические внешние дефибрилляторы и внутрикостные имплантаты.[18]
Европейский союз (ЕС) и Европейская ассоциация свободной торговли (EFTA)
Классификация медицинских изделий в Европейском Союзе изложена в Статье IX Директивы Совета 93/42 / EEC и Приложении VIII к Регулирование медицинского оборудования ЕС. В основном существует четыре класса: от низкого риска до высокого риска.
- Класс I (включая стерильные I, I с функцией измерения и многоразовые хирургические инструменты класса I)
- Класс IIa
- Класс IIb
- III класс
Разрешение на медицинское оборудование гарантируется Декларацией соответствия. Эта декларация выдается самим производителем, но для продуктов классов Is, Im, Ir, IIa, IIb или III она должна быть подтверждена Сертификат соответствия выпущенный Уполномоченный орган. Уполномоченный орган - это государственная или частная организация, которая была аккредитована для подтверждения соответствия устройства Европейской директиве. Медицинские изделия, относящиеся к классу I (при условии, что они не требуют стерилизации или не измеряют функцию), могут продаваться исключительно путем самосертификации.
Европейская классификация зависит от правил, касающихся продолжительности контакта медицинского устройства с телом, инвазивного характера, использования источника энергии, воздействия на центральную циркуляцию или нервную систему, диагностического воздействия или включения лекарственного средства. Сертифицированные медицинские изделия должны иметь Знак CE на упаковке, вкладках-вкладышах и т. д. Эти упаковки должны также содержать согласованные пиктограммы и EN стандартизированные логотипы для обозначения основных функций, таких как инструкции по применению, срок годности, производитель, стерильность, недопустимость повторного использования и т. д.
В ноябре 2018 г. Федеральный административный суд Швейцарии решили, что приложение Sympto, используемое для анализа менструального цикла женщины, является медицинским устройством, поскольку оно рассчитывает окно фертильности для каждой женщины, используя личные данные. Производитель Sympto-Therm Foundation утверждал, что это был дидактический, а не медицинский процесс. суд постановил, что приложение является медицинским устройством, если оно будет использоваться для каких-либо медицинских целей, предусмотренных законом, и создает или изменяет информацию о здоровье путем расчетов или сравнения, предоставляя информацию об отдельном пациенте.[22]
Япония
Медицинские изделия (за исключением диагностики in vitro) в Японии подразделяются на четыре класса в зависимости от степени риска:[11]
- I класс
- II класс
- III класс
- IV класс
Классы I и II различают устройства с крайне низким и низким уровнем риска. Классы III и IV, среднего и высокого риска соответственно, относятся к медицинским изделиям с строгим и специально контролируемым контролем. У диагностики in vitro есть три классификации риска.[23]
Остальной мир
Для остальных регионов мира классификации рисков в целом аналогичны классификации рисков США, Европейского Союза и Японии или представляют собой вариант, сочетающий две или более из трех классификаций рисков стран.
Австралия
Классификация медицинских изделий в Австралии изложена в разделе 41BD Закона о терапевтических товарах 1989 г. и Положении 3.2 Правил о лечебных товарах 2002 г., под контролем Управление терапевтических товаров. Как и в классификации ЕС, они ранжируются в несколько категорий в порядке возрастания риска и соответствующего необходимого уровня контроля. Различные правила определяют категорию устройства[24]
| Классификация | Уровень риска |
|---|---|
| I класс | Низкий |
| Класс I - измерительный или Класс I - поставляется стерильным или класс IIa | Низкий - средний |
| Класс IIb | Средней высоты |
| III класс | Высоко |
| Активные имплантируемые медицинские устройства (AIMD) | Высоко |
Канада

Бюро медицинского оборудования Министерство здравоохранения Канады распознает четыре класса медицинских изделий в зависимости от уровня контроля, необходимого для обеспечения безопасности и эффективности изделия. Устройства класса I представляют наименьший потенциальный риск и не требуют лицензии. Устройства класса II требуют декларации производителя о безопасности и эффективности, в то время как устройства класса III и IV представляют больший потенциальный риск и подлежат тщательной проверке.[13] Руководство по классификации устройств опубликовано Министерством здравоохранения Канады.[25]
Канадские классы медицинских устройств соответствуют устройствам Директивы Европейского Совета 93/42 / EEC (MDD):[25]
- Класс IV (Канада) в целом соответствует Классу III (ECD),
- Класс III (Канада) в целом соответствует Классу IIb (ECD),
- Класс II (Канада) в целом соответствует Классу IIa (ECD) и
- Класс I (Канада) в целом соответствует Классу I (ECD)
Примеры включают хирургические инструменты (класс I), контактные линзы и ультразвуковые сканеры (класс II), ортопедические имплантаты и гемодиализ машины (класс III), и кардиостимуляторы (Класс IV).[26]
Иран
Иран производит около 2000 видов медицинских устройств и медицинских принадлежностей, таких как бытовая техника, стоматологические принадлежности, одноразовые стерильные медицинские изделия, лабораторное оборудование, различные биоматериалы и зубные имплантаты. 400 медицинских изделий производятся с классом риска C и D, и все они лицензированы Министерством здравоохранения Ирана с точки зрения безопасности и производительности в соответствии со стандартами ЕС.
Некоторые иранские медицинские устройства производятся в соответствии с Евросоюз стандарты.
Некоторые производители в Иране экспортируют медицинские устройства и расходные материалы, соответствующие требованиям Евросоюз стандарты для стран-кандидатов, включая 40 азиатских и европейских стран.
Некоторые иранские производители экспортируют свою продукцию в зарубежные страны.[27]
Проблемы стандартизации и регулирования
В ISO Стандарты для медицинских изделий охватываются ICS 11.100.20 и 11.040.01.[28][29] Качество и управление рисками по теме для нормативных целей созывается ISO 13485 и ISO 14971. ISO 13485: 2016 применим ко всем поставщикам и производителям медицинских устройств, компонентов, контрактных услуг и дистрибьюторов медицинских устройств. Стандарт является основой для соответствие нормативным требованиям на местных рынках и на большинстве экспортных рынков.[30][31][32] Кроме того, ISO 9001: 2008 устанавливает приоритет, потому что это означает, что компания участвует в создании новых продуктов. Это требует, чтобы разработка производимых продуктов имела процесс утверждения и набор строгих стандартов качества и записи о разработке до того, как продукт будет распространен.[33] Дополнительные стандарты IEC 60601-1 который предназначен для электрических устройств (как от сети, так и от батарей), EN 45502-1 который предназначен для активных имплантируемых медицинских устройств, и IEC 62304 для медицинского программного обеспечения. В США FDA также опубликовал серию руководств для промышленности по этой теме против 21 CFR 820 Подраздел H - Медицинское оборудование.[34] Подчасть B включает требования к системе качества, важным компонентом которых является: элементы управления дизайном (21 CFR 820.30). Чтобы соответствовать требованиям этих отраслевых нормативных стандартов, все большее число дистрибьюторов медицинского оборудования ставят процесс управления жалобами во главу угла. управление качеством практики. Такой подход дополнительно снижает риски и повышает видимость проблем с качеством.[35]
С конца 1980-х гг.[36] FDA увеличило свое участие в обзоре разработки программного обеспечения для медицинских устройств. Поводом к изменениям стал аппарат лучевой терапии (Терак-25 ), которые вызывали передозировку пациентов из-за ошибок в программном коде.[37] В настоящее время FDA сосредоточено на нормативном надзоре за процессом разработки программного обеспечения для медицинских устройств и тестированием на уровне системы.[38]
Исследование 2011 г. Диана Цукерман и Пол Браун из Национальный центр медицинских исследований, и Доктор Стивен Ниссен из Кливлендская клиника, опубликовано в Архивы внутренней медицины, показали, что большинство медицинских устройств, отозванных за последние пять лет по поводу «серьезных проблем со здоровьем или смерти», были ранее одобрены FDA с использованием менее строгого и более дешевого процесса 510 (k). В некоторых случаях устройства считались настолько низкоопасными, что не подвергались нормативному контролю FDA. Из 113 отозванных устройств 35 были предназначены для сердечно-сосудистых заболеваний.[39] Это исследование было темой слушаний в Конгрессе, посвященных переоценке процедур и надзора FDA.
Исследование 2014 г. Диана Цукерман, Пол Браун и доктор Адити Дас из Национальный центр медицинских исследований, опубликованная в JAMA Internal Medicine, исследовала общедоступные научные данные о медицинских имплантатах, одобренных FDA 510 (k) в 2008–2012 годах. Они обнаружили, что научные доказательства, подтверждающие «существенную эквивалентность» другим устройствам, уже имеющимся на рынке, по закону должны быть общедоступными, но информация была доступна только для 16% случайно выбранных имплантатов, и только 10% предоставили клинические данные. Из более чем 1100 предикатных имплантатов, которым новые имплантаты были практически эквивалентны, только 3% имели какие-либо общедоступные научные доказательства, и только 1% имел клинические доказательства безопасности или эффективности.[40] Исследователи пришли к выводу, что общедоступные научные данные об имплантатах необходимы для защиты здоровья населения.
В 2014–2015 годах было заключено новое международное соглашение - Программа единого аудита медицинских изделий (MDSAP) с пятью странами-участницами: Австралией, Бразилией, Канадой, Японией и США. Целью этой программы было «разработать процесс, позволяющий проводить единый аудит или инспекцию, чтобы гарантировать выполнение нормативных требований к медицинскому оборудованию для всех пяти стран».[41]
В 2017 году исследование доктора Джея Ронкильо и Доктор Диана Цукерман опубликованная в рецензируемом политическом журнале Milbank Quarterly, обнаружила, что электронные медицинские карты и другое программное обеспечение устройств были отозваны из-за опасных для жизни недостатков. В статье указывалось на отсутствие мер защиты от взлома и других угроз кибербезопасности, заявляя, что «действующие правила необходимы, но недостаточны для обеспечения безопасности пациентов путем выявления и устранения опасных дефектов в программном обеспечении, которое в настоящее время присутствует на рынке».[42] Они добавили, что изменения в законодательстве, вытекающие из закона, озаглавленного «Закон о лечении 21 века», «приведут к дальнейшему дерегулированию информационных технологий в сфере здравоохранения, уменьшив меры предосторожности, облегчающие отчетность и своевременный отзыв о некорректном медицинском программном обеспечении, которое может нанести вред пациентам».
В исследовании доктора Стефани Фокс-Роулингс и его коллег из Национального центра исследований в области здравоохранения, опубликованном в 2018 году в журнале Milbank Quarterly, изучается, являются ли исследования, рассмотренные FDA для медицинских устройств высокого риска, безопасными и эффективными для женщин. меньшинства или пациенты старше 65 лет.[43] Закон поощряет разнообразие пациентов в клинических испытаниях, представляемых на рассмотрение FDA, но не требует этого. Исследование показало, что большинство медицинских устройств высокого риска не тестируются и не анализируются, чтобы гарантировать, что они безопасны и эффективны для всех основных демографических групп, особенно расовых и этнических меньшинств и людей старше 65 лет. Следовательно, они не предоставляют информации о безопасности или эффективности. это поможет пациентам и врачам принимать обоснованные решения.
В 2018 году расследование с участием журналистов из 36 стран, которое координировало Международный консорциум журналистов-расследователей (ICIJ) вызвали призывы к реформе в Соединенных Штатах, особенно в отношении 510 (k) существенная эквивалентность процесс;[44] расследование вызвало аналогичные звонки в Великобритании и Европейском союзе.[45]
Стандарты упаковки

Медицинский прибор упаковка строго регулируется. Часто медицинские изделия и изделия стерилизуют в упаковке.[46]Стерильность должна поддерживаться на протяжении всего процесса распространения, чтобы врачи могли сразу же использовать ее. Серия специальных тесты упаковки измерить способность упаковки сохранять стерильность. Соответствующие стандарты включают:
- ASTM F2097 - Стандартное руководство по проектированию и оценке первичной гибкой упаковки для медицинских продуктов
- ASTM F2475-11 - Стандартное руководство по оценке биосовместимости материалов упаковки медицинских устройств[47]
- EN 868 Упаковочные материалы и системы для стерилизуемых медицинских изделий, Общие требования и методы испытаний
- ISO 11607 Упаковка для окончательно стерилизованных медицинских изделий
Тестирование пакетов является частью система менеджмента качества включая верификация и валидация. Важно задокументировать и обеспечить соответствие упаковки нормативным требованиям и требованиям конечного использования. Производственные процессы должны контролироваться и проверяться для обеспечения стабильной работы.[48][49] EN ISO 15223-1 определяет символы, которые могут использоваться для передачи важной информации на упаковке и этикетке.
Стандарты биосовместимости
- ISO 10993 - Биологическая оценка медицинских изделий
Стандарты чистоты
Чистота медицинских устройств стала предметом более пристального внимания с 2000 года, когда компания Sulzer Orthopaedics отозвала несколько тысяч металлических имплантатов бедра, которые содержали производственные остатки.[50] На основе этого события ASTM учредило новую рабочую группу (F04.15.17) для установленных методов испытаний, руководящих документов и других стандартов, касающихся чистоты медицинских устройств. На сегодняшний день эта рабочая группа выпустила два стандарта для постоянных имплантатов: 1. ASTM F2459: Стандартный метод испытаний для извлечения остатков металлических медицинских компонентов и количественного определения с помощью гравиметрического анализа.[51] 2. ASTM F2847: Стандартная практика отчетности и оценки остатков на одноразовых имплантатах.[52] 3. ASTM F3172: Стандартное руководство по валидации процессов очистки, используемых при производстве медицинских устройств.[53]
Кроме того, чистота устройств многократного использования привела к появлению ряда стандартов, в том числе:
- ASTM E2314: Стандартный метод испытаний для определения эффективности процессов очистки многоразовых медицинских инструментов с использованием микробиологического метода (испытание на моделирование использования) »[54]
- ASTM D7225: Стандартное руководство по эффективности очистки крови моющими средствами и моечно-дезинфицирующими средствами[55]
- ASTM F3208: Стандартное руководство по выбору тестовых грунтов для проверки методов очистки многоразовых медицинских устройств[53]
Рабочая группа ASTM F04.15.17 работает над несколькими новыми стандартами, которые включают разработку имплантатов для очистки, выбор и тестирование щеток для очистки устройств многократного использования, а также оценку очистки медицинских устройств, изготовленных аддитивным производством.[56] Кроме того, FDA устанавливает новые рекомендации по переработке многоразовых медицинских устройств, таких как ортоскопические бритвы, эндоскопы и аспирационные трубки.[57] Новое исследование опубликовано в Прикладные интерфейсы и материалы ACS чтобы держать Медицинские инструменты патогенами свободными.[58]
Стандарты безопасности
Дизайн, прототипирование и разработка продукта
Производство медицинских устройств требует определенного уровня контроля процесса в соответствии с классификацией устройства. Более высокий риск; больше элементов управления. На начальном этапе исследований и разработок производители начинают проектировать с учетом технологичности. Это означает, что продукты могут быть более точно спроектированы для производства, что приведет к сокращению времени выполнения заказа, более жестким допускам и более продвинутым спецификациям и прототипам. В наши дни, с помощью САПР или платформ моделирования, работа теперь выполняется намного быстрее, и это также может выступать в качестве инструмента для создания стратегического дизайна, а также в качестве инструмента маркетинга.[59]
Несоблюдение плановых затрат приведет к значительным потерям для организации. Кроме того, в условиях глобальной конкуренции исследования и разработки новых устройств - это не просто необходимость, это императив для производителей медицинских устройств. Реализация нового дизайна может быть очень дорогостоящей, особенно с более коротким жизненным циклом продукта. По мере развития технологий уровень качества, безопасности и надежности, как правило, растет со временем в геометрической прогрессии.[59]
Например, первоначальные модели искусственного водителя ритма сердца были внешними опорными устройствами, которые передают электрические импульсы в сердечные мышцы через электроды на груди. Электроды контактируют с сердцем напрямую через грудную клетку, позволяя импульсам стимуляции проходить через тело. Реципиенты этого обычно страдали инфекцией на входе электродов, что привело к последующему испытанию первого внутреннего кардиостимулятора с электродами, прикрепленными к миокарду посредством торакотомии. Дальнейшие разработки привели к созданию изотопного источника энергии, которого хватило бы на всю жизнь пациента.[страница нужна ]
Программного обеспечения
Мобильные медицинские приложения
С ростом использования смартфонов в медицинской сфере в 2013 году FDA издало мобильные медицинские приложения и защитить пользователей от их непреднамеренного использования, за которым вскоре последовали европейские и другие регулирующие органы. В этом руководстве различаются приложения, подпадающие под действие нормативных требований, на основе маркетинговых заявлений приложений.[60] Включение руководящих принципов на этапе разработки таких приложений можно рассматривать как разработку медицинского устройства; правила должны быть адаптированы, и могут потребоваться предложения для ускоренного утверждения в связи с характером «версий» мобильное приложение разработка.[61][62]
25 сентября 2013 г. FDA выпустило проект руководящего документа по регулированию мобильных медицинских приложений, чтобы уточнить, какие виды мобильных приложений, связанных со здоровьем, не будут регулироваться, а какие -.[63][64]
Информационная безопасность
Медицинские устройства, такие как кардиостимуляторы, инсулиновые помпы, операционная комната мониторы, дефибрилляторы, и хирургические инструменты, включая стимуляторы глубокого мозга, могут обладать способностью передавать жизненно важные информация о здоровье от тела пациента к медицинские работники.[65] Некоторыми из этих устройств можно управлять дистанционно. Это вызвало беспокойство по поводу вопросов конфиденциальности и безопасности,[66] человеческая ошибка, и технические глюки с этой технологией. Хотя лишь несколько исследований изучали подверженность медицинских устройств взлому, риск все же существует.[67][68][69] В 2008 году компьютерные ученые доказали, что кардиостимуляторы и дефибрилляторы можно взломать по беспроводной сети с помощью радиооборудования, антенны и персонального компьютера.[70] Эти исследователи показали, что они могут отключить комбинированный дефибриллятор сердца и кардиостимулятор и перепрограммировать его для нанесения потенциально смертельного разряда или разрядки батареи. Джей Рэдклифф, исследователь безопасности, интересующийся безопасностью медицинских устройств, выразил опасения по поводу безопасности этих устройств. Он поделился своими опасениями на конференции по безопасности Black Hat.[71] Рэдклифф опасается, что устройства уязвимы, и обнаружил, что возможно смертельное нападение на тех, у кого есть инсулиновые помпы и мониторы глюкозы. Некоторые производители медицинских устройств преуменьшают опасность таких атак и утверждают, что продемонстрированные атаки были выполнены квалифицированными исследователями безопасности и вряд ли произойдут в реальном мире. В то же время другие производители попросили экспертов по безопасности программного обеспечения исследовать безопасность своих устройств.[72] Совсем недавно, в июне 2011 года, эксперты по безопасности показали, что, используя легкодоступное оборудование и руководство пользователя, ученый может использовать информацию о системе беспроводной инсулиновой помпы в сочетании с глюкометром. С помощью ПИН-кода устройства ученый мог контролировать дозировку инсулина по беспроводной сети.[73] Ананд Рагхунатан, исследователь в этом исследовании, объясняет, что медицинские устройства становятся все меньше и легче, поэтому их можно легко носить. Обратной стороной является то, что дополнительные функции безопасности увеличивают нагрузку на аккумулятор и размер, а также повышают цены. Д-р Уильям Майзел поделился некоторыми мыслями о мотивации заниматься этим занятием. Мотивация для взлома может включать в себя получение частной информации с целью получения финансовой выгоды или конкурентного преимущества; нанесение ущерба репутации производителя устройства; саботаж; с намерением причинить злоумышленнику финансовую или личную травму или справедливое удовлетворение.[74] Исследователи предлагают несколько мер предосторожности. Один из них - использовать скользящие коды. Другое решение - использовать технологию, называемую «телесной связью», которая использует человеческую кожу в качестве волновода для беспроводной связи. 28 декабря 2016 г. Управление по контролю за продуктами и лекарствами опубликовал свои рекомендации, не имеющие юридической силы в отношении того, как медицинские производители устройств должен поддерживать безопасность подключенных к Интернету устройств.[75][76]
Подобно опасностям, угрозы и уязвимости кибербезопасности не могут быть устранены полностью, но должны контролироваться и снижаться до разумного уровня.[77] При разработке медицинских устройств уровень риска кибербезопасности следует определять на ранней стадии процесса, чтобы установить уязвимость кибербезопасности и подход к управлению (включая набор мер кибербезопасности). элементы управления дизайном ). Используемый подход к проектированию медицинских изделий должен соответствовать Структура кибербезопасности NIST для управления рисками, связанными с кибербезопасностью.
В августе 2013 года FDA выпустило более 20 правил, направленных на повышение безопасности данных в медицинских устройствах,[78] в ответ на растущие риски ограниченного информационная безопасность.
Медицинское оборудование
Эта статья нужны дополнительные цитаты для проверка. (Январь 2008 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
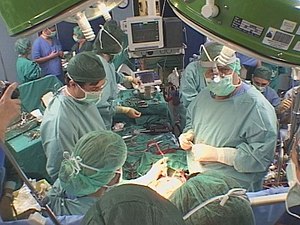
Медицинское оборудование (также известный как вооружение[79]) предназначен для помощи в диагноз, мониторинг или лечение медицинские условия.
Типы
Выделяют несколько основных типов:
- Диагностический оборудование включает медицинская визуализация машины, используемые для помощи в диагностике. Примеры УЗИ и МРТ машины, ДОМАШНИЙ ПИТОМЕЦ и CT сканеры и рентгеновские аппараты.
- Лечебное оборудование включает инфузионные насосы, медицинские лазеры и ЛАСИК хирургические машины.
- Жизненная поддержка оборудование используется для поддерживать телесные функции пациента. Это включает в себя аппараты искусственной вентиляции легких, инкубаторы, анестезиологические аппараты, аппараты искусственного кровообращения, ЭКМО, и аппараты для диализа.
- Медицинские мониторы позволить медицинскому персоналу измерить состояние здоровья пациента. Мониторы могут измерять жизненно важные функции пациента и другие параметры, включая ЭКГ, ЭЭГ, и артериальное давление.
- Медицинское лабораторное оборудование автоматизирует или помогает анализировать кровь, моча, гены, и растворенные газы в крови.
- Диагностическое медицинское оборудование также может использоваться в домашних условиях для определенных целей, например для контроля сахарный диабет сахарный диабет
- Терапевтический: физиотерапевтические аппараты, такие как машины с непрерывным пассивным диапазоном движения (CPM)
Идентификация медицинских устройств была недавно улучшена за счет введения Уникальная идентификация устройства (UDI) и стандартизованное именование с использованием Глобальная номенклатура медицинских устройств (GMDN), которые были одобрены Международным форумом по регулированию медицинских изделий (IMDRF).[80]
А техник по биомедицинскому оборудованию (BMET ) является жизненно важным компонентом системы оказания медицинской помощи. BMET, в основном работающие в больницах, - это люди, отвечающие за техническое обслуживание медицинского оборудования учреждения. BMET в основном действует как интерфейс между врачом и оборудованием.
Пожертвование медицинского оборудования
Есть проблемы, связанные с доступностью медицинского оборудования из глобальное здоровье В перспективе страны с низким уровнем ресурсов не могут получить или позволить себе необходимое жизненно необходимое оборудование. В таких условиях добровольное пожертвование оборудования из стран с высоким или низким уровнем ресурсов - часто используемая стратегия для решения этой проблемы через частных лиц, организации, производителей и благотворительные организации. Однако проблемы с обслуживанием, наличие специалисты по биомедицинскому оборудованию (BMET ), цепочки поставок, обучение пользователей и уместность пожертвований означает, что они часто не приносят желаемых выгод. В ВОЗ По оценкам, 95% медицинского оборудования в странах с низким и средним уровнем доходов (СНСД) импортируется, а 80% его финансируется международными донорами или иностранными правительствами. В то время как до 70% медицинского оборудования в странах Африки к югу от Сахары передается в дар, только 10–30% переданного оборудования становится действующим.[81] Обзор текущей практики и руководящих принципов дарения медицинского оборудования для хирургической и анестезиологической помощи в СНСД продемонстрировал высокий уровень сложности процесса дарения и многочисленные недостатки. Требуется более тесное сотрудничество и планирование между донорами и получателями, а также оценка программ пожертвований и согласованная пропаганда для ознакомления доноров и получателей с существующими руководящими принципами и политиками пожертвования оборудования.[82]
Академические ресурсы
- Журнал "Медицинская, биологическая инженерия и вычислительная техника"
- Журнал "Экспертиза медицинских изделий"
- Журнал клинической инженерии[83]
Университетские научно-исследовательские институты упаковки
- Университет Миннесоты - Центр медицинского оборудования (MDC)
- Стратклайдский университет - Институт медицинских устройств Стратклайда (SIMD)
- Университет Флиндерса - Научно-исследовательский институт медицинских устройств (MDRI)
- Университет штата Мичиган - Школа упаковки (SoP)[84]
- ИИТ Бомбей - Центр биомедицинской инженерии и технологий (инкубационный) (BETiC)
Рекомендации
- ^ «Человек каменного века использовал дрель дантиста». 6 апреля 2006 г. - через news.bbc.co.uk.
- ^ «Хирургические инструменты из Древнего Рима». Библиотека служб здравоохранения Клода Мура Университета Вирджинии. 2007 г.. Получено 16 сентября 2014.
- ^ «История регулирования и надзора за медицинским оборудованием в США». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 2018-11-03. Получено 16 марта 2019.
- ^ «Обзор рынка: мировой рынок медицинского оборудования». Acmite Market Intelligence. 2014 г.. Получено 15 июн 2014.
- ^ Шастри, Винни (2013). Пластмассы в медицинских устройствах: свойства, требования и области применения (2-е изд.). Эльзевир. ISBN 9780323265638.
- ^ "Является ли продукт медицинским устройством?". Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 2018-11-03. Получено 12 марта 2019.
- ^ "Директива Совета 93/42 / EEC от 14 июня 1993 г. о медицинских устройствах". eur-lex.europa.eu. Получено 15 марта 2019.
- ^ "Евр-лекс Европа". 2005. Получено 15 июн 2014.
- ^ «Директива 2007/47 / ec Европейского парламента и совета». Eur-lex Europa. 5 сентября 2007 г.. Получено 15 июн 2014.
- ^ «Пересмотр директив по медицинскому оборудованию». Европейская комиссия. 2013. Получено 15 июн 2014.
- ^ а б Вонг, Джек; Кайю, Раймонд Тонг (27.03.2013). Справочник по вопросам регулирования медицинского оборудования в Азии. ISBN 9789814411226.[страница нужна ]
- ^ "Закон Канады о пищевых продуктах и лекарствах". canada.ca. 2008-07-11.
- ^ а б «Положение о медицинских изделиях СОР / 98-282» (PDF). Министерство юстиции Канады. 16 декабря 2011 г.. Получено 25 августа 2014.
- ^ «Правила медицинского оборудования (SOR / 98-282)». Закон о пищевых продуктах и лекарствах. 2019-03-04. Получено 15 марта 2019.
- ^ а б c «Классификация устройств». Медицинское оборудование. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 2010-10-15.
- ^ «Раздел 21 - Продукты питания и лекарства: Глава i - Управление пищевыми продуктами и лекарствами: Департамент здравоохранения и социальных служб: Подраздел H - Медицинские устройства: Часть 860 Процедуры классификации медицинских устройств». CFR - Свод федеральных правил, раздел 21. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 15 октября 2010.
- ^ «Общий контроль за медицинским оборудованием». Медицинское оборудование. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 2010-10-15.
- ^ а б c d е «Общий и особый контроль». Медицинское оборудование. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 2010-10-15.
- ^ «Часто задаваемые вопросы об акупунктуре». Американский колледж акупунктуры и восточной медицины. Архивировано из оригинал 18 марта 2014 г.
- ^ (PDF) https://www.accessdata.fda.gov/cdrh_docs/pdf18/K180352.pdf. Отсутствует или пусто
| название =(помощь) - ^ {{Хирургическая робототехника: системные приложения и зрение. Весна. 2011 г. ISBN 978-1-4419-1125-4.
- ^ "BVGer-Urteil zur rechtlichen Qualifikation von Gesundheitsapps: Die App" Sympto "ist ein Medizinprodukt". Лексология. 6 ноября 2018 г.. Получено 13 декабря 2018.
- ^ Тайс, Вэл (2015-08-03). Нормативная практика в отношении медицинских изделий: международная перспектива. CRC Press. ISBN 9789814669115.
- ^ TGA, Австралийские нормативные требования для медицинских устройств (ARGMD), версия 1.1, май 2011 г., http://www.tga.gov.au/pdf/devices-argmd-01.pdf
- ^ а б «Руководящий документ - Руководство по системе классификации на основе рисков для диагностических устройств, не связанных с in vitro (не IVDD)». Министерство здравоохранения Канады. 2015-04-23. Получено 2016-04-21.
- ^ «Регулирование медицинских устройств в Канаде: учебник» (PDF). Обновление технологий здравоохранения. № 5. Оттава: Канадское агентство по лекарствам и технологиям в области здравоохранения. 2007-01-12. стр. 2–3. Получено 2016-04-21.
- ^ "Медицинское оборудование Ирана вкратце". IMED.ir. Получено 2018-11-10.
- ^ Международная организация по стандартизации. «11.100.20: Биологическая оценка медицинских изделий». Получено 10 апреля 2009.
- ^ Международная организация по стандартизации. «11.040: Медицинское оборудование». Получено 26 апреля 2009.
- ^ «ISO 13485: 2003 - Медицинские изделия. Системы менеджмента качества. Требования для целей регулирования». www.iso.org. Получено 27 марта 2018.
- ^ Канада, Здоровье (2003-01-02). «Системы качества ISO 13485 - Canada.ca». www.hc-sc.gc.ca. Получено 27 марта 2018.
- ^ «ISO 13485 в США» (PDF). fda.gov. Получено 27 марта 2018.
- ^ «Стандарты ISO, применяемые к производству медицинских устройств» (PDF). МК точность. Получено 27 октября 2014.
- ^ Управление по контролю за продуктами и лекарствами Стандарты (медицинские приборы) Последнее обновление страницы: 11 марта 2014 г. Проверено 18 мая 2014 г.
- ^ «Подготовка системы жалоб / eMDR для предстоящего мандата FDA». Спарта Системс. 18 мая 2015.
- ^ «Хронология Therac-25». Computingcases.org. Получено 2011-01-04.
- ^ Джонс, Пол; Джетли, Рауль; Авраам, Джей (09.02.2010). «Основанный на формальных методах подход к проверке программного обеспечения медицинского устройства». Проектирование встроенных систем. Получено 2016-04-21.
- ^ FDA (08.09.2010). «Исследование безопасности программного обеспечения инфузионного насоса в FDA». FDA. Получено 2010-09-09.
- ^ Цукерман, Диана (2011 г.), «Отзыв медицинских устройств и процесс утверждения FDA», Архивы внутренней медицины, 171 (11): 1006–11, Дои:10.1001 / archinternmed.2011.30, PMID 21321283
- ^ Цукерман, Диана; Браун, Пол; Дас, Адити (1 ноября 2014 г.). «Отсутствие общедоступных научных данных о безопасности и эффективности имплантированных медицинских устройств». JAMA Internal Medicine. 174 (11): 1781–7. Дои:10.1001 / jamainternmed.2014.4193. PMID 25265047.
- ^ Траутман, Ким (16 января 2015 г.). «Австралия, Бразилия, Канада, Япония и США: защита медицинских устройств». Голос FDA. Управление по контролю за продуктами и лекарствами.
- ^ Ронкильо, Джей Дж .; Цукерман, Диана М. (сентябрь 2017 г.). «Отзыв информационных технологий и других медицинских устройств, связанных с программным обеспечением: последствия для регулирования цифрового здравоохранения FDA». The Milbank Quarterly. 95 (3): 535–553. Дои:10.1111/1468-0009.12278. ЧВК 5594275. PMID 28895231.
- ^ Фокс-Ролингс С ,. Готтшалк Л. Б., Доамекпор Л., Цукерман Д. М. (2018) Разнообразие клинических испытаний медицинских устройств: знаем ли мы, что работает для каких пациентов? Milbank Quarterly, 96 (3); 499-529.
- ^ Ленцер, Жанна (27 ноября 2018 г.). «FDA рекомендует« модернизировать »обзор устройств после глобального расследования». BMJ. 363: k5026. Дои:10.1136 / bmj.k5026. PMID 30482750.
- ^ Кумбс, Ребекка (26 ноября 2018 г.). «Хирурги требуют обязательного учета всех новых медицинских изделий». BMJ. 363: k5010. Дои:10.1136 / bmj.k5010. PMID 30478186.
- ^ Дэйси, D (2010), «Оптимизация дизайна упаковки для стерилизации EtO», Медицинское оборудование и диагностическая промышленность, 33 (1)
- ^ "ASTM International - Международные стандарты". www.astm.org. Получено 2017-08-23.
- ^ Bix, L .; Фуэнте, Дж. (2009), «Упаковка для медицинских устройств», в Яме, К. Л. (ред.), Энциклопедия упаковочных технологий Wiley, Wiley, ISBN 978-0-470-08704-6[страница нужна ]
- ^ Fotis, N .; Бикс, Л. (2006), «Выбор размера выборки с использованием подхода на погрешность», Медицинское оборудование и диагностическая промышленность, 28 (10): 80–89
- ^ Шпигельберг, С.Х., Делуцио, К.Дж., Муратоглу, О.К. (2003). Выделяемый остаток из отозванных оболочек вертлужной впадины Inter-Op (PDF). 49-е ежегодное собрание Общества ортопедических исследований.CS1 maint: несколько имен: список авторов (связь)
- ^ «Стандартный метод испытаний для извлечения остатков из металлических медицинских компонентов и количественного определения с помощью гравиметрического анализа». Продукты и услуги ASTM International. Получено 15 июн 2014.
- ^ «Стандартная практика отчетности и оценки остатков на одноразовых имплантатах». Продукты и услуги ASTM. Получено 15 июн 2014.
- ^ а б "ASTM F3208 - 17 Стандартное руководство по выбору тестовых грунтов для проверки методов очистки для многоразовых медицинских устройств". www.astm.org. Получено 27 марта 2018.
- ^ «Стандартный метод испытаний для определения эффективности процессов очистки многоразовых медицинских инструментов с использованием микробиологического метода (испытание на моделировании использования)». ASTM International - Продукция и услуги. Получено 15 июн 2014.
- ^ «Стандартное руководство по эффективности очистки крови моющими средствами и моечно-дезинфицирующими средствами». 2014. Получено 15 июн 2014.
- ^ «Комитет F04 по медицинским и хирургическим материалам и устройствам». 2014. Получено 15 июн 2014.
- ^ «Обработка многоразового медицинского оборудования». Министерство здравоохранения и социальных служб США - Управление по контролю за продуктами и лекарствами - Медицинское оборудование. 2014. Получено 15 июн 2014.
- ^ АНИ (08.12.2019). «Исследователи находят способы защитить медицинские инструменты от патогенов». Бизнес-стандарт Индии. Получено 2019-12-10.
- ^ а б Вонг, К., Ту, Дж., Сан, З., и Диссанаяке, Д. В. (2013). Методы исследования и разработки биомедицинских устройств. Мировое научное издательство. Дои:10.1142/8621. ISBN 978-981-4434-99-7.CS1 maint: несколько имен: список авторов (связь)[страница нужна ]
- ^ «Архивная копия». Архивировано из оригинал на 2015-09-04. Получено 2020-02-26.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Йетисен, Али Кемаль; Martinez-Hurtado, J. L .; да Крус Васконселлос, Фернандо; Симсеклер, М. К. Эмре; Акрам, Мухаммад Сафван; Лоу, Кристофер Р. (2014). «Регулирование мобильных медицинских приложений». Лаборатория на чипе. 14 (5): 833–40. Дои:10.1039 / C3LC51235E. PMID 24425070.
- ^ Винсент, Кристофер Джеймс; Низен, Геррит; О'Кейн, Эйслинг Энн; Ставарц, Катажина (3 июня 2015 г.). "Могут ли стандарты и правила идти в ногу с технологиями здравоохранения?". JMIR mHealth и uHealth. 3 (2): e64. Дои:10.2196 / mhealth.3918. ЧВК 4526895. PMID 26041730.
- ^ FDA Мобильные медицинские приложения: руководство для сотрудников промышленности и Управления по контролю за продуктами и лекарствами
- ^ Пиккардо, Кармелита (28 июля 2014 г.). «FDA облегчает разработку новых продуктов». NPI Services, Inc. Получено 17 февраля 2016.
- ^ Джордан Робертсон. Ассошиэйтед Пресс, 04.08.2011
- ^ Altawy, R; Юссеф, А (2016). «Компромиссы безопасности в киберфизических системах: обзор практических примеров имплантируемых медицинских устройств». Доступ IEEE. 4: 959–979. Дои:10.1109 / ACCESS.2016.2521727.
- ^ Новая опасность для здоровья: медицинские имплантаты, которые можно взломать. Технология MSNBC.com
- ^ Камара, Кармен; Перис-Лопес, Педро; Тапиадор, Хуан Э. (июнь 2015 г.). «Проблемы безопасности и конфиденциальности имплантируемых медицинских устройств: всестороннее исследование». Журнал биомедицинской информатики. 55: 272–289. Дои:10.1016 / j.jbi.2015.04.007. PMID 25917056.
- ^ Пикрофт, Лори; Boccard, Sandra G .; Оуэн, Сара Л.Ф .; Штейн, Джон Ф .; Фитцджеральд, Джеймс Дж .; Грин, Александр Л .; Азиз, Типу З. (август 2016 г.). "Brainjacking: проблемы безопасности имплантатов при инвазивной нейромодуляции". Мировая нейрохирургия. 92: 454–462. Дои:10.1016 / j.wneu.2016.05.010. PMID 27184896.
- ^ Такахаши, декан (8 августа 2008 г.). "Извините, я выключу ваш кардиостимулятор". Венчурный бит.
- ^ Взлом медицинских устройств для развлечения и инсулина: взлом человеческой системы SCADA
- ^ Глобус и почта. Четверг, 27 октября 2011 г. Джим Финкль. Инсулиновые насосы уязвимы для атак хакеров
- ^ Daily Tech 15 июня 2011 г. Нидхи Суббараман
- ^ Daily Tech 15 июня 2011 г. Нидхи Суббараман
- ^ Беккер, Рэйчел (27 декабря 2016 г.). «Новые рекомендации по кибербезопасности для медицинских устройств позволяют бороться с развивающимися угрозами». Грани. Получено 29 декабря 2016.
- ^ «Постмаркетинговое управление кибербезопасностью в медицинских устройствах» (PDF). 28 декабря 2016 г.. Получено 29 декабря 2016.
- ^ «Содержание предпродажных материалов по управлению кибербезопасностью медицинских устройств». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 15 марта 2019.
- ^ "Федеральный регистр Том 78, № 151, стр. 47712 " (PDF). Издательство правительства США. 6 августа 2013 г.. Получено 17 февраля 2016.
- ^ "ар · ма · мен · тар · и · ум". www.thefreedictionary.com. Получено 14 ноября 2013.
- ^ «Международный форум регуляторов медицинского оборудования». www.imdrf.org.
- ^ ВОЗ (2010). «Барьеры на пути к инновациям в области медицинских устройств: справочный документ 6». Цитировать журнал требует
| журнал =(помощь) - ^ Marks IH, Thomas H, Bakhet M, Fitzgerald E (2019). «Пожертвование медицинского оборудования в условиях ограниченных ресурсов: обзор литературы и руководств по хирургии и анестезии в странах с низким и средним уровнем доходов». BMJ Global Health. Дои:10.1136 / bmjgh-2019-001785. PMID 31637029.
- ^ Липпинкотт Уильямс и Уилкинс. «Информация о журнале». Получено 10 апреля 2009.
- ^ «Школа упаковки». Школа упаковки. Получено 2017-08-23.
внешняя ссылка
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США - Центр устройств и радиологического здоровья
- FDA - Является ли продукт медицинским устройством?
- MHRA - Регулирование и безопасность медицинского оборудования
- EC - Медицинские изделия
- Министерство здравоохранения Канады - Список признанных стандартов для медицинских устройств (Международный)
- ISO - Каталог стандартов: 11.040.01: Медицинское оборудование в целом
- Радиочастотная беспроводная технология в медицинских устройствах - Руководство для сотрудников промышленности и Управления по санитарному надзору за качеством пищевых продуктов и медикаментов. FDA (2013)
- История регулирования и надзора за медицинским оборудованием в США.FDA (2019)
