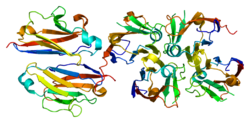Полимерный рецептор иммуноглобулина - Polymeric immunoglobulin receptor
Полимерный рецептор иммуноглобулина (pIgR) - это трансмембранный белок что у людей кодируется СВИНЬЯ ген.[5] Это Рецептор Fc что облегчает трансцитоз растворимых полимерных изоформ иммуноглобулин А , и иммунные комплексы. pIgR в основном расположены на эпителиальной выстилке слизистых оболочек желудочно-кишечного тракта. Состав рецептора сложный, включая 6 иммуноглобулиноподобных доменов, трансмембранную область и внутриклеточный домен.[6] Экспрессия pIgR находится под сильной регуляцией цитокинов, гормонов и патогенных стимулов.[6][7]
Структура
pIgR производится, среди прочего, кишечные эпителиальные клетки (IEC) и клетки бронхиального эпителия. pIgR принадлежит к семейству типа I трансмембранные белки. Внеклеточная часть белка содержит 6 доменов: 5 эволюционно консервативных иммуноглобулиноподобных доменов и 1 негомологичный домен, который участвует в протеолитическое расщепление комплекса pIg-pIgR с апикальной стороны IEC. Достаточно длинный внутриклеточный домен рецептора, наряду с трансмембранной областью, отвечает за передачу высококонсервативных сигналов.[7][8] В течение трансцитоз, неотъемлемая часть pIgR, секреторный компонент, присоединяется к лиганду и позже расщепляется лигандом с образованием полностью функционирующего секретируемого IgA.[9]
Функция
Полимерный рецептор иммуноглобулина отвечает за трансцитоз растворимых димерные IgA и иммунные комплексы от базолатеральной к апикальной поверхности эпителиальных клеток слизистой оболочки. pIgR имеет сильную специфичность к полимерным иммуноглобулинам и не реагирует на мономерный иммуноглобулин.[10] Лиганда J-цепь отвечает за связывание pIgR с его лигандом.[7][9]
Трансцитоз

Процесс транспортировки полимерных иммуноглобулинов от базолатеральной к апикальной стороне, известный как трансцитоз, состоит из нескольких отдельных этапов. Трансцитоз инициируется либо связыванием димерного IgA с рецептором, либо фосфорилированием остатка Ser-664 рецептора.[8] Интернализация как свободного, так и связанного с IgA pIgR опосредуется клатрин покрытие. Интернализованный рецептор транспортируется к базолатеральной ранней эндосомы. Следующий этап транспортировки pIgR через клетку (через тубуло-везикулярные компартменты к апикальной рециклирующей эндосоме) зависит от микротрубочки.[8] Когда pIgR достигает апикальной мембраны, протеолитическое расщепление генерирует либо свободный секреторный компонент комплекса SC-IgA, который высвобождается в апикальный просвет.[7] Расщепление происходит на стыке трансмембранной области рецептора и домена 5.[6]
Устранение иммунных комплексов
pIgR способны улавливать IgA, связанный с антигеном (иммунные комплексы (IC)) с таким же сродством, как IgA, и переносить их на апикальную сторону. IC возникают в результате захвата антигена антителом. IgA IC образуются в слизистых оболочках в ответ на инородное вторжение.[11] Накопление ИК на базолатеральной стороне слизистых слоев может иметь пагубные последствия. Трансцитоз IgA IC из мест образования представляет собой важный механизм устранения циркулирующих антигенов и минимизации их негативных эффектов.[11][12]
Регулирование
Цитокинетическая регуляция
Экспрессия pIgR критически регулируется провоспалительными цитокинами, такими как Ил-1, Ил-4, TNF-α, и IFN-γ. Регуляция транскрипции разными цитокинами происходит схожими путями с участием NF-kB Обратная связь. Взаимодействие IL-1 и TNF-α с их рецепторами в конечном итоге приводит к транскрипционной активации СВИНЬЯ ген из-за ядерной транслокации NF-kB. NF-kB взаимодействует с интроном 1 СВИНЬЯ ген для запуска синтеза мРНК pIgR.[6]
Помимо пути NF-kB, индукция транскрипции также происходит в ответ на IFN-γ, повышая экспрессию pIgR.[6][7]
Кроме того, вместо обычного антагонистического поведения, IL-4 действует синергетически с IFN-γ, индуцируя транскрипцию pIgR. Их комбинация проявляет повышающий эффект в СВИНЬЯ экспрессии из-за присутствия энхансера STAT6, основного нижестоящего эффектора IL-4, сайта связывания в СВИНЬЯинтрон 1.[13]
Гормональная регуляция
Уровень pIgR в слизистой оболочке репродуктивного тракта сильно зависит от активности половые гормоны и соотносится с эстральный цикл фазы. Пики экспрессии pIgR в фазах проэструса и эструса обусловлены доминирующей активностью эстроген, который действует как агонист pIgR. Низкие уровни pIgR во время диэструса связаны с подавляющей активностью прогестерон, который достигает пика во время этой фазы и способен обратить вспять активность эстрогена.[14] Андрогены являются агонистами экспрессии pIgR как в мужских, так и в женских репродуктивных тканях.[6]
5’-фланговая область Свинья ген содержит элемент ответа на глюкокортикоиды. Этот класс гормонов увеличивает устойчивые уровни экспрессии мРНК pIgR в клетках кишечника.[13][15]
Пролактин повышает уровень IRF-1 через Путь Jak-STAT. Известно, что IRF-1 является прямым агонистом экспрессии pIgR. Учитывая эту связь, считается, что пролактин косвенно повышает уровень pIgR во время беременности и кормления грудью.[6]
Патогенная стимуляция
IECs выражают различные Толл-подобные рецепторы (TLR), активация которых в конечном итоге приводит к активации pIgR во время инфекции.[6][7] Наиболее известные модуляторы регуляции pIgR состоят из TLR4 и TLR3, которые распознают бактериальные липополисахарид и вирусная дцРНК соответственно. TLR4, как и большинство TLR, хотя и преобразует сигнал MyD88 адаптер и выполняет функцию через NF-kB, который стимулирует экспрессию pIgR путем связывания с интроном 1 гена. TLR3, с другой стороны, включает регуляцию с помощью IRF-1, который способен способствовать транскрипции гена PIGR путем связывания с экзоном 1.[13][15]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000162896 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000026417 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ген Entrez: полимерный рецептор иммуноглобулина PIGR».
- ^ а б c d е ж грамм час Kaetzel CS (август 2005 г.). «Полимерный рецептор иммуноглобулина: мостик врожденного и адаптивного иммунных ответов на поверхности слизистой оболочки». Иммунологические обзоры. 206: 83–99. Дои:10.1111 / j.0105-2896.2005.00278.x. PMID 16048543.
- ^ а б c d е ж Асано М., Комияма К. (июнь 2011 г.). «Полимерный рецептор иммуноглобулина». Журнал оральной науки. 53 (2): 147–56. Дои:10.2334 / josnusd.53.147. PMID 21712618.
- ^ а б c Мостов К. (декабрь 1991 г.). «Полимерный рецептор иммуноглобулина». Семинары по клеточной биологии. 2 (6): 411–8. PMID 1813030.
- ^ а б Оуэн, Джудит А; Пунт, Дженни; Стрэнфорд, Шэрон А; Джонс, Патриция П.; Куби, Янис (2013). Кубы иммунология. Нью-Йорк: W.H. Фримен. ISBN 9781429219198. OCLC 820117219.
- ^ Kaetzel CS, Blanch VJ, Hempen PM, Phillips KM, Piskurich JF, Youngman KR (май 1997 г.). «Полимерный рецептор иммуноглобулина: структура и синтез». Сделки Биохимического Общества. 25 (2): 475–80. Дои:10.1042 / bst0250475. PMID 9191139.
- ^ а б Kaetzel CS, Robinson JK, Chintalacharuvu KR, Vaerman JP, Lamm ME (октябрь 1991 г.). «Полимерный рецептор иммуноглобулина (секреторный компонент) опосредует транспорт иммунных комплексов через эпителиальные клетки: локальная защитная функция для IgA». Труды Национальной академии наук Соединенных Штатов Америки. 88 (19): 8796–800. Дои:10.1073 / пнас.88.19.8796. ЧВК 52597. PMID 1924341.
- ^ Phalipon A, Corthésy B (февраль 2003 г.). «Новые функции полимерного рецептора Ig: далеко за пределами транспорта иммуноглобулинов». Тенденции в иммунологии. 24 (2): 55–8. Дои:10.1016 / с 1471-4906 (02) 00031-5. PMID 12547499.
- ^ а б c Johansen FE, Kaetzel CS (ноябрь 2011 г.). «Регулирование полимерного рецептора иммуноглобулина и транспорта IgA: новые достижения в факторах окружающей среды, которые стимулируют экспрессию pIgR, и его роль в иммунитете слизистой оболочки». Иммунология слизистой оболочки. 4 (6): 598–602. Дои:10.1038 / миль.2011.37. ЧВК 3196803. PMID 21956244.
- ^ Каушич К., Ричардсон Дж. М., Вира С. Р. (июль 1995 г.). «Регулирование экспрессии рибонуклеиновой кислоты полимерного иммуноглобулина А рецептора посыльного в матке грызунов: влияние половых гормонов». Эндокринология. 136 (7): 2836–44. Дои:10.1210 / эндо.136.7.7789308. PMID 7789308.
- ^ а б Kaetzel CS (декабрь 2014 г.). «Кооперативность между секреторным IgA, полимерным рецептором иммуноглобулина и кишечной микробиотой способствует взаимопониманию между хозяином и микробами». Письма иммунологии. 162 (2 балла A): 10–21. Дои:10.1016 / j.imlet.2014.05.008. ЧВК 4246051. PMID 24877874.
дальнейшее чтение
- Kaetzel CS (август 2005 г.). «Полимерный рецептор иммуноглобулина: соединение врожденных и адаптивных иммунных ответов на поверхности слизистой оболочки». Иммунологические обзоры. 206: 83–99. Дои:10.1111 / j.0105-2896.2005.00278.x. PMID 16048543.
- Krajci P, Kvale D, Taskén K, Brandtzaeg P (сентябрь 1992 г.). «Молекулярное клонирование и экзон-интронное картирование гена, кодирующего трансмембранный секреторный компонент человека (рецептор поли-Ig)». Европейский журнал иммунологии. 22 (9): 2309–15. Дои:10.1002 / eji.1830220920. PMID 1355431.
- Krajci P, Grzeschik KH, Geurts van Kessel AH, Olaisen B, Brandtzaeg P (октябрь 1991 г.). «Трансмембранный секреторный компонент человека (поли-Ig-рецептор): молекулярное клонирование, полиморфизм длины рестрикционных фрагментов и сублокализация хромосом». Генетика человека. 87 (6): 642–8. Дои:10.1007 / BF00201717. PMID 1682231.
- Eiffert H, Quentin E, Wiederhold M, Hillemeir S, Decker J, Weber M, Hilschmann N (февраль 1991 г.). «Определение молекулярной структуры свободного секреторного компонента человека». Биологическая химия Хоппе-Зейлер. 372 (2): 119–28. Дои:10.1515 / bchm3.1991.372.1.119. PMID 1859628.
- Бакос М.А., Курский А., Гольдблюм Р.М. (ноябрь 1991 г.). «Характеристика критического сайта связывания человеческого полимерного Ig на секреторном компоненте». Журнал иммунологии. 147 (10): 3419–26. PMID 1940346.
- Крайчи П., Сольберг Р., Сандберг М., Ойен О., Янсен Т., Брандтзаег П. (февраль 1989 г.). «Молекулярное клонирование трансмембранного секреторного компонента человека (рецептор поли-Ig) и его экспрессия мРНК в тканях человека». Сообщения о биохимических и биофизических исследованиях. 158 (3): 783–9. Дои:10.1016 / 0006-291X (89) 92790-3. PMID 2920039.
- Дэвидсон МК, Ле Бо М.М., Эдди Р.Л., Шоу ТБ, ДиПьетро Л.А., Кингзетт М., Хэнли В.К. (1989). «Генетическое картирование гена рецептора человеческого полимерного иммуноглобулина в области хромосомы 1q31 ---- q41». Цитогенетика и клеточная генетика. 48 (2): 107–11. Дои:10.1159/000132601. PMID 3197448.
- Eiffert H, Quentin E, Decker J, Hillemeir S, Hufschmidt M, Klingmüller D, Weber MH, Hilschmann N (декабрь 1984 г.). «[Первичная структура свободного секреторного компонента человека и расположение дисульфидных связей]». Hoppe-Seyler's Zeitschrift für Physiologische Chemie. 365 (12): 1489–95. Дои:10.1515 / bchm2.1984.365.2.1489. PMID 6526384.
- Мидзогути А., Мидзуочи Т., Кобата А. (август 1982 г.). «Структуры углеводных частей секреторного компонента, очищенного из грудного молока». Журнал биологической химии. 257 (16): 9612–21. PMID 7107583.
- Coyne RS, Siebrecht M, Peitsch MC, Casanova JE (декабрь 1994 г.). «Мутационный анализ полимерных взаимодействий рецептор иммуноглобулина / лиганд. Доказательства участия множественных определяющих комплементарность областей (CDR) -подобных петель в рецепторном домене I». Журнал биологической химии. 269 (50): 31620–5. PMID 7989333.
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Пискурич JF, Франция JA, Тамер CM, Willmer CA, Kaetzel CS, Kaetzel DM (март 1993). «Интерферон-гамма индуцирует мРНК полимерного рецептора иммуноглобулина в эпителиальных клетках кишечника человека по механизму, зависящему от синтеза белка». Молекулярная иммунология. 30 (4): 413–21. Дои:10.1016 / 0161-5890 (93) 90071-I. PMID 8455639.
- Пискурич Дж. Ф., Янгман К. Р., Филлипс К. М., Хемпен П. М., Бланшар М. Х., Франция Дж. А., Кетцель К. С. (январь 1997 г.). «Транскрипционная регуляция гена рецептора человеческого полимерного иммуноглобулина интерфероном-гамма». Молекулярная иммунология. 34 (1): 75–91. Дои:10.1016 / S0161-5890 (96) 00079-X. PMID 9182878.
- Hughes GJ, Frutiger S, Savoy LA, Reason AJ, Morris HR, Jaton JC (июнь 1997 г.). «Свободный секреторный компонент человека состоит из первых 585 аминокислотных остатков полимерного рецептора иммуноглобулина». Письма FEBS. 410 (2–3): 443–6. Дои:10.1016 / S0014-5793 (97) 00629-7. PMID 9237679.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К., Суяма А., Сугано С. (октябрь 1997 г.). «Создание и характеристика полноразмерной библиотеки кДНК, обогащенной по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
- Акерманн Л.В., Волленвебер Л.А., Деннинг Г.М. (май 1999 г.). «IL-4 и IFN-гамма увеличивают устойчивые уровни мРНК полимерного Ig-рецептора в эпителиальных клетках дыхательных путей человека и кишечника». Журнал иммунологии. 162 (9): 5112–8. PMID 10227981.
- Рё М., Нордерхауг И.Н., Брандтзаег П., Йохансен ИП (май 1999 г.). «Тонкая специфичность лиганд-связывающего домена 1 в полимерном Ig-рецепторе: важность CDR2-содержащей области для взаимодействия IgM». Журнал иммунологии. 162 (10): 6046–52. PMID 10229845.
- Norderhaug IN, Johansen FE, Krajci P, Brandtzaeg P (октябрь 1999 г.). «Делеции домена в человеческом полимерном рецепторе Ig раскрывают различия между взаимодействием его димерного IgA и пентамерного IgM». Европейский журнал иммунологии. 29 (10): 3401–9. Дои:10.1002 / (SICI) 1521-4141 (199910) 29:10 <3401 :: AID-IMMU3401> 3.0.CO; 2-G. PMID 10540352.
- Мостов К.Е., Фридлендер М, Блобель Г (1984). «Рецептор трансэпителиального транспорта IgA и IgM содержит несколько иммуноглобулиноподобных доменов». Природа. 308 (5954): 37–43. Дои:10.1038 / 308037a0. PMID 6322002.
- Hughes GJ, Reason AJ, Savoy L, Jaton J, Frutiger-Hughes S (сентябрь 1999 г.). «Углеводные фрагменты секреторного компонента человека». Biochimica et Biophysica Acta (BBA) - Структура белка и молекулярная энзимология. 1434 (1): 86–93. Дои:10.1016 / S0167-4838 (99) 00168-5. PMID 10556562.
внешняя ссылка
- Полимерный + иммуноглобулин + рецептор в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.