Pilus - Pilus
А пилус (латинский для «волос»; множественное число: пили) представляет собой волосовидный отросток, обнаруженный на поверхности многих бактерии и археи.[1] Условия пилус и фимбрия (На латыни «бахрома»; множественное число: фимбрии) могут использоваться как взаимозаменяемые, хотя некоторые исследователи оставляют за собой право использовать термин пилус для придатка, необходимого для бактериальная конъюгация. Все пили в последнем смысл в основном состоят из пилин белки, которые олигомерный.
Десятки таких структур могут существовать на поверхности бактерий и архей. Некоторые бактерии, вирусы или же бактериофаги прикрепить к рецепторы на пили в начале их репродуктивный цикл.
Пили антигенный. Они также хрупкие и постоянно заменяются пилями различного состава, что приводит к изменению антигенности. Специфические реакции хозяина на старую структуру пилей не действуют на новую структуру. Рекомбинационные гены пилей кодируют вариабельную (V) и константную (C) области пилей (аналогично иммуноглобулин разнообразие). В качестве первичных антигенных детерминант факторы вирулентности и факторы безнаказанности на клеточной поверхности ряда видов грамотрицательных и некоторых грамположительных бактерий, включая Энтербоактерии, Pseudomonadaceae, и Neisseriaceae, существует большой интерес к изучению пилей как органелл адгезии и компонентов вакцины. Первое подробное исследование пилей было проведено Бринтоном и его коллегами, которые продемонстрировали существование двух различных фаз в пределах одного бактериального штамма: пилотируемая (p +) и не имеющая пилинга)[2]
Типы
Конъюгативные пили
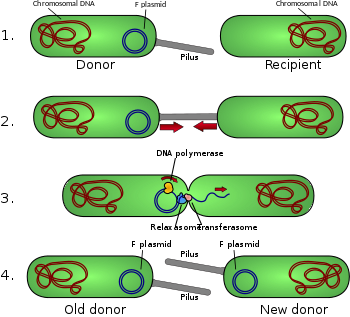
Конъюгативные пили позволяют переносить ДНК между бактериями, в процессе бактериальная конъюгация. Иногда их называют «секс-пили», по аналогии с половое размножение, потому что они позволяют обмениваться генами посредством образования «пар спаривания». Пожалуй, наиболее изученной является пилус кишечная палочка, кодируемый плодородием F половой фактор.
Пилей обычно от 6 до 7. нм в диаметре. Во время конъюгации ворсинка, выходящая из донорской бактерии, захватывает реципиентную бактерию, притягивает ее к себе и, в конечном итоге, запускает образование стыковочный мост, который устанавливает прямой контакт и образование контролируемой поры, которая позволяет передавать ДНК от донора к реципиенту. Как правило, переносимая ДНК состоит из генов, необходимых для создания и переноса пилей (часто кодируемых на плазмида ), и это своего рода эгоистичная ДНК; однако другие фрагменты ДНК часто переносятся совместно, и это может привести к распространению генетических признаков среди бактериальной популяции, таких как устойчивость к антибиотикам. Не все бактерии могут образовывать конъюгативные пили, но конъюгация может происходить между бактериями разных видов.[нужна цитата ]
Пили IV типа

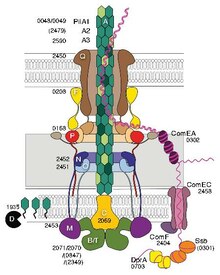
Некоторые пили, называемые пилями IV типа (T4P), создают подвижный силы.[4] Внешние концы пилей прилипают к твердому субстрату, либо к поверхности, к которой прикреплена бактерия, либо к другим бактериям. Затем, когда пили сокращаются, они тянут бактерии вперед, как крюк. Пили типа IV обычно отрывистые, поэтому их называют подергивание моторики, в отличие от других форм подвижности бактерий, таких как жгутики. Однако некоторые бактерии, например Myxococcus xanthus, выставка скользящая подвижность. Бактериальные пили IV типа похожи по строению на компонент флагеллины из архаэлла (жгутики архей), и оба связаны с Система секреции типа II.[5] Помимо архей, многие археи продуцируют адгезивные пили типа 4, которые позволяют архейным клеткам прикрепляться к различным субстратам. N-концевые альфа-спиральные части пилинов и архаеллинов архейного типа 4 гомологичны соответствующим областям бактериального T4P; однако С-концевые домены, богатые бета-цепью, по-видимому, не связаны между собой в бактериальных и архейных пилинах.[6]
Генетическая трансформация это процесс, с помощью которого бактериальная клетка-реципиент берет ДНК из соседней клетки и интегрирует эту ДНК в свой геном путем гомологичная рекомбинация. В Neisseria meningitidis (также называемый менингококком), трансформация ДНК требует наличия коротких Последовательности захвата ДНК (DUS), которые представляют собой 9-10 мономеров, находящихся в кодирующие области донорской ДНК. Специфическое распознавание DUS опосредуется типом IV пилин.[7] Пили менингококка IV типа связывают ДНК через минорный пилин ComP через электроположительную полосу, которая, как предполагается, обнажается на поверхности нити. ComP отображает изысканные настройки привязки для выборочных DUS. Распределение ООС в пределах N. meningitides геном отдает предпочтение определенным генам, предполагая, что существует смещение в отношении генов, участвующих в поддержании и восстановлении генома.[8][9]
Фимбрии
Инициировать формирование биопленка, фимбрии должен прикреплять бактерии к поверхностям хозяина для колонизации во время инфекции. А фимбрия представляет собой короткую пилюсу, которая используется для прикрепления бактерии к поверхности. Иногда их называют «пили прикрепления». Фимбрии либо расположены на полюсах клетки, либо равномерно распределены по всей ее поверхности. Мутант бактерии, у которых отсутствуют фимбрии, не могут прикрепиться к своим обычным целевым поверхностям и, следовательно, не могут вызывать болезни.
Некоторые фимбрии могут содержать лектины. Лектины необходимы для прикрепления к клеткам-мишеням, потому что они могут распознавать олигосахарид единиц на поверхности этих клеток-мишеней. Другие фимбрии связываются с компонентами внеклеточный матрикс. Фимбрии найдены в Грамотрицательный имеют ковалентно связанные субъединицы пилина.
Немного аэробные бактерии образуют тонкий слой на поверхности бульонной культуры. Этот слой, называемый пленкой, состоит из множества аэробных бактерий, которые прикрепляются к поверхности своими фимбриями или «пили прикрепления». Таким образом, фимбрии позволяют аэробным бактериям оставаться в бульоне, из которого они получают питательные вещества, в то время как они собираются рядом с воздухом.[нужна цитата ]
Вирулентность
Пили несут ответственность за вирулентность патогенных штаммов многих бактерий, в том числе Кишечная палочка, Холерный вибрион, и многие штаммы Стрептококк.[10][11] Это связано с тем, что наличие пилей значительно увеличивает способность бактерий связываться с тканями тела, что затем увеличивает скорость репликации и способность взаимодействовать с организмом-хозяином.[10] Если у какого-либо вида бактерий есть несколько штаммов, но только некоторые из них являются патогенными, вполне вероятно, что патогенные штаммы будут иметь пили, а непатогенные штаммы - нет.[12][13]
Затем развитие прикрепляющих пилей может привести к развитию дополнительных признаков вирулентности. Непатогенные штаммы V. cholerae первые образовавшиеся пили, позволяющие им связываться с тканями человека и образовывать микроколонии.[10][13] Эти пили затем служили сайтами связывания для лизогенный бактериофаг который несет болезнетворные токсин.[10][13] Ген этого токсина, однажды включенный в геном бактерии, экспрессируется, когда экспрессируется ген, кодирующий пилус (отсюда и название "пилус, опосредованный токсином").[10]
Смотрите также
Рекомендации
- ^ "пилус " в Медицинский словарь Дорланда
- ^ Бринтон, Чарльз (1954). «Электрофорез и исследования чувствительности к фагам на продуцирующем нити варианте бактерии E. coli». Biochimica et Biophysica Acta. 15 (4): 533–542. Дои:10.1016/0006-3002(54)90011-6. PMID 13230101.
- ^ Джоан, Слончевский (2017). Микробиология: развивающаяся наука. Фостер, Джон Уоткинс (Четвертое изд.). Нью-Йорк: W. W. Norton & Company. С. 1000–1002. ISBN 9780393614039. OCLC 951925510.
- ^ Мэттик Дж. С. (2002). «Пили IV типа и подергивание моторики». Анну. Rev. Microbiol. 56 (1): 289–314. Дои:10.1146 / annurev.micro.56.012302.160938. PMID 12142488.
- ^ Джаррелл; и другие. (2009). «Архейские жгутики и пили». Пили и жгутики: текущие исследования и будущие тенденции. Caister Academic Press. ISBN 978-1-904455-48-6.
- ^ Ванга, Ф; Цвиркайте-Крупович, В; Кройцбергер, МАБ; Вс, З; де Оливейра, GAP; Осинский, Т; Шерман, Н; DiMaio, F; Wall, JS; Прангишвили, Д; Крупович, М; Эгельман, EH (2019). «Экстенсивно гликозилированный пильс архей выживает в экстремальных условиях». Природная микробиология. 4 (8): 1401–1410. Дои:10.1038 / с41564-019-0458-х. ЧВК 6656605. PMID 31110358.
- ^ Сеховин А., Симпсон П.Дж., МакДауэлл М.А., Браун Д.Р., Ношезе Р., Паллетт М., Брэди Дж., Болдуин Г.С., Ли С.М., Мэтьюз С.Дж., Пеликич В. (2013). «Специфическое распознавание ДНК, опосредованное пилином типа IV». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 110 (8): 3065–70. Bibcode:2013PNAS..110.3065C. Дои:10.1073 / pnas.1218832110. ЧВК 3581936. PMID 23386723.
- ^ Дэвидсен Т., Рёдланд Э.А., Лагесен К., Сиберг Э., Рогнес Т., Тоньюм Т. (2004). «Смещенное распределение последовательностей захвата ДНК по отношению к генам поддержания генома». Нуклеиновые кислоты Res. 32 (3): 1050–8. Дои:10.1093 / нар / гх255. ЧВК 373393. PMID 14960717.
- ^ Caugant DA, Maiden MC (2009). «Менингококковое носительство и болезнь - популяционная биология и эволюция». Вакцина. 27 Приложение 2: B64–70. Дои:10.1016 / j.vaccine.2009.04.061. ЧВК 2719693. PMID 19464092.
- ^ а б c d е Крейг, Лиза; Тейлор, Рональд (2014). «Глава 1: Пилус с коагуляцией токсина холерного вибриона: структура, сборка и функция с последствиями для разработки вакцины». В Барокки, Мишель; Телфорд, Джон (ред.). Бактериальные пили: структура, синтез и роль в заболевании. ТАКСИ. Международный. С. 1–16. ISBN 978-1-78064-255-0.
- ^ Ринаудо, Даниэла; Moschioni, Моника (2014). «Глава 13: Разработка вакцины на основе пилюса для стрептококков: изменчивость, разнообразие и иммунологические реакции». В Барокки, Мишель; Телфорд, Джон (ред.). Бактериальные пили: структура, синтез и роль в заболевании. ТАКСИ. Международный. С. 182–202. ISBN 978-1-78064-255-0.
- ^ Тодар, Кеннет. «Учебник бактериологии: структура бактерий в зависимости от патогенности». Учебник бактериологии. Получено 24 ноября 2017.
- ^ а б c Георгиаду, Микаэлла; Пеличич, Владимир (2014). «Глава 5: Пили типа IV: функции и биогенез». В Барокки, Мишель; Телфорд, Джон (ред.). Бактериальные пили: структура, синтез и роль в заболевании. ТАКСИ. Международный. С. 71–84. ISBN 978-1-78064-255-0.
внешняя ссылка
- Секс + Пилус в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Бактериальный + Пилус в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
