PCSK9 - PCSK9
Пропротеинконвертаза субтилизин / кексин типа 9 (PCSK9) является фермент закодировано PCSK9 ген у людей на хромосома 1.[5] Это 9-й участник пропротеин конвертаза семейство белков, активирующих другие белки.[6] Подобные гены (ортологи ) встречаются у многих видов. Как и многие белки, PCSK9 неактивен при первом синтезе, потому что часть пептидных цепей блокирует их активность; пропротеин конвертазы удалите этот участок, чтобы активировать фермент.[7] В PCSK9 ген также содержит один из 27 места связано с повышенным риском ишемическая болезнь сердца.[8]
PCSK9 повсеместно экспрессируется во многих тканях и типах клеток.[9] PCSK9 связывается с рецептором для липопротеин низкой плотности частицы (ЛПНП), которые обычно переносят от 3000 до 6000 молекул жира (включая холестерин ) на частицу, в пределах внеклеточной жидкости. В Рецептор ЛПНП (LDLR), на печень и другие клеточные мембраны, связывает и инициирует попадание частиц ЛПНП из внеклеточной жидкости в клетки, тем самым снижая концентрацию частиц ЛПНП. Если PCSK9 заблокирован, большее количество LDLR повторно используется и присутствует на поверхности клеток, чтобы удалить частицы LDL из внеклеточной жидкости.[10] Следовательно, блокирование PCSK9 может снизить концентрацию частиц ЛПНП в крови.[11][12]
PCSK9 имеет медицинское значение, поскольку действует в составе липопротеинов. гомеостаз. Агенты, которые блокируют PCSK9, могут снижать концентрацию частиц ЛПНП. Первые два ингибитора PCSK9, алирокумаб и эволокумаб, были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США в качестве инъекций раз в две недели для снижения концентрации частиц ЛПНП при статины и другие препараты были недостаточно эффективными или плохо переносились. Стоимость этих новых лекарств по состоянию на 2015 г.[Обновить]при полной розничной продаже составляла 14 000 долларов в год; некоторые судят о неясной экономической эффективности.[13] Хотя эти лекарства выписывают многие врачи, страховые компании часто отказывают в оплате рецептов.[14][15][16] В результате производители фармацевтики снизили цены на эти препараты.[17]
История
В феврале 2003 г. Набил Сейдах, ученый из Институт клинических исследований Монреаля в Канаде обнаружил нового человека пропротеин конвертаза, ген которого располагался на коротком плече хромосома 1.[18] Тем временем лаборатория под руководством Катрин Буало в Больница Necker-Enfants Malades в Париже следили за семьями с семейная гиперхолестеринемия, генетическое заболевание, которое в 90% случаев вызывает ишемическая болезнь сердца (Исследование FRAMINGHAM) и в 60% случаев может привести к преждевременной смерти;[19] они идентифицировали мутацию на хромосоме 1, принадлежащую некоторым из этих семейств, но не смогли идентифицировать соответствующий ген. Лаборатории собрались вместе и к концу года опубликовали свою работу, связывающую мутации в гене, который теперь идентифицирован как PCSK9, с этим заболеванием.[20][18] В своей статье они предположили, что мутации могут сделать ген сверхактивным. В том же году следователи Рокфеллеровский университет и Юго-Западный Техасский университет открыл тот же белок у мышей и разработал новый путь что регулирует Холестерин ЛПНП в котором участвует PCSK9, и вскоре стало ясно, что мутации, идентифицированные во Франции, привели к чрезмерной активности PCSK9 и, следовательно, чрезмерному удалению рецептора ЛПНП, в результате чего у людей, несущих мутации, было слишком много холестерина ЛПНП.[18] Тем временем доктор Хелен Хоббс и доктор Джонатан Коэн из Юго-Западного Юта изучали людей с очень высоким и очень низким уровнем холестерина и собирали образцы ДНК.[21] Обладая новыми знаниями о роли PCSK9 и его расположении в геноме, они секвенировали соответствующую область хромосомы 1 у людей с очень низким уровнем холестерина и обнаружили: бессмысленные мутации в гене, таким образом подтверждая PCSK9 как биологическая мишень за открытие лекарств.[18][22]
В июле 2015 г. FDA одобрил первые лекарственные средства ингибитора PCSK9 для медицинского применения.[23]
Структура
Ген
В PCSK9 ген находится на хромосоме 1 в полосе 1p32.3[24] и включает 13 экзоны.[25] Этот ген производит два изоформы через альтернативное сращивание.[26]
Протеин
PCSK9 является членом пептидаза S8 семья.[26]
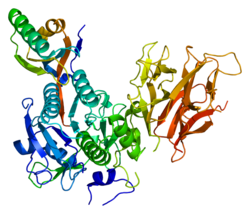
Решенная структура PCSK9 выявляет четыре основных компонента в предварительно обработанном белке: сигнальный пептид (остатки 1-30); в N-концевой продомен (остатки 31-152); в каталитический домен (остатки 153-425); и С-концевой домен (остатки 426-692), который далее разделен на три модуля.[27] N-концевой продомен имеет гибкую кристаллическую структуру и отвечает за регулирование функции PCSK9, взаимодействуя и блокируя каталитический домен, который в противном случае связывает фактор роста эпидермиса -подобный повтор A (EGF-A) домен LDLR.[27][28][29] Хотя предыдущие исследования показали, что C-концевой домен не участвует в связывании LDLR,[30][31] недавнее исследование Du et al. продемонстрировали, что C-концевой домен действительно связывает LDLR.[27] Секреция PCSK9 в значительной степени зависит от авторасщепления сигнального пептида и N-концевого продомена, хотя N-концевой продомен сохраняет свою связь с каталитическим доменом. В частности, остатки 61-70 в N-концевом продомене имеют решающее значение для его автопроцессинга.[27]
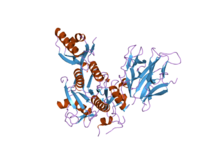 2p4e: Кристаллическая структура PCSK9[32] | 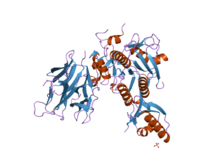 2pmw: Кристаллическая структура пропротеинконвертазы субтилизин кексин типа 9 (PCSK9).[33] |
Функция
Роль и регулирующая функция
Этот белок играет важную регулирующую роль в холестерин гомеостаз, в основном за счет снижения уровня ЛПНП на плазматической мембране. Снижение уровня ЛПНП приводит к снижению метаболизма частиц ЛПНП, что может привести к гиперхолестеринемия.[34] Когда ЛПНП связывается с ЛПНП, он вызывает интернализацию комплекса ЛПНП-ЛПНП внутри эндосомы. Кислотность эндосомальной среды побуждает ЛПНП принимать конформацию шпильки.[35] Конформационное изменение заставляет ЛПНП высвобождать свой лиганд ЛПНП, и рецептор возвращается обратно в плазматическую мембрану. Однако, когда PCSK9 связывается с LDLR (через домен EGF-A), PCSK9 предотвращает конформационное изменение комплекса рецептор-лиганд. Это ингибирование вместо этого перенаправляет ЛПНП в лизосомы.[35]
PCSK9 синтезируется как растворимый зимоген который подвергается автокаталитической внутримолекулярной переработке в эндоплазматический ретикулум. Белок может действовать как пропротеинконвертаза.[7] PCSK9 экспрессируется в основном в печени, кишечнике, почках и центральной нервной системе.[36] PCSK9 также играет важную роль в богатых триглицеридами кишечных липопротеин апоВ продукция в тонком кишечнике и постпрандиальная липемия.[37][38][39]
После процессинга в ER PCSK9 локализуется совместно с белком сортилин на своем пути через Гольджи и комплекс Транс-Гольджи. Предполагается, что взаимодействие PCSK9-сортилин необходимо для клеточной секреции PCSK9.[40] У здоровых людей уровни PCSK9 в плазме напрямую коррелируют с уровнями сортилина в плазме после суточный ритм похож на синтез холестерина.[41][42] Концентрация PCSK9 в плазме выше у женщин по сравнению с мужчинами, а концентрация PCSK9 снижается с возрастом у мужчин, но увеличивается у женщин, что позволяет предположить, что уровень эстрогена, скорее всего, играет роль.[43][44] Экспрессия гена PCSK9 может регулироваться белки, связывающие элемент ответа на стерол (SREBP-1/2), который также контролирует экспрессию LDLR.[41]
PCSK9 также может играть роль в дифференцировке нейронов коры.[5]
Клиническое значение
Варианты PCSK9 могут снижать или повышать уровень холестерина в крови. Частицы ЛПНП удаляются из крови, когда они связываются с ЛПНП на поверхности клеток, в том числе клетки печени, и берутся внутри ячеек. Когда PCSK9 связывается с LDLR, рецептор разрушается вместе с частицей LDL. PCSK9 разрушает LDLR, предотвращая конформационные изменения LDLR в форме шпильки.[45] Если PCSK9 не связывается, рецептор вернется на поверхность клетки и сможет продолжать удалять частицы ЛПНП из кровотока.[46]
Другие варианты связаны с редким аутосомно-доминантным семейная гиперхолестеринемия (HCHOLA3).[47][20][48] Мутации увеличивают его протеазную активность, снижая уровни ЛПНП и препятствуя поглощению холестерина клетками.[20]
У людей PCSK9 был первоначально обнаружен как белок выражается в головном мозге.[49] Однако он также был описан в почках, поджелудочной железе, печени и тонком кишечнике.[49] Недавние данные показывают, что PCSK9 высоко экспрессируется в стенках артерий, таких как эндотелий, гладкая мышца клетки и макрофаги, с местным действием, которое может регулировать гомеостаз сосудов и атеросклероз.[50][51][52] Соответственно, теперь ясно, что PCSK9 обладает проатеросклеротическим действием и регулирует липопротеин синтез.[53]
Поскольку PCSK9 связывается с LDLR, что предотвращает удаление ЛПНП-частицы из плазмы крови несколько исследований определили потенциальное использование ингибиторов PCSK9 при лечении гиперлипопротеинемии (обычно называемой гиперхолестеринемией).[13][49][54][55][56][57][58][59] Кроме того, мутации с потерей функции в гене PCSK9 приводят к снижению уровня ЛПНП и защите от сердечно-сосудистых заболеваний.[53][60][61]
Помимо своего синтетического липопротеинового и проатеросклеротического эффектов, PCSK9 участвует в метаболизм глюкозы и ожирение,[62] регулирование реабсорбции натрия почками, что актуально при артериальной гипертензии.[63][64] Более того, PCSK9 может быть вовлечен в бактериальные или вирусные инфекции и сепсис.[65][66] В мозге роль PCSK9 остается спорным и может быть либо про-апоптотический или защитный в развитии нервной системы.[5] Уровни PCSK9 были обнаружены в спинномозговая жидкость в 50-60 раз ниже, чем в сыворотке крови.[67]
Клинический маркер
Мультилокусное исследование генетического риска, основанное на комбинации из 27 локусов, включая ген PCSK9, выявило лиц с повышенным риском как инцидентных, так и рецидивирующих событий ИБС, а также увеличило клиническую пользу от терапии статинами. Исследование было основано на когортном исследовании сообщества (исследование Malmo Diet and Cancer) и четырех дополнительных рандомизированных контролируемых исследованиях когорт первичной профилактики (JUPITER и ASCOT) и когорт вторичной профилактики (CARE и PROVE IT-TIMI 22).[8]
Препараты-ингибиторы PCSK9
Несколько исследований определили потенциальное использование ингибиторов PCSK9 при лечении гиперлипопротеинемии (обычно называемой гиперхолестеринемия ).[13][49] Кроме того, мутации с потерей функции в гене PCSK9 приводят к снижению уровня ЛПНП и защите от сердечно-сосудистых заболеваний.[53]
Препараты-ингибиторы PCSK9 в настоящее время одобрены FDA для лечения семейной гиперхолестеринемии.[14]
Как мишень для наркотиков
Лекарства могут ингибировать PCSK9, что приводит к снижению концентрации циркулирующих частиц ЛПНП. Поскольку многие эксперты считают, что концентрация частиц ЛПНП является движущей силой сердечно-сосудистые заболевания подобно сердечные приступы, вполне вероятно, что эти препараты могут также снизить риск таких заболеваний. Клинические исследования, в том числе клинические испытания III фазы, сейчас находятся в стадии разработки, чтобы описать влияние ингибирования PCSK9 на сердечно-сосудистые заболевания, а также профиль безопасности и эффективности препаратов.[68][69][70][71][72] Среди ингибиторов, разрабатываемых в декабре 2013 г., были антитела. алирокумаб, эволокумаб, 1D05-IgG2 (Merck ), RG-7652 и LY3015014, а также РНКи терапевтический инклюзивный.[73] Ингибиторы PCSK9 являются многообещающими терапевтическими средствами для лечения людей с непереносимостью статинов или в качестве способа обхода частых доз статинов для более высокого снижения концентрации ЛПНП.[74][75]
В обзоре, опубликованном в 2015 году, сделан вывод о том, что эти агенты при использовании у пациентов с высокими концентрациями частиц ЛПНП (таким образом, со значительно повышенным риском сердечно-сосудистых заболеваний) кажутся безопасными и эффективными для снижения смертности от всех причин, смертности от сердечно-сосудистых заболеваний и сердечные приступы.[76] Однако в более поздних обзорах делается вывод о том, что, хотя лечение ингибитором PCSK9 обеспечивает дополнительные преимущества помимо максимально переносимой терапии статинами у лиц с высоким риском,[77] Использование ингибитора PCSK9, вероятно, приводит к незначительной разнице в смертности или ее отсутствию.[78][нуждается в обновлении ]
Regeneron Pharmaceuticals (в сотрудничестве с Санофи ) стал первым на рынке ингибитором PCSK9 вместе с конкурентом Amgen выход на рынок чуть позже.[14] Препараты одобрены FDA для лечения гиперхолестеринемии, особенно гетерозиготного генетического состояния семейная гиперхолестеринемия который вызывает высокий уровень холестерина и сердечные приступы в молодом возрасте.[19] Совсем недавно эти препараты были одобрены FDA для снижения сердечно-сосудистых событий, включая снижение смертности от всех причин.[79]
Предупреждение
Предупреждение FDA в марте 2014 г. о возможных нежелательных когнитивных эффектах ингибирования PCSK9 вызвало обеспокоенность, поскольку FDA попросило компании включить нейрокогнитивные тесты в свои Фаза III клинические испытания.[80]
Моноклональные антитела
Номер моноклональные антитела которые связываются и ингибируют PCSK9 рядом с каталитическим доменом, по состоянию на 2014 г. проходили клинические испытания.[Обновить]. К ним относятся эволокумаб (Amgen ), бокоцизумаб (Pfizer ), и алирокумаб (Санофи /Regeneron Pharmaceuticals ).[81] По состоянию на июль 2015 г.[Обновить], согласно сообщению информационного агентства Medscape, ЕС одобрил эти препараты, в том числе Evolocumab / Amgen. А метаанализ из 24 клинических испытаний показали, что моноклональные антитела против PCSK9 могут снижать уровень холестерина, сердечные приступы и смертность от всех причин.[76] Последние рекомендации по контролю холестерина от Американская Ассоциация Сердца и Американский колледж кардиологии теперь предоставляют рекомендации относительно того, когда следует рассматривать применение ингибиторов PCSK9, уделяя особое внимание случаям, в которых максимально допустимы статины и эзетимиб не удается достичь цели снижения ЛПНП.[82]
Возможным побочным эффектом моноклонального антитела может быть раздражение в месте инъекции. Перед инфузиями участники получали пероральные кортикостероиды, блокаторы гистаминовых рецепторов и ацетаминофен, чтобы снизить риск реакций, связанных с инфузией, которые сами по себе вызывают несколько побочных эффектов.[83]
Пептидные имитаторы
Пептиды, имитирующие домен EGFA LDLR, который связывается с PCSK9, были разработаны для ингибирования PCSK9.[84]
Подавление гена
PCSK9 антисмысловой олигонуклеотид увеличивает экспрессию ЛПНП и снижает уровень общего холестерина в крови у мышей.[85] Блокированная нуклеиновая кислота, восстановленная PCSK9 мРНК уровни у мышей.[86][87] Первоначальные клинические испытания показали положительные результаты ALN-PCS, который действует посредством РНК-интерференция.[72][88][89]
Вакцинация
Вакцина, нацеленная на PCSK9, была разработана для лечения высоких концентраций частиц ЛПНП. В вакцине используется VLP (вирусоподобная частица ) в качестве иммуногенного носителя антигенного пептида PCSK9. VLP - это вирусы, у которых была удалена ДНК, так что они сохраняют свою внешнюю структуру для отображения антигена, но не могут реплицироваться; они могут вызывать иммунный ответ, не вызывая инфекции. У мышей и макак, вакцинированных VLP бактериофага, демонстрирующих пептиды, производные от PCSK9, развился высокий титр IgG антитела это связано с распространением PCSK9. Вакцинация была связана со значительным снижением общего холестерина, свободного холестерина, фосфолипидов и триглицеридов.[90]
Ингибиторы природного происхождения
Растительный алкалоид берберин подавляет транскрипцию гена PCSK9 в иммортализованных гепатоцитах человека in vitro,[91] и снижает сывороточный PCSK9 у мышей и хомяков in vivo.[92] Было высказано предположение[92] что это действие способствует способности берберина снижать уровень холестерина в сыворотке.[93] Аннексин А2, эндогенный белок, является естественным ингибитором активности PCSK9.[94]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000169174 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000044254 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c Сейда Н.Г., Бенджаннет С., Викхэм Л., Марцинкевич Дж., Жасмин С.Б., Стифани С., Басак А., Прат А., Кретьен М. (февраль 2003 г.). «Секреторная пропротеинконвертаза, регулируемая апоптозом нейронов конвертаза 1 (NARC-1): регенерация печени и дифференцировка нейронов». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 100 (3): 928–33. Bibcode:2003ПНАС..100..928С. Дои:10.1073 / pnas.0335507100. ЧВК 298703. PMID 12552133.
- ^ Чжан Л., Сун К., Чжу М., Ши Дж., Чжан Х., Сюй Л., Чен Ю. (2016). «Пропротеинконвертаза субтилизин / кексин типа 9 (PCSK9) при липидном обмене, атеросклерозе и ишемическом инсульте». Международный журнал неврологии. 126 (6): 675–680. Дои:10.3109/00207454.2015.1057636. PMID 26040332.
- ^ а б Lagace TA (октябрь 2014 г.). «Деградация PCSK9 и LDLR: регуляторные механизмы в кровообращении и в клетках». Текущее мнение в липидологии. 25 (5): 387–93. Дои:10.1097 / MOL.0000000000000114. ЧВК 4166010. PMID 25110901.
- ^ а б Mega JL, Stitziel NO, Smith JG, Chasman DI, Caulfield MJ, Devlin JJ, Nordio F, Hyde CL, Cannon CP, Sacks FM, Poulter NR, Sever PS, Ridker PM, Braunwald E, Melander O, Kathiresan S, Sabatine MS (Июнь 2015 г.). «Генетический риск, события ишемической болезни сердца и клиническая польза от терапии статинами: анализ испытаний первичной и вторичной профилактики». Ланцет. 385 (9984): 2264–71. Дои:10.1016 / S0140-6736 (14) 61730-X. ЧВК 4608367. PMID 25748612.
- ^ «BioGPS - ваша система генного портала». biogps.org. Получено 2016-08-19.
- ^ Вайнрайх М, Фришман WH (2014). «Антигиперлипидемическая терапия, направленная на PCSK9». Кардиология в обзоре. 22 (3): 140–6. Дои:10.1097 / CRD.0000000000000014. PMID 24407047.
- ^ Gearing ME (18 мая 2015 г.). «Потенциальное новое оружие против болезней сердца: ингибиторы PCSK9». Наука в новостях. Гарвардский университет.
- ^ Джозеф Л., Робинсон Дж. Г. (2015). «Ингибирование пропротеин-конвертазы, субтилизина / кексина типа 9 (PCSK9) и будущее липидоснижающей терапии». Прогресс сердечно-сосудистых заболеваний. 58 (1): 19–31. Дои:10.1016 / j.pcad.2015.04.004. PMID 25936907.
- ^ а б c Хлатки М.А., Кази Д.С. (2017). «Ингибиторы PCSK9: экономика и политика». Журнал Американского колледжа кардиологии. 70 (21): 2677–2687. Дои:10.1016 / j.jacc.2017.10.001. PMID 29169476.
- ^ а б c Джина Колата, «Эти редукторы холестерина могут спасти жизни. Так почему же они не получаются сердечными пациентами?», Нью-Йорк Таймс, 2 октября 2018 г. Проверено 5 октября 2018 г.
- ^ Баум С.Дж., Тот П.П., Ундерберг Дж.А., Джеллингер П., Росс Дж., Вилемон К. (2017). «Барьеры доступа к ингибитору PCSK9 - проблемы и рекомендации: улучшение процесса доступа для пациентов, врачей и плательщиков». Клиническая кардиология. 40 (4): 243–254. Дои:10.1002 / clc.22713. ЧВК 5412679. PMID 28328015.
- ^ Навар А.М., Тейлор Б., Малдер Х., Фьевиц Э., Монда К.Л., Фьевиц А., Майя Дж. Ф., Лопес Дж. А., Петерсон Э.Д. (2017). «Связь предварительного разрешения и наличных расходов с доступом пациента к терапии ингибитором PCSK9». JAMA Кардиология. 2 (11): 1217–1225. Дои:10.1001 / jamacardio.2017.3451. ЧВК 5963012. PMID 28973087. Сложить резюме – Thomson Reuters.
- ^ «Идет матч по снижению цен на PCSK9, поскольку Regeneron и Sanofi сокращают отметку Praluent на 60%». FiercePharma. Получено 2019-05-18.
- ^ а б c d Зал СС (апрель 2013 г.). «Генетика: ген редкого действия». Природа. 496 (7444): 152–5. Bibcode:2013Натура.496..152H. Дои:10.1038 / 496152a. PMID 23579660.
- ^ а б Sijbrands EJ, Westendorp RG, Defesche JC, de Meier PH, Smelt AH, Kastelein JJ (2001). «Смертность в течение двух столетий в большой родословной с семейной гиперхолестеринемией: исследование смертности от генеалогического дерева». BMJ (под ред. Клинических исследований). 322 (7293): 1019–23. Дои:10.1136 / bmj.322.7293.1019. ЧВК 31037. PMID 11325764.
- ^ а б c Abifadel M, Varret M, Rabès JP, Allard D, Ouguerram K, Devillers M, Cruaud C, Benjannet S, Wickham L, Erlich D, Derré A, Villéger L, Farnier M, Beucler I, Bruckert E, Chambaz J, Chanu B. , Lecerf JM, Luc G, Moulin P, Weissenbach J, Prat A, Krempf M, Junien C, Seidah NG, Boileau C (июнь 2003 г.). «Мутации в PCSK9 вызывают аутосомно-доминантную гиперхолестеринемию». Nat. Genet. 34 (2): 154–6. Дои:10,1038 / ng1161. PMID 12730697.
- ^ Параг Х. Джоши, Сет С. Мартин и Роджер С. Блюменталь "Захватывающая история ингибирования PCSK9: идеи и перспективы ACC ", Кардиология сегодня, Май 2014. Дата обращения 5 октября 2018.
- ^ Абифадель М., Эльбитар С., Эль-Хури П., Галеб И., Химали М., Муссалли М.Л., Рабес Дж. П., Варрет М., Буало С. (сентябрь 2014 г.). «Приключение PCSK9: от идентификации нового гена семейной гиперхолестеринемии к потенциально новому классу антихолестериновых препаратов». Текущие отчеты об атеросклерозе. 16 (9): 439. Дои:10.1007 / s11883-014-0439-8. PMID 25052769.
- ^ «FDA одобряет использование Praluent для лечения некоторых пациентов с высоким уровнем холестерина». www.fda.gov. Получено 2015-07-26.
- ^ Ген PCSK9 - Домашний справочник по генетике
- ^ "PCSK9 пропротеин конвертаза субтилизин / кексин типа 9 [Homo sapiens (человек)] - Ген - NCBI". www.ncbi.nlm.nih.gov. Получено 2016-08-19.
- ^ а б «PCSK9 - предшественник пропротеинконвертазы субтилизина / кексина типа 9 - Homo sapiens (Human) - ген и белок PCSK9». www.uniprot.org. Получено 2016-08-19.
- ^ а б c d Du F, Hui Y, Zhang M, Linton MF, Fazio S, Fan D (декабрь 2011 г.). «Взаимодействие нового домена регулирует секрецию белка пропротеинконвертазы субтилизин / кексин типа 9 (PCSK9)». Журнал биологической химии. 286 (50): 43054–61. Дои:10.1074 / jbc.M111.273474. ЧВК 3234880. PMID 22027821.
- ^ Ло Сурдо П., Боттомли М.Дж., Кальцетта А., Сеттембре Е.К., Чирилло А., Пандит С., Ни Ю.Г., Хаббард Б., Ситлани А., Карфи А. (декабрь 2011 г.). «Механистические последствия деградации рецепторов LDL из структуры PCSK9 / LDLR при нейтральном pH». EMBO отчеты. 12 (12): 1300–5. Дои:10.1038 / embor.2011.205. ЧВК 3245695. PMID 22081141.
- ^ Пайпер Д.Е., Джексон С., Лю К., Романоу В.Г., Шеттерли С., Тибо С.Т., Шан Б., Уокер Н.П. (май 2007 г.). «Кристаллическая структура PCSK9: регулятор холестерина ЛПНП в плазме». Структура. 15 (5): 545–52. Дои:10.1016 / j.str.2007.04.004. PMID 17502100.
- ^ Боттомли М.Дж., Чирилло А., Орсатти Л., Руджери Л., Фишер Т.С., Санторо Д.С., Каммингс Р.Т., Куббон Р.М., Ло Сурдо П., Кальцетта А., Ното А., Байсарович Дж., Матту М., Таламо Ф., Де Франческо Р., Воробей С.П., Ситлани А., Карфи А. (январь 2009 г.). «Структурная и биохимическая характеристика комплекса PCSK9-EGF (AB) дикого типа и мутантов с естественной семейной гиперхолестеринемией» (PDF). Журнал биологической химии. 284 (2): 1313–23. Дои:10.1074 / jbc.M808363200. PMID 19001363.
- ^ Kwon HJ, Lagace TA, McNutt MC, Horton JD, Deisenhofer J (февраль 2008 г.). «Молекулярная основа распознавания рецептора ЛПНП с помощью PCSK9». Труды Национальной академии наук Соединенных Штатов Америки. 105 (6): 1820–5. Bibcode:2008ПНАС..105.1820К. Дои:10.1073 / pnas.0712064105. ЧВК 2538846. PMID 18250299.
- ^ PDB: 2П4Э Каннингем Д., Дэнли Д.Е., Геогхеган К.Ф., Гриффор М.С., Хокинс Д.Л., Субаши Т.А., Варгез А.Х., Аммирати М.Дж., Калп Дж.С., Хот Л.Р., Мансур М.Н., МакГрат К.М., Седдон А.П., Шеноликар С., Штутцман-Энгвал К.Дж., Уоррен Л.К., Ся Д, Цю Х (2007). «Структурные и биофизические исследования PCSK9 и его мутантов, связанных с семейной гиперхолестеринемией». Nat. Struct. Мол. Биол. 14 (5): 413–9. Дои:10.1038 / nsmb1235. PMID 17435765.
- ^ PDB: 2 вечера Пайпер Д.Е., Джексон С., Лю К., Романов В.Г., Шеттерли С., Тибо С.Т., Шан Б., Уокер Н.П. (2007). «Кристаллическая структура PCSK9: регулятор холестерина ЛПНП в плазме». Структура. 15 (5): 545–52. Дои:10.1016 / j.str.2007.04.004. PMID 17502100.
- ^ «Растущая роль модуляции PCSK9 в регуляции холестерина ЛПНП». Архивировано из оригинал 18 мая 2015 г.. Получено 13 мая 2015.
- ^ а б Чжан Д.В. и др. (Июнь 2007 г.). «Связывание пропротеинконвертазы субтилизин / кексин типа 9 с эпидермальным фактором роста-подобным повтором А рецептора липопротеинов низкой плотности снижает рециклинг рецептора и увеличивает деградацию». J Biol Chem. 282 (25): 18602–18612. Дои:10.1074 / jbc.M702027200. PMID 17452316.
- ^ Нората Г.Д., Тиболла Г., Катапано А.Л. (01.01.2014).«Нацеливание PCSK9 на гиперхолестеринемию». Ежегодный обзор фармакологии и токсикологии. 54: 273–93. Дои:10.1146 / annurev-pharmtox-011613-140025. PMID 24160703.
- ^ Бержерон Н., Фан Б.А., Дин И, Фонг А., Краусс Р.М. (октябрь 2015 г.). «Ингибирование пропротеинконвертазы субтилизин / кексин типа 9: новый терапевтический механизм для снижения риска сердечно-сосудистых заболеваний». Тираж. 132 (17): 1648–66. Дои:10.1161 / CIRCULATIONAHA.115.016080. PMID 26503748.
- ^ Ле Мэй С., Куримат С., Ланги С., Шетиво М., Жарри А., Комера С., Колле Х, Кейперс Ф., Кремпф М., Кариу Б., Костет П. (май 2009 г.). «Пропротеинконвертаза, субтилизин-кексин, нулевые мыши типа 9 защищены от постпрандиальной триглицеридемии». Артериосклероз, тромбоз и биология сосудов. 29 (5): 684–90. Дои:10.1161 / ATVBAHA.108.181586. PMID 19265033.
- ^ Рашид С., Тавори Х., Браун П. Е., Линтон М. Ф., Хе Дж., Джунциони И., Фацио С. (июль 2014 г.). «Пропротеинконвертаза субтилизин-кексин типа 9 способствует гиперпродукции в кишечнике богатых триглицеридами липопротеинов аполипопротеина B посредством как зависимых от рецепторов липопротеинов низкой плотности, так и независимых механизмов». Тираж. 130 (5): 431–41. Дои:10.1161 / CIRCULATIONAHA.113.006720. ЧВК 4115295. PMID 25070550.
- ^ Gustafsen C, Kjolby M, Nyegaard M, Mattheisen M, Lundhede J, Buttenschøn H, Mors O, Bentzon JF, Madsen P, Nykjaer A, Glerup S (февраль 2014 г.). «Ген риска гиперхолестеринемии SORT1 способствует секреции PCSK9». Клеточный метаболизм. 19 (2): 310–8. Дои:10.1016 / j.cmet.2013.12.006. PMID 24506872.
- ^ а б Schulz R, Schlüter KD, Laufs U (март 2015 г.). «Молекулярная и клеточная функция пропротеинконвертазы субтилизин / кексин типа 9 (PCSK9)». Фундаментальные исследования в кардиологии. 110 (2): 4. Дои:10.1007 / s00395-015-0463-z. ЧВК 4298671. PMID 25600226.
- ^ Кариу Б., Ланги С., Ле Бра М., Бортолотти М., Ле КА, Онитаз Ф, Ле Мэй С., Гайомарч-Деласалле Б., Заир И., Крайс Р., Бош С., Кремпф М., Таппи Л., Костет П. (2013- 01-01). «Концентрации PCSK9 в плазме во время пероральной жировой нагрузки и после краткосрочной диеты с высоким содержанием жиров, высоким содержанием жиров и высоким содержанием белка и высоким содержанием фруктозы». Питание и обмен веществ. 10 (1): 4. Дои:10.1186/1743-7075-10-4. ЧВК 3548771. PMID 23298392.
- ^ Лакоски С.Г., Лагас Т.А., Коэн Дж. К., Хортон Дж. Д., Хоббс Х. Х. (июль 2009 г.). «Генетические и метаболические детерминанты плазменных уровней PCSK9». Журнал клинической эндокринологии и метаболизма. 94 (7): 2537–43. Дои:10.1210 / jc.2009-0141. ЧВК 2708952. PMID 19351729.
- ^ Баасс А., Дубук Дж., Тремблей М., Делвин Е. Е., О'Лафлин Дж., Леви Е., Давиньон Дж., Ламберт М. (сентябрь 2009 г.). «Плазменный PCSK9 связан с возрастом, полом и множественными метаболическими маркерами в выборке детей и подростков». Клиническая химия. 55 (9): 1637–45. Дои:10.1373 / Clinchem.2009.126987. PMID 19628659.
- ^ Чжан Д.В., Гарути Р., Тан В.Дж., Коэн Дж.С., Хоббс Х.Х. (сентябрь 2008 г.). «Структурные требования для PCSK9-опосредованной деградации рецептора липопротеинов низкой плотности». Труды Национальной академии наук Соединенных Штатов Америки. 105 (35): 13045–50. Bibcode:2008PNAS..10513045Z. Дои:10.1073 / pnas.0806312105. ЧВК 2526098. PMID 18753623.
- ^ Поллак А (5 ноября 2012 г.). «Новые препараты от липидов вызывают гонку». Нью-Йорк Таймс.
- ^ "Ген Entrez: пропротеин конвертаза PCSK9 субтилизин / кексин типа 9".
- ^ Дубук Г., Чемберленд А., Вассеф Х., Давиньон Дж., Сейда Н. Г., Бернье Л., Прат А. (август 2004 г.). «Статины активируют PCSK9, ген, кодирующий пропротеин-конвертазу, регулируемую апоптозом нейрального апоптоза конвертазу-1, участвующую в семейной гиперхолестеринемии». Артериосклер. Тромб. Васк. Биол. 24 (8): 1454–9. Дои:10.1161 / 01.ATV.0000134621.14315.43. PMID 15178557.
- ^ а б c d Нората Г.Д., Тавори Н., Пирилло А., Фацио С., Катапано А.Л. (август 2016 г.). «Биология PCSK9: помимо снижения холестерина ЛПНП». Сердечно-сосудистые исследования. 112 (1): 429–42. Дои:10.1093 / cvr / cvw194. ЧВК 5031950. PMID 27496869.
- ^ Ферри Н., Тиболла Дж., Пирилло А., Чиполлоне Ф., Мезцетти А., Пачиа С., Корсини А., Катапано А. Л. (февраль 2012 г.). «Пропротеинконвертаза субтилизин-кексин типа 9 (PCSK9), секретируемая культивируемыми гладкомышечными клетками, снижает уровни ЛПНП макрофагов». Атеросклероз. 220 (2): 381–6. Дои:10.1016 / j.atherosclerosis.2011.11.026. PMID 22176652.
- ^ У CY, Тан Чж, Цзян Л., Ли XF, Цзян Ц.С., Лю Л.С. (январь 2012 г.). «SiRNA PCSK9 ингибирует апоптоз HUVEC, индуцированный ox-LDL через путь Bcl / Bax-caspase9-caspase3». Молекулярная и клеточная биохимия. 359 (1–2): 347–58. Дои:10.1007 / s11010-011-1028-6. PMID 21847580.
- ^ Джунзиони И., Тавори Х, Коваррубиас Р., Майор А.С., Динг Л., Чжан И, ДеВэй Р.М., Хонг Л., Фан Д., Предацци И.М., Рашид С., Линтон М.Ф., Фацио С. (январь 2016 г.). «Местные эффекты человеческого PCSK9 на атеросклеротическое поражение». Журнал патологии. 238 (1): 52–62. Дои:10.1002 / путь.4630. ЧВК 5346023. PMID 26333678.
- ^ а б c Коэн Дж. С., Бервинкль Э, Мосли Т. Х., Хоббс Х. Х. (март 2006 г.). «Вариации последовательности PCSK9, низкий уровень ЛПНП и защита от ишемической болезни сердца». Медицинский журнал Новой Англии. 354 (12): 1264–72. Дои:10.1056 / NEJMoa054013. PMID 16554528.
- ^ Гроувс С., Шетти С., Стрэндж Р.С., Уолдрон Дж., Рамачандран С. (август 2016 г.). «Исследование с участием пациентов с высоким риском, прошедших максимальное предварительное лечение, с целью определения потенциального использования ингибиторов PCSK9 при различных порогах общего уровня холестерина и холестерина ЛПНП» (PDF). Последипломный медицинский журнал. 93 (1098): postgradmedj – 2016–134062. Дои:10.1136 / postgradmedj-2016-134062. PMID 27531965.
- ^ Робинсон Дж. Г. (август 2016 г.). «Нестатины и ингибиторы пропротеин-конвертазы субтилизина / кексина типа 9 (PCSK9): роль в несемейной гиперхолестеринемии». Прогресс сердечно-сосудистых заболеваний. 59 (2): 165–171. Дои:10.1016 / j.pcad.2016.07.011. PMID 27498088.
- ^ Розенсон Р.С., Якобсон Т.А., Прейсс Д., Джеджос С.К., Дент Р., Мосты I, Миллер М. (август 2016 г.). «Исправление к: Эффективность и безопасность ингибитора PCSK9 Evolocumab у пациентов со смешанной гиперлипидемией». Сердечно-сосудистые препараты и терапия. 30 (5): 537. Дои:10.1007 / s10557-016-6684-z. ЧВК 6828239. PMID 27497929.
- ^ Пэн В., Цян Ф., Пэн В., Цянь З., Ке З., Йи Л., Цзянь З., Чонгронг К. (июль 2016 г.). «Терапевтическая эффективность моноклональных антител к PCSK9 у пациентов с гиперхолестеринемией и дислипидемией, не отвечающих на статины: систематический обзор и метаанализ». Международный журнал кардиологии. 222: 119–129. Дои:10.1016 / j.ijcard.2016.07.239. PMID 27494723.
- ^ Урбан Д., Пёсс Дж, Бём М., Лауфс У. (октябрь 2013 г.). «Нацеленность на пропротеинконвертазу субтилизин / кексин типа 9 для лечения дислипидемии и атеросклероза». Журнал Американского колледжа кардиологии. 62 (16): 1401–8. Дои:10.1016 / j.jacc.2013.07.056. PMID 23973703.
- ^ Нората Г.Д., Тиболла Г., Катапано А.Л. (август 2014 г.). «Ингибирование PCSK9 для лечения гиперхолестеринемии: перспективы и новые проблемы». Сосудистая фармакология. 62 (2): 103–11. Дои:10.1016 / j.vph.2014.05.011. PMID 24924410.
- ^ Коэн Дж., Перцемлидис А., Котовски И.К., Грэм Р., Гарсия К.К., Хоббс Х.Х. (февраль 2005 г.). «Низкий уровень холестерина ЛПНП у лиц африканского происхождения в результате частых бессмысленных мутаций в PCSK9». Природа Генетика. 37 (2): 161–5. Дои:10,1038 / ng1509. PMID 15654334.
- ^ Kathiresan S (май 2008 г.). «Миссенс-вариант PCSK9, связанный со сниженным риском инфаркта миокарда с ранним началом». Медицинский журнал Новой Англии. 358 (21): 2299–300. Дои:10.1056 / NEJMc0707445. PMID 18499582.
- ^ Ридкер П.М., Прадхан А., Макфадьен Дж. Г., Либби П., Глинн Р. Дж. (Август 2012 г.). «Польза для сердечно-сосудистой системы и риски диабета при терапии статинами в первичной профилактике: анализ исследования JUPITER». Ланцет. 380 (9841): 565–71. Дои:10.1016 / S0140-6736 (12) 61190-8. ЧВК 3774022. PMID 22883507.
- ^ Berger JM, Vaillant N, Le May C., Calderon C, Brégeon J, Prieur X, Hadchouel J, Loirand G, Cariou B. (март 2015 г.). «Дефицит PCSK9 не изменяет кровяное давление и баланс натрия в мышиных моделях гипертонии». Атеросклероз. 239 (1): 252–9. Дои:10.1016 / j.atherosclerosis.2015.01.012. PMID 25621930.
- ^ Шаротри В., Кольер Д.М., Олсон Д.Р., Чжоу Р., Снайдер П.М. (июнь 2012 г.). «Регулирование движения эпителиальных натриевых каналов с помощью пропротеинконвертазы субтилизин / кексин типа 9 (PCSK9)». Журнал биологической химии. 287 (23): 19266–74. Дои:10.1074 / jbc.M112.363382. ЧВК 3365958. PMID 22493497.
- ^ Нората Г.Д., Пирилло А., Аммирати Е., Катапано А.Л. (январь 2012 г.). «Возникающая роль липопротеинов высокой плотности как игрока в иммунной системе». Атеросклероз. 220 (1): 11–21. Дои:10.1016 / j.atherosclerosis.2011.06.045. PMID 21783193.
- ^ Дидрих Г (сентябрь 2006 г.). «Как вирус гепатита С попадает в клетки?». Журнал FEBS. 273 (17): 3871–85. Дои:10.1111 / j.1742-4658.2006.05379.x. PMID 16934030.
- ^ Чен Ю.К., Траутт Дж. С., Конрад Р. Дж. (Май 2014 г.). «PCSK9 присутствует в спинномозговой жидкости человека и поддерживается в удивительно постоянных концентрациях в течение дня». Липиды. 49 (5): 445–55. Дои:10.1007 / s11745-014-3895-6. PMID 24659111.
- ^ Лопес Д. (2008). «Ингибирование PCSK9 как новая стратегия лечения гиперхолестеринемии». Перспектива новостей о наркотиках. 21 (6): 323–30. Дои:10.1358 / dnp.2008.21.6.1246795. PMID 18836590.
- ^ Стейнберг Д., Витцтум Дж. Л. (июнь 2009 г.). «Ингибирование PCSK9: мощное оружие для достижения идеального уровня холестерина ЛПНП». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 106 (24): 9546–7. Bibcode:2009ПНАС..106.9546С. Дои:10.1073 / pnas.0904560106. ЧВК 2701045. PMID 19506257.
- ^ Майер Дж., Порье С., Сейда Н. Г. (ноябрь 2008 г.). «Аннексин А2 представляет собой C-концевой белок, связывающий PCSK9, который регулирует уровни эндогенных рецепторов липопротеинов низкой плотности». J. Biol. Chem. 283 (46): 31791–801. Дои:10.1074 / jbc.M805971200. PMID 18799458.
- ^ «Bristol-Myers Squibb выбирает препарат Isis, нацеленный на PCSK9, в качестве кандидата на разработку для профилактики и лечения сердечно-сосудистых заболеваний». Пресс-релиз. FierceBiotech. 2008-04-08. Получено 2010-09-18.
- ^ а б Фицджеральд, Кевин; Уайт, Суэлен; Бородовский, Анна; Bettencourt, Brian R .; Страс, Эндрю; Клаузен, Валери; Вейнгаард, Питер; Хортон, Джей Д .; Таубель, Йорг; Брукс, Эшли; Фернандо, Чамикара; Кауфман, Роберт С .; Калленд, Дэвид; Вайшнау, Акшай; Саймон, Эми (2017). "Терапевтический ингибитор PCSK9 с высокой прочностью на РНКи". Медицинский журнал Новой Англии. 376 (1): 41–51. Дои:10.1056 / NEJMoa1609243. ISSN 0028-4793. ЧВК 5778873. PMID 27959715.
- ^ Шеридан С (декабрь 2013 г.). "Данные фазы 3 для ингибитора PCSK9 вау". Природа Биотехнологии. 31 (12): 1057–8. Дои:10.1038 / nbt1213-1057. PMID 24316621.
- ^ Stein EA, Raal FJ (декабрь 2014 г.). «Новые методы лечения холестерина липопротеинов низкой плотности». Клиники эндокринологии и метаболизма Северной Америки. 43 (4): 1007–33. Дои:10.1016 / j.ecl.2014.08.008. PMID 25432394.
- ^ Фогель Р.А. (июнь 2012 г.). "Ингибирование PCSK9: следующий статин?". Журнал Американского колледжа кардиологии. 59 (25): 2354–5. Дои:10.1016 / j.jacc.2012.03.011. PMID 22465426.
- ^ а б Navarese EP, Kolodziejczak M, Schulze V, Gurbel PA, Tantry U, Lin Y, Brockmeyer M, Kandzari DE, Kubica JM, D'Agostino RB, Kubica J, Volpe M, Agewall S, Kereiakes DJ, Kelm M (июль 2015 г.) . «Эффекты антител к субтилизину / кексину 9 типа пропротеин-конвертазы у взрослых с гиперхолестеринемией: систематический обзор и метаанализ». Анналы внутренней медицины. 163 (1): 40–51. Дои:10.7326 / M14-2957. PMID 25915661.
- ^ Дурайрадж А., Сабатес А., Ньевес Дж., Мораес Б., Баум С. (август 2017 г.). "Proprotein Convertase Subtilisin / Kexin Type 9 (PCSK9) and its Inhibitors: a Review of Physiology, Biology, and Clinical Data". Современные варианты лечения в сердечно-сосудистой медицине. 19 (8): 58. Дои:10.1007 / s11936-017-0556-0. PMID 28639183.
- ^ Шмидт А.Ф., Пирс Л.С., Уилкинс Дж. Т., Оверингтон Дж. П., Хингорани А. Д., Касас Дж. П. (апрель 2017 г.). «Моноклональные антитела PCSK9 для первичной и вторичной профилактики сердечно-сосудистых заболеваний». Кокрановская база данных систематических обзоров. 4: CD011748. Дои:10.1002 / 14651858.CD011748.pub2. ЧВК 6478267. PMID 28453187.
- ^ "Медскейп". medscape.com. Получено 2019-05-18.
- ^ Кэрролл Дж. (7 марта 2014 г.). «Акции Regeneron, Sanofi и Amgen страдают от беспокойства FDA по поводу класса PCSK9». FierceBiotech.
- ^ Lambert G, Sjouke B, Choque B, Kastelein JJ, Hovingh GK (декабрь 2012 г.). «Десятилетие PCSK9». J. Lipid Res. 53 (12): 2515–24. Дои:10.1194 / мл. R026658. ЧВК 3494258. PMID 22811413.
- ^ Alenghat, Francis J .; Дэвис, Эндрю М. (2019). «Управление холестерином в крови». JAMA. 321 (8): 800–801. Дои:10.1001 / jama.2019.0015. ISSN 0098-7484. ЧВК 6679800. PMID 30715135.
- ^ Фицджеральд К., Франк-Каменецкий М., Шульга-Морская С., Либов А., Беттенкур Б. Р., Сазерленд Дж. Э., Хутабарат Р. М., Клаузен В. А., Карстен В., Чехельски Дж., Ночур С. В., Котелянски В., Хортон Дж., Мант Т., Кьеза Дж., Риттер Дж., Мунисами М., Вайшнау А.К., Голлоб Дж. А., Саймон А. (январь 2014 г.). «Влияние препарата для интерференции РНК на синтез пропротеинконвертазы субтилизин / кексин типа 9 (PCSK9) и концентрацию холестерина ЛПНП в сыворотке крови здоровых добровольцев: рандомизированное, простое слепое, плацебо-контролируемое исследование фазы 1». Ланцет. 383 (9911): 60–8. Дои:10.1016 / S0140-6736 (13) 61914-5. ЧВК 4387547. PMID 24094767.
- ^ Шан Л., Панг Л., Чжан Р., Мурголо Н.Дж., Лан Х., Хедрик Д.А. (октябрь 2008 г.). «PCSK9 связывается с множеством рецепторов и может функционально ингибироваться пептидом EGF-A». Biochem. Биофиз. Res. Сообщество. 375 (1): 69–73. Дои:10.1016 / j.bbrc.2008.07.106. PMID 18675252.
- ^ Грэм MJ, Lemonidis KM, Whipple CP, Subramaniam A, Monia BP, Crooke ST, Crooke RM (апрель 2007 г.). «Антисмысловое ингибирование пропротеинконвертазы субтилизин / кексин типа 9 снижает уровень ЛПНП в сыворотке у мышей с гиперлипидемией». J. Lipid Res. 48 (4): 763–7. Дои:10.1194 / мл. C600025-JLR200. PMID 17242417.
- ^ Гупта Н., Фискер Н., Асселин М.С., Линдхольм М., Розенбом С., Орум Х., Элмен Дж., Сейда Н.Г., Страаруп Е.М. (2010). Деб С. (ред.). «Антисмысловой олигонуклеотид с заблокированной нуклеиновой кислотой (LNA) заглушает PCSK9 и усиливает экспрессию LDLR in vitro и in vivo». PLoS ONE. 5 (5): e10682. Bibcode:2010PLoSO ... 510682G. Дои:10.1371 / journal.pone.0010682. ЧВК 2871785. PMID 20498851.
- ^ Линдхольм М.В., Элмен Дж., Фискер Н., Хансен Х.Ф., Перссон Р., Мёллер М.Р., Розенбом С., Орум Х., Страаруп Е.М., Кох Т. (февраль 2012 г.). «Антисмысловые олигонуклеотиды PCSK9 LNA вызывают устойчивое снижение холестерина ЛПНП у нечеловеческих приматов». Мол. Ther. 20 (2): 376–81. Дои:10.1038 / мт.2011.260. ЧВК 3277239. PMID 22108858.
- ^ «Alnylam сообщает о положительных предварительных клинических результатах ALN-PCS, РНКи-терапевтического нацеливания на PCSK9 для лечения тяжелой гиперхолестеринемии». Пресс-релиз. BusinessWire. 2011-01-04. Архивировано из оригинал на 21.02.2013. Получено 2011-01-04.
- ^ Франк-Каменецкий М., Грефхорст А., Андерсон Н. Н., Рэйси Т. С., Брамлаг Б., Акинк А., Батлер Д., Чарисс К., Доркин Р., Фан Y, Гамба-Витало С., Хадвигер П., Джаяраман М., Джон М., Джаяпракаш К. Н., Майер M, Nechev L, Rajeev KG, Read T, Röhl I, Soutschek J, Tan P, Wong J, Wang G, Zimmermann T., de Fougerolles A, Vornlocher HP, Langer R, Anderson DG, Manoharan M, Koteliansky V, Horton JD , Фицджеральд К. (август 2008 г.). «Терапевтическая РНКи, нацеленная на PCSK9, резко снижает уровень холестерина в плазме у грызунов и холестерина ЛПНП у нечеловеческих приматов». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 105 (33): 11915–20. Bibcode:2008PNAS..10511915F. Дои:10.1073 / pnas.0805434105. ЧВК 2575310. PMID 18695239.
- ^ Кросси Э., Амар М.Дж., Сэмпсон М., Пибоди Дж., Шиллер Д.Т., Чакериан Б., Ремалей А.Т. (октябрь 2015 г.). «Вакцина VLP, снижающая уровень холестерина, нацелена на PCSK9». Вакцина. 33 (43): 5747–55. Дои:10.1016 / j.vaccine.2015.09.044. ЧВК 4609631. PMID 26413878.
- ^ Ли Х, Донг Б., Пак С.В., Ли Х.С., Чен В., Лю Дж. (Август 2009 г.). «HNF1α играет решающую роль в транскрипции и регуляции гена PCSK9 с помощью природного гипохолестеринемического соединения берберина». Журнал биологической химии. 284 (42): 28885–95. Дои:10.1074 / jbc.M109.052407. ЧВК 2781434. PMID 19687008.
- ^ а б Донг Б., Ли Х., Сингх А.Б., Цао А., Лю Дж. (Февраль 2015 г.). «Ингибирование транскрипции PCSK9 берберином включает подавление экспрессии белка HNF1α в печени посредством пути деградации убиквитин-протеасома». Журнал биологической химии. 290 (7): 4047–58. Дои:10.1074 / jbc.M114.597229. ЧВК 4326815. PMID 25540198.
- ^ Донг Х, Чжао Й, Чжао Л., Лу Ф (апрель 2013 г.). «Влияние берберина на липиды крови: системный обзор и метаанализ рандомизированных контролируемых исследований». Planta Medica. 79 (6): 437–46. Дои:10.1055 / с-0032-1328321. PMID 23512497.
- ^ Сейда Н.Г., Пуарье С., Денис М., Паркер Р., Мяо Б., Мапелли С., Прат А., Вассеф Х., Давиньон Дж., Хаджар К.А., Майер Г. (2012). «Аннексин А2 является естественным внепеченочным ингибитором вызванной PCSK9 деградации рецептора ЛПНП». PLoS ONE. 7 (7): e41865. Bibcode:2012PLoSO ... 741865S. Дои:10.1371 / journal.pone.0041865. ЧВК 3407131. PMID 22848640.
дальнейшее чтение
- Абифадель М., Рабес Дж. П., Буало С., Варре М. (июнь 2007 г.). «[После рецептора ЛПНП и аполипопротеина B аутосомно-доминантная гиперхолестеринемия обнаруживает своего третьего главного героя: PCSK9]». Анна. Эндокринол. (На французском). 68 (2–3): 138–46. Дои:10.1016 / j.ando.2007.02.002. PMID 17391637.
- Allard D, Amsellem S, Abifadel M, Trillard M, Devillers M, Luc G, Krempf M, Reznik Y, Girardet JP, Fredenrich A, Junien C, Varret M, Boileau C, Benlian P, Rabès JP (ноябрь 2005 г.). «Новые мутации гена PCSK9 вызывают вариабельный фенотип аутосомно-доминантной гиперхолестеринемии». Гм. Мутат. 26 (5): 497. Дои:10.1002 / humu.9383. PMID 16211558.
- Бенджаннет С., Райндс Д., Эссалмани Р., Мейн Дж., Викхэм Л., Джин В., Асселин М.С., Хамелин Дж., Варрет М., Аллард Д., Триллард М., Абифадель М., Тебон А., Атти А. Д., Рейдер Д. Д., Буало С., Бриссет Л. , Кретьен М., Прат А., Сейда Н.Г. (ноябрь 2004 г.). «NARC-1 / PCSK9 и его естественные мутанты: расщепление зимогена и влияние на рецептор липопротеинов низкой плотности (ЛПНП) и холестерин ЛПНП». J. Biol. Chem. 279 (47): 48865–75. Дои:10.1074 / jbc.M409699200. PMID 15358785.
- Lalanne F, Lambert G, Amar MJ, Chétiveaux M, Zaïr Y, Jarnoux AL, Ouguerram K, Friburg J, Seidah NG, Brewer HB, Krempf M, Costet P (июнь 2005 г.). «PCSK9 дикого типа ингибирует клиренс ЛПНП, но не влияет на выработку апоВ-содержащих липопротеинов в мышах и культивируемых клетках». J. Lipid Res. 46 (6): 1312–9. Дои:10.1194 / мл. M400396-JLR200. PMID 15741654.
- Ламберт Дж. (Июнь 2007 г.). «Раскрытие функционального значения PCSK9». Curr. Мнение. Липидол. 18 (3): 304–9. Дои:10.1097 / MOL.0b013e3281338531. PMID 17495605.
- Лерен Т.П. (май 2004 г.). «Мутации в гене PCSK9 у норвежских субъектов с аутосомно-доминантной гиперхолестеринемией». Clin. Genet. 65 (5): 419–22. Дои:10.1111 / j.0009-9163.2004.0238.x. PMID 15099351.
- Максвелл К.Н., Бреслоу Дж. Л. (май 2004 г.). «Опосредованная аденовирусом экспрессия Pcsk9 у мышей приводит к фенотипу нокаута рецепторов липопротеинов низкой плотности». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 101 (18): 7100–5. Bibcode:2004ПНАС..101.7100М. Дои:10.1073 / pnas.0402133101. ЧВК 406472. PMID 15118091.
- Максвелл К.Н., Социо Р.Э., Дункан Е.М., Сехайек Е., Бреслоу Дж. Л. (ноябрь 2003 г.). «Новые предполагаемые гены-мишени SREBP и LXR, идентифицированные с помощью микроматричного анализа в печени мышей, получавших холестерин». J. Lipid Res. 44 (11): 2109–19. Дои:10.1194 / мл. M300203-JLR200. PMID 12897189.
- Наумова Р.П., Този И., Патель Д., Нойвирт К., Хорсвелл С.Д., Марэ А.Д., ван Хейнинген С., Сутар А.К. (декабрь 2005 г.). «Тяжелая гиперхолестеринемия в четырех британских семьях с мутацией D374Y в гене PCSK9: долгосрочное наблюдение и ответ на лечение». Артериосклер. Тромб. Васк. Биол. 25 (12): 2654–60. Дои:10.1161 / 01.ATV.0000190668.94752.ab. PMID 16224054.
- Наурекиене С., Ма Л., Срикумар К., Пурандаре Ю., Ло К. Ф., Хуанг И, Чан Л. В., Гренье Дж. М., Озенбергер Б. А., Якобсен Дж. С., Кеннеди Д. Д., ДиСтефано П. С., Вуд А, Бингем Б. (декабрь 2003 г.). «Функциональная характеристика Narc 1, новой протеиназы, родственной протеиназе K». Arch. Biochem. Биофизы. 420 (1): 55–67. Дои:10.1016 / j.abb.2003.09.011. PMID 14622975.
- Угеррам К., Четиво М., Заир И., Костет П., Абифадель М., Варрет М., Буало С., Магот Т., Кремпф М. (август 2004 г.). «Метаболизм аполипопротеина B100 при аутосомно-доминантной гиперхолестеринемии, связанный с мутациями в PCSK9». Артериосклер. Тромб. Васк. Биол. 24 (8): 1448–53. Дои:10.1161 / 01.ATV.0000133684.77013.88. PMID 15166014.
- Пишотта Л., Приоре Олива С., Чефалу А.Б., Ното Д., Беллоккио А., Фреза Р., Кантафора А., Патель Д., Аверна М., Таруги П., Каландра С., Бертолини С. (июнь 2006 г.). «Аддитивный эффект мутаций в генах LDLR и PCSK9 на фенотип семейной гиперхолестеринемии». Атеросклероз. 186 (2): 433–40. Дои:10.1016 / j.atherosclerosis.2005.08.015. PMID 16183066.
- Сибата Н., Охнума Т., Хигаши С., Хигаши М., Усуи С., Окубо Т., Ватанабэ Т., Кавасима Р., Китадзима А., Уэки А., Нагао М., Араи Х. (декабрь 2005 г.). «Нет генетической связи между полиморфизмом PCSK9 и болезнью Альцгеймера и уровнем холестерина в плазме у японских пациентов». Психиатр. Genet. 15 (4): 239. Дои:10.1097/00041444-200512000-00004. PMID 16314752.
- Sun XM, Eden ER, Tosi I, Neuwirth CK, Wile D, Naoumova RP, Soutar AK (май 2005 г.). «Доказательства воздействия мутанта PCSK9 на секрецию аполипопротеина B как причины необычно тяжелой доминантной гиперхолестеринемии». Гм. Мол. Genet. 14 (9): 1161–9. Дои:10.1093 / hmg / ddi128. PMID 15772090.
- Тиммс К.М., Вагнер С., Сэмюэлс М.Э., Форби К., Голдфайн Х, Джаммулапати С., Сколник М.Х., Хопкинс П.Н., Хант С.К., Шаттак Д.М. (март 2004 г.). «Мутация в PCSK9, вызывающая аутосомно-доминантную гиперхолестеринемию в родословной Юты». Гм. Genet. 114 (4): 349–53. Дои:10.1007 / s00439-003-1071-9. PMID 14727179.
- Varret M, Rabès JP, Saint-Jore B, Cenarro A, Marinoni JC, Civeira F, Devillers M, Krempf M, Coulon M, Thiart R, Kotze MJ, Schmidt H, Buzzi JC, Kostner GM, Bertolini S, Pocovi M, Роза А., Фарнье М., Мартинес М., Жуниен С., Буало С. (май 1999 г.). «Третий главный локус аутосомно-доминантной гиперхолестеринемии соответствует 1p34.1-p32». Являюсь. J. Hum. Genet. 64 (5): 1378–87. Дои:10.1086/302370. ЧВК 1377874. PMID 10205269.