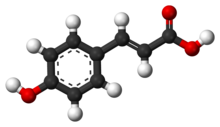
П-кумаровая кислота - P-Coumaric acid
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC (2E) -3- (4-гидроксифенил) проп-2-еновая кислота | |
| Другие имена (E) -3- (4-гидроксифенил) -2-пропеновая кислота (E) -3- (4-гидроксифенил) акриловая кислота параграф-Кумаровая кислота 4-гидроксикоричная кислота β- (4-гидроксифенил) акриловая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 2207383 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.116.210 |
| Номер ЕС |
|
| 2245630 | |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C9ЧАС8О3 | |
| Молярная масса | 164.160 г · моль−1 |
| Температура плавления | От 210 до 213 ° C (от 410 до 415 ° F; от 483 до 486 K) |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H301, H302, H311, H314, H315, H317, H319, H335 | |
| P260, P261, P264, P270, P271, P272, P280, P301 + 310, P301 + 312, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P312, P321, P322, P330, P332 + 313, P333 + 313, P337 + 313, P361, P362, P363 | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
п-Кумаровая кислота это гидроксикоричная кислота, органическое соединение, которое является гидрокси производная от коричная кислота. Есть три изомеры из кумаровая кислота —о-куаровая кислота, м-куаровая кислота и п-куаровая кислота - которые различаются положением гидроксизамещения фенильной группы. п-Кумаровая кислота - самый распространенный изомер из трех в природе. п-Кумаровая кислота существует в двух формах транс-п-куаровая кислота и СНГ-п-куаровая кислота.
Это твердое кристаллическое вещество, которое слабо растворяется в воде, но хорошо растворяется в этиловый спирт и диэтиловый эфир.
Природные явления
п-Кумаровую кислоту можно найти в Gnetum cleistostachyum.[1]
В еде
п-Кумаровую кислоту можно найти в самых разных съедобных растениях и грибах, таких как арахис, морская фасоль, помидоры, морковь, Бэзил и чеснок.[нужна цитата ] Он находится в вино и уксус.[2] Он также встречается в ячмень зерно.[3]
п-Кумаровая кислота из пыльца является составной частью медовый.[4]
Производные
п-Глюкозид кумаровой кислоты также можно найти в коммерческих хлеб содержащий Льняное.[5]
Диэфиры п-куаровая кислота содержится в карнаубский воск.
Метаболизм
Биосинтез
Биосинтезируется из коричная кислота действием P450 -зависимый фермент Гидроксилаза 4-коричной кислоты (C4H).
Также производится из L-тирозин действием тирозин аммиаклиаза (TAL).

 + NH3 + H+
+ NH3 + H+
Биосинтетический строительный блок
п-Кумаровая кислота является предшественником 4-этилфенол произведенный дрожжи Brettanomyces в вине. Фермент циннамат декарбоксилаза катализирует превращение масла п-куаровая кислота в 4-винилфенол.[6] Винилфенолредуктаза затем катализирует восстановление 4-винилфенола до 4-этилфенола. Кумаровую кислоту иногда добавляют в микробиологические среды, что позволяет точно идентифицировать Brettanomyces по запаху.
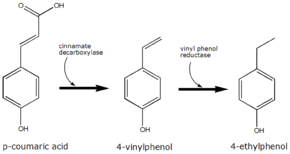 Преобразование п-куаровая кислота в 4-этифенол путем Brettanomyces
Преобразование п-куаровая кислота в 4-этифенол путем Brettanomyces
СНГ-п-Кумарат глюкозилтрансфераза это фермент, который использует уридиндифосфат глюкоза и СНГ-п-кумарат производить 4′-О-β-D-глюкозил-СНГ-п-кумарат и уридиндифосфат (UDP). Этот фермент принадлежит к семейству гликозилтрансфераз, в частности гексозилтрансфераз.[7]
Флоретиновая кислота, найденный в рубец из овца скармливаемый сушеной травой, образуется путем гидрогенизации 2-пропеновой боковой цепи п-куаровая кислота.[8]
Фермент, ресвератрол синтаза, также известный как стильбенсинтаза, катализирует синтез ресвератрол в конечном итоге из тетракетида, полученного из 4-кумароил КоА.[9]
п-Кумаровая кислота является кофактором фотоактивные желтые белки (PYP), гомологичная группа белков, обнаруженная во многих эубактериях.[10]
Смотрите также
- Кумарин
- Кумароил-Коэнзим А
- Феруловая кислота
- Коричная кислота
- Содержание фенолов в вине
- п-Кумароилированные антоцианы
Рекомендации
- ^ Яо К.С., Линь М., Лю Х, Ван Й. (апрель 2005 г.). «Производные стилябена из Gnetum cleistostachyum». Журнал азиатских исследований натуральных продуктов. 7 (2): 131–7. Дои:10.1080/10286020310001625102. PMID 15621615.
- ^ Гальвес М.С., Баррозо К.Г., Перес-Бустаманте Я.А. (1994). «Анализ полифенольных соединений различных образцов уксуса». Zeitschrift für Lebensmittel-Untersuchung und -Forschung. 199: 29–31. Дои:10.1007 / BF01192948.
- ^ Quinde-Axtell Z, Baik BK (декабрь 2006 г.). «Фенольные соединения зерна ячменя и их влияние на изменение цвета пищевых продуктов». Журнал сельскохозяйственной и пищевой химии. 54 (26): 9978–84. Дои:10.1021 / jf060974w. PMID 17177530.
- ^ Мао В., Шулер М.А., Беренбаум М.Р. (май 2013 г.). «Компоненты меда активируют гены детоксикации и иммунитета у западной медоносной пчелы Apis mellifera». Труды Национальной академии наук Соединенных Штатов Америки. 110 (22): 8842–6. Bibcode:2013ПНАС..110.8842М. Дои:10.1073 / pnas.1303884110. ЧВК 3670375. PMID 23630255.
- ^ Страндос С., Камал-Элдин А., Андерссон Р., Аман П. (октябрь 2008 г.). «Фенольные глюкозиды в хлебе, содержащем льняное семя». Пищевая химия. 110 (4): 997–9. Дои:10.1016 / j.foodchem.2008.02.088. PMID 26047292.
- ^ «Мониторинг Brettanomyces с помощью анализа 4-этилфенола и 4-этилгуаякола». etslabs.com. Архивировано из оригинал 19 февраля 2008 г.
- ^ Расмуссен С, Рудольф Х (1997). «Выделение, очистка и характеристика UDP-глюкозы: СНГ-п-куаровая кислота-β-D-глюкозилтрансфераза из sphagnum fallax ». Фитохимия. 46 (3): 449–453. Дои:10.1016 / S0031-9422 (97) 00337-3.
- ^ Чессон А., Стюарт К. С., Уоллес Р. Дж. (Сентябрь 1982 г.). «Влияние фенольных кислот растений на рост и целлюлозолитическую активность бактерий рубца». Прикладная и экологическая микробиология. 44 (3): 597–603. ЧВК 242064. PMID 16346090.
- ^ Ван, Чуаньхун; Чжи, Шуанг; Лю, Чанъин; Сюй Фэнсян; Чжао, Айчунь; Ван, Силин; Рен, Яньхун; Ли, Чжэнган; Ю, Маоде (2017). «Характеристика генов стильбен-синтазы в шелковице (Morus atropurpurea) и метаболической инженерии для производства ресвератрола в кишечная палочка". Журнал сельскохозяйственной и пищевой химии. 65 (8): 1659–1668. Дои:10.1021 / acs.jafc.6b05212. PMID 28168876.
- ^ Hoff WD, Düx P, Hård K, Devreese B, Nugteren-Roodzant IM, Crielaard W., Boelens R, Kaptein R, van Beeumen J, Hellingwerf KJ (ноябрь 1994 г.). "Тиоловый эфир связанный п-куаровая кислота как новая фотоактивная простетическая группа в белке с фотохимией, подобной родопсину ». Биохимия. 33 (47): 13959–62. Дои:10.1021 / bi00251a001. PMID 7947803.






