Алкеновый комплекс переходных металлов - Transition metal alkene complex
В металлоорганическая химия, а алкеновый комплекс переходных металлов это координационное соединение содержащие один или несколько алкенов лиганды. Такие соединения являются промежуточными продуктами многих каталитических реакций, которые превращают алкены в другие органические продукты.[1]
Моно- и диалкены часто используются в качестве лигандов в стабильных комплексах.
Моноалкены
Самый простой моноалкен - это этилен. Известно много комплексов этилена, в том числе Соль Цейзе (см. рисунок), Rh2Cl2(C2ЧАС4)4, Cp *2Ti (C2ЧАС4), а гомолептик Ni (C2ЧАС4)3. Замещенный моноалкен включает циклический циклооктен, как найдено в хлорбис (циклооктен) димер родия. Алкены с электроноакцепторными группами обычно прочно связываются с низковалентными металлами. Примеры таких лигандов: TCNE, тетрафторэтилен, малеиновый ангидрид, эфиры фумаровая кислота. Эти акцепторы образуют аддукты со многими нульвалентными металлами.
Диены, триены, полиены, кетоалкены и другие сложные алкеновые лиганды
Бутадиен, циклооктадиен, и норборнадиен являются хорошо изученными хелатирующими агентами. Триены и даже некоторые тетраены могут связываться с металлами через несколько соседних углеродных центров. Распространенными примерами таких лигандов являются циклогептатриен и циклооктатетраен. Склеивание часто обозначают с помощью осязание формализм. Кетоалкены представляют собой тетрагапто-лиганды, которые стабилизируют высоконенасыщенные низковалентные металлы, как обнаружено в (бензилиденацетон) трикарбонил железа и трис (дибензилиденацетон) дипалладий (0).
- Алкеновые комплексы металлов.
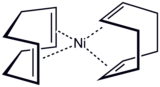
Бис (циклооктадиен) никель (0), катализатор и источник «голого никеля».

Анион в Соль Цейзе, первый алкеновый комплекс.

Димер хлорбис (циклооктен) родия, источник «RhCl».
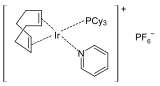
Катализатор Крэбтри, очень активный катализатор гидрирования.

(Бензилиденацетон) трикарбонил железа, источник Fe (CO)3".

[[Et3П]2Pt]6(η2: η2: η2: η2: η2: η2-C60), а фуллереновый комплекс.
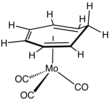
Пн (C7ЧАС8) (CO)3, комплекс циклогептатриен.

Fe (C8ЧАС8)2, комплекс циклооктатетраен

(Норборнадиен) тетракарбонил молибдена, источник «Mo (CO)4".
Склеивание
Связь между алкенами и переходными металлами описывается Модель Дьюара – Чатта – Дункансона, который включает в себя отдачу электронов на пи-орбитали алкена пустым орбиталям на металле. Это взаимодействие усиливается обратной связью, которая влечет за собой разделение электронов на других металлических орбиталях на пустой в противном случае уровень пи-антисвязи на алкене. Ранние металлы с низкой степенью окисления (Ti (II), Zr (II), Nb (III) и т. Д.) Являются сильными пи-донорами, а их алкеновые комплексы часто называют металламиклопропанами. Обработка таких видов кислотами дает алканы. Поздние металлы (Ir (I), Pt (II)), которые являются более бедными пи-донорами, имеют тенденцию задействовать алкен в качестве Кислота Льюиса –База Льюиса взаимодействие.
- Склеивание изображений

Орбитальные взаимодействия в комплексе металл-этилен, как описано Модель Дьюара – Чатта – Дункансона
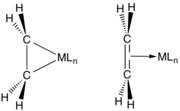
Два крайних изображения M --- C2ЧАС4 взаимодействия.
Вращательный барьер
Барьер для вращения алкена вокруг вектора М-центроида является мерой прочности пи-связи М-алкена. Комплексы этилена с низкой симметрией, например Cp Rh (C2ЧАС4)2, подходят для анализа барьеров вращения, связанных со связью металл-этилен. В анионе Цейзе ([PtCl3(C2ЧАС4)]−) этот вращательный барьер не может быть оценен ЯМР-спектроскопия потому что все четыре протона эквивалентны.
Реакции
Алкеновые лиганды теряют большую часть своего ненасыщенного характера при комплексообразовании. Наиболее известно, что алкеновый лиганд подвергается миграционная вставка, где он подвергается внутримолекулярной атаке алкильными и гидридными лигандами с образованием новых алкильных комплексов. Катионные алкеновые комплексы подвержены атаке нуклеофилов.
Катализ
Алкеновые комплексы металлов являются промежуточными продуктами во многих или большинстве реакций алкенов, катализируемых переходными металлами: полимеризация., гидрирование, гидроформилирование, и многие другие реакции.
Естественное явление
Металл-алкеновые комплексы необычны в природе, за одним исключением. Этилен влияет на созревание фруктов и цветов за счет образования комплекса с центром Cu (I) в фактор транскрипции.[2]
Рекомендации
- ^ Эльшенбройх, К. «Металлоорганические соединения» (2006) Wiley-VCH: Weinheim. ISBN 3-527-29390-6
- ^ Хосе М. Алонсо, Анна Н. Степанова "Путь передачи сигналов этилена" Наука 2004, т. 306, с. 1513-1515. Дои:10.1126 / science.1104812











