Третичная структура нуклеиновой кислоты - Nucleic acid tertiary structure

Третичная структура нуклеиновой кислоты это трехмерный форма нуклеиновая кислота полимер.[1] РНК и ДНК молекулы способны выполнять различные функции, начиная от молекулярное распознавание к катализ. Такие функции требуют точной трехмерной третичная структура. Хотя такие структуры разнообразны и кажутся сложными, они состоят из повторяющихся, легко узнаваемых мотивов третичной структуры, которые служат молекулярными строительными блоками. Некоторые из наиболее распространенных мотивов для РНК и третичная структура ДНК описаны ниже, но эта информация основана на ограниченном количестве решенных структур. По мере получения структурных характеристик новых молекул РНК и ДНК будет обнаружено еще много третичных структурных мотивов.
Винтовые конструкции

Двойная спираль
Двойная спираль - это доминирующая третичная структура биологической ДНК, а также возможная структура для РНК. Считается, что в природе встречаются три конформации ДНК: А-ДНК, B-ДНК, и Z-ДНК. Форма "B", описанная Джеймс Д. Уотсон и Фрэнсис Крик считается преобладающим в клетках.[2] Джеймс Д. Уотсон и Фрэнсис Крик описал эту структуру как двойную спираль радиусом 10 Å и шаг 34 Å, делая один полный оборот вокруг своей оси каждые 10 бп последовательности.[3] Двойная спираль совершает один полный оборот вокруг своей оси через каждые 10,4–10,5 пар оснований в растворе. Эта частота скручивания (известная как спиральная подача) в значительной степени зависит от сил складывания, которые каждая база оказывает на своих соседей по цепочке. Двухспиральная РНК принимает конформацию, аналогичную структуре А-формы.
Возможны другие конформации; фактически, теперь доступны только буквы F, Q, U, V и Y для описания любой новой структуры ДНК, которая может появиться в будущем.[4][5] Однако большинство этих форм были созданы синтетически и не наблюдались в природных биологических системах.

Триплексы с большой и малой бороздками
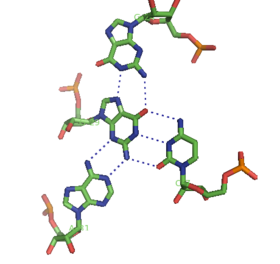
Малая тройка канавок - это повсеместная РНК структурный мотив. Поскольку взаимодействие с малая бороздка часто опосредуются 2'-ОН рибоза сахар, этот мотив РНК очень отличается от его ДНК эквивалент. Наиболее распространенный пример тройной малой бороздки - мотив ля минор или вставка аденозин основания в малую канавку (см. выше). Однако этот мотив не ограничивается аденозинами, как другие азотистые основания также наблюдали взаимодействие с малой бороздкой РНК.
Малая канавка представляет собой почти идеальное дополнение для вставной базы. Это позволяет оптимально van der Waals контакты, обширный водородная связь и гидрофобный поверхностное захоронение и создает энергетически выгодное взаимодействие.[8] Поскольку тройки малых канавок способны стабильно упаковывать свободную петлю и спираль, они являются ключевыми элементами в структуре больших рибонуклеотиды, включая интрон группы I,[9] интрон группы II,[10] и рибосома.
Хотя большая бороздка стандартной A-формы РНК довольно узкая и поэтому менее доступна для триплексного взаимодействия, чем малая бороздка, триплексные взаимодействия большой бороздки могут наблюдаться в нескольких структурах РНК. Эти структуры состоят из нескольких комбинаций базовая пара и взаимодействия Хугстина. Например, триплекс GGC (GGC амино (N-2) -N-7, иминокарбонил, карбониламино (N-4); Watson-Crick), наблюдаемый в 50S рибосома, состоящий из пары G-C типа Уотсона-Крика и входящей G, которая образует псевдо-хугстиновскую сеть взаимодействий водородных связей между обоими основаниями, участвующими в каноническом спаривании.[11] Другие известные примеры триплексов с большими бороздками включают (i) каталитическое ядро интрон группы II показано на рисунке слева [6] (ii) каталитически важный тройная спираль наблюдается у человека теломеразная РНК[7] и (iii) Рибопереключатель SAM-II.[13]
Трехцепочечная ДНК также возможно из Хугстина или обратные водородные связи Хугстина в основной канавке B-форма ДНК.
Квадруплексы
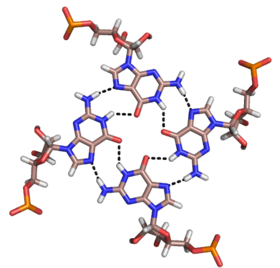
Помимо двойные спирали и упомянутые выше триплексы, РНК и ДНК оба могут также образовывать четверные спирали. Существуют различные структуры квадруплексов оснований РНК. Четыре подряд гуанин остатки могут образовывать квадруплекс в РНК за счет Hoogsteen водородные связи с образованием «кольца Хугстина» (см. рисунок).[11] Пары G-C и A-U также могут образовывать базовый квадруплекс с комбинацией Уотсон-Крик спаривание и неканоническое спаривание в малая бороздка.[14]
Ядро малахитового зеленого аптамер также является разновидностью базового квадруплекса с другим рисунком водородных связей (см. рисунок).[12] Квадруплекс может повторяться несколько раз подряд, образуя чрезвычайно стабильную структуру.
Уникальная структура квадруплексных областей в РНК может выполнять различные функции в биологической системе. Две важные функции - это потенциал связывания с лиганды или белки, и его способность стабилизировать весь третичная структура ДНК или РНК. Сильная структура может подавлять или модулировать транскрипция и репликация, например, в теломеры хромосом и UTR мРНК.[15] Идентичность основания важна для связывания лиганда. G-квартет обычно связывает одновалентные катионы, такие как калий, в то время как другие основания могут связывать множество других лигандов, таких как гипоксантин, в квадруплексе U-U-C-U.[14]
Наряду с этими функциями G-квадруплекс в мРНК вокруг участков связывания рибосом может служить регулятором экспрессия гена в бактерии.[16] Возможно, еще предстоит открыть более интересные структуры и функции. in vivo.
Коаксиальный стек

Коаксиальная укладка, также известная как спиральная укладка, является основным фактором, определяющим третичную структуру РНК более высокого порядка. Коаксиальный стэкинг происходит, когда два дуплекса РНК образуют непрерывную спираль, которая стабилизируется базовая укладка на стыке двух спиралей. Коаксиальная укладка отмечена в Кристальная структура тРНАФе.[18] Совсем недавно коаксиальное наложение было обнаружено в структурах более высокого порядка многих рибозимы, в том числе многие формы самосращивания группа I и группа II интроны. Общие мотивы коаксиального стека включают цикл поцелуев взаимодействие и псевдоузел. Стабильность этих взаимодействий можно предсказать, адаптировав «правила Тернера».[19]
В 1994 году Уолтер и Тернер определили вклад свободной энергии взаимодействий стекирования ближайших соседей в интерфейсе спираль-спираль, используя модельную систему, которая создавала границу раздела спираль-спираль между короткими олигомер и четырех-нуклеотид свес в конце ножка шпильки . Их эксперименты подтвердили, что термодинамический вклад наложения оснований между двумя спиральными вторичными структурами близко имитирует термодинамику образования стандартного дуплекса (взаимодействия ближайших соседей предсказывают термодинамическую стабильность полученной спирали). Относительная стабильность взаимодействий ближайших соседей может быть использована для предсказания благоприятного коаксиального стэкинга на основе известной вторичной структуры. Уолтер и Тернер обнаружили, что в среднем предсказание структуры РНК улучшилось с 67% до 74% точности, когда были включены вклады коаксиального стека.[20]
Наиболее хорошо изученные третичные структуры РНК содержат примеры коаксиального стэкинга. Некоторыми яркими примерами являются тРНК-Phe, интроны группы I, интроны группы II и рибосомные РНК. Кристаллические структуры тРНК выявили наличие двух протяженных спиралей, которые являются результатом коаксиального стэкинга акцепторного стержня аминокислоты с Т-плечом и стэкинга D- и антикодонного плеч. Эти взаимодействия внутри тРНК Ориентируйте ножку антикодона перпендикулярно аминокислотной ножке, чтобы получить функциональную L-образную третичную структуру.[18] Было показано, что в интронах группы I спирали P4 и P6 коаксиально укладываются в стопку с использованием комбинации биохимических[21] и кристаллографические методы. Кристаллическая структура P456 предоставила подробное представление о том, как коаксиальная укладка стабилизирует упаковку спиралей РНК в третичные структуры.[22] В самосплайсинговом интроне группы II из Oceanobacillus iheyensis стебли IA и IB коаксиально штабелируются и вносят вклад в относительную ориентацию составляющих спиралей пятистороннего соединения.[6] Такая ориентация способствует правильному складыванию активный сайт функционального рибозима. Рибосома содержит множество примеров коаксиального стэкинга, включая стэкированные сегменты длиной до 70 п.н.[23]

Два распространенных мотива, включающих коаксиальную укладку, - это петли для поцелуев и псевдоузлы. При взаимодействии целующейся петли участки одноцепочечной петли двух шпилек взаимодействуют посредством спаривания оснований, образуя составную, коаксиально уложенную спиралью. Примечательно, что эта структура позволяет всем нуклеотидам в каждой петле участвовать во взаимодействиях спаривания оснований и стэкинга. Этот мотив был визуализирован и изучен с помощью ЯМР-анализа Ли и Кротерс.[24] Мотив псевдоузла возникает, когда одноцепочечный участок петли шпильки спаривается с последовательностью, расположенной выше или ниже в той же цепи РНК. Две результирующие дуплексные области часто накладываются друг на друга, образуя стабильную коаксиально уложенную составную спираль. Одним из примеров мотива псевдоузла является высокостабильный рибозим вируса гепатита дельта, в котором остов имеет общую топологию двойного псевдоузла.[25]
Эффект, аналогичный коаксиальному наложению, наблюдался в рационально разработанный Структуры ДНК. ДНК оригами структуры содержат большое количество двойных спиралей с оголенными тупыми концами. Было обнаружено, что эти структуры слипались по краям, которые содержали эти открытые тупые концы, из-за гидрофобных взаимодействий при штабелировании.[26]
Другие мотивы
Тетрапетля-рецепторные взаимодействия

Взаимодействия тетрапетли с рецептором сочетают в себе взаимодействия спаривания оснований и стэкинга между нуклеотидами петли тетрапетля мотив и мотив рецептора, расположенные в дуплексе РНК, создают третичный контакт, который стабилизирует глобальную третичную складку РНК молекула. Тетрапетли также являются возможными структурами в дуплексах ДНК.[28]
Стеблевые петли могут сильно различаться по размеру и последовательности, но тетрапетли из четырех нуклеотиды очень распространены и обычно относятся к одной из трех категорий в зависимости от последовательности.[29] Эти три семейства - это CUYG, UNCG и GNRA. (см. рисунок справа) тетрапетли.[30] В каждом из этих семейств тетрапетлей второй и третий нуклеотиды образуют виток в цепи РНК и пара оснований между первым и четвертым нуклеотидами стабилизирует структуру петли. В целом было определено, что стабильность тетрапетли зависит от состава оснований внутри петли и от состава этой «замыкающей пары оснований».[31] Семейство GNRA тетрапетлей чаще всего наблюдается во взаимодействиях тетрапетлей и рецепторов. Кроме того, известно, что тетрапетли UMAC являются альтернативными версиями петель GNRA, оба имеют сходные опорные структуры; несмотря на сходство, они различаются возможными дальнодействующими взаимодействиями, на которые они способны. [32].

«Мотивы рецептора тетрапетли» - это дальнодействующие третичные взаимодействия[33] состоящий из водородная связь между базами в тетрапетля к последовательностям стволовой петли в дистальных участках вторичной структуры РНК.[34] Помимо водородных связей, стэкинг-взаимодействия являются важным компонентом этих третичных взаимодействий. Например, при взаимодействиях GNRA-тетрапетля второй нуклеотид тетрапетли укладывается непосредственно на мотив А-платформы (см. Выше) внутри рецептора.[22] Последовательность тетрапетли и ее рецептора часто коварифицируется, так что один и тот же тип третичного контакта может быть установлен с разными изоформами тетрапетли и его родственного рецептора.[35]
Например, самосплайсинговый интрон группы I зависит от мотивов рецептора тетралупа для своей структуры и функции.[22][34] В частности, три остатка аденина канонического мотива GAAA укладываются на вершину спирали рецептора и образуют множественные стабилизирующие водородные связи с рецептором. Первый аденин последовательности GAAA образует тройную пару оснований с AU основаниями рецептора. Второй аденин стабилизируется водородными связями с тем же уридином, а также через его 2'-ОН с рецептором и через взаимодействия с гуанином тетрапетли GAAA. Третий аденин образует тройную пару оснований.
Мотив ля минор

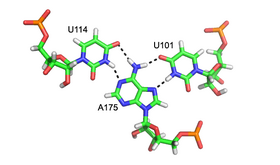
Мотив A-минор - это повсеместная РНК третичный структурный мотив. Образуется вставкой непарного нуклеозид в малую бороздку дуплекса РНК. Таким образом, это пример малая канавка тройная. Хотя гуанозин, цитозин и уридин также могут образовывать тройные взаимодействия малых бороздок, взаимодействия аденина с малыми бороздками очень распространены. В случае аденина край N1-C2-N3 вставляемой основы образует водородные связи с одним или обоими 2’-OH дуплекса, а также с основаниями дуплекса (см. рисунок: A-минорные взаимодействия). Дуплекс хоста часто представляет собой базовую пару G-C.
Мотивы ля минор были разделены на четыре класса:[8] типы от 0 до III, в зависимости от положения вставной базы относительно двух 2’-OH Watson-Crick базовая пара. В минорных мотивах A типов I и II, N3 аденина вставлен глубоко в малую бороздку дуплекса (см. Рисунок: Взаимодействие A-минор - взаимодействие типа II), и существует хорошая комплементарность формы с парой оснований. В отличие от типов 0 и III, взаимодействия типов I и II специфичны для аденина из-за взаимодействий водородных связей. При взаимодействии типа III как O2 ', так и N3 вставляющей основы менее тесно связаны с малой бороздкой дуплекса. Мотивы типов 0 и III более слабые и неспецифические, потому что они опосредуются взаимодействиями с одним 2’-OH (см. Рисунок: A-минорные взаимодействия - взаимодействия типов 0 и III).
A-минорный мотив является одним из наиболее распространенных структурных мотивов РНК в рибосоме, где он способствует связыванию тРНК с субъединицей 23S.[37] Чаще всего они стабилизируют дуплексные взаимодействия РНК в петлях и спиралях, например, в ядре интронов группы II.[6]
Интересный пример ля минор - его роль в антикодон признание. Рибосома должна различать правильные и неправильные пары кодон-антикодон. Частично это происходит за счет введения оснований аденина в малую бороздку. Неправильные пары кодон-антикодон будут иметь искаженную спиральную геометрию, что не позволит взаимодействию A-минор стабилизировать связывание и увеличит скорость диссоциации неправильной тРНК.[38]
Анализ мотивов ля минор в 23S рибосомная РНК выявил иерархическую сеть структурных зависимостей, предположительно связанных с эволюцией рибосом и порядком событий, которые привели к развитию современной большой бактериальной субъединицы.[39]
Рибозная молния
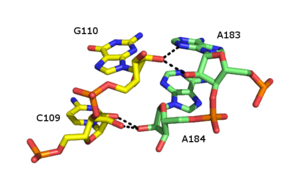
Рибозная молния - это РНК третичный структурный элемент, в котором две цепи РНК удерживаются вместе посредством водородная связь взаимодействия с участием 2’OH рибоза сахара на разных нитях. 2'OH может вести себя как донор, так и акцептор водородных связей, что позволяет образовывать раздвоенные водородные связи с другим 2 ’OH.[40][41]
Сообщалось о многочисленных формах рибозной застежки-молнии, но общий тип включает четыре водородные связи между 2'-ОН группами двух соседних сахаров. Застежки-молнии из рибозы обычно образуют массивы, которые стабилизируют взаимодействия между отдельными цепями РНК.[42] Рибозные молнии часто встречаются как Стебель-петля взаимодействия с очень низкой специфичностью последовательности. Однако в малых и больших рибосомальный субъединиц, существует склонность к рибозным застежкам-молниям последовательности CC / AA - два цитозины на первой цепочке в паре с двумя аденины на второй цепочке.
Роль ионов металлов

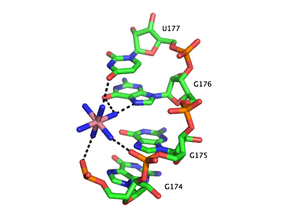
Функциональный РНК часто представляют собой свернутые, стабильные молекулы трехмерной формы, а не гибкие линейные нити.[44] Катионы необходимы для термодинамической стабилизации третичных структур РНК. Катионы металлов, связывающие РНК, могут быть одновалентными, двухвалентными или трехвалентными. Калий (K+) - это обычный одновалентный ион, связывающий РНК. Обычный двухвалентный ион, связывающий РНК, - это магний (Мг2+). Другие ионы, включая натрий (Na+), кальций (Ca2+) и марганец (Mn2+) связывают РНК in vivo и in vitro. Многовалентные органические катионы, такие как спермидин или спермин, также содержатся в клетках, и они вносят важный вклад в укладку РНК. Трехвалентные ионы, такие как гексамин кобальта или ионы лантаноидов, такие как тербий (Tb3+) являются полезными экспериментальными инструментами для изучения связывания металлов с РНК.[45][46]
Ион металла может взаимодействовать с РНК множеством способов. Ион может диффузно связываться с основной цепью РНК, защищая в противном случае неблагоприятные электростатические взаимодействия. Экранирование заряда часто осуществляется одновалентными ионами. Связанные с сайтом ионы стабилизируют определенные элементы третичной структуры РНК. Связанные с сайтом взаимодействия можно далее подразделить на две категории в зависимости от того, опосредует ли вода связывание металла. Взаимодействия «внешней сферы» опосредуются молекулами воды, которые окружают ион металла. Например, гексагидрат магния взаимодействует и стабилизирует определенные мотивы третичной структуры РНК посредством взаимодействия с гуанозин в большой канавке. И наоборот, взаимодействия «внутренней сферы» напрямую опосредуются ионом металла. РНК часто складывается в несколько стадий, и эти стадии могут быть стабилизированы различными типами катионов. На ранних стадиях РНК образует второстепенные конструкции стабилизируется за счет связывания одновалентных катионов, двухвалентных катионов и полианионных аминов с целью нейтрализации полианионной основной цепи. Более поздние стадии этого процесса включают образование третичной структуры РНК, которая стабилизируется почти в основном за счет связывания двухвалентных ионов, таких как магний, с возможным вкладом связывания калия.
Сайты связывания металлов часто локализуются в глубокой и узкой большой бороздке дуплекса РНК, координируя Hoogsteen края пурины. В частности, металл катионы стабилизируют участки скручивания позвоночника в местах плотной упаковки фосфаты приводит к образованию области плотного отрицательного заряда. В дуплексах РНК есть несколько мотивов связывания ионов металлов, которые были идентифицированы в кристаллических структурах. Например, в области P4-P6 системы Tetrahymena thermophila группа I интрон, несколько ион-связывающих сайтов состоят из тандемных G-U колебательные пары и тандем G-A несоответствия, в котором двухвалентный катионы взаимодействуют с краем Хугстина гуанозина через O6 и N7.[47][48][49] Другой ион-связывающий мотив в Тетрахимена интрон группы I представляет собой платформенный мотив A-A, в котором последовательные аденозины в одной цепи РНК образуют неканоническую пару псевдоснований.[50] В отличие от тандемного мотива G-U, мотив платформы A-A связывается преимущественно с одновалентными катионами. Во многих из этих мотивов отсутствие одновалентных или двухвалентных катионов приводит либо к большей гибкости, либо к потере третичной структуры.
Ионы двухвалентных металлов, особенно магний, было обнаружено, что они важны для структуры соединений ДНК, таких как Холлидей Джанкшн промежуточное звено в генетическая рекомбинация. Ион магния экранирует отрицательно заряженные фосфатные группы в соединении и позволяет им располагаться ближе друг к другу, обеспечивая сложенную конформацию, а не конформацию без стопки.[51] Магний жизненно важен для стабилизации таких соединений в искусственно созданный конструкции, используемые в ДНК-нанотехнологии, например, мотив двойного кроссовера.[52]
История
Самые ранние работы в области структурной биологии РНК более или менее совпадали с работой, проводимой над ДНК в начале 1950-х годов. В своей основополагающей статье 1953 года Уотсон и Крик предположили, что скопление ван-дер-Ваальса группой 2`OH рибозы не позволит РНК принять двойную спиральную структуру, идентичную предложенной ими модели - то, что мы теперь знаем как B-форма ДНК.[53] Это вызвало вопросы о трехмерной структуре РНК: может ли эта молекула образовывать какой-то тип спиральной структуры, и если да, то как?
В середине 1960-х годов интенсивно изучалась роль тРНК в синтезе белка. В 1965 году Холли и другие. очистил и секвенировал первую молекулу тРНК, первоначально предполагая, что она приняла структуру клеверного листа, основанную в основном на способности определенных участков молекулы образовывать структуры петли стебля.[54] Выделение тРНК оказалось первой крупной удачей в структурной биологии РНК. В 1971 году Ким и другие. совершил еще один прорыв, производя кристаллы дрожжевой тРНКPHE которая дифрагировала до разрешения 2-3 Ангстрема с использованием спермина, природного полиамина, который связывается с тРНК и стабилизирует ее.[55]
В течение значительного времени после появления первых структур тРНК, область структуры РНК не претерпевала значительных успехов. Возможность изучения структуры РНК зависела от возможности выделить РНК-мишень. Это оказалось ограничивающим поле в течение многих лет, отчасти потому, что другие известные цели, т. Е. рибосома - было значительно труднее изолировать и кристаллизовать. Таким образом, в течение примерно двадцати лет после первоначальной публикации тРНКPHE структуры, были решены структуры только нескольких других РНК-мишеней, причем почти все они принадлежали семейству РНК-переносчиков.[56]
Этот досадный недостаток возможностей в конечном итоге будет преодолен в значительной степени благодаря двум крупным достижениям в исследованиях нуклеиновых кислот: идентификации рибозимы, и возможность производить их через in vitro транскрипция. После публикации Тома Чеха о причастности Тетрахимена интрон группы I как автокаталитический рибозим,[57] и отчет Сидни Альтмана о катализе рибонуклеазой Р РНК,[58] несколько других каталитических РНК были идентифицированы в конце 1980-х годов,[59] включая рибозим «головка молотка». В 1994 году Маккей и другие. опубликовали структуру «комплекса РНК-ДНК-рибозим-ингибитор в форме головки молотка» с разрешением 2,6 Ангстрема, в котором автокаталитическая активность рибозима была нарушена путем связывания с субстратом ДНК.[60] В дополнение к успехам, достигнутым в определении глобальной структуры с помощью кристаллографии, в начале 1990-х годов также была внедрена реализация ЯМР как мощного метода в структурной биологии РНК. Подобные исследования позволили более точно охарактеризовать взаимодействия спаривания оснований и стэкинга оснований, которые стабилизировали глобальные складки больших молекул РНК.
Возрождение структурной биологии РНК в середине 1990-х годов вызвало настоящий взрыв в области структурных исследований нуклеиновых кислот. С момента публикации головки молотка и P4-6 структур, были сделаны многочисленные важные вклады в эту область. Некоторые из наиболее примечательных примеров включают структуры Группа I и Интроны группы II,[6] и Рибосома.[36] Первые три конструкции были изготовлены с использованием in vitro транскрипция, и что ЯМР сыграл роль в исследовании частичных компонентов всех четырех структур - свидетельство необходимости обоих методов для исследования РНК. Нобелевская премия по химии 2009 г. была присуждена Ада Йонат, Венкатраман Рамакришнан, и Томас Штайц за их структурную работу над рибосома, демонстрируя выдающуюся роль структурной биологии РНК в современной молекулярной биологии.
Смотрите также
Рекомендации
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "третичная структура ". Дои:10.1351 / goldbook.T06282
- ^ Ричмонд Т.Дж., Дэйви, Калифорния (май 2003 г.). «Структура ДНК в ядре нуклеосомы». Природа. 423 (6936): 145–50. Bibcode:2003Натура.423..145р. Дои:10.1038 / природа01595. PMID 12736678.
- ^ Уотсон Дж. Д., Крик Ф. Х. (апрель 1953 г.). «Молекулярная структура нуклеиновых кислот; структура нуклеиновой кислоты дезоксирибозы» (PDF). Природа. 171 (4356): 737–8. Bibcode:1953 г., природа. 171..737 Вт. Дои:10.1038 / 171737a0. PMID 13054692.
- ^ Бансал М (2003). "Структура ДНК: Возвращаясь к двойной спирали Уотсона-Крика". Текущая наука. 85 (11): 1556–1563.
- ^ Гош А, Бансал М (2003). «Словарь структур ДНК от А до Я». Acta Crystallogr D. 59 (4): 620–626. Дои:10.1107 / S0907444903003251. PMID 12657780.
- ^ а б c d е PDB: 3BWP; Тоор Н., Китинг К.С., Тейлор С.Д., Пайл А.М. (апрель 2008 г.). «Кристаллическая структура самосплайсированного интрона группы II». Наука. 320 (5872): 77–82. Bibcode:2008Научный ... 320 ... 77Т. Дои:10.1126 / science.1153803. ЧВК 4406475. PMID 18388288.; оказано с PyMOL
- ^ а б PDB: 2К95; Ким Н.К., Чжан К., Чжоу Дж., Теймер К.А., Петерсон Р.Д., Фейгон Дж. (Декабрь 2008 г.). «Структура раствора и динамика псевдоузла дикого типа теломеразной РНК человека». J. Mol. Биол. 384 (5): 1249–61. Дои:10.1016 / j.jmb.2008.10.005. ЧВК 2660571. PMID 18950640.; оказано с PyMOL
- ^ а б Доэрти Е.А., Бейти Р.Т., Маскида Б., Дудна Д.А. (апрель 2001 г.). «Универсальный способ упаковки спирали в РНК». Nat. Struct. Биол. 8 (4): 339–43. Дои:10.1038/86221. PMID 11276255.
- ^ Шевчак А.А., Ортолева-Доннелли Л., Райдер С.П., Moncoeur E, Strobel SA (декабрь 1998 г.). «Тройная спираль РНК с малой бороздкой в каталитическом ядре интрона группы I». Nat. Struct. Биол. 5 (12): 1037–42. Дои:10.1038/4146. PMID 9846872.
- ^ Boudvillain M, de Lencastre A, Pyle AM (июль 2000 г.). «Третичное взаимодействие, которое связывает домены активного сайта с 5'-сайтом сплайсинга интрона группы II». Природа. 406 (6793): 315–8. Дои:10.1038/35018589. PMID 10917534.
- ^ а б c PDB: 1РАУ; Cheong C, Moore PB (сентябрь 1992 г.). «Структура раствора необычайно стабильного тетраплекса РНК, содержащего G- и U-квартетные структуры». Биохимия. 31 (36): 8406–14. Дои:10.1021 / bi00151a003. PMID 1382577.; оказано с PyMOL
- ^ а б PDB: 1FIT; Baugh C, Grate D, Wilson C (август 2000 г.). «2.8 Кристаллическая структура аптамера малахитового зеленого». J. Mol. Биол. 301 (1): 117–28. Дои:10.1006 / jmbi.2000.3951. PMID 10926496.; оказано с PyMOL
- ^ Гилберт С.Д., Рэмбо Р.П., Ван Тайн Д., Бейти Р.Т. (февраль 2008 г.). «Структура рибопереключателя SAM-II, связанного с S-аденозилметионином». Nat. Struct. Мол. Биол. 15 (2): 177–82. Дои:10.1038 / nsmb.1371. PMID 18204466.
- ^ а б Батей Р.Т., Гилберт С.Д., Монтанж РК (ноябрь 2004 г.). «Структура природного гуанин-чувствительного рибопереключателя в комплексе с метаболитом гипоксантина». Природа. 432 (7015): 411–5. Bibcode:2004Натура.432..411Б. Дои:10.1038 / природа03037. PMID 15549109.
- ^ Артанари Х., Болтон PH (март 2001 г.). «Функциональные и дисфункциональные роли квадруплексной ДНК в клетках». Chem. Биол. 8 (3): 221–30. Дои:10.1016 / S1074-5521 (01) 00007-2. PMID 11306347.
- ^ Оливер А.В., Богдарина И., Шредер Е., Тейлор И.А., Книл Г.Г. (август 2000 г.). «Предпочтительное связывание белка гена 5 fd с тетраплексными структурами нуклеиновых кислот». J. Mol. Биол. 301 (3): 575–84. Дои:10.1006 / jmbi.2000.3991. PMID 10966771.
- ^ PDB: 6тна; Суссман Дж. Л., Холбрук С. Р., Warrant RW, Church GM, Kim SH (август 1978 г.). «Кристаллическая структура дрожжевой фенилаланиновой транспортной РНК. I. Кристаллографическое уточнение». J. Mol. Биол. 123 (4): 607–30. Дои:10.1016/0022-2836(78)90209-7. PMID 357742.; предоставлено через PyMOL.
- ^ а б Куигли Дж. Дж., Рич А. (ноябрь 1976 г.). «Структурные домены молекул транспортной РНК». Наука. 194 (4267): 796–806. Bibcode:1976Научный ... 194..796Q. Дои:10.1126 / science.790568. PMID 790568.
- ^ "Дуглас Х. Тернер". Правила Тернера. Кафедра химии Рочестерского университета.
- ^ Уолтер А.Е., Тернер Д.Х., Ким Дж., Литтл М.Х., Мюллер П., Мэтьюз Д.Х., Цукер М. (сентябрь 1994 г.). «Коаксиальная укладка спиралей усиливает связывание олигорибонуклеотидов и улучшает предсказание сворачивания РНК». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 91 (20): 9218–22. Bibcode:1994PNAS ... 91.9218W. Дои:10.1073 / пнас.91.20.9218. ЧВК 44783. PMID 7524072.
- ^ Мерфи Флорида, Ван Й.Х., Гриффит Дж. Д., Чех TR (сентябрь 1994 г.). «Коаксиально уложенные спирали РНК в каталитическом центре рибозима Tetrahymena». Наука. 265 (5179): 1709–12. Bibcode:1994Научный ... 265.1709М. Дои:10.1126 / science.8085157. PMID 8085157.
- ^ а б c Cate JH, Gooding AR, Podell E, Zhou K, Golden BL, Kundrot CE, Cech TR, Doudna JA (сентябрь 1996 г.). «Кристаллическая структура домена рибозима группы I: принципы упаковки РНК». Наука. 273 (5282): 1678–85. Bibcode:1996Sci ... 273.1678C. Дои:10.1126 / science.273.5282.1678. PMID 8781224.
- ^ Ноллер HF (сентябрь 2005 г.). «Структура РНК: чтение рибосомы». Наука. 309 (5740): 1508–14. Bibcode:2005Наука ... 309.1508N. Дои:10.1126 / science.1111771. PMID 16141058.
- ^ Ли AJ, Кротерс DM (август 1998 г.). «Структура решения комплекса петля-петля РНК: последовательность перевернутой петли ColE1». Структура. 6 (8): 993–1005. Дои:10.1016 / S0969-2126 (98) 00101-4. PMID 9739090.
- ^ Ферре-Д'Амаре А.Р., Чжоу К., Дудна Д.А. (октябрь 1998 г.). «Кристаллическая структура рибозима вируса гепатита дельта». Природа. 395 (6702): 567–74. Bibcode:1998Натура.395..567F. Дои:10.1038/26912. PMID 9783582.
- ^ Ротемунд, Пол В. К. (2006). «Складывание ДНК для создания наноразмерных форм и узоров» (PDF). Природа. 440 (7082): 297–302. Bibcode:2006Натура.440..297R. Дои:10.1038 / природа04586. ISSN 0028-0836. PMID 16541064.
- ^ а б c d PDB: 1GID; Cate JH, Gooding AR, Podell E, Zhou K, Golden BL, Kundrot CE, Cech TR, Doudna JA (сентябрь 1996 г.). «Кристаллическая структура домена рибозима группы I: принципы упаковки РНК». Наука. 273 (5282): 1678–85. Bibcode:1996Sci ... 273.1678C. Дои:10.1126 / science.273.5282.1678. PMID 8781224.; оказано с PyMOL
- ^ Накано М., Муди Э.М., Лян Дж., Бевилаква П.С. (декабрь 2002 г.). «Отбор термодинамически стабильных тетрапетлей ДНК с использованием гель-электрофореза в градиенте температуры выявляет четыре мотива: d (cGNNAg), d (cGNABg), d (cCNNGg) и d (gCNNGc)». Биохимия. 41 (48): 14281–92. Дои:10.1021 / bi026479k. PMID 12450393.
- ^ Мур ПБ (1999). «Структурные мотивы в РНК». Анну. Преподобный Biochem. 68 (1): 287–300. Дои:10.1146 / annurev.biochem.68.1.287. PMID 10872451.
- ^ Абрамовиц Д.Л., Пайл А.М. (февраль 1997 г.). «Замечательная морфологическая изменчивость общего мотива сворачивания РНК: взаимодействие тетрапетли GNRA с рецептором». J. Mol. Биол. 266 (3): 493–506. Дои:10.1006 / jmbi.1996.0810. PMID 9067606.
- ^ Moody EM, Feerrar JC, Bevilacqua PC (июнь 2004 г.). «Доказательства того, что сворачивание шпильки тетрапетли РНК менее кооперативно, чем ее двойник ДНК». Биохимия. 43 (25): 7992–8. Дои:10.1021 / bi049350e. PMID 15209494.
- ^ Чжао Кью, Хуанг ХК, Нагасвами У, Ся И, Гао Х, Fox GE (август 2012 г.). «Тетрапетли UNAC: насколько они имитируют тетрапетли GNRA?». Биополимеры. 97 (8): 617–628. Дои:10.1002 / bip.22049. PMID 22605553.
- ^ Уильямс Д.Х., Походка MJ, Лоакс Д. (2006). Нуклеиновые кислоты в химии и биологии. Кембридж, Великобритания: RSC Pub. ISBN 0-85404-654-2.
- ^ а б Jaeger L, Michel F, Westhof E (март 1994). «Участие тетрапетли GNRA в третичных взаимодействиях РНК дальнего действия». J. Mol. Биол. 236 (5): 1271–6. Дои:10.1016/0022-2836(94)90055-8. PMID 7510342.
- ^ Мишель Ф., Вестхоф Э. (декабрь 1990 г.). «Моделирование трехмерной архитектуры каталитических интронов группы I на основе сравнительного анализа последовательностей». J. Mol. Биол. 216 (3): 585–610. Дои:10.1016 / 0022-2836 (90) 90386-Z. PMID 2258934.
- ^ а б c PDB: 1ФФК; Ban N, Nissen P, Hansen J, Moore PB, Steitz TA (август 2000 г.). «Полная атомная структура большой субъединицы рибосомы при разрешении 2,4 А». Наука. 289 (5481): 905–20. Bibcode:2000Sci ... 289..905B. Дои:10.1126 / science.289.5481.905. PMID 10937989.; оказано с PyMOL
- ^ Nissen P, Ippolito JA, Ban N, Moore PB, Steitz TA (апрель 2001 г.). «Третичные взаимодействия РНК в большой субъединице рибосомы: A-минорный мотив». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 98 (9): 4899–903. Bibcode:2001PNAS ... 98.4899N. Дои:10.1073 / pnas.081082398. ЧВК 33135. PMID 11296253.
- ^ Йошизава С., Фурми Д., Пуглиси Д. Д. (сентябрь 1999 г.). «Распознавание кодон-антикодоновой спирали рибосомной РНК». Наука. 285 (5434): 1722–5. Дои:10.1126 / наука.285.5434.1722. PMID 10481006.
- ^ Боков К., Стейнберг С.В. (февраль 2009 г.). «Иерархическая модель эволюции 23S рибосомной РНК». Природа. 457 (7232): 977–80. Bibcode:2009Натура.457..977Б. Дои:10.1038 / природа07749. PMID 19225518.
- ^ Батей Р.Т., Рэмбо Р.П., Дудна Д.А. (август 1999 г.). «Третичные мотивы в структуре и сворачивании РНК». Энгью. Chem. Int. Эд. Англ.. 38 (16): 2326–2343. Дои:10.1002 / (SICI) 1521-3773 (19990816) 38:16 <2326 :: AID-ANIE2326> 3.0.CO; 2-3. PMID 10458781.
- ^ Тамура М., Холбрук С. Р. (июль 2002 г.). «Последовательность и структурная консервация в рибозных застежках-молнии РНК». J. Mol. Биол. 320 (3): 455–74. Дои:10.1016 / S0022-2836 (02) 00515-6. PMID 12096903.
- ^ PDB: 3IGI; Тоор Н., Китинг К.С., Федорова О., Раджашанкар К., Ван Дж., Пайл А.М. (январь 2010 г.). «Третичная архитектура интрона группы II Oceanobacillus iheyensis». РНК. 16 (1): 57–69. Дои:10.1261 / rna.1844010. ЧВК 2802037. PMID 19952115.; визуализировано с использованием PyMOL.
- ^ PDB: 1ZZN; Stahley MR, Strobel SA (сентябрь 2005 г.). «Структурные доказательства механизма сплайсинга интронов группы I с двумя ионами металлов». Наука. 309 (5740): 1587–90. Bibcode:2005Научный ... 309.1587С. Дои:10.1126 / science.1114994. PMID 16141079.; оказано с PyMOL
- ^ Celander DW, Чех TR (январь 1991 г.). «Визуализация сворачивания высшего порядка каталитической молекулы РНК». Наука. 251 (4992): 401–7. Bibcode:1991Научный ... 251..401C. Дои:10.1126 / science.1989074. PMID 1989074.
- ^ Пайл AM (сентябрь 2002 г.). «Ионы металлов в структуре и функциях РНК». J. Biol. Неорг. Chem. 7 (7–8): 679–90. Дои:10.1007 / s00775-002-0387-6. PMID 12203005.
- ^ Морроу-младший, Андолина С.М. (2012). «Глава 6. Спектроскопические исследования связывания иона лантаноида с нуклеиновыми кислотами». В Sigel A, Sigel H, Sigel RK (ред.). Взаимодействие между ионами металлов и нуклеиновыми кислотами. Ионы металлов в науках о жизни. 10. Springer. С. 171–197. Дои:10.1007/978-94-007-2172-2_6. PMID 22210339.
- ^ Кейт Дж. Х., Дудна Дж. А. (октябрь 1996 г.). «Сайты связывания металлов в большой бороздке большого домена рибозима». Структура. 4 (10): 1221–9. Дои:10.1016 / S0969-2126 (96) 00129-3. PMID 8939748.
- ^ Kieft JS, Tinoco I (май 1997 г.). «Структура раствора металлсвязывающего сайта в большой бороздке РНК в комплексе с гексаммином кобальта (III)». Структура. 5 (5): 713–21. Дои:10.1016 / S0969-2126 (97) 00225-6. PMID 9195889.
- ^ Рюдиссер С., Тиноко I (февраль 2000 г.). «Структура раствора гексаммина кобальта (III) в комплексе с тетрапетлей GAAA и связывание ионов металла с несоответствиями G · A». J. Mol. Биол. 295 (5): 1211–23. Дои:10.1006 / jmbi.1999.3421. PMID 10653698.
- ^ Буркхард С., Захариас М. (октябрь 2001 г.). «Моделирование связывания ионов с мотивами платформы AA в РНК: исследование континуального растворителя, включая конформационную адаптацию». Нуклеиновые кислоты Res. 29 (19): 3910–8. Дои:10.1093 / nar / 29.19.3910. ЧВК 60250. PMID 11574672.
- ^ Панютин И.Г., Бисвас И., Се П. (апрель 1995 г.). «Ключевая роль структуры соединения Холлидея в миграции ветви ДНК». Журнал EMBO. 14 (8): 1819–26. Дои:10.1002 / j.1460-2075.1995.tb07170.x. ЧВК 398275. PMID 7737132.
- ^ Fu TJ, Seeman NC (апрель 1993 г.). «Молекулы двойного кроссовера ДНК». Биохимия. 32 (13): 3211–20. Дои:10.1021 / bi00064a003. PMID 8461289.
- ^ Уотсон Дж. Д., Крик Ф. Х. (апрель 1953 г.). «Молекулярная структура нуклеиновых кислот; структура нуклеиновой кислоты дезоксирибозы» (PDF). Природа. 171 (4356): 737–738. Bibcode:1953 г., природа. 171..737 Вт. Дои:10.1038 / 171737a0. PMID 13054692.
- ^ Холли, Р. У., Апгар, Дж., Эверетт, Джорджия, Мэдисон, Дж. Т., Маргисс, М., Меррилл, Ш., Пенвик, Дж. Р., Замир (март 1965 г.). «Строение рибонуклеиновой кислоты». Наука. 147 (3664): 1462–5. Bibcode:1965Научный ... 147.1462H. Дои:10.1126 / science.147.3664.1462. PMID 14263761.CS1 maint: несколько имен: список авторов (связь)
- ^ Ким С.Х., Куигли Дж., Саддат Флорида, Рич А. (апрель 1971 г.). «Картины дифракции рентгеновских лучей с высоким разрешением кристаллической транспортной РНК, на которых видны спиральные области». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 68 (4): 841–5. Bibcode:1971ПНАС ... 68..841К. Дои:10.1073 / pnas.68.4.841. ЧВК 389056. PMID 5279525.
- ^ Шен LX, Цай З., Тиноко I (август 1995 г.). «Структура РНК в высоком разрешении». FASEB J. 9 (11): 1023–33. Дои:10.1096 / fasebj.9.11.7544309. PMID 7544309.
- ^ Чех Т.Р., Зауг А.Д., Грабовски П.Дж. (декабрь 1981 г.). «Сплайсинг in vitro предшественника рибосомной РНК Tetrahymena: участие гуанозинового нуклеотида в вырезании промежуточной последовательности». Клетка. 27 (3 Pt 2): 487–96. Дои:10.1016/0092-8674(81)90390-1. PMID 6101203.
- ^ Старк BC, Коле Р., Боуман Э. Дж., Альтман С. (август 1978 г.). «Рибонуклеаза P: фермент с важным компонентом РНК». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 75 (8): 3717–21. Bibcode:1978PNAS ... 75.3717S. Дои:10.1073 / pnas.75.8.3717. ЧВК 392857. PMID 358197.
- ^ Проди Г.А., Бакос Дж. Т., Бузаян Дж. М., Шнайдер И. Р., Брюнинг Дж. (Март 1986 г.). "Автолитический процессинг сателлитной РНК димерного вируса растений". Наука. 231 (4745): 1577–1580. Bibcode:1986Научный ... 231.1577П. Дои:10.1126 / science.231.4745.1577. PMID 17833317.
- ^ Pley HW, Flaherty KM, McKay DB (ноябрь 1994 г.). «Трехмерная структура рибозима головки молотка». Природа. 372 (6501): 68–74. Bibcode:1994Натура 372 ... 68П. Дои:10.1038 / 372068a0. PMID 7969422.