Определение структуры нуклеиновой кислоты - Nucleic acid structure determination
Экспериментальные подходы к определению структура из нуклеиновые кислоты, Такие как РНК и ДНК, можно в основном разделить на биофизический и биохимический методы. Биофизические методы используют фундаментальные физические свойства молекул для определения структуры, в том числе: Рентгеновская кристаллография, ЯМР и крио-ЭМ. Биохимические методы используют химические свойства нуклеиновых кислот с использованием конкретных реагенты и условия для проба структура нуклеиновых кислот.[1] Такие методы могут включать химическое зондирование с использованием определенных реагентов или полагаться на нативные или аналог химия. Различные экспериментальные подходы обладают уникальными достоинствами и подходят для различных экспериментальных целей.
Биофизические методы
Рентгеновская кристаллография
Эта секция нуждается в расширении с: его значимый вклад в изучение структур нуклеиновых кислот и некоторые примеры. Вы можете помочь добавляя к этому. (Декабрь 2018 г.) |
Рентгеновская кристаллография не является общей для одних только нуклеиновых кислот, поскольку ни ДНК, ни РНК не образуют кристаллов. Это происходит из-за большей степени внутреннего беспорядка и динамизма в структурах нуклеиновых кислот и отрицательно заряженных (дезокси) рибозо-фосфатных скеллах, которые отталкиваются друг от друга в непосредственной близости. Следовательно, кристаллизованные нуклеиновые кислоты имеют тенденцию образовывать комплекс с представляющим интерес белком, чтобы обеспечить структурный порядок и нейтрализовать отрицательный заряд.[нужна цитата ]
Спектроскопия ядерного магнитного резонанса (ЯМР)
ЯМР нуклеиновых кислот - это использование ЯМР-спектроскопии для получения информации о структуре и динамике нуклеиновая кислота молекулы, такие как ДНК или же РНК. По состоянию на 2003 год почти половина всех известных структур РНК была определена с помощью ЯМР-спектроскопии.[2]
ЯМР нуклеиновых кислот использует те же методы, что и ЯМР белков, но имеет несколько отличий. Нуклеиновые кислоты имеют меньший процент атомов водорода, которые обычно наблюдаются в ЯМР, и потому что двойные спирали нуклеиновых кислот жесткие и примерно линейные, они не складываются сами по себе, создавая «дальнодействующие» корреляции.[3] Типы ЯМР, обычно выполняемые с нуклеиновыми кислотами: 1H или протонный ЯМР, 13C ЯМР, 15N ЯМР, и 31P ЯМР. Двумерный ЯМР почти всегда используются методы, такие как корреляционная спектроскопия (COSY) и спектроскопия передачи полной когерентности (TOCSY) для обнаружения ядерных взаимодействий через сквозные связи, и ядерный эффект Оверхаузера спектроскопия (NOESY) для обнаружения взаимодействий между ядрами, которые находятся близко друг к другу в космосе.[4]
Параметры, взятые из спектра, в основном кросс-пики NOESY и константы связи, может использоваться для определения местных структурных особенностей, таких как гликозидная связь углы, двугранные углы (с использованием Уравнение Карплюса ) и конформации сахарной складки. Для крупномасштабной структуры эти локальные параметры должны быть дополнены другими структурными допущениями или моделями, потому что ошибки складываются при прохождении двойной спирали, и, в отличие от белков, двойная спираль не имеет компактной внутренней части и не сворачивается назад. сам. ЯМР также полезен для исследования нестандартных геометрий, таких как изогнутые спирали, не-Ватсона – Крика, и коаксиальная укладка. Это было особенно полезно при исследовании структуры природных олигонуклеотидов РНК, которые имеют тенденцию принимать сложные конформации, такие как стебель-петли и псевдоузлы. ЯМР также полезен для исследования связывания молекул нуклеиновой кислоты с другими молекулами, такими как белки или лекарственные препараты, путем наблюдения за тем, какие резонансы смещаются при связывании другой молекулы.[4]
Криогенная электронная микроскопия (крио-ЭМ)
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Март 2020 г.) |
Криогенная электронная микроскопия (крио-ЭМ) - это метод, в котором используется электронный луч для изображения образцов, которые были криогенно сохранены в водном растворе. Жидкие образцы наносятся пипеткой на маленькие металлические решетки и погружаются в жидкий раствор этана / пропана, который поддерживается очень холодным с помощью ванны с жидким азотом. После этого процесса замораживания молекулы воды в образце не успевают образовать гексагональные решетки, как во льду, и поэтому образец сохраняется в стекловидном водоподобном состоянии (также называемом остеклованный лед ), что упрощает визуализацию этих образцов с помощью электронного луча. Преимущество крио-ЭМ перед рентгеновской кристаллографией состоит в том, что образцы сохраняются в состоянии их водного раствора и не подвергаются влиянию образования кристаллов образца. Одним из недостатков является то, что трудно разрешить структуры нуклеиновой кислоты или белка, размер которых меньше ~ 75. килодальтон отчасти из-за сложности получения достаточного контраста для определения местонахождения частиц в этом застеклованном водном растворе. Еще один недостаток состоит в том, что для получения информации о структуре образца на атомном уровне требуется сделать много изображений (часто называемых электронными микрофотографиями) и усреднить эти изображения в процессе, называемом одночастичная реконструкция. Это вычислительно-интенсивный процесс.
Cryo-EM - это более новая, менее пертурбативная версия просвечивающая электронная микроскопия (ТЕМ). Это менее опасно, потому что образец не сушится на поверхности, этот процесс сушки часто выполняется в ТЕМ с отрицательным окрашиванием, и потому что Cryo-EM не требует контрастного вещества, такого как соли тяжелых металлов (например, уранилацетат или фотовольфрамовая кислота), которые также могут влиять на структуру биомолекулы. Просвечивающая электронная микроскопия, как метод, использует тот факт, что образцы взаимодействуют с пучком электронов, и только части образца, которые не взаимодействуют с электронным пучком, могут «проходить» в систему обнаружения электронов. ТЕМ, в целом, является полезным методом определения структуры нуклеиновых кислот с 1960-х годов.[5][6]. Хотя структура двухцепочечной ДНК (дцДНК) традиционно не может считаться структурой, в типичном смысле чередования сегментов одно- и двухцепочечных областей, на самом деле дцДНК - это не просто идеально упорядоченная двойная спираль в каждом месте ее длины. из-за тепловых колебаний в ДНК и альтернативных структур, которые могут формироваться как g-квадруплексы. КриоЭМ нуклеиновой кислоты была проведена на рибосомах. [7], вирусная РНК [8], и одноцепочечные структуры РНК в вирусах[9][10]. Эти исследования позволили разрешить структурные особенности при разном разрешении от уровня азотистых оснований (2-3 ангстрем) до мотивов третичной структуры (более нанометра).
Химическое зондирование
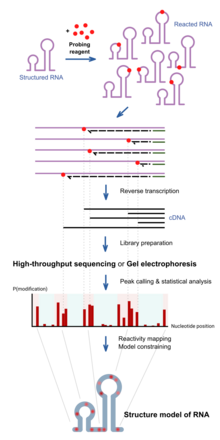
При химическом зондировании РНК используются химические вещества, которые вступают в реакцию с РНК. Важно отметить, что их реакционная способность зависит от локальной структуры РНК, например. основание пары или доступность. Следовательно, различия в реактивности могут служить следом структуры вдоль последовательности. Различные реагенты реагируют в разных положениях в структуре РНК и имеют разные спектры реакционной способности.[1] Последние достижения позволяют одновременно изучать структуру многих РНК (зондирование всего транскриптома)[11] и прямой анализ молекул РНК в их клеточном окружении (внутриклеточное зондирование).[12]
Структурированная РНК сначала реагирует с зондирующими реагентами в течение заданного времени инкубации. Эти реагенты образуют ковалентный аддукт на РНК в месте реакции. Когда РНК подвергается обратной транскрипции с использованием обратная транскриптаза в копию ДНК, полученная ДНК усекается в местах реакции, потому что фермент блокируется аддуктами. В коллекция молекул ДНК различной укороченной длины, таким образом, сообщает частоту реакции в каждой позиции основания, что отражает профиль структуры вдоль РНК. Это традиционно проверяется запуск ДНК на геле, а интенсивность полос сообщает частоту наблюдения усечения в каждой позиции. Последние подходы используют высокопроизводительное секвенирование для достижения той же цели с большей пропускной способностью и чувствительностью.
Профиль реактивности может использоваться для изучения степени структуры в определенных положениях для конкретных гипотез или использоваться в сочетании с вычислительные алгоритмы для создания полной экспериментально подтвержденной модели конструкции.[13]
В зависимости от используемого химического реагента некоторые реагенты, например гидроксильные радикалы, вместо этого расщепляют молекулу РНК. Результат в усеченной ДНК такой же. Некоторые реагенты, например DMS, иногда не блокируют обратную транскриптазу, а вместо этого вызывают ошибку на сайте в копии ДНК. Их можно обнаружить при использовании методов высокопроизводительного секвенирования, и иногда они используются для улучшения результатов зондирования в качестве мутационного профилирования (MaP).[14][15]
Положения на РНК могут быть защищены от реагентов не только локальной структурой, но и связывающим белком над этим положением. Это привело к некоторой работе по использованию химического зондирования для анализа связывания с белками.[16]
Исследование гидроксильных радикалов
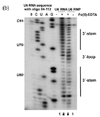
В качестве гидроксильные радикалы недолговечны в растворе, их нужно генерировать в результате эксперимента. Это можно сделать с помощью H2О2, аскорбиновая кислота и комплекс Fe (II) -EDTA. Эти реагенты образуют систему, которая генерирует гидроксильные радикалы через Фентон химия. Затем гидроксильные радикалы могут реагировать с молекулами нуклеиновой кислоты.[17] Гидроксильные радикалы атакуют рибозно-дезоксирибозное кольцо, что приводит к разрыву сахарно-фосфатного остова. Сайты, защищенные от связывающих белков или третичной структуры РНК, будут расщепляться гидроксильным радикалом с меньшей скоростью.[17] Следовательно, эти положения будут проявляться как отсутствие полос на геле или низкий сигнал при секвенировании.[17][18]
DMS
Диметилсульфат, известный как DMS, представляет собой химическое вещество, которое можно использовать для модификации нуклеиновых кислот с целью определения вторичной структуры. Реакция с DMS добавляет метиловый аддукт на сайт, известный как метилирование. В частности, DMS метилирует N1 из аденин (А) и N3 из цитозин (С),[19] оба расположены в месте естественных водородных связей при спаривании оснований. Следовательно, модификация может происходить только в азотистых основаниях A и C, которые являются одноцепочечными, с парными основаниями на конце спирали или в паре оснований на или рядом с GU. колебательная пара, причем последние два являются положениями, в которых пары оснований могут иногда открываться. Более того, поскольку модифицированные сайты не могут быть спарены по основанию, сайты модификации могут быть обнаружены с помощью RT-PCR, где обратная транскриптаза отстает на метилированных основаниях и дает различные усеченные кДНК. Эти усеченные кДНК можно идентифицировать с помощью гель-электрофореза или высокопроизводительного секвенирования.
Улучшение методов, основанных на усечении, мутационное профилирование DMS с секвенированием (DMS-MaPseq) может обнаруживать несколько модификаций DMS в одной молекуле РНК, что позволяет получить больше информации за одно чтение (для чтения 150 нт, обычно две-три мутации сайтов, а не сайтов усечения от нуля до единицы), определяют структуры РНК с низким содержанием и идентифицируют субпопуляции РНК с альтернативными вторичными структурами.[20] DMS-MaPseq использует термостабильная обратная транскриптаза интрона группы II (TGIRT), который создает мутацию (а не усечение) в кДНК когда он встречает основание, метилированное DMS, но в противном случае он выполняет обратную транскрипцию с высокой точностью. Секвенирование полученной кДНК позволяет определить, какие основания были мутированы во время обратной транскрипции; эти основания не могли быть спаренными в исходной РНК.
Модификация DMS также может быть использована для ДНК, например, во взаимодействии ДНК-белок.[21]
ФОРМА
Sфакультатив 2'-часгидроксил аЦилирование проанализировано пример еxtension или ФОРМА, использует преимущества реагентов, которые предпочтительно модифицируют основную цепь РНК в структурно гибких областях.

Реагенты, такие как ангидрид N-метилизатовой кислоты (NMIA) и ангидрид 1-метил-7-нитроизатовой кислоты (1M7). [22] реагируют с 2'-гидроксильной группой с образованием аддуктов на 2'-гидроксиле основной цепи РНК. По сравнению с химическими веществами, используемыми в других методах зондирования РНК, эти реагенты имеют то преимущество, что они в значительной степени беспристрастны к идентичности оснований, оставаясь при этом очень чувствительными к конформационной динамике. Нуклеотиды, которые ограничены (обычно спариванием оснований), демонстрируют меньшее образование аддуктов, чем нуклеотиды, которые являются неспаренными. Образование аддукта количественно определяют для каждого нуклеотида в данной РНК путем удлинения комплементарного праймера ДНК с помощью обратной транскриптазы и сравнения полученных фрагментов с фрагментами из немодифицированного контроля.[23] Таким образом, SHAPE сообщает о структуре РНК на уровне отдельных нуклеотидов. Эти данные можно использовать в качестве входных для создания высокоточных моделей вторичных структур.[24] SHAPE использовалась для анализа различных структур РНК, в том числе всего генома ВИЧ-1.[25] Лучше всего использовать комбинацию химических реагентов и экспериментальных данных.[26] В SHAPE-Seq SHAPE расширяется за счет мультиплексирования на основе штрих-кода в сочетании с РНК-Seq и может выполняться с высокой пропускной способностью.[27]
Карбодиимиды

В карбодиимид фрагмент может также образовывать ковалентные аддукты на открытых азотистых основаниях, которые урацил, и в меньшей степени гуанин при нуклеофильной атаке депротонированного N. Они реагируют в первую очередь с N3 урацила и N1 гуанина, модифицируя два сайта, ответственные за водородные связи на основаниях.[19]
1-циклогексил- (2-морфолиноэтил) карбодиимид мето-п-толуолсульфонат, также известный как CMCT или CMC, является наиболее часто используемым карбодиимидом для исследования структуры РНК.[29][30] Подобно DMS, его можно обнаружить с помощью обратной транскрипции с последующим гель-электрофорезом или высокопроизводительным секвенированием. Поскольку он реагирует на G и U, его можно использовать для дополнения данных экспериментов по зондированию DMS, которые информируют A и C.[31]
1-этил-3- (3-диметиламинопропил) карбодиимид, также известный как EDC, представляет собой водорастворимый карбодиимид, который проявляет такую же реакционную способность, как CMC, а также используется для химического исследования структуры РНК. EDC может проникать в клетки и поэтому используется для прямого внутриклеточного исследования РНК в их естественной среде.[32][28]
Кетоксаль, глиоксаль и производные


Некоторые 1,2-дикарбонил соединения способны реагировать с одноцепочечным гуанином (G) по N1 и N2, образуя пятичленный кольцевой аддукт на грани Уотсона-Крика.
1,1-дигидрокси-3-этокси-2-бутанон, также известный как кетоксал, имеет структуру, относящуюся к 1,2-дикарбонилам, и был первым в этой категории, широко используемым для химического исследования РНК. Кетоксал вызывает модификацию гуанина, специфически изменяя N1 и экзоциклическую аминогруппу (N2) одновременно за счет ковалентного взаимодействия.[35]
Глиоксаль, метилглиоксаль и фенилглиоксаль, которые все несут ключевой 1,2-дикарбонильный фрагмент, все реагируют со свободными гуанинами, как кетоксал, и могут использоваться для исследования неспаренных оснований гуанина в структурированной РНК. Благодаря своим химическим свойствам эти реагенты могут легко проникать в клетки и, следовательно, могут использоваться для анализа РНК в их естественной клеточной среде.[34]
ЛАЗЕРНОЕ или НАЗ-зондирование
Светоактивируемое структурное исследование РНК (ЛАЗЕР) При зондировании используется ультрафиолетовый свет для активации никотиноилазида (NAz), генерирующего в воде высокореактивный катион нитрения, который вступает в реакцию с доступным для растворителя гуанозином и аденозином РНК в положении C-8 через безбарьерный Фридель- Ремесла реакция. ЛАЗЕРНОЕ зондирование нацелено как на одноцепочечные, так и на двухцепочечные остатки, если они доступны для растворителя. Поскольку зондирование гидроксильных радикалов требует синхротронного излучения для измерения доступности РНК для растворителей. in vivo, для многих лабораторий трудно применить зондирование гидроксильных радикалов к следовой РНК в клетках. Напротив, при лазерном зондировании используется ручная УФ-лампа (20 Вт) для возбуждения, гораздо проще применить ЛАЗЕРНОЕ зондирование для in vivo изучение доступности растворителей РНК. Этот метод химического зондирования регулируется светом и исследует доступность нуклеиновых оснований для растворителя, что, как было показано, оставляет след в клетках, связывающих белки, связывающие РНК.[36]
Встроенное зондирование

Встроенное зондирование не включает обработку каким-либо химическим веществом или реагентом для модификации структур РНК. В этом типе анализа используется структурно-зависимое расщепление РНК; одноцепочечные области более гибкие и нестабильные и со временем будут деградировать.[38] Процесс поточного зондирования часто используется для определения изменений в структуре из-за связывания лиганда. Связывание лиганда может приводить к различным моделям расщепления. Процесс встроенного зондирования включает инкубацию структурных или функциональных РНК в течение длительного периода времени. Этот период может составлять несколько дней, но варьируется в каждом эксперименте. Затем инкубированные продукты наносят на гель для визуализации полос. Этот эксперимент часто проводят с использованием двух разных условий: 1) с лигандом и 2) в отсутствие лиганда.[37] Расщепление приводит к более короткой длине полос и указывает на области, которые не спарены по основанию, поскольку спаренные по основанию области имеют тенденцию быть менее чувствительными к спонтанному расщеплению.[38] In-line зондирование - это функциональный анализ, который можно использовать для определения структурных изменений РНК в ответ на связывание лиганда. Он может напрямую показать изменение гибкости и связывания участков РНК в ответ на лиганд, а также сравнить этот ответ на аналогичные лиганды. Этот анализ обычно используется в динамических исследованиях, особенно при исследовании рибопереключатели.[38]
Картирование интерференции нуклеотидных аналогов (NAIM)
Картирование интерференции нуклеотидных аналогов (NAIM) - это процесс использования нуклеотидных аналогов, молекул, которые в некотором смысле похожи на нуклеотиды, но не имеют функции, для определения важности функциональной группы в каждом месте молекулы РНК.[39][40] Процесс NAIM заключается во вставке однонуклеотидного аналога в уникальный сайт. Это можно сделать, расшифровав короткую РНК с помощью РНК-полимераза Т7, затем синтезируют короткий олигонуклеотид, содержащий аналог в определенном положении, а затем лигируют их вместе на матрице ДНК с использованием лигазы.[39] Аналоги нуклеотидов маркируют фосфоротиоатом, затем активные члены популяции РНК отделяют от неактивных членов, затем из неактивных членов удаляют фосфоротиоатную метку и идентифицируют сайты аналогов с использованием гель-электрофореза и авторадиографии.[39] Это указывает на функционально важный нуклеотид, так как расщепление фосфоротиоата йодом приводит к образованию РНК, которая расщепляется в месте вставки аналога нуклеотида. Путем обработки этих усеченных молекул РНК на геле интересующий нуклеотид может быть идентифицирован с помощью эксперимента по секвенированию.[40] Результаты сайт-направленного включения указывают на важные положения, в которых при работе с гелем функциональные РНК, содержащие аналог, включенный в это положение, будут иметь полосу, но если аналог приводит к нефункциональности, когда функциональные молекулы РНК запускаются на гель не будет полосы, соответствующей этому положению на геле.[41] Этот процесс можно использовать для оценки всей области, где аналоги размещены в конкретных местах, отличающихся одним нуклеотидом, затем, когда функциональные РНК выделяются и запускаются на геле, все области, где образуются полосы, указывают на несущественные нуклеотиды, но области, где полосы отсутствуют в функциональной РНК, указывают на то, что вставка аналога нуклеотида в это положение приводила к тому, что молекула РНК становилась нефункциональной.[39]
Рекомендации
- ^ а б Недели, Кевин (2010). «Достижения в области анализа структуры РНК химическим зондированием». Текущее мнение в структурной биологии. 20 (3): 295–304. Дои:10.1016 / j.sbi.2010.04.001. ЧВК 2916962. PMID 20447823.
- ^ Фюртиг Б., Рихтер С., Вёнерт Дж., Швальбе Х. (октябрь 2003 г.). «ЯМР-спектроскопия РНК». ChemBioChem. 4 (10): 936–62. Дои:10.1002 / cbic.200300700. PMID 14523911.
- ^ Addess, Kenneth J .; Фейгон, Джули (1996). "Введение в 1H ЯМР-спектроскопия ДНК ». In Hecht, Sidney M. (ed.). Биоорганическая химия: нуклеиновые кислоты. Нью-Йорк: Издательство Оксфордского университета. ISBN 0-19-508467-5.
- ^ а б Wemmer, Дэвид (2000). «Глава 5: Структура и динамика ЯМР». В Блумфилде, Виктор А .; Crothers, Donald M .; Тиноко, Игнасио (ред.). Нуклеиновые кислоты: структура, свойства и функции. Саусалито, Калифорния: Научные книги университета. ISBN 0-935702-49-0.
- ^ [GOMATOS PJ, STOECKENIUS W. ИССЛЕДОВАНИЯ НА ЭЛЕКТРОННОМ МИКРОСКОПЕ НА РНК РЕОВИРУСА. Труды Национальной академии наук Соединенных Штатов Америки. 1964 декабрь; 52: 1449-1455. DOI: 10.1073 / pnas.52.6.1449]
- ^ [Майкл Бир и Ричард Зобель (1961) "Электронные пятна II: Электронно-микроскопические исследования видимости окрашенных молекул ДНК" J. Mol. Биол. Том 3, выпуск 6, декабрь 1961 г., страницы 717–726, IN3 – IN5 "]
- ^ Франк, Дж; Penczek, P; Грассуччи, Р. Srivastava, S (ноябрь 1991 г.). «Трехмерная реконструкция рибосомы 70S Escherichia coli во льду: распределение рибосомной РНК». Журнал клеточной биологии. 115 (3): 597–605. Дои:10.1083 / jcb.115.3.597. ЧВК 2289182. PMID 1918155.
- ^ Гопал, А; Чжоу, ZH; Knobler, CM; Гелбарт, WM (2012). «Визуализация больших молекул РНК в растворе». РНК. 18 (2): 284–299. Дои:10.1261 / rna.027557.111. ЧВК 3264915. PMID 22190747.
- ^ Конинг Р., Гомес-Бланко Дж., Акопьяна И. и др. Асимметричная крио-ЭМ реконструкция фага MS2 выявляет структуру генома in situ. Нац Коммуна 7, 12524 (2016). https://doi.org/10.1038/ncomms12524
- ^ Дай, X .; Ли, З .; Lai, M .; и другие. (2017). «Структуры генома in situ и устройство доставки генома в вирусе с одноцепочечной РНК». Природа. 541 (7635): 112–116. Дои:10.1038 / природа20589. ЧВК 5701785. PMID 27992877.
- ^ Квок, Чун Кит; Тан, Инь; Ассманн, Сара; Бевилаква, Филипп (апрель 2015 г.). «Структуром РНК: исследование структуры транскриптома с секвенированием следующего поколения». Тенденции в биохимических науках. 40 (4): 221–232. Дои:10.1016 / j.tibs.2015.02.005. PMID 25797096.
- ^ Кубота, М; Тран, С; Спитале, Р. (2015). «Прогресс и проблемы химического исследования структуры РНК внутри живых клеток». Природа Химическая Биология. 11 (12): 933–941. Дои:10.1038 / nchembio.1958. ЧВК 5068366. PMID 26575240.
- ^ Мэтьюз, DH; Дисней, Мэриленд; Чайлдс, JL; Schroeder, SJ; Цукер, М; Тернер Д.Х. (2004). «Включение ограничений химической модификации в алгоритм динамического программирования для прогнозирования вторичной структуры РНК». Труды Национальной академии наук. 101 (19): 7287–7292. Bibcode:2004ПНАС..101.7287М. Дои:10.1073 / pnas.0401799101. ЧВК 409911. PMID 15123812.
- ^ Зигфрид, N; Пусан, S; Недели, К. (2014). «Открытие мотивов РНК с помощью SHAPE и мутационного профилирования (SHAPE-MaP)». Природные методы. 11 (9): 959–965. Дои:10.1038 / nmeth.3029. ЧВК 4259394. PMID 25028896.
- ^ Секстон, А; Ван, П; Рутенберг-Шенберг, М; Саймон, М (2017). «Интерпретация обратного прекращения транскриптазы и событий мутации для лучшего понимания химического исследования РНК». Биохимия. 56 (35): 4713–3721. Дои:10.1021 / acs.biochem.7b00323. ЧВК 5648349. PMID 28820243.
- ^ Смола, М; Калабрезе, Дж; Недели, К. (2015). «Обнаружение РНК-белковых взаимодействий в живых клетках с SHAPE». Биохимия. 54 (46): 6867–6875. Дои:10.1021 / acs.biochem.5b00977. ЧВК 4900165. PMID 26544910.
- ^ а б c d Карадуман Р., Фабрицио П., Хартмут К., Урлауб Г., Лурманн Р. (2006). «Структура РНК и взаимодействия РНК-белок в очищенных дрожжевых мяРНП U6». J. Mol. Биол. 356 (5): 1248–1262. Дои:10.1016 / j.jmb.2005.12.013. HDL:11858 / 00-001M-0000-0012-E5F8-4. PMID 16410014.
- ^ Туллий, Т. Д .; Домброски, Б.А. (1986). «Футпринтинг гидроксильных радикалов»: информация в высоком разрешении о контактах ДНК-белок и приложение к лямбда-репрессору и Cro-белку ». Труды Национальной академии наук. 83 (15): 5469–5473. Bibcode:1986PNAS ... 83.5469T. Дои:10.1073 / пнас.83.15.5469. ЧВК 386308. PMID 3090544.
- ^ а б Тиджерина П., Мор С., Рассел Р. (2007). «DMS-футпринтинг структурированных РНК и комплексов РНК-белок». Нат Проток. 2 (10): 2608–23. Дои:10.1038 / nprot.2007.380. ЧВК 2701642. PMID 17948004.
- ^ Зубрадт, Меган; Гупта, Паромита; Персад, Ситара; Ламбовиц, Алан; Вайсман, Джонатан; Рускин, Сильви (2017). «DMS-MaPseq для полногеномного или целевого исследования структуры РНК in vivo». Природные методы. 14 (1): 75–82. Дои:10.1038 / nmeth.4057. ЧВК 5508988. PMID 27819661.
- ^ Альберт С. Болдуин-младший; Марджори Эттингер и Кевин Штрул (1996). «Блок 12.3: Метилирование и анализ интерференции урацила для анализа взаимодействий белок-ДНК». Текущие протоколы в молекулярной биологии. Глава 12. Вайли. С. Раздел 12.3. Дои:10.1002 / 0471142727.mb1203s36. PMID 18265086.
- ^ Мортимер С.А., Недели К.М. (2007). «Быстродействующий реагент для точного анализа вторичной и третичной структуры РНК с помощью химии SHAPE». J Am Chem Soc. 129 (14): 4144–45. Дои:10.1021 / ja0704028. PMID 17367143.
- ^ Мерино EJ, Уилкинсон KA, Coughlan JL, Weeks KM (2005). «Анализ структуры РНК при разрешении одного нуклеотида путем селективного 2'-гидроксилацилирования и удлинения праймера (SHAPE)». J Am Chem Soc. 127 (12): 4223–31. Дои:10.1021 / ja043822v. PMID 15783204.
- ^ Дейган К.Е., Ли Т.В., Мэтьюз Д.Х., Weeks KM (2009). «Точное определение структуры РНК по SHAPE». Proc Natl Acad Sci USA. 106 (1): 97–102. Bibcode:2009ПНАС..106 ... 97Д. Дои:10.1073 / pnas.0806929106. ЧВК 2629221. PMID 19109441.
- ^ Уоттс Дж. М., Данг К. К., Горелик Р. Дж., Леонард К. В., Бесс Дж. В. Младший, Суонстром Р., Берч К. Л., Недели КМ (2009). «Архитектура и вторичная структура всего генома РНК ВИЧ-1». Природа. 460 (7256): 711–6. Bibcode:2009 Натур.460..711Вт. Дои:10.1038 / природа08237. ЧВК 2724670. PMID 19661910.
- ^ Wipapat Kladwang; Кристофер К. ВанЛанг; Пабло Кордеро; Риджу Дас (7 сентября 2011 г.). «Понимание ошибок моделирования структуры РНК с помощью SHAPE». Биохимия. 50 (37): 8049–8056. arXiv:1103.5458. Bibcode:2011arXiv1103.5458K. Дои:10.1021 / bi200524n. ЧВК 3172344. PMID 21842868.
- ^ Лакс Дж. Б., Мортимер С. А., Трапнелл С., Луо С., Авиран С., Шрот Г. П., Пахтер Л, Дудна Я.А., Аркин А.П. (2011). «Характеристика мультиплексной структуры РНК с селективным 2'-гидроксилацилированием, анализируемая секвенированием удлинения праймера (SHAPE-Seq)». Proc Natl Acad Sci USA. 108 (27): 11063–8. Bibcode:2011PNAS..10811063L. Дои:10.1073 / pnas.1106501108. ЧВК 3131332. PMID 21642531.
- ^ а б Wang, PY; Секстон, АН; Каллиган, штат Висконсин; Саймон, доктор медицины (2019). «Карбодиимидные реагенты для химического исследования структуры РНК в клетках». РНК. 25 (1): 135–146. Дои:10.1261 / rna.067561.118. ЧВК 6298570. PMID 30389828.
- ^ Фриц Дж. Дж., Левин А., Хаусвирт В., Агарвал А., Грант М., Шоу Л. (2002). «Разработка рибозимов в форме головки молотка для модуляции экспрессии эндогенных генов для функциональных исследований». Методы. 28 (2): 276–285. Дои:10.1016 / S1046-2023 (02) 00233-5. PMID 12413427.
- ^ Metz, D; Браун, G (1969). «Исследование вторичной структуры нуклеиновой кислоты с помощью химической модификации карбодиимидным реагентом. II. Взаимодействие между N-циклогексил-N'-β- (4-метилморфолиниум) этилкарбодиимидом и переносящей рибонуклеиновой кислотой». Биохимия. 8 (6): 2329–2342. Дои:10.1021 / bi00834a013. PMID 4895018.
- ^ Инкарнато, D; Neri, F; Ансельми, Ф; Оливьеро, S (2014). «Полногеномное профилирование вторичных структур мышиных РНК выявляет ключевые особенности транскриптома млекопитающих». Геномная биология. 15 (491): 491. Дои:10.1186 / s13059-014-0491-2. ЧВК 4220049. PMID 25323333.
- ^ Mitchell, D; Ренда, А; Доудс, C; Бабицке, П; Ассманн, S; Бевилаква, П. (2019). «In vivo РНК-структурное исследование спаривания оснований урацила и гуанина с помощью 1-этил-3- (3-диметиламинопропил) карбодиимида (EDC)». РНК. 25 (1): 147–157. Дои:10.1261 / rna.067868.118. ЧВК 6298566. PMID 30341176.
- ^ Ноллер Х. Ф., Председатель Дж. Б. (1972). «Функциональная модификация 16S рибосомной РНК кетоксалом». Proc. Natl. Акад. Sci. Соединенные Штаты Америки. 69 (11): 3115–3118. Bibcode:1972ПНАС ... 69.3115Н. Дои:10.1073 / пнас.69.11.3115. ЧВК 389716. PMID 4564202.
- ^ а б Mitchell, D; Ричи, L; Парк, H; Бабицке, П; Ассманн, S; Бевилаква, П. (2018). «Глиоксали как структурные зонды РНК in vivo для спаривания гуаниновых оснований». РНК. 24 (1): 114–124. Дои:10.1261 / rna.064014.117. ЧВК 5733565. PMID 29030489.
- ^ Литт, М; Хэнкок, V (1967). «Кетоксал - потенциально полезный реагент для определения нуклеотидных последовательностей в одноцепочечных областях переноса рибонуклеиновой кислоты». Биохимия. 6 (6): 1848–1854. Дои:10.1021 / bi00858a036. PMID 6035923.
- ^ Фенг С., Чан Д., Джозеф Дж., Мууронен М., Колдрен У.Х., Дай Н., Корреа-младший И.Р., Фурче Ф., Хадад С.М., Спитале Р.К. (2018). «Светоактивируемое химическое зондирование доступности растворителей азотистых оснований внутри клеток». Nat Chem Biol. 14 (3): 276–283. Дои:10.1038 / nchembio.2548. ЧВК 6203945. PMID 29334380.
- ^ а б Мюльбахер Дж, Лафонтен Д.А. (2007). «Детерминанты распознавания лиганда гуаниновых рибопереключателей». Исследования нуклеиновых кислот. 35 (16): 5568–5580. Дои:10.1093 / нар / гкм572. ЧВК 2018637. PMID 17704135.
- ^ а б c Регульский, Э; Брейкер, Р. (2008). Wilusz, J (ред.). «Поточный зондовый анализ рибопереключателей». Посттранскрипционная регуляция генов. Методы молекулярной биологии ™. Тотова, Нью-Джерси: Humana Press. 419: 53–67. Дои:10.1007/978-1-59745-033-1_4. ISBN 978-1-58829-783-9. PMID 18369975.
- ^ а б c d Райдер С.П., Штробель С.А. (1999). «Картирование интерференции с аналогами нуклеотидов». Методы. 18 (1): 38–50. Дои:10.1006 / мет.1999.0755. PMID 10208815.
- ^ а б Вальдсих С (2008). «Рассечение сворачивания РНК с помощью картирования интерференции нуклеотидных аналогов (NAIM)». Протоколы природы. 3 (5): 811–823. Дои:10.1038 / nprot.2008.45. ЧВК 2873565. PMID 18451789.
- ^ Штробель С.А., Шетти К. (1997). «Определение химических групп, необходимых для функции интрона группы I тетрахимены путем картирования интерференции нуклеотидных аналогов». Proc. Natl. Акад. Sci. Соединенные Штаты Америки. 94 (7): 2903–2908. Bibcode:1997PNAS ... 94.2903S. Дои:10.1073 / пнас.94.7.2903. ЧВК 20295. PMID 9096319.
