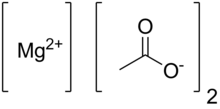
Ацетат магния - Magnesium acetate
 | |
| Имена | |
|---|---|
| Название ИЮПАК Ацетат магния | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.005.050 |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| Mg (CH3COO)2 | |
| Молярная масса | 142,394 (безводный) 214,455 (тетрагидрат) |
| Внешность | Белые гигроскопичные кристаллы |
| Плотность | 1,45 г / см3 |
| Температура плавления | 80 ° С (176 ° F, 353 К) (тетрагидрат) |
| Растворимый | |
| −116.0·10−6 см3/ моль (+4 H2О | |
| Родственные соединения | |
Другой катионы | Ацетат кальция |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Безводный ацетат магния имеет химическую формулу Mg (C2ЧАС3О2)2 и в его гидратированной форме, тетрагидрате ацетата магния, он имеет химическую формулу Mg (CH3COO)2 • 4H2О. В этом соединении магний имеет степень окисления 2+. Ацетат магния - это магний соль уксусная кислота.[1] это расплывающийся и при нагревании разлагается с образованием оксид магния.[2] Ацетат магния обычно используется в качестве источника магния в биологических реакциях.[3]
Физические свойства
Ацетат магния выглядит как белый гигроскопичный кристаллы. Пахнет уксусной кислотой, растворяется в воде. Когда он находится в водном растворе, его pH будет щелочным или нейтральным.[4][5]
Место хранения
Из-за того, что он очень гигроскопичен, его необходимо хранить вдали от воды. Он также несовместим с сильными окислителями и не должен смешиваться с ними.[6]
Синтез
Синтез ацетата магния по реакции гидроксида магния с уксусной кислотой.[7]
- 2 канала3COOH + Mg (OH)2 → (CH3COO)2Mg + 2 H2О
Карбонат магния суспендировали в дистиллированной воде с 20% раствором уксусной кислоты.[8]
- 2 канала3COOH + MgCO3 → Mg (CH3COO)2 + CO2 + H2О
Реакция металлического магния с уксусной кислотой, растворенной в сухом бензоле, вызывает образование ацетата магния с выделением газообразного водорода.[9]
- Mg +2 CH3COOH → Mg (CH3COO)2 + H2
Использование и приложения
В 1881 году Чарльз Клэмонд изобрел Корзина для моллюсков, один из первых эффективных газовые мантии. Реагенты, используемые в этом изобретении, включали ацетат магния, гидроксид магния, и вода.
Ацетат магния обычно используется в качестве источника магния или ацетат-иона в химических экспериментах. Одним из примеров этого является использование ацетата магния и нитрата магния для проведения моделирования молекулярной динамики и измерения поверхностного натяжения. В ходе эксперимента авторы обнаружили, что ацетат имеет более сильное сродство к поверхности по сравнению с нитрат-ионом и что Mg2+ сильно отталкивается от воздушных / жидкостных помех. Они также обнаружили, что Mg2+ имел более сильную тенденцию связываться с ионом ацетата по сравнению с нитратом.[10]
Одно из наиболее распространенных применений ацетата магния - это смесь под названием ацетат кальция и магния (CMA). Это смесь ацетата кальция и ацетата магния. CMA считается экологически чистой альтернативой NaCl и CaCl.2. CMA также действует как мощный SO2, НЕТИкси агент для контроля выбросов токсичных твердых частиц в процессах сжигания угля для уменьшения кислотных дождей и в качестве эффективного катализатора для облегчения сжигания угля.[11]
Было обнаружено, что ацетат магния вызывает конформационные изменения в кишечная палочка фермент Primase. В этом эксперименте Mg (OAc)2, MnCl2, CaCl2, NaOAc, LiCl, MgSO4 и MgCl2 все сравнивали, чтобы увидеть, какое влияние они оказали на кишечная палочка фермент примаза. Экспериментаторы обнаружили, что Mg (OAc)2 вызвало лучшее конформационное изменение. MgSO4 и MgCl2 вызывали эффект незначительно, а остальные нет.[12]
Когда ацетат магния смешивают с перекисью водорода, он действует как бактерицидное средство.[13]
Было показано, что ацетат магния эффективен для озоления органических соединений при подготовке к анализу на фтор, когда присутствуют высокие или низкие концентрации фтора.[14]
Безопасность
Ацетат магния - относительно безопасное соединение, которому присвоена нулевая оценка опасности для здоровья. Однако всегда следует обращаться с ним в перчатках и защитных очках. При попадании в глаза, на кожу, при проглатывании или вдыхании он вызовет раздражение в соответствующих областях: глазах, коже, пищеварительной системе и легких.[15]
использованная литература
- ^ Ацетат магния. Hazard.com. Проверено 12 апреля 2012.
- ^ Поставщик ацетата магния и техническая информация Американские элементы Проверено 12 апреля 2012.
- ^ «Информационный бюллетень Sigma-Aldrich по ацетату магния» (PDF). Получено 2012-04-26.
- ^ "Информационный бюллетень Unisenchem Ацетат магния". Получено 2012-04-27.
- ^ "Информационный бюллетень Unisenchem Ацетат магния" (PDF). Архивировано из оригинал (PDF) на 2010-07-08. Получено 2013-12-16.
- ^ "Информационный бюллетень Unisenchem Ацетат магния". Получено 2012-04-27.
- ^ Стоуффер, М. ". Адсорбенты для удаления H2s, «Другие соединения, вызывающие запах, и кислые газы из газовых потоков, и методы производства и использования этих адсорбентов». Получено 2012-04-25.
- ^ Стащук, П .; Пекальская, J. (2003). «Способы получения органических соединений магния из природного доломита». Физиохимические проблемы переработки полезных ископаемых. 37: 149–158.
- ^ Энциклопедия химических реакций. 1957. с. 399.
- ^ Минофар, Бабак; Вача, Роберт; Вахаб, Абдул; Махиуддин, Сех; Кунц Вернер; Юнгвирт, Павел (2006). «Склонность к интерфейсу воздух / вода и образованию пар ионов в растворах ацетата магния и нитрата магния: моделирование молекулярной динамики и измерения поверхностного натяжения». J. Phys. Chem. 110 (32): 15939–15944. Дои:10.1021 / jp060627p. PMID 16898748.
- ^ Дионисий, Дионисий; Циану, Марина; Ботсарис, Григорий (2000). «Экстрактивная кристаллизация для производства ацетата кальция и ацетата магния из источников карбоната». Ind. Eng. Chem. Res. 39 (11): 4192–4202. Дои:10.1021 / ie9906823.
- ^ Урлахер, Тереза М .; Грип, Марк А. (1995). «Ацетат магния вызывает изменение конформации в примазе Escherichia coli». Биохимия. 34 (51): 16708–16714. Дои:10.1021 / bi00051a020. PMID 8527445.
- ^ Виго, Т.Л., Данна, Г.Ф. «Продукты реакции ацетата магния и пероксида водорода для придания антибактериальной активности волокнистым субстратам». Патент. Получено 2012-04-26.
- ^ Кратчфилд, У. мл. (1942). «Ацетат магния в качестве озоляющего агента в анализе фтора». Ind. Eng. Chem. Анальный. Эд. 14: 57–58. Дои:10.1021 / i560101a023.
- ^ «Паспорт безопасности материалов Sigma-Aldrich». https://www.lakeland.edu/AboutUs/MSDS/PDFs/1083/Magnesium%20Acetate%20Tetrahydrate%20(Sigma).pdf. 2009-02-07. Внешняя ссылка в
| publisher =(Помогите); Отсутствует или пусто| url =(Помогите)
Ацетилгалогениды и соли ацетат ион | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | Он | ||||||||||||||||||
| LiOAc | Быть (OAc)2 BeAcOH | B (OAc)3 | AcOAc ROAc | NH4OAc | AcOOH | FAc | Ne | ||||||||||||
| NaOAc | Mg (OAc)2 | Al (OAc)3 АЛСОЛ Al (OAc)2ОЙ Al2ТАК4(OAc)4 | Si | п | S | ClAc | Ar | ||||||||||||
| KOAc | Ca (OAc)2 | Sc (OAc)3 | Ti (OAc)4 | VO (OAc)3 | Cr (OAc)2 Cr (OAc)3 | Mn (OAc)2 Mn (OAc)3 | Fe (OAc)2 Fe (OAc)3 | Co (OAc)2, Co (OAc)3 | Ni (OAc)2 | Cu (OAc)2 | Zn (OAc)2 | Ga (OAc)3 | Ge | Как (OAc)3 | Se | BrAc | Kr | ||
| RbOAc | Sr (OAc)2 | Y (OAc)3 | Zr (OAc)4 | Nb | Пн (OAc)2 | Tc | Ru (OAc)2 Ru (OAc)3 Ru (OAc)4 | Rh2(OAc)4 | Pd (OAc)2 | AgOAc | Cd (OAc)2 | В | Sn (OAc)2 Sn (OAc)4 | Sb (OAc)3 | Te | IAc | Xe | ||
| CsOAc | Ba (OAc)2 | Hf | Та | W | Re | Операционные системы | Ir | Pt (OAc)2 | Au | Hg2(OAc)2, Hg (OAc)2 | TlOAc Tl (OAc)3 | Pb (OAc)2 Pb (OAc)4 | Би (OAc)3 | По | В | Rn | |||
| Пт | Ра | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла (OAc)3 | Ce (OAc)Икс | Pr | Nd | Вечера | Sm (OAc)3 | Eu (OAc)3 | Gd (OAc)3 | Tb | Dy (OAc)3 | Хо (OAc)3 | Э | Тм | Yb (OAc)3 | Лу (OAc)3 | |||||
| Ac | Чт | Па | UO2(OAc)2 | Np | Пу | Am | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||
