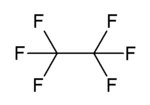
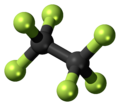
Гексафторэтан - Hexafluoroethane
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гексафторэтан | |||
| Другие имена Гексафторид углерода, 1,1,1,2,2,2-гексафторэтан, перфторэтан, этфоран, галогенуглерод 116, PFC-116, CFC-116, R-116, Arcton 116, галон 2600, ООН 2193 | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.855 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C2F6 | |||
| Молярная масса | 138,01 г / моль−1 | ||
| Внешность | Бесцветный газ без запаха | ||
| Плотность | 5.734 кг.м−3 при 24 ° C | ||
| Температура плавления | -100,6 ° С (-149,1 ° F, 172,6 К) | ||
| Точка кипения | -78,2 ° С (-108,8 ° F, 195,0 К) | ||
| 0.0015% | |||
| бревно п | 2 | ||
Закон Генри постоянный (kЧАС) | 0,000058 моль.кг−1.бар−1 | ||
| Опасности | |||
| Паспорт безопасности | Видеть: страница данных | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Негорючий | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Гексафторэтан это перфторуглерод аналог углеводород этан. Это негорючий газ, практически не растворимый в воды и мало растворим в алкоголь. Это чрезвычайно мощный и долговечный парниковый газ.
Физические свойства
Гексафторэтана твердая фаза имеет два полиморфы. В научной литературе разные фаза перехода указаны температуры. Последние работы определяют его при 103 К (-170 ° C). Ниже 103 К он имеет слегка разупорядоченную структуру, а над точкой перехода имеет объемно центрированный кубический структура.[1] Критическая точка находится при 19,89 ° C (293,04 K) и 30,39 бар.[2]
Таблица плотностей:
| Состояние, температура | Плотность (кг.м−3) |
|---|---|
| жидкость, −78,2 ° C | 16.08 |
| газ, −78,2 ° C | 8.86 |
| газ, 15 ° C | 5.84 |
| газ, 20,1 ° C | 5.716 |
| газ, 24 ° C | 5.734 |
Плотность пара составляет 4,823 (воздух = 1), удельный вес при 21 ° C составляет 4,773 (воздух = 1), а удельный объем при 21 ° C составляет 0,1748 м3.3/кг.
Использует
Гексафторэтан используется как универсальный травить в полупроводник изготовление. Может использоваться для селективного травления металла. силициды и оксидов по сравнению с их металлическими подложками, а также для травления диоксид кремния над кремний. Производство первичного алюминия и полупроводников является основным источником выбросов гексафторэтана, использующего Процесс Холла-Эру.
Вместе с трифторметан он используется в хладагенты R508A (61%) и R508B (54%).
Экологические последствия

Из-за высокой энергии связей C-F гексафторэтан почти инертен и, таким образом, действует как чрезвычайно стабильный парниковый газ, с атмосферным продолжительность жизни 10 000 лет (другие источники: 500 лет).[3] Оно имеет потенциал глобального потепления (GWP) 9200 и озоноразрушающая способность (ODP) 0. Гексафторэтан входит в Список парниковых газов МГЭИК.
Гексафторэтан не существовал в значительных количествах в окружающей среде до промышленного производства. В начале 21 века атмосферная концентрация гексафторэтана достигла 3 pptv.[4] Его полосы поглощения в инфракрасной части спектра вызывают радиационное воздействие около 0,001 Вт / м2.
Риск для здоровья
Из-за своей высокой относительной плотности он собирается в низинных районах, а при высоких концентрациях может вызывать удушье. Другие эффекты для здоровья аналогичны тетрафторметан.
Смотрите также
Рекомендации
- ^ Zeng, S.X .; Simmons, R.O .; Timms, D.N .; Эванс, A.C. (1999). «Динамика и структура твердого гексафторэтана». Журнал химической физики. 110 (3): 1650–61. Bibcode:1999ЖЧФ.110.1650З. Дои:10.1063/1.477806.
- ^ Гельмут Шан: Handbuch der reinsten Gase. Springer, 2005 г., ISBN 978-3-540-23215-5, С. 307.
- ^ «Перфторэтан CASRN: 76-16-4». Сеть токсикологических данных TOXNET. Национальная медицинская библиотека. 2016-10-25.
- ^ «Изменение климата 2001: научная основа». Архивировано из оригинал на 2007-06-15. Получено 2007-06-02.
- Бозин С.Е. и соавт. (1968). «Рост ионизационных токов в тетрафториде углерода и гексафторэтане». J. Phys. D: Прил. Phys. 1 (3): 327–334. Bibcode:1968JPhD .... 1..327B. Дои:10.1088/0022-3727/1/3/309.
внешняя ссылка
- Процесс очистки гексафторэтана
- Протокол измерения тетрафторметана и гексафторэтана при производстве первичного алюминия
- De Maré, G.R .; Панченко, Ю. Н. (март 2006 г.). "Ab initio колебательный анализ гексафторэтана C2F6". Журнал структурной химии. 47 (2): 232–240. Дои:10.1007 / s10947-006-0291-y.
- Протокол измерения тетрафторметана (CF
4) и гексафторэтан (C
2F
6) Выбросы от производства первичного алюминия - Таблица данных термохимии на сайте chemnet.ru