Кофактор инженерия - Cofactor engineering
Кофактор инженерия, подмножество метаболическая инженерия, определяется как манипулирование использованием кофакторы в организме метаболические пути. В инженерии кофакторов концентрации кофакторов меняются, чтобы максимизировать или минимизировать метаболические потоки. Этот вид инженерии можно использовать для оптимизации производства метаболит продукта или для повышения эффективности метаболическая сеть. Использование инженерных одноклеточных организмов для создания прибыльных химикатов из дешевого сырья растет, и разработка кофакторов может сыграть решающую роль в максимальном увеличении производства. Эта область приобрела большую популярность за последнее десятилетие и имеет несколько практических применений в химической промышленности, биоинженерии и фармацевтике.[1]
Кофакторы небелок соединения, которые связываются с белками и необходимы для нормального функционирования белков каталитический функциональность. Кофакторы можно рассматривать как «вспомогательные молекулы» в биологической активности, и они часто влияют на функциональность ферментов. Кофакторы могут быть как органическими, так и неорганическими соединениями. Некоторыми примерами неорганических кофакторов являются железо или магний, а некоторые примеры органических кофакторов включают АТФ или же кофермент А. Органические кофакторы более конкретно известны как коферменты, и многие ферменты требуют добавления коферментов для выполнения нормальной каталитической функции в метаболической реакции. Коферменты связываются с активным центром фермента, способствуя катализу. Создавая кофакторы и коферменты, можно управлять естественной метаболической реакцией, чтобы оптимизировать выход метаболической сети.[2][3][4]
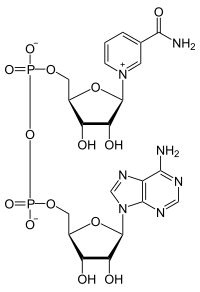
Фон
Кофакторы были открыты Артур Харден и Уильям Янг в 1906 г., когда они обнаружили, что скорость спиртовое брожение в некипяченом дрожжи количество экстрактов увеличивалось при добавлении вареного дрожжевого экстракта.[5] Через несколько лет Ганс фон Эйлер-Челпин идентифицировал кофактор в вареном экстракте как НАД+. Другие кофакторы, такие как АТФ и кофермент А были открыты позже, в 1900-х годах. Механизм кофактор активность была обнаружена, когда, Отто Генрих Варбург в 1936 г. определил, что НАД+ функционировал как акцептор электронов. После этих первоначальных открытий ученые начали понимать, что манипуляции с концентрацией кофакторов можно использовать как инструменты для улучшения метаболические пути.[1]
Важная группа органических кофакторы это семья молекулы упоминается как витамины. Витамин B12 (кобаламин), например, играет решающую роль в организме человека, в то время как коэнзим B12, его производная находится в метаболизм каждого типа клеток в нашем теле. Его присутствие влияет на синтез и регуляцию клеточного ДНК а также участие в синтез жирных кислот и производство энергии. Кофакторы требуются для многих важных метаболические пути, и возможно, что концентрации одного типа кофактора влияют на потоки многих различных путей.
Минералы и ионы металлов, которые организмы поглощают с пищей, являются яркими примерами неорганический кофакторы. Например Zn2+ необходимо, чтобы помочь фермент карбоангидраза как он преобразует углекислый газ и вода бикарбонат и протоны. Широко признанным минералом, который действует как кофактор, является железо, которое необходимо для правильного функционирования гемоглобин белок, переносящий кислород, обнаруженный в красные кровяные тельца. Этот пример, в частности, подчеркивает важность кофакторов в организме животных. метаболизм.
Значимость
Кофакторная инженерия играет важную роль в манипулировании метаболические пути. Метаболический путь - это серия химических реакций, происходящих в организме. Метаболическая инженерия является предметом изменения потоков в метаболическом пути. В метаболической инженерии метаболический путь можно напрямую изменить, изменив функциональность ферменты участвует в пути. Кофакторная инженерия предлагает особый подход и некоторые преимущества для изменения метаболического пути. Вместо изменения ферментов, используемых в метаболическом пути, можно изменить кофакторы. Это может дать метаболическим инженерам преимущество благодаря определенным свойствам кофакторов и способам их модификации.
Метаболические пути могут использоваться инженерами-метаболиками для создания желаемого продукта. Изменяя типы используемых кофакторов и время, в которое они используются, результат метаболической сети может измениться. Чтобы увеличить производство продукта, инженеры-метаболисты имеют возможность снабдить сеть любым кофактором, который лучше всего подходит для этого конкретного процесса. Это приводит к оптимизации сетей для увеличения производства желаемой продукции. Кроме того, изменение кофакторов, используемых в сети, может быть гениальным решением сложной проблемы. Сеть, которая присутствует в ячейке, но часто не используется, может иметь желаемый продукт. Вместо разработки совершенно нового набора способов производства продукта можно применить кооперативную инженерию. За счет замены ферментов на использование кофакторов, легко доступных в клетке, обычно неиспользуемая сеть больше не ограничивается кофакторами, и производство может быть увеличено.
Помимо изменения выхода метаболических сетей, изменение кофакторов, используемых в сети, может снизить эксплуатационные расходы при попытке сформировать желаемый продукт. НАДН и НАДФН - два чрезвычайно распространенных клеточных кофактора, различающиеся только наличием фосфатной группы. Однако эта фосфатная группа делает НАДФН намного менее стабильным, чем НАДН, и, следовательно, более дорогим для синтеза. Таким образом, полезно попробовать и использовать NADH в некоторых сотовых сетях, потому что он часто дешевле, более доступный и выполняет ту же задачу, что и NADPH.
Инструменты и процессы
Кофакторная инженерия чаще всего связана с манипулированием микроорганизмы Такие как Saccharomyces cerevisiae и кишечная палочка, и поэтому требует использования рекомбинантная ДНК техники. В этих техниках используются небольшие круглые сегменты ДНК называется плазмиды, которые могут быть занесены и внедрены микроорганизмами, такими как кишечная палочка. Эти плазмиды специально разработаны в лабораториях, чтобы их можно было легко включить и воздействовать на экспрессию различных белок, метаболиты и ферменты. Например, конкретная плазмида может вызывать изменение фермента. аминокислота последовательность, которая может увеличить его сродство к определенному субстрат.
Микроорганизмам требуется среда для роста, и одна, обычно используемая для культур кишечная палочка - бульон Лурия-Бертани (ЛБ). Эта среда часто дополняется глюкоза и часто будет содержать дополнительные молекулы разработан для обеспечения оптимального роста культур. Затем предварительные культуры можно выращивать во встряхиваемых колбах. Они просто подключены Колбы Эрленмейера которые остаются на орбитальном шейкере, который вращается на очень высокой Об / мин. Этот процесс обеспечивает аэрацию культуры, что необходимо для оптимального роста. Как только прекультуры готовы, плазмиды, необходимые для конкретных экспериментов, добавляются к каждой культуре отдельно, а затем каждую культуру переносят в биореактор. Биореакторы - это системы, которые позволяют культурам расти в контролируемой среде. Это оставляет введенные плазмиды в качестве единственной независимой переменной. Требуемая температура, pH, концентрации метаболитов и различные другие факторы окружающей среды могут поддерживаться биореактором, обеспечивая идентичные условия роста для каждой культуры.
После того, как образцам дают возможность расти в реакторе в течение определенного периода, их можно удалить и изучить, чтобы определить, очевидны ли предполагаемые изменения в организме. Так как кофакторная инженерия чаще всего имеет дело с метаболические пути, эти организмы часто изучаются, но вводятся специфические помеченные флуоресцентный метаболиты и документирование их продвижения различными путями. В других случаях результаты более очевидны и легко наблюдаемы, например, при уменьшении этиловый спирт изготовление дрожжи упоминается ниже.[3][4]
Приложения
Изменение кофактора фермента с НАДФН на НАДН
Биокатализаторы необходимы для производства хиральный строительные блоки, необходимые для производства фармацевтических препаратов и других химических веществ, используемых обществом. Многие такие биокатализаторы требуют НАДФН как кофактор. НАДФН, кофактор, очень похожий на НАДН, более дорогой и менее стабильный, чем его аналог. НАДН. По этим причинам производители предпочли бы, чтобы биокатализаторы, которые они используют в своих производственных линиях, принимали НАДН, а не НАДФН. Кофакторная инженерия недавно оказалась успешной в изменении ферментов, которые предпочли НАДН в качестве кофактора вместо НАДФН. В 2010 году группа ученых выполнила разработку кофактора на фермент Gre2p, предпочитающий НАДФН дегидрогеназа нашел в Saccharomyces cerevisiae. Gre2p восстанавливает соединение дикетон 2,5-гександион до хиральных строительных блоков (5S) -гидрокси-2-гексанон и (2S, 5S) -гександиол. Ученые определили, что Asn9 (Аспарагин, позиция 9) была важной аминокислота активный сайт Gre2p. В частности, Asn9 связывается с 3’-гидроксильной группой и 2’-атомом кислорода аденил-рибозы. часть. Через прямой мутагенез, ученые обменяли Asn9 на Asp (Аспарагиновая кислота ) и Glu (Глютаминовая кислота ). Это изменение привело к снижению зависимости Gre2p от NADPH и к увеличению сродства к NADH. Это привело к увеличению активности Gre2p при использовании NADH. Было замечено, что замена Asn9 на Glu дает больший эффект, чем замена Asn9 на Asp. Asn содержит полярную незаряженную боковую цепь, в то время как как Asp, так и Glu содержат полярно заряженную боковую цепь. Повышенный эффект Glu вызван дополнительным углеродом в его боковой цепи, который приближает его к аденил-рибозной части. Это позволяет усилить водородная связь между 2’- и 3’-рибозой гидроксил группы и боковая цепь карбоксил группа. Максимальная скорость реакции увеличилась вдвое при использовании NADH, когда Asn9 был заменен Glu. Получив эти результаты, ученые успешно сконструировали Gre2p, который предпочел НАДН над НАДФН, и увеличили скорость восстановления 2,5-гександиона. Это позволит химическим компаниям снизить свои производственные затраты за счет использования NADH вместо NADPH, по крайней мере, для этого конкретного сокращения.[6]
Изменение предпочтения кофактора сети
Альтернативный пример изменения предпочтения фермента кофакторам - это изменение НАДН-зависимой реакции на НАДФН-зависимые реакции. В этом примере сами ферменты не изменяются, но вместо этого выбираются разные ферменты, которые проводят ту же реакцию с использованием другого кофактора. Был создан инженерный путь, чтобы 1-бутанол из Ацетил-КоА изменяя ферменты метаболического пути S. elongatus. В Clostridium род, как известно, продуцирует 1-бутанол, обеспечивая путь, который может быть встроен в S. elongatus. Этот путь синтезирует 1-бутанол с использованием пути обратного β-окисления. Ферменты, участвующие в этом недавно созданном пути, были НАДН-специфичными, что было проблематично для репликации этого пути у S. elongatus, поскольку цианобактерии производят намного больше НАДФН, чем НАДН.
Затем исследовательская группа определила ферменты, которые используют НАДФН или одновременно НАДФН и НАДН путем биоразведка. Было обнаружено, что ацетоацетил-КоА-редуктаза (PhaB) является подходящей заменой гидроксимасляной дегидрогеназы (Hbd). Чтобы заменить AdhE2, исследователи обнаружили, что НАДФ-зависимая алкогольдегидрогеназа (YqhD) из E. coli эффективна для этого пути. Кроме того, исследователям нужна была дегидрогеназа, чтобы заменить способность AdhE2 к альдегиддегидрогеназе. Было обнаружено, что КоА-ацилирующая бутиральдегиддегидрогеназа (Bldh) из C. saccharoperbutylacetonicum является хорошим вариантом. Вместе PhaB, Bldh, YqhD могут заменять Hbd и AdhE2 соответственно, чтобы изменить предпочтение кофактора восстановления 3-кетобутирил-КоА с использования NADH на использование NADPH. Затем авторы сконструировали различные комбинации различных ферментов (из тех, что присутствуют в пути обратного окисления и ферментов, использующих НАДФН) путем сверхэкспрессии различных генов в культурах S. elongatus PCC 7942. Для этого они сконструировали плазмиды содержащие гены, соответствующие ферментам, и объединили их в геном S. elongates. После ферментных анализов штамм цианобактерий, экспрессирующих НАДФН с использованием ферментов, продуцировал наибольшее количество 1-бутанола (29,9 мг / л), в четыре раза превышающее количество штаммов, не содержащих НАДФН, использующих ферменты. В целом, 1-бутанол продуцировался в S. elongatus с использованием пути из другого организма. Этот путь был модифицирован, чтобы соответствовать предпочтительному восстанавливающему кофактору цианобактерий.[7]

Модификация метаболитного флюса с помощью равновесия кофакторов
В кофакторной инженерии метаболический путь изменяется путем изменения концентраций определенных кофакторов, которые продуцируются либо на этом конкретном пути, либо на отдельном пути. Например, гипотетический организм может иметь два произвольных пути, называемых A и B, где некоторые ферменты как в A, так и в B используют одни и те же кофакторы. Если ученые захотят уменьшить выработку пути А, они могут сначала рассмотреть вопрос о непосредственной инженерии ферментов, участвующих в пути А, возможно, для уменьшения определенного активный сайт близость к его субстрат. Однако в некоторых случаях ферменты в A может быть трудно сконструировать по разным причинам, или может быть невозможно сконструировать их без опасного воздействия на какой-то третий метаболический путь C, который использует те же ферменты. В качестве отдельного варианта ученые могут увеличить поток B, что может быть проще в инженерии. Это, в свою очередь, может «связать» кофакторы, необходимые для A, что замедлит ферментативная активность, уменьшая выход в A. Это один гипотетический пример того, как можно использовать кофакторную инженерию, но есть много других уникальных случаев, когда ученые используют кофакторы как способ изменения метаболических путей. Основным преимуществом кофакторной инженерии является то, что ученые могут использовать ее для успешного изменения метаболических путей, которые сложно спроектировать с помощью обычной метаболической инженерии. Это достигается за счет воздействия на более легко конструируемые ферменты отдельными путями, в которых используются одни и те же кофакторы. Поскольку многие кофакторы используются разными ферментами в нескольких путях, инженерия кофакторов может быть эффективной и рентабельной альтернативой существующим методам метаболической инженерии.[8]
Дрожжи обычно используются в пивоваренной и винодельческой промышленности, потому что они способны эффективно производить этиловый спирт сквозь метаболический путь ферментация при отсутствии кислорода. Ферментация требует фермента глицерин-3-фосфатдегидрогеназа (GPDH), который зависит от кофактора НАДН. Этот путь включает преобразование глюкоза как этанол, так и глицерин, оба из которых используют НАДН в качестве кофактор. Ученые создали Saccharomyces cerevisiae перепроизводить GPDH, что сдвигает клетки метаболический поток от этанола к глицерину, ограничивая доступность НАДН в части пути производства этанола. Противоположный эффект был достигнут путем воздействия на отдельный путь в клетке, Глутамат Путь синтеза. Инактивация экспрессии фермента глутаматдегидрогеназа, который НАДФН зависимая и сверхэкспрессирующая ферменты глютамин синтетаза и глутаматсинтетаза, которые полагаются на НАДН в качестве кофактора, сдвинули баланс кофакторов в пути синтеза глутамата. Этот путь теперь зависит от НАДН, а не от НАДФН, что снижает доступность НАДН в пути ферментации. Это, в свою очередь, приводит к увеличению производства этанола и снижению глицерин производство. Этот метод манипулирования метаболические потоки можно представить себе так же, как глобальные рынки топлива, где рост производства этанола для использования в автомобильной промышленности снизит его доступность в пищевой промышленности. По сути, производство большего количества двигателей, работающих на этаноле, может привести к снижению потребления переработанных сладостей, содержащих кукурузный сироп с высоким содержанием фруктозы. Эта разработка кофакторов применима к пивоваренной и винодельческой промышленности, поскольку она позволяет регулировать уровень этанола в алкогольных напитках. Достижения в винодельческой промышленности привели к постоянному увеличению содержания этанола, поэтому виноделы, в частности, будут заинтересованы в возможности снижения уровня этанола в некоторых из своих вин.[3]
Цикл лимонной кислоты
Коэнзим А (CoA) и ацетил-КоА два промежуточных метаболиты, особенно в Цикл лимонной кислоты, которые участвуют в более чем 100 различных реакциях метаболизм микроорганизмов. Недавние эксперименты показали, что чрезмерное выражение фермент пантотенаткиназа и добавление пантотеновая кислота в пути биосинтеза КоА позволили регулировать потоки как КоА, так и ацетил-КоА. Эта повышенная концентрация кофакторов привела к увеличению потока углерода в изоамилацетат путь синтеза, повысить эффективность производства изоамилацетата. Изоамилацетат используется в промышленности для искусственного ароматизатора и для проверки эффективности респираторы. Помимо производства изоамилацетата, манипуляции с биосинтезом КоА во время пируват гидрогеназа реакция также вызывает увеличение производства обоих сукцинат и ликопин, каждый из которых благотворно влияет на человеческий организм. Повышение концентрации сукцината, который используется как катализатор, может привести к увеличению скорости цикла лимонной кислоты и, следовательно, к увеличению метаболизм. Было показано, что увеличение концентрации ликопина снижает риск рак простаты. Потенциальные выгоды от повторения такого подвига разработки кофакторов и их успешного внедрения в отраслевую практику бесчисленны.[4][9][10]
Производство бумаги
Многие важные промышленные ферменты использовать кофакторы для катализа реакций. Используя кофакторы для управления метаболические пути, можно снизить стоимость материалов, исключить этапы производства, сократить время производства, уменьшить загрязнение и повысить общую эффективность производства. Один случай, демонстрирующий некоторые из этих производственных преимуществ, связан с генной инженерией осина деревья. В процессе производства бумаги производственные предприятия должны выходить из строя. лигнин, биохимическое соединение, которое придает жесткость стволу дерева, чтобы сформировать мякоть, используемую на протяжении всего остального производства. Процесс химической варки целлюлозы требует от производственного предприятия использования значительного количества энергии, а также многих дорогих и токсичных химикатов. Группа генных инженеров через кофакторная инженерия, сконструировал генетически превосходный осина дерево, производившее меньше лигнина. Эти генно-инженерные деревья позволили бумажным фабрикам сократить свои затраты, загрязнение окружающей среды и время производства.[1][11]
Другие примеры
| Организм | Что изменилось | Что это значит |
|---|---|---|
| Микобактерии смегматис | Коэнзим F420 | Может отключить Кофактор что приводит к лекарственной устойчивости Туберкулез[12] |
| Цианобактерии | Кофактор железо-молибденовый | Производство водородного газа для энергетики[13] |
| Королевство Archea | Молибден Нитрогеназа Кофактор | Повышение эффективности Фиксация азота[14] |
| Термоанаэробактерии mathranii | глицериндегидрогеназа | Делать Термофильный Бактерии производят Этиловый спирт Более эффективно [15] |
Краткое описание других важных примеров использования кофакторной инженерии.
Примечания
- ^ а б c Рааб, Михаил; Кейт Тайро; Грегори Стефанопулос (2005). «Метаболическая инженерия». Достижения в области биохимической инженерии / биотехнологии. 100 (763): 1–17. Дои:10.1007 / b136411. PMID 16270654.
- ^ Поллак, Н; C Dolle; М. Циглер (2006). «Способность восстанавливать: пиридиновые нуклеотиды - небольшие молекулы с множеством функций». Биохимия. 402 (2): 205–218. Дои:10.1042 / BJ20061638. ЧВК 1798440. PMID 17295611.
- ^ а б c Хе, Стефани; Реми Качон; Сильви Декуин (2006). «Кофакторная инженерия в Saccharomyces cerevisiae: экспрессия H2O-образующей NADH-оксидазы и влияние на окислительно-восстановительный метаболизм». Метаболическая инженерия. 8 (4): 303–314. Дои:10.1016 / j.ymben.2005.12.003. PMID 16473032.
- ^ а б c Вадали, Равишанкар; Джордж Беннетт (апрель 2004 г.). «Кофакторная инженерия внутриклеточного КоА / ацетил-КоА и его влияние на перераспределение метаболического потока в Escherichia coli». Метаболическая инженерия. 6 (2): 133–139. Дои:10.1016 / j.ymben.2004.02.001. PMID 15113566.
- ^ Артур Харден и Уильям Джон Янг. «Алкогольная закваска дрожжевого сока». Труды Лондонского королевского общества. Серия B, содержащая статьи биологического характера, Vol. 77, No. 519 (12 апреля 1906 г.), стр. 405-420 JSTOR
- ^ Кацберг, Майкл; Надя Скорупа-Парачин; Мари-Франсуаза Горва-Грауслунд; Мартин Бертау (2010). «Предпочтение инженерных кофакторов для биокатализаторов, восстанавливающих кетон: исследование мутагенеза γ-дикетонредуктазы из дрожжевых Saccharomyces cerevisiae». Международный журнал молекулярных наук. 11 (4): 1735–1758. Дои:10.3390 / ijms11041735. ЧВК 2871135. PMID 20480039.
- ^ Итан Лан; Джеймс Ляо. «АТФ способствует прямому фотосинтетическому производству 1-бутанола у цианобактерий». Труды Национальной академии наук. Получено 11 декабря 2012.
- ^ Сан, Ка-Ю; Джордж Н. Беннетт; Сусана Дж. Берриос-Ривера; Рави В. Вадали; Йеа-Тынг Ян; Эмили Хортон; Фред Б. Рудольф; Берна Сарияр; Кимати Блэквуд (апрель 2002 г.). «Метаболическая инженерия через манипуляции с кофактором и ее влияние на перераспределение метаболического потока в кишечной палочке». Метаболическая инженерия. 4 (2): 182–193. Дои:10.1006 / мбен.2001.0220. PMID 12009797.[мертвая ссылка ]
- ^ Джованнуччи, Эдвард; Альберто Аскерио; Эрик Римм; Меир Штампфер; Грэм Колдиц; Уолтер Уиллетт (май 1995 г.). «Потребление каротиноидов и ретино в связи с риском рака простаты». Журнал Национального института рака. 87 (23): 1767–1776. Дои:10.1093 / jnci / 87.23.1767. PMID 7473833.
- ^ Потера, Кэрол (декабрь 2005 г.). «Как сделать сукцинат более успешным». Перспективы гигиены окружающей среды. 113 (12): A832 – A835. Дои:10.1289 / ehp.113-a832. ЧВК 1314946. PMID 16330341.
- ^ Хорват, Ласло; Илона Пешлен; Перри Перальта; Богумил Касал; Лайгенг Ли (2010). «Механические свойства генно-инженерной молодой осины с измененным содержанием и / или структурой лигнина». Наука о древесине и волокне. 42.
- ^ Башири, Г; Rehan, AM; Гринвуд, ДР; Диксон, JM; Бейкер, EN (2010). «Метаболическая инженерия производства кофактора F420 у Mycobacterium smegmatis». PLOS One. 5 (12): e15803. Дои:10.1371 / journal.pone.0015803. ЧВК 3012119. PMID 21209917.
- ^ Масукава, H; Иноуэ, К; Сакураи, H; Wolk, CP; Hausinger, RP. (2010). «Сайт-направленный мутагенез активного сайта нитрогеназы штамма Anabaena PCC 7120 для увеличения фотобиологической продукции водорода». Прикладная и экологическая микробиология. 76 (20): 6741–50. Дои:10.1128 / aem.01056-10. ЧВК 2953041. PMID 20709836.
- ^ Hernandez, JA; Curatti, L; Азнар, CP; Перова, З .; Britt, RD; Рубио, Л. (2008). «Транспортировка металлов для фиксации азота: NifQ передает молибден NifEN / NifH для биосинтеза нитрогеназного кофактора FeMo». Труды Национальной академии наук Соединенных Штатов Америки. 105 (33): 11679–8. Дои:10.1073 / pnas.0803576105. ЧВК 2575292. PMID 18697927.
- ^ Яо, S; Mikkelsen, MJ. (2010). «Метаболическая инженерия для улучшения производства этанола в Thermoanaerobacter mathranii». Прикладная микробиология и биотехнология. 88 (1): 199–208. Дои:10.1007 / s00253-010-2703-3. PMID 20552355.
