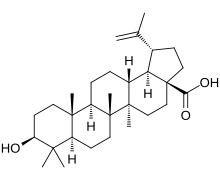
Бетулиновая кислота - Betulinic acid
 | |
| Имена | |
|---|---|
| Название ИЮПАК (3β) -3-Гидрокси-lup-20 (29) -ен-28-овая кислота | |
| Другие имена Бетулиновая кислота Майрин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.006.773 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C30ЧАС48О3 | |
| Молярная масса | 456.711 г · моль−1 |
| Температура плавления | От 316 до 318 ° C (от 601 до 604 ° F; от 589 до 591 K) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бетулиновая кислота пентациклический тритерпеноид у которого есть антиретровирусный, антималярийный, и противовоспалительное средство свойства, а также недавно открытый потенциал в качестве противоракового агента, путем ингибирования топоизомераза.[2] Он находится в лаять нескольких видов растений, в основном белая береза (Betula pubescens)[3] от которого оно и получило свое название, а также бердерево (Ziziphus mauritiana ), самоисцеление (Prunella vulgaris ), тропический хищные растения Triphyophyllum peltatum и Ancistrocladus heyneanus, Diospyros leucomelas, член хурма семья, Tetracera boiviniana, джамбул (Сизигий формозан),[4] айва цветущая (Псевдоцидония китайская, бывший Chaenomeles sinensis KOEHNE),[5] Розмари,[6]и Pulsatilla китайский.[7]
Противоопухолевое действие
Эта статья нужно больше медицинские справки за проверка или слишком сильно полагается на основные источники, в частности: Раздел. (Сентябрь 2014 г.) |
В 1995 году бетулиновая кислота была названа селективным ингибитор человека меланома.[8]Затем было продемонстрировано, что апоптоз в нейробластоме человека in vitro и in vivo в модельных системах.[9] В свое время он подвергался разработка лекарств при поддержке программы Rapid Access to Intervention Development Национальный институт рака.[3]Также была обнаружена активная бетулиновая кислота. in vitro против нейроэктодермального (нейробластома, медуллобластома, саркома Юинга[10]) и злокачественные опухоли головного мозга,[4][11] рак яичников,[4] в человеческом лейкемия Ячейки HL-60,[7] и линии клеток злокачественной плоскоклеточной карциномы головы и шеи SCC25 и SCC9.[12]Напротив, эпителиальные опухоли, такие как грудь, двоеточие, мелкоклеточное легкое и почечно-клеточный рак, а также Т-клеточный лейкоз клетки, совершенно не реагировали на лечение бетулиновой кислотой.[10]
Установлено, что эффекты бетулиновой кислоты как противоопухолевого средства при раке груди каннабиноидный рецептор зависимый. Бетулиновая кислота ведет себя как CB1 антагонист и CB2 агонист.[13]
Способ действия
Взяв во внимание образ действий бетулиновой кислоты, о ее антипролиферативный и апоптоз -индуцирующие механизмы. В нейроэктодермальных опухолевых клетках апоптоз, вызванный бетулиновой кислотой, сопровождается каспаза активация, митохондриальный мембранные изменения и ДНК фрагментация.[10][12] Каспазы производятся как неактивные проферменты, которые протеолитически процессируются до их активных форм. Эти протеазы могут взаимодействовать в протеолитических каскадах, в которых каспазы активируют себя и друг друга. Инициирование каскада каспаз может привести к активации эндонуклеазы такие как ДНКаза, активируемая каспазой (CAD). После активации CAD способствует деградации ДНК.[12] Бетулиновая кислота вызывает апоптоз путем прямого воздействия на митохондрии, что приводит к высвобождению цитохрома-С, который, в свою очередь, регулирует активацию каспазы «ниже по течению».[12]Бетулиновая кислота обходит устойчивость к CD95 и доксорубицин апоптоз, обусловленный другим молекулярным механизмом апоптоза, индуцированного бетулиновой кислотой.
Роль p53 в отношении апоптоза, вызванного бетулиновой кислотой, остается спорным. Фульда предположил p53-независимый механизм апоптоза, основанный на отсутствии накопления p53 дикого типа, обнаруженного при обработке бетулиновой кислотой, тогда как белок p53 дикого типа сильно увеличивался после обработки доксорубицином.[10] Предложение подтверждается исследованиями Раисовой.[14] С другой стороны, Рибер предположил, что бетулиновая кислота оказывает ингибирующее действие на метастатическую меланому человека, частично за счет увеличения p53.[15]
Исследование также продемонстрировало преимущественный апоптотический эффект бетулиновой кислоты на метастатические клетки меланомы C8161 с большей фрагментацией ДНК и остановкой роста и более ранней потерей жизнеспособности, чем их неметастатический аналог C8161 / neo 6.3.[15]Сравнивая бетулиновую кислоту с другими методами лечения, Зуко продемонстрировал, что она менее чем на 10% эффективнее доксорубицина и показала in vitro антипролиферативная активность в отношении линий клеток меланомы и немеланомы, в том числе устойчивых к доксорубицину. В нормальной линии клеток дерматобласта человека бетулиновая кислота была от половины до одной пятой токсичнее доксорубицина.[4] Способность бетулиновой кислоты вызывать два разных эффекта (цитотоксический и цитостатический) на два клона, происходящих от одного и того же метастаза меланомы человека, предполагает, что развитие клонов, устойчивых к этому агенту, будет более маловероятным, чем к обычным цитотоксическим препаратам. Более того, несмотря на более низкую эффективность по сравнению с доксорубицином, бетулиновая кислота, по-видимому, является селективной в отношении опухолевых клеток с минимальной токсичностью в отношении нормальных клеток.[4] Эффект бетулиновой кислоты на клеточные линии меланомы сильнее, чем ее ингибирующий рост эффект на первичные меланоциты.[16] Исследование комбинации бетулиновой кислоты с γ-облучением показало явно аддитивные эффекты и указывало, что они различаются по способам действия.[16]
С-3 этерификация бетулиновой кислоты привела к открытию бевиримат, ВИЧ-1 ингибитор созревания запатентовано Рона-Пуленк (теперь Санофи-Авентис). Однако клиническая разработка была остановлена из-за плохой фармакодинамический характеристики.[17]
Биосинтез
Saccharomyces cerevisiae был разработан для производства бетулиновой кислоты из мевалонатный путь, со сквален-2,3-эпоксидом в качестве промежуточного продукта. Ацетил-КоА конвертируется в сквален за счет использования 3-гидроксил-3-метилглутарил-КоА редуктазы (HMGR) и бифункционального фарнезил-дифосфат фарнезилтрансфераза и скваленсинтаза (ERG9) и окисление НАДФН до НАДФ+. Затем он дополнительно насыщается кислородом скваленмонооксигеназа (ERG1) в сквален-2,3-эпоксид. Это циклически лупеол посредством Arabidopsis thaliana лупеолсинтаза (AtLUP1). Наконец, лупеол превращается в бетулиновую кислоту через Катарантус розовый Монооксигеназа Р450 (CrAO) с окислением НАДФН в НАДП+.[18]

Противораковые производные
Основное неудобство для будущей клинической разработки бетулиновой кислоты и аналогов заключается в их плохой растворимости в водных средах, таких как сыворотка крови и полярные растворители, используемые для биоанализов. Чтобы обойти эту проблему водорастворимости и улучшить фармакологические свойства, многие производные были синтезированы и оценены на цитотоксическую активность. Одно исследование показало, что модификации C-20 приводят к потере цитотоксичности. Другое исследование продемонстрировало важность присутствия группы -COOH, поскольку соединения, замещенные в этом положении, такие как лупеол и метил бетулинат были менее активны в отношении меланомы человека, чем бетулиновая кислота. Более того, некоторые производные C-28 аминокислот и фталатов C-3 проявляли более высокую цитотоксическую активность против линий раковых клеток с улучшенной селективной токсичностью и растворимостью в воде. Чаттерджи и другие. получили 28-O-β-D-глюкопиранозид бетулиновой кислоты путем микробной трансформации с Каннингхамелла виды, в то время как Баглин и др. получил его путем органического синтеза. Этот глюкозид не показал каких-либо значительных in vitro активность на клеточных линиях меланомы человека (MEL-2) и колоректальной аденокарциномы человека (HT-29), что подтверждает важность функции карбоновой кислоты для сохранения цитотоксичности. Недавно Готье и другие. синтезировали серию 3-О-гликозиды бетулиновой кислоты, которые обладают сильнодействующим действием in vitro противораковая активность против линий раковых клеток человека.[19]
Смотрите также
Рекомендации
- ^ https://echa.europa.eu
- ^ Чоудхури А.Р., Мандал С., Миттра Б., Шарма С., Мукхопадхьяй С., Маджумдер, Гонконг (июль 2002 г.). «Бетулиновая кислота, мощный ингибитор эукариотической топоизомеразы I: определение стадии ингибирования, основной ответственной функциональной группы и разработка более мощных производных». Монитор медицинских наук. 8 (7): BR254–65. PMID 12118187.
- ^ а б Тан Й, Ю. Р., Пеццуто Дж. М. (июль 2003 г.). «Индуцированная бетулиновой кислотой запрограммированная гибель клеток в клетках меланомы человека включает активацию митоген-активируемой протеинкиназы». Клинические исследования рака. 9 (7): 2866–75. PMID 12855667.
- ^ а б c d е Zuco V, Supino R, Righetti SC, Cleris L, Marchesi E, Gambacorti-Passerini C, Formelli F (январь 2002 г.). «Избирательная цитотоксичность бетулиновой кислоты на линиях опухолевых клеток, но не на нормальных клетках». Письма о раке. 175 (1): 17–25. Дои:10.1016 / S0304-3835 (01) 00718-2. PMID 11734332.
- ^ Гао Х., Ву Л., Куроянаги М., Харада К., Кавахара Н., Накане Т., Умехара К., Хирасава А., Накамура И. (ноябрь 2003 г.). «Противоопухолевые компоненты Chaenomeles sinensis KOEHNE и их активность в эпидермальных клетках мышей JB6». Химико-фармацевтический бюллетень. 51 (11): 1318–21. Дои:10.1248 / cpb.51.1318. PMID 14600382. (Chaenomeles sinensis KOEHNE теперь назван Псевдоцидония китайская )
- ^ Абэ Ф, Ямаути Т., Нагао Т., Киндзё Дж., Окабе Х., Хиго Х., Акахане Х. (ноябрь 2002 г.). «Урсоловая кислота как трипаноцидный компонент розмарина». Биологический и фармацевтический бюллетень. 25 (11): 1485–7. Дои:10.1248 / bpb.25.1485. PMID 12419966.
- ^ а б Цзи З. Н., Е В. К., Лю Г. Г., Сяо В. Л. (ноябрь 2002 г.). «Апоптоз, опосредованный 23-гидроксибетулиновой кислотой, сопровождается снижением экспрессии bcl-2 и теломеразной активности в клетках HL-60». Науки о жизни. 72 (1): 1–9. Дои:10.1016 / S0024-3205 (02) 02176-8. PMID 12409140.
- ^ Пиша Е., Чай Х., Ли И.С., Чагведера Т.Е., Фарнсворт Н.Р., Корделл Г.А., Бичер С.В., Фонг Х.Х., Кингхорн А.Д., Браун Д.М. (октябрь 1995 г.). «Открытие бетулиновой кислоты в качестве селективного ингибитора меланомы человека, который действует за счет индукции апоптоза». Природа Медицина. 1 (10): 1046–51. Дои:10,1038 / нм 1095-1046. PMID 7489361. S2CID 24752850.
- ^ Шмидт М.Л., Кузманов К.Л., Линг-Индек Л., Пеццуто Дж. М. (октябрь 1997 г.). «Бетулиновая кислота индуцирует апоптоз клеточных линий нейробластомы человека». Европейский журнал рака. 33 (12): 2007–10. Дои:10.1016 / S0959-8049 (97) 00294-3. PMID 9516843.
- ^ а б c d Фульда С., Фризен С., Лос М., Скаффиди С., Миер В., Бенедикт М., Нуньес Г., Краммер П. Х., Питер М. Е., Дебатин К. М. (ноябрь 1997 г.). «Бетулиновая кислота запускает CD95 (APO-1 / Fas) - и p53-независимый апоптоз посредством активации каспаз в нейроэктодермальных опухолях». Исследования рака. 57 (21): 4956–64. PMID 9354463.
- ^ Вик В., Гриммел С., Вагенкнехт Б., Дичганс Дж., Веллер М. (июнь 1999 г.). «Индуцированный бетулиновой кислотой апоптоз в клетках глиомы: последовательное требование для синтеза нового белка, образования активных форм кислорода и процессинга каспазы». Журнал фармакологии и экспериментальной терапии. 289 (3): 1306–12. PMID 10336521.
- ^ а б c d Thurnher D, Turhani D, Pelzmann M, Wannemacher B, Knerer B, Formanek M, Wacheck V, Selzer E (сентябрь 2003 г.). «Бетулиновая кислота: новое цитотоксическое соединение против злокачественных клеток рака головы и шеи». Голова и шея. 25 (9): 732–40. Дои:10.1002 / хед.10231. PMID 12953308.
- ^ Лю Х, Джутору И., Лей П., Ким К., Ли СО, Бренц Л.К., Пратер П.Л., Safe S (июль 2012 г.). «Бетулиновая кислота нацелена на YY1 и ErbB2 посредством каннабиноидного рецептора-зависимого разрушения микроРНК-27a: ZBTB10 при раке груди». Молекулярная терапия рака. 11 (7): 1421–31. Дои:10.1158 / 1535-7163.MCT-12-0026. ЧВК 4924623. PMID 22553354.
- ^ Раисова М., Хоссини А.М., Эберле Дж., Рибелинг К., Видер Т., Штурм I, Даниэль П.Т., Орфанос К.Э., Гейлен С.К. (август 2001 г.). «Отношение Bax / Bcl-2 определяет восприимчивость клеток меланомы человека к CD95 / Fas-опосредованному апоптозу». Журнал следственной дерматологии. 117 (2): 333–40. Дои:10.1046 / j.0022-202x.2001.01409.x. PMID 11511312.
- ^ а б Рибер М., Страсберг Рибер М. (май 1998 г.). «Индукция p53 без увеличения p21WAF1 при гибели клеток, опосредованной бетулиновой кислотой, является предпочтительной для метастатической меланомы человека». ДНК и клеточная биология. 17 (5): 399–406. Дои:10.1089 / dna.1998.17.399. PMID 9628583.
- ^ а б Зельцер Э., Пиментель Э., Вачек В., Шлегель В., Пехамбергер Х., Янсен Б., Кодым Р. (май 2000 г.). «Эффекты бетулиновой кислоты отдельно и в сочетании с облучением на клетки меланомы человека». Журнал следственной дерматологии. 114 (5): 935–40. Дои:10.1046 / j.1523-1747.2000.00972.x. PMID 10771474.
- ^ Новые 3,28-дизамещенные производные бетулиновой кислоты в качестве эффективных агентов против ВИЧ Цели / гипотеза Out-лицензирования. iptechex Pharmalicensing, IP Technology Exchange (2013)
- ^ а б Ли, Цзин; Чжан, Яньшэн (19 июня 2014 г.). "Регулирование производства бетулиновой кислоты в Saccharomyces cerevisiae управляя внутриклеточными поставками кофактора НАДФН и кислорода ». Журнал биологии и биоинженерии. 119 (1): 77–81. Дои:10.1016 / j.jbiosc.2014.06.013. PMID 25043336.
- ^ Готье С., Лего Дж, Лебрен М., Дюфур П., Пишет А (октябрь 2006 г.). «Гликозидирование тритерпеноидов лупанового типа как сильнодействующих цитотоксических агентов in vitro». Биоорганическая и медицинская химия. 14 (19): 6713–25. Дои:10.1016 / j.bmc.2006.05.075. PMID 16787747.
