X-инактивация - X-inactivation

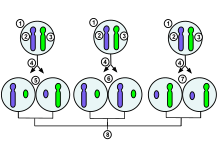
1. Ранняя стадия эмбриональной клетки женщины-человека
2. материнская Х-хромосома
3. отцовская Х-хромосома
4. митоз и случайная инактивация Х-хромосомы
5.Отцовская хромосома случайным образом инактивирована в одной дочерней клетке, материнская хромосома инактивирована в другой.
6.Отцовская хромосома случайным образом инактивирована в обеих дочерних клетках.
7. материнская хромосома случайным образом инактивирована в обеих дочерних клетках.
8. три возможных результата случайной комбинации
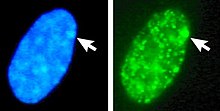
Слева: ядро, окрашенное ДНК (DAPI). Стрелка указывает местонахождение тела Барра (Си). Справа: ассоциированная ДНК гистоны белок обнаружен
X-инактивация (также называется Лионизация, в честь английского генетика Мэри Лайон ) - это процесс, при котором одна из копий Х хромосома инактивирован в терианец женский пол млекопитающие. Неактивная Х-хромосома подавляется за счет упаковки в транскрипционно неактивную структуру, называемую гетерохроматин. Поскольку почти все самки млекопитающих имеют две X-хромосомы, X-инактивация не позволяет им иметь вдвое больше X-хромосом. генные продукты так как самцы, у которых есть только одна копия Х-хромосомы (см. компенсация дозировки ).
Выбор того, какая Х-хромосома будет инактивирована, является случайным. плацентарные млекопитающие такие как люди, но как только Х-хромосома инактивирована, она остается неактивной на протяжении всей жизни клетки и ее потомков в организме. В отличие от случайной X-инактивации у плацентарных млекопитающих, инактивация у сумчатые применяется исключительно к отцовской X-хромосоме.
Механизм
Цикл активации Х-хромосомы у грызунов
Приведенные ниже абзацы относятся только к грызунам и не отражают XI у большинства млекопитающих. Х-инактивация является частью цикла активации Х-хромосомы на протяжении всей жизни самки. Яйцо и оплодотворенная зигота изначально используют материнские транскрипты, и весь эмбриональный геном заглушается до активации зиготического генома. После этого все клетки мыши подвергаются раннему, отпечатанный инактивация отцовской Х-хромосомы в 4–8 клеточная стадия эмбрионы.[3][4][5][6] В внеэмбриональные ткани (которые приводят к плацента и другие ткани, поддерживающие эмбрион) сохраняют эту раннюю импринтированную инактивацию, и, таким образом, в этих тканях активна только материнская Х-хромосома.
Рано бластоциста, эта начальная импринтированная инактивация X обращена в клетках внутренняя клеточная масса (которые дают начало эмбриону), и в этих клетках обе Х-хромосомы снова становятся активными. Затем каждая из этих клеток независимо и случайным образом инактивирует одну копию Х-хромосомы.[5] Это событие инактивации необратимо в течение всей жизни человека, за исключением зародышевой линии. В женском зародышевый перед вступлением в мейоз происходит обратная инактивация X, так что после мейоза все гаплоидные ооциты содержат одну активную Х-хромосому.
Обзор
В Си отмечает неактивное, Ха активная Х-хромосома. Иксп обозначает отцовский, а ИксM обозначает материнскую Х-хромосому. Когда яйцо (несущее ИксM), оплодотворяется спермой (несущей Y или Иксп) образуется диплоидная зигота. От зиготы до взрослой стадии и до следующего поколения яиц Х-хромосома претерпевает следующие изменения:
- Сип СиM зигота → проходит активация зиготического генома, ведущие к:
- Хап ХаM → прохождение отпечатанный (по отцовской линии) X-инактивация, ведущие к:
- Сип ХаM → прохождение X-активация рано бластоциста этап, ведущий к:
- Хап ХаM → прохождение случайная X-инактивация в эмбриональной линии (внутренней клеточной массе) на стадии бластоцисты, что приводит к:
- Сип ХаM ИЛИ Хап СиM → прохождение X-реактивация в первичные половые клетки перед мейоз, ведущие к:
- ХаM Хап диплоидные половые клетки в остановке мейоза. Поскольку мейоз я завершаю только с овуляция, половые клетки человека существуют на этой стадии от первых недель развития до полового созревания. Завершение мейоза приводит к:
- ХаM И Хап гаплоидные половые клетки (яйца).
Цикл активации X лучше всего изучен на мышах, но есть множество исследований на людях. Поскольку большая часть доказательств поступает от мышей, приведенная выше схема представляет события у мышей. Завершение мейоза здесь упрощено для ясности. Шаги 1–4 можно изучить на эмбрионах, оплодотворенных in vitro, и на дифференцирующихся стволовых клетках; Х-реактивация происходит в развивающемся эмбрионе и последующие (6–7) шаги внутри женского тела, поэтому изучать ее гораздо сложнее.
Время
Время каждого процесса зависит от вида, и во многих случаях точное время активно обсуждается. [Целая часть времени появления Х-инактивации у человека в этой таблице весьма сомнительна и должна быть удалена, пока не будет должным образом подтверждено эмпирическими данными]
| Обработать | Мышь | Человек | |
| 1 | Активация зиготического генома | 2–4 клеточная стадия[7] | 2–8 клеточная стадия[7] |
| 2 | Отпечатанная (отцовская) Х-инактивация | 4–8 клеточная стадия[6][8] | Неясно, имеет ли это место у людей[9] |
| 3 | X-активация | Ранняя стадия бластоцисты | Ранняя стадия бластоцисты |
| 4 | Случайная X-инактивация в эмбриональном клоне (внутренняя клеточная масса) | Поздняя стадия бластоцисты | Поздняя стадия бластоцисты, после имплантации[9] |
| 5 | Х-реактивация в первичных половых клетках перед мейозом | С 4-й недели до 14-й недели развития[10][11] |
Наследование статуса инактивации между поколениями клеток
Потомки каждой клетки, которая инактивировала определенную Х-хромосому, также инактивирует ту же самую хромосому. Это явление, которое можно наблюдать при окраске черепаховые кошки когда женщины гетерозиготный для Х-сцепленный ген, не следует путать с мозаика, который конкретно относится к различиям в генотип различных популяций клеток у одного и того же человека; X-инактивация, которая эпигенетический изменение, которое приводит к другому фенотипу, не изменение в генотипический уровень. Следовательно, для отдельной клетки или линии инактивация перекошенный или же 'не случайно ', и это может вызвать легкие симптомы у женщин-носительниц Х-связанный генетические нарушения.[12]
Выбор одной активной Х-хромосомы
Нормальные женщины обладают двумя X-хромосомами, и в любой данной клетке одна хромосома будет активной (обозначена как Xa), а другая - неактивной (Xi). Однако исследования людей с дополнительные копии Х-хромосомы показывают, что в клетках с более чем двумя Х-хромосомами остается только один Ха, а все остальные Х-хромосомы инактивированы. Это указывает на то, что состояние Х-хромосомы по умолчанию у женщин - инактивация, но всегда выбирается одна Х-хромосома, чтобы оставаться активной.
Понятно, что инактивация Х-хромосомы - это случайный процесс, происходящий примерно во время гаструляция в эпибласт (клетки, которые дадут начало эмбриону). Материнские и отцовские Х-хромосомы имеют равную вероятность инактивации. Это предполагает, что женщины будут страдать от Х-хромосом примерно на 50% чаще, чем мужчины (потому что у женщин две Х-хромосомы, а у мужчин только одна); однако в действительности встречаемость этих расстройств у женщин намного ниже. Одно из объяснений этого несоответствия заключается в том, что 12–20% [13] генов на инактивированной Х-хромосоме остаются экспрессированными, что обеспечивает женщинам дополнительную защиту от дефектных генов, кодируемых Х-хромосомой. Немного[кто? ] предполагают, что это несоответствие должно свидетельствовать о предпочтительной (неслучайной) инактивации. Преимущественная инактивация отцовской Х-хромосомы происходит как у сумчатых, так и в клеточных линиях, образующих мембраны, окружающие эмбрион,[14] тогда как у плацентарных млекопитающих X-хромосома материнского или отцовского происхождения может быть инактивирована в разных клеточных линиях.[15]
Период времени для инактивации Х-хромосомы объясняет это несоответствие. Инактивация происходит в эпибласте во время гаструляции, которая дает зародыш.[16] Инактивация происходит на клеточном уровне, что приводит к мозаичной экспрессии, при которой участки клеток имеют неактивную материнскую X-хромосому, в то время как другие участки имеют неактивную отцовскую X-хромосому. Например, женщина, гетерозиготная по гемофилии (Х-сцепленное заболевание), будет иметь примерно половину клеток печени, функционирующих должным образом, чего обычно достаточно для обеспечения нормального свертывания крови.[17][18] Шанс может привести к значительно большему количеству дисфункциональных клеток; однако такие статистические крайности маловероятны. Генетические различия в хромосоме также могут повысить вероятность инактивации одной Х-хромосомы. Кроме того, если одна X-хромосома имеет мутацию, препятствующую ее росту или делающую ее нежизнеспособной, клетки, которые случайным образом инактивировали эту X, будут иметь избирательное преимущество перед клетками, которые случайным образом инактивировали нормальный аллель. Таким образом, хотя инактивация изначально является случайной, клетки, которые инактивируют нормальный аллель (оставляя мутированный аллель активным), в конечном итоге перерастают и заменяются функционально нормальными клетками, в которых почти все имеют активированную Х-хромосому.[17]
Предполагается[кем? ] что существует аутосомно-кодируемый «блокирующий фактор», который связывается с Х-хромосомой и предотвращает ее инактивацию. Модель постулирует, что существует ограничивающий блокирующий фактор, поэтому, как только доступная молекула блокирующего фактора связывается с одной Х-хромосомой, оставшаяся Х-хромосома (-ы) не защищены от инактивации. Эта модель подтверждается существованием одного Ха в клетках со многими Х-хромосомами и наличием двух активных Х-хромосом в клеточных линиях с вдвое большим количеством аутосом.[19]
Последовательности на X центр инактивации (XIC), присутствующие на Х-хромосоме, контролируют подавление Х-хромосомы. Предполагается, что гипотетический фактор блокировки будет связываться с последовательностями в XIC.
Выражение Х-сцепленных нарушений у гетерозиготных женщин
Эффект гетерозиготности самок по X проявляется в некоторых локализованных признаках, таких как уникальный рисунок шерсти ситцевой кошки. Однако может быть труднее полностью понять проявление нелокализованных признаков у этих женщин, таких как проявление болезни.
Поскольку у мужчин есть только одна копия Х-хромосомы, все экспрессированные Х-хромосомы гены (или аллели в случае множественных вариантов форм для данного гена в популяции) расположены на этой копии хромосомы. Однако самки в первую очередь будут экспрессировать гены или аллели, расположенные на копии Х-хромосомы, которая остается активной. Рассмотрение ситуации для одного гена или нескольких генов, вызывающих индивидуальные различия в конкретных фенотип (т.е. вызывая вариации, наблюдаемые в популяции для этого фенотипа), у гомозиготных женщин не имеет особого значения, какая копия хромосомы инактивирована, поскольку аллели обеих копий одинаковы. Однако у женщин, гетерозиготных по причинным генам, инактивация одной копии хромосомы по сравнению с другой может иметь прямое влияние на их фенотипическую ценность. Из-за этого явления наблюдается увеличение фенотипической изменчивости у самок, гетерозиготных по задействованному гену или генам, чем у самок, гомозиготных по этому или этим генам.[20] Фенотипические вариации могут проявляться разными способами. Во многих случаях гетерозиготные самки могут протекать бессимптомно или иметь лишь незначительные симптомы данного заболевания, такие как Х-сцепленная адренолейкодистрофия.[21]
Дифференциации фенотипа у гетерозиготных самок способствует наличие асимметрии инактивации X. Обычно каждая Х-хромосома заглушается в половине клеток, но этот процесс искажается, когда происходит предпочтительная инактивация хромосомы. Считается, что перекос происходит либо случайно, либо из-за физической характеристики хромосомы, которая может заставить ее замолчать более или менее часто, например, из-за неблагоприятной мутации.[22][23]
В среднем каждая Х-хромосома инактивирована в половине клеток, однако у 5-20% «явно нормальных» женщин наблюдается перекос в отношении инактивации Х-хромосомы.[22] В случаях, когда присутствует перекос, может возникать широкий диапазон проявления симптомов, в результате чего выражение варьируется от незначительного до тяжелого в зависимости от пропорции перекоса. Крайний случай этого был замечен, когда у монозиготных близнецов женского пола были крайние различия в выражении Болезнь Менкеса (Х-сцепленное заболевание), приведшее к смерти одного близнеца, в то время как другой оставался бессимптомным.[24]
Считается, что перекос X-инактивации может быть вызван проблемами в механизме, вызывающем инактивацию, или проблемами в самой хромосоме.[22][23] Однако связь между фенотипом и перекосом все еще ставится под сомнение, и ее следует исследовать в каждом конкретном случае. Исследование, в котором изучались женщины с симптомами и бессимптомно, гетерозиготные по Дюшенн и мышечные дистрофии Беккера (DMD) не обнаружили очевидной связи между экспрессией транскрипта и искаженной X-инактивацией. Исследование предполагает, что оба механизма регулируются независимо, и есть другие неизвестные факторы.[25]
Хромосомный компонент
Центр инактивации X (или просто XIC) на X-хромосоме - это необходимо и достаточно вызвать X-инактивацию. Хромосомные транслокации которые помещают XIC на аутосому, приводят к инактивации аутосомы, а X-хромосомы, лишенные XIC, не инактивируются.[26][27]
XIC содержит четыре не-переведено РНК гены Xist, Tsix, Jpx и Ftx, которые участвуют в X-инактивации. XIC также содержит сайты связывания как для известных, так и для неизвестных регуляторные белки.[28]
Xist и Tsix РНК
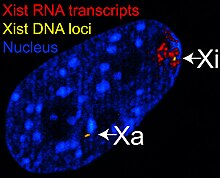
X-неактивный специфический транскрипт (Xist ) ген кодирует большой некодирующая РНК который отвечает за специфическое молчание Х-хромосомы, с которой он транскрибируется.[29] Неактивная Х-хромосома покрыта РНК Xist,[30] тогда как Xa - нет (см. рисунок справа). Х-хромосомы, в которых отсутствует ген Xist, не могут быть инактивированы.[31] Искусственное размещение и экспрессия гена Xist на другой хромосоме приводит к подавлению этой хромосомы.[32][26]
До инактивации обе Х-хромосомы слабо экспрессируют РНК Xist из гена Xist. Во время процесса инактивации будущий Ха перестает экспрессировать Xist, тогда как будущий Xi резко увеличивает продукцию РНК Xist. В будущем Xi РНК Xist постепенно покрывает хромосому, распространяясь из XIC;[32] РНК Xist не локализуется в Xa. В молчание генов вдоль Xi происходит вскоре после покрытия Xist РНК.
Как и Xist, Tsix Ген кодирует большую РНК, которая, как считается, не кодирует белок. РНК Tsix транскрибируется антисмысловой к Xist, что означает, что ген Tsix перекрывает ген Xist и является записано на противоположной стороне ДНК от гена Xist.[27] Tsix - негативный регулятор Xist; Х-хромосомы, лишенные экспрессии Tsix (и, следовательно, имеющие высокий уровень транскрипции Xist), инактивируются гораздо чаще, чем нормальные хромосомы.
Как и Xist, до инактивации обе Х-хромосомы слабо экспрессируют Tsix РНК из гена Tsix. После начала X-инактивации будущий Xi перестает экспрессировать Tsix РНК (и увеличивает экспрессию Xist), тогда как Xa продолжает экспрессировать Tsix в течение нескольких дней.
Rep A - это длинная некодирующая РНК, которая работает с другой длинной некодирующей РНК, Xist, для инактивации X. Rep A подавляет функцию Tsix, антисмысловую функцию Xist, в сочетании с устранением экспрессии Xite. Он способствует метилированию области Tsix, привлекая PRC2 и, таким образом, инактивируя одну из Х-хромосом.[28]
Отключение звука
Неактивная Х-хромосома не экспрессирует большинство своих генов, в отличие от активной Х-хромосомы. Это происходит из-за того, что Си заставляет замолчать репрессивные гетерохроматин, который уплотняет ДНК Xi и предотвращает экспрессию большинства генов.
По сравнению с Xa, Xi имеет высокий уровень Метилирование ДНК, низкий уровень ацетилирование гистонов, низкий уровень гистон H3 лизин-4 метилирование, а также высокие уровни метилирования лизина-9 гистона H3 и метки метилирования лизина-27 H3, которая помещается Комплекс PRC2 рекрутирован Xist, все из которых связаны с подавлением генов.[33] PRC2 регулирует хроматин уплотнение и ремоделирование хроматина в нескольких процессах, включая Повреждение ДНК отклик.[34] Кроме того, вариант гистона, называемый macroH2A (H2AFY ) находится исключительно на нуклеосомы вдоль Си.[35][36]
Тела Барра
ДНК, упакованная в гетерохроматин, например Xi, более конденсирована, чем ДНК, упакованная в эухроматин, например Xa. Неактивный X образует дискретное тело внутри ядра, называемое Тело Барра.[37] Корпус Барра обычно располагается на периферии ядро, поздно копирование в пределах клеточный цикл, и, поскольку он содержит Xi, содержит модификации гетерохроматина и РНК Xist.
Экспрессированные гены на неактивной Х-хромосоме
Часть генов вдоль X-хромосомы избегает инактивации на Xi. Ген Xist экспрессируется на высоком уровне на Xi и не экспрессируется на Xa.[38] Многие другие гены избегают инактивации; некоторые экспрессируются одинаково из Xa и Xi, а другие, хотя и экспрессируются из обеих хромосом, все еще преимущественно экспрессируются из Xa.[39][40][41] До четверти генов Xi человека способны к побегу.[39] Исследования на мышах показывают, что в любом данном типе клеток от 3% до 15% генов избегают инактивации, и что идентичность этих генов варьируется в зависимости от ткани.[40][41]
Многие из генов, которые избегают инактивации, присутствуют в областях Х-хромосомы, которые, в отличие от большинства Х-хромосомы, содержат гены, также присутствующие на Y-хромосома. Эти регионы называются псевдоавтосомальный регионов, поскольку люди любого пола получат по две копии каждого гена в этих регионах (например, аутосома), в отличие от большинства генов, расположенных вдоль половых хромосом. Поскольку люди любого пола получат по две копии каждого гена в псевдоавтосомальная область доза компенсации не требуется для самок, поэтому постулируется, что эти области ДНК развили механизмы, чтобы избежать X-инактивации. Гены псевдоавтосомных областей Xi не имеют типичных модификаций Xi и мало связаны с Xist РНК.
Существование генов вдоль неактивной X-хромосомы, которые не заглушаются, объясняет дефекты у людей с аномальным числом X-хромосомы, такие как Синдром Тернера (X0) или Синдром Клайнфельтера (XXY). Теоретически X-инактивация должна устранить различия в дозировке генов между пораженными людьми и людьми с нормальным набором хромосом. У пораженных людей, однако, X-инактивация является неполной, и дозировка этих генов, не вызывающих молчания, будет отличаться, поскольку они избегают X-инактивации, аналогично аутосомной. анеуплоидия.
Точные механизмы, которые контролируют ускользание от X-инактивации, неизвестны, но было показано, что области молчания и ускользания имеют различные метки хроматина.[40][42] Было высказано предположение, что уход от X-инактивации может быть опосредован экспрессией длинная некодирующая РНК (днРНК) в убегающих хромосомных доменах.[2]
Использование в экспериментальной биологии
Стэнли Майкл Гартлер использовали инактивацию Х-хромосомы, чтобы продемонстрировать клональное происхождение рака. Исследование нормальных тканей и опухолей гетерозиготных женщин на изоферменты сцепленных с полом G6PD ген продемонстрировал, что опухолевые клетки от таких индивидуумов экспрессируют только одну форму G6PD, тогда как нормальные ткани состоят из почти равной смеси клеток, экспрессирующих два разных фенотипа. Эта модель предполагает, что одна клетка, а не популяция, перерастает в рак.[43] Однако было доказано, что этот образец неверен для многих типов рака, предполагая, что некоторые виды рака могут иметь поликлональное происхождение.[44]
Кроме того, измерение статуса метилирования (инактивации) полиморфного рецептора андрогенов человека (HUMARA), расположенного на X-хромосоме, считается наиболее точным методом оценки клональности в биопсиях женского рака.[45] С помощью этого метода было исследовано большое количество опухолей, некоторые, например, почечно-клеточный рак,[46] обнаружены моноклональные, в то время как другие (например, мезотелиома[47]) были зарегистрированы поликлональные.
Исследователи также исследовали использование инактивации Х-хромосомы для подавления активности аутосомных хромосом. Например, Цзян и другие. вставил копию гена Xist в одну копию хромосомы 21 в стволовые клетки получен от человека с трисомией 21 (Синдром Дауна ).[48] Вставленный ген Xist индуцирует формирование тельца Барра, запускает стабильные модификации гетерохроматина и подавляет большинство генов в дополнительной копии хромосомы 21. В этих модифицированных стволовых клетках подавление опосредованного Xist гена, по-видимому, устраняет некоторые из дефектов, связанных с Down синдром.
История
В 1959 г. Сусуму Оно показали, что две X-хромосомы млекопитающих были разными: одна оказалась похожей на аутосомы; другой был конденсированным и гетерохроматическим.[49] Это открытие показало, независимо от двух групп исследователей, что одна из Х-хромосом подверглась инактивации.
В 1961 г. Мэри Лайон предложил случайную инактивацию одной женской Х-хромосомы для объяснения пятнистого фенотипа самок мышей гетерозиготный для цвета шерсти гены.[50] Гипотеза Лиона также учитывала открытия, что одна копия Х-хромосомы в женских клетках была сильно конденсированной, и что мыши только с одной копией Х-хромосомы развивались как бесплодные самки. Это предполагало[51] к Эрнест Бейтлер, изучая гетерозиготных самок на предмет глюкозо-6-фосфатдегидрогеназа (G6PD), что в таких гетерозиготах присутствовали две популяции эритроцитов эритроцитов: дефектные клетки и нормальные клетки,[52] в зависимости от того, содержит ли инактивированная Х-хромосома (в ядре клетки-предшественника эритроцитов) нормальный или дефектный аллель G6PD.
Смотрите также
- Система определения пола
- Компенсация дозировки
- Тело Барра
- Гетерохроматин
- Эпигенетика
- Искаженная X-инактивация
- Расстройства развития, которые, как считается, связаны с X-инактивацией:
использованная литература
- ^ Гартлер С.М., Варадараджан К.Р., Луо П., Кэнфилд Т.К., Трейнор Дж., Франк Ю., Хансен Р.С. (сентябрь 2004 г.). «Нормальные модификации гистонов на неактивной Х-хромосоме в клетках ICF и синдрома Ретта: последствия для белков, связывающих метил-CpG». BMC Биология. 2: 21. Дои:10.1186/1741-7007-2-21. ЧВК 521681. PMID 15377381.
- ^ а б Рейниус Б., Ши С., Хэншо Л., Сандху К.С., Радомска К.Дж., Розен Г.Д., Лу Л., Кулландер К., Уильямс Р.В., Джазин Э. (ноябрь 2010 г.). «Смещенная к самкам экспрессия длинных некодирующих РНК в доменах, которые избегают X-инактивации у мышей». BMC Genomics. 11: 614. Дои:10.1186/1471-2164-11-614. ЧВК 3091755. PMID 21047393.
- ^ Такаги Н., Сасаки М. (август 1975 г.). «Предпочтительная инактивация отцовской Х-хромосомы во внеэмбриональных мембранах мыши». Природа. 256 (5519): 640–2. Bibcode:1975Натура.256..640Т. Дои:10.1038 / 256640a0. PMID 1152998.
- ^ Cheng MK, Disteche CM (август 2004 г.). «Молчание отцов: ранняя инактивация Х». BioEssays. 26 (8): 821–4. Дои:10.1002 / bies.20082. PMID 15273983.[мертвая ссылка ]
- ^ а б Окамото И., Отте А.П., Аллис С.Д., Рейнберг Д., Херд Э (январь 2004 г.). «Эпигенетическая динамика импринтированной инактивации X во время раннего развития мышей». Наука. 303 (5658): 644–9. Bibcode:2004Наука ... 303..644O. Дои:10.1126 / science.1092727. PMID 14671313.
- ^ а б Дэн К., Рамскельд Д., Рейниус Б., Сандберг Р. (январь 2014 г.). «Single-cell RNA-seq обнаруживает динамическую, случайную экспрессию моноаллельного гена в клетках млекопитающих». Наука. 343 (6167): 193–6. Bibcode:2014Наука ... 343..193D. Дои:10.1126 / science.1245316. PMID 24408435.
- ^ а б Сюэ З., Хуан К., Цай Ц., Цай Л., Цзян Ц.Й., Фэн И, Лю Цз., Цзэн Ц., Ченг Л., Сунь Й.Е., Лю Ц. Ю., Хорват С., Фан Г (август 2013 г.). «Генетические программы ранних эмбрионов человека и мыши, выявленные с помощью секвенирования одноклеточной РНК». Природа. 500 (7464): 593–7. Bibcode:2013Натура.500..593X. Дои:10.1038 / природа12364. ЧВК 4950944. PMID 23892778.
- ^ Боренштейн М., Сикс Л., Анселин К., Диабангуая П., Пикард С., Лю Т., Лян Дж. Б., Василев И., Галупа Р., Слуга Н., Бариллот Е., Сурани А., Чен С. Дж., Херд Э (март 2017 г.). «Xist-зависимая импринтированная инактивация X и последствия его отказа на раннем этапе развития». Структурная и молекулярная биология природы. 24 (3): 226–233. Дои:10.1038 / nsmb.3365. ЧВК 5337400. PMID 28134930.
- ^ а б Дэн Х, Берлетч Дж. Б., Нгуен Д. К., Disteche CM (июнь 2014 г.). «Регуляция Х-хромосомы: различные паттерны в развитии, тканях и заболеваниях». Обзоры природы. Генетика. 15 (6): 367–78. Дои:10.1038 / nrg3687. ЧВК 4117651. PMID 24733023.
- ^ Вертези Б, Ариндрарто В., Руст М.С., Рейниус Б., Торренс-Хуанеда В., Бялецкая М. и др. (Май 2018). «Родительские гаплотип-специфичные одноклеточные транскриптомики выявляют неполное эпигенетическое репрограммирование в женских половых клетках человека». Nature Communications. 9 (1): 1873. Bibcode:2018НатКо ... 9,1873V. Дои:10.1038 / s41467-018-04215-7. ЧВК 5951918. PMID 29760424.
- ^ Guo F, Yan L, Guo H, Li L, Hu B, Zhao Y и др. (Июнь 2015 г.). «Транскриптом и пейзажи ДНК-метилома первичных зародышевых клеток человека». Ячейка. 161 (6): 1437–52. Дои:10.1016 / j.cell.2015.05.015. PMID 26046443.
- ^ Пак Дж. М., Уиллард Х. Ф. (январь 1998 г.). «Инактивация Х у женщин с Х-сцепленным заболеванием». Медицинский журнал Новой Англии. 338 (5): 325–8. Дои:10.1056 / NEJM199801293380611. PMID 9445416.
- ^ Балатон Б.П., Коттон А.М., Браун С.Дж. (30 декабря 2015 г.). «Получение консенсусного статуса инактивации для X-сцепленных генов из полногеномных исследований». Биология половых различий. 6 (35): 35. Дои:10.1186 / s13293-015-0053-7. ЧВК 4696107. PMID 26719789.
- ^ Грейвс JA (1996). «Млекопитающие, нарушающие правила: генетика сумчатых и одноплодных». Ежегодный обзор генетики. 30: 233–60. Дои:10.1146 / annurev.genet.30.1.233. PMID 8982455.
- ^ Lyon MF (январь 1972 г.). «Инактивация Х-хромосомы и паттерны развития у млекопитающих». Биологические обзоры Кембриджского философского общества. 47 (1): 1–35. Дои:10.1111 / j.1469-185X.1972.tb00969.x. PMID 4554151.
- ^ Мигеон, Б. (2010). «Инактивация Х-хромосомы в клетках человека». Коллекция биомедицины и наук о жизни. Генри Стюарт Тэлкс, Лтд., Стр. 1–54.. Получено 15 декабря 2013.
- ^ а б Гартлер С.М., Гольдман М.А. (2001). «Инактивация Х-хромосомы» (PDF). Энциклопедия наук о жизни. Издательская группа «Природа»: 1–2.
- ^ Connallon T, Clark AG (апрель 2013 г.). «Дифференциальный по полу отбор и эволюция стратегий инактивации X». PLOS Genetics. 9 (4): e1003440. Дои:10.1371 / journal.pgen.1003440. ЧВК 3630082. PMID 23637618.
- ^ Баракат Т.С., Грибнау Ж (2010). «Инактивация Х-хромосомы и эмбриональные стволовые клетки». В Meshorer E, Plath K (ред.). Клеточная биология стволовых клеток. Landes Bioscience и Springer Science + Business Media.
- ^ Ма Л., Хоффман Г., Кейнан А. (март 2015 г.). «X-инактивация дает информацию о тестировании на основе дисперсии для определения X-связанной ассоциации количественного признака». BMC Genomics. 16: 241. Дои:10.1186 / s12864-015-1463-у. ЧВК 4381508. PMID 25880738.
- ^ Habekost CT, Pereira FS, Vargas CR, Coelho DM, Torrez V, Oses JP, Portela LV, Schestatsky P, Felix VT, Matte U, Torman VL, Jardim LB (октябрь 2015 г.). «Скорость прогрессирования миелопатии у гетерозигот с X-сцепленной адренолейкодистрофией». Метаболическое заболевание мозга. 30 (5): 1279–84. Дои:10.1007 / s11011-015-9672-2. PMID 25920484.
- ^ а б c Бельмонт JW (июнь 1996 г.). «Генетический контроль инактивации X и процессы, приводящие к искажению X-инактивации». Американский журнал генетики человека. 58 (6): 1101–8. ЧВК 1915050. PMID 8651285.
- ^ а б Холле Дж. Р., Марш Р. А., Холдкрофт А. М., Дэвис С. М., Ван Л., Чжан К., Джордан МБ (июль 2015 г.). «Гемофагоцитарный лимфогистиоцитоз у пациентки из-за гетерозиготной мутации XIAP и инактивации искаженной Х-хромосомы». Детская кровь и рак. 62 (7): 1288–90. Дои:10.1002 / pbc.25483. PMID 25801017.
- ^ Burgemeister AL, Zirn B, Oeffner F, Kaler SG, Lemm G, Rossier E, Büttel HM (ноябрь 2015 г.). «Болезнь Менкеса с дискордантным фенотипом у монозиготных близнецов женского пола». Американский журнал медицинской генетики. Часть А. 167A (11): 2826–9. Дои:10.1002 / ajmg.a.37276. ЧВК 6475897. PMID 26239182.
- ^ Бриоши С., Гуаланди Ф., Скоттон С., Армароли А., Боволента М., Фальзарано М. С., Сабателли П., Селватичи Р., Д'Амико А., Пане М., Риччи Дж., Сицилиано Г., Тедески С., Пини А., Верчелли Л., Де Грандис Д. , Меркури Е., Бертини Е., Мерлини Л., Монджини Т., Ферлини А. (август 2012 г.). «Генетическая характеристика у женщин с симптомами МДД: отсутствие связи между Х-инактивацией, транскрипционным балансом аллелей МДД и фенотипом». BMC Medical Genetics. 13: 73. Дои:10.1186/1471-2350-13-73. ЧВК 3459813. PMID 22894145.
- ^ а б Ли Дж. Т., Джениш Р. (март 1997 г.). "Дальние цис-эффекты эктопической X-инактивации центров на аутосоме мыши". Природа. 386 (6622): 275–9. Bibcode:1997 Натур.386..275L. Дои:10.1038 / 386275a0. PMID 9069285.
- ^ а б Ли Дж. Т., Дэвидоу Л. С., Варшавски Д. (апрель 1999 г.). «Tsix, ген, антисмысловой к Xist в центре инактивации X». Природа Генетика. 21 (4): 400–4. Дои:10.1038/7734. PMID 10192391.
- ^ а б Мерсер, Т.Р., Динджер, М.Э., Маттик, Дж. С. (2009). Длинные некодирующие РНК: понимание функций. Природа Обзоры Генетики. (10) 155–159.
- ^ Хоки Ю., Кимура Н., Канбаяси М., Амакава И., Охата Т., Сасаки Н., Садо Т. (январь 2009 г.). «Проксимальный консервативный повтор в гене Xist важен как геномный элемент для X-инактивации у мышей». Развитие. 136 (1): 139–46. Дои:10.1242 / dev.026427. PMID 19036803.
- ^ Нг К., Пуллирш Д., Либ М., Вутц А. (январь 2007 г.). «Xist и порядок замалчивания» (Обзорная статья). EMBO отчеты. 8 (1): 34–9. Дои:10.1038 / sj.embor.7400871. ЧВК 1796754. PMID 17203100.
Рис. 1. РНК Xist охватывает X, с которого она транскрибируется.
- ^ Пенни Г.Д., Кей Г.Ф., Ширдаун С.А., Растан С., Брокдорф Н (1996). «Требование Xist в инактивации Х-хромосомы». Природа. 379 (6561): 131–7. Bibcode:1996Натура 379..131П. Дои:10.1038 / 379131a0. PMID 8538762.
- ^ а б Герцинг Л. Б., Ромер Дж. Т., Хорн Дж. М., Эшворт А. (март 1997 г.). «Xist обладает свойствами центра инактивации Х-хромосомы». Природа. 386 (6622): 272–5. Bibcode:1997Натура.386..272H. Дои:10.1038 / 386272a0. PMID 9069284.
- ^ Нг К., Пуллирш Д., Либ М., Вутц А. (январь 2007 г.). «Xist и порядок замалчивания» (Обзорная статья). EMBO отчеты. 8 (1): 34–9. Дои:10.1038 / sj.embor.7400871. ЧВК 1796754. PMID 17203100.
Таблица 1 Особенности неактивной X-территории
- Возник из;
Чоу Дж. К., Йен З., Зиеше С. М., Браун Си Джей (2005). «Молчание Х-хромосомы млекопитающих». Ежегодный обзор геномики и генетики человека. 6: 69–92. Дои:10.1146 / annurev.genom.6.080604.162350. PMID 16124854.
Луччези Дж. К., Келли В. Г., Паннинг Б. (2005). «Ремоделирование хроматина при дозовой компенсации». Ежегодный обзор генетики. 39: 615–51. CiteSeerX 10.1.1.328.2992. Дои:10.1146 / annurev.genet.39.073003.094210. PMID 16285873. - ^ Veneti Z, Gkouskou KK, Eliopoulos AG (июль 2017 г.). «Репрессорный комплекс Polycomb 2 при геномной нестабильности и раке». Int J Mol Sci. 18 (8): 1657. Дои:10.3390 / ijms18081657. ЧВК 5578047. PMID 28758948.
- ^ Костанци С., Пирсон Дж. Р. (июнь 1998 г.). «Гистон macroH2A1 сконцентрирован в неактивной Х-хромосоме самок млекопитающих». Природа. 393 (6685): 599–601. Bibcode:1998Натура.393..599C. Дои:10.1038/31275. PMID 9634239.
- ^ Костанци К., Штейн П., Уоррад Д.М., Шульц Р.М., Персон Дж. Р. (июнь 2000 г.). «Гистон macroH2A1 сконцентрирован в неактивной Х-хромосоме самок доимплантационных эмбрионов мыши» (PDF). Развитие. 127 (11): 2283–9. PMID 10804171.
- ^ Барр М.Л., Бертрам Э.Г. (апрель 1949 г.). «Морфологические различия между нейронами мужского и женского пола и поведение ядрышкового сателлита во время ускоренного синтеза нуклеопротеидов». Природа. 163 (4148): 676–677. Bibcode:1949 г.Натура.163..676Б. Дои:10.1038 / 163676a0. PMID 18120749.
- ^ Плат К., Млынарчик-Эванс С., Нусинов Д.А., Паннинг Б. (2002). «Xist РНК и механизм инактивации Х-хромосомы». Ежегодный обзор генетики. 36: 233–78. Дои:10.1146 / annurev.genet.36.042902.092433. PMID 12429693.
- ^ а б Каррел Л., Уиллард Х. Ф. (март 2005 г.). «Профиль X-инактивации показывает обширную вариабельность экспрессии X-сцепленного гена у женщин». Природа. 434 (7031): 400–4. Bibcode:2005Натура.434..400С. Дои:10.1038 / природа03479. PMID 15772666.
- ^ а б c Calabrese JM, Sun W, Song L, Mugford JW, Williams L, Yee D, Starmer J, Mieczkowski P, Crawford GE, Magnuson T (ноябрь 2012 г.). «Сайт-специфическое молчание регуляторных элементов как механизм инактивации X». Ячейка. 151 (5): 951–63. Дои:10.1016 / j.cell.2012.10.037. ЧВК 3511858. PMID 23178118.
- ^ а б Ян Ф, Бабак Т., Шендурэ Дж., Disteche CM (май 2010 г.). «Глобальный обзор побега от инактивации X путем секвенирования РНК у мышей». Геномные исследования. 20 (5): 614–22. Дои:10.1101 / гр.103200.109. ЧВК 2860163. PMID 20363980.
- ^ Берлетч Дж. Б., Ян Ф, Disteche CM (июнь 2010 г.). «Спасение от инактивации X у мышей и людей». Геномная биология. 11 (6): 213. Дои:10.1186 / gb-2010-11-6-213. ЧВК 2911101. PMID 20573260.
- ^ Линдер Д., Гартлер С.М. (октябрь 1965 г.). «Мозаицизм глюкозо-6-фосфатдегидрогеназы: использование в качестве клеточного маркера при изучении лейомиом». Наука. 150 (3692): 67–9. Bibcode:1965Научный ... 150 ... 67Л. Дои:10.1126 / science.150.3692.67. PMID 5833538.
- ^ Парсонс Б.Л. (2008). «Многие различные типы опухолей имеют поликлональное опухолевое происхождение: доказательства и последствия». Мутационные исследования. 659 (3): 232–47. Дои:10.1016 / j.mrrev.2008.05.004. PMID 18614394.
- ^ Чен Г.Л., Прчал Дж. Т. (сентябрь 2007 г.). «Тестирование X-связанной клональности: интерпретация и ограничения». Кровь. 110 (5): 1411–9. Дои:10.1182 / кровь-2006-09-018655. ЧВК 1975831. PMID 17435115.
- ^ Петерсон Ф., Бранзовский Дж., Мартинек П., Корабекна М., Круслин Б., Хора М. и др. (Июль 2014 г.). «Лейомиоматозная строма почечно-клеточного рака является поликлональной и не является частью неопластического процесса». Вирховский архив. 465 (1): 89–96. Дои:10.1007 / s00428-014-1591-9. PMID 24838683.
- ^ Comertpay S, Pastorino S, Tanji M, Mezzapelle R, Strianese O, Napolitano A, Baumann F, Weigel T, Friedberg J, Sugarbaker P, Krausz T, Wang E, Powers A, Gaudino G, Kanodia S, Pass HI, Parsons BL , Ян Х, Карбон М (декабрь 2014 г.). «Оценка клонального происхождения злокачественной мезотелиомы». Журнал трансляционной медицины. 12: 301. Дои:10.1186 / s12967-014-0301-3. ЧВК 4255423. PMID 25471750.
- ^ Jiang J, Jing Y, Cost GJ, Chiang JC, Kolpa HJ, Cotton AM и др. (Август 2013). «Перевод дозовой компенсации на трисомию 21». Природа. 500 (7462): 296–300. Bibcode:2013Натура.500..296J. Дои:10.1038 / природа12394. ЧВК 3848249. PMID 23863942.
- ^ Оно С., Каплан В. Д., Киносита Р. (октябрь 1959 г.). «Формирование полового хроматина одной Х-хромосомой в клетках печени Rattus norvegicus». Экспериментальные исследования клеток. 18 (2): 415–8. Дои:10.1016 / 0014-4827 (59) 90031-X. PMID 14428474.
- ^ Lyon MF (апрель 1961 г.). «Действие генов в Х-хромосоме мыши (Mus musculus L.)». Природа. 190 (4773): 372–3. Bibcode:1961Натура.190..372L. Дои:10.1038 / 190372a0. PMID 13764598.
- ^ Beutler E (январь 2008 г.). «Дефицит глюкозо-6-фосфатдегидрогеназы: историческая перспектива». Кровь. 111 (1): 16–24. Дои:10.1182 / кровь-2007-04-077412. PMID 18156501.
- ^ Beutler E, Yeh M, Fairbanks VF (январь 1962 г.). «Нормальная человеческая женщина как мозаика активности Х-хромосомы: исследования с использованием гена дефицита C-6-PD в качестве маркера». Труды Национальной академии наук Соединенных Штатов Америки. 48 (1): 9–16. Bibcode:1962ПНАС ... 48 .... 9Б. Дои:10.1073 / pnas.48.1.9. ЧВК 285481. PMID 13868717.
дальнейшее чтение
- Huynh KD, Lee JT (май 2005 г.). «Инактивация Х-хромосомы: гипотеза, связывающая онтогенез и филогению». Обзоры природы. Генетика. 6 (5): 410–8. Дои:10.1038 / nrg1604. PMID 15818384.
- Гото Т., Монах М. (июнь 1998 г.). «Регулирование инактивации Х-хромосомы в развитии у мышей и людей» (Обзорная статья). Обзоры микробиологии и молекулярной биологии. 62 (2): 362–78. Дои:10.1128 / MMBR.62.2.362-378.1998. ЧВК 98919. PMID 9618446.
- Lyon MF (декабрь 2003 г.). «Лион и гипотеза ЛИНИИ». Семинары по клеточной биологии и биологии развития (Обзорная статья). 14 (6): 313–8. Дои:10.1016 / j.semcdb.2003.09.015. PMID 15015738.
- Нг К., Пуллирш Д., Либ М., Вутц А. (январь 2007 г.). «Xist и порядок замалчивания» (Обзорная статья). EMBO отчеты. 8 (1): 34–9. Дои:10.1038 / sj.embor.7400871. ЧВК 1796754. PMID 17203100.
- Cerase A, Pintacuda G, Tattermusch A, Avner P (август 2015 г.). «Локализация и функции Xist: новые идеи с разных уровней». Геномная биология. 16: 166. Дои:10.1186 / s13059-015-0733-у. ЧВК 4539689. PMID 26282267.
внешние ссылки
 СМИ, связанные с Инактивация Х-хромосомы в Wikimedia Commons
СМИ, связанные с Инактивация Х-хромосомы в Wikimedia Commons- Крушельницкий К. (11.02.2004). "Гибридные аутоиммунные женщины 3". ABC Science.

