Эритропоэтическая протопорфирия - Erythropoietic protoporphyria
Эта статья требует внимания специалиста по патологии. (Март 2011 г.) |
| Эритропоэтическая протопорфирия | |
|---|---|
| Другие имена | EPP[1] |
 | |
| Хронические поражения кожи при ЭПП | |
| Специальность | Эндокринология, дерматология |
| Факторы риска | боль и раздражение |
Эритропоэтическая протопорфирия это форма порфирия, которые различаются по степени тяжести и могут быть очень болезненными. Возникает из-за дефицита фермента феррохелатаза, что приводит к аномально высокому уровню протопорфирин в красные кровяные тельца (эритроциты), плазма, кожа и печень.[2] Степень тяжести значительно варьируется от человека к человеку.
Клинически подобная форма порфирии, известная как доминантная протопорфирия, сцепленная с Х-хромосомой, была идентифицирована в 2008 году.[3]
Презентация
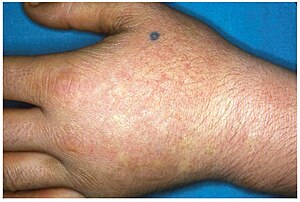
В детстве ПОП обычно проявляется острой светочувствительностью кожи. Он влияет на участки, подверженные воздействию солнца, и, как правило, трудно поддается лечению. Несколько минут пребывания на солнце вызывают кожный зуд, эритему, отек и боль. Более длительное воздействие может вызвать ожоги второй степени. После многократного воздействия у пациентов могут появиться лихенификация, гипопигментация, гиперпигментация и рубцевание кожи.[4][5]
ПОП обычно впервые проявляется в детстве и чаще всего поражает лицо, верхние поверхности рук, кистей и стоп, а также открытые поверхности ног. У большинства пациентов, если ПОП не такое серьезное, симптомы проявляются с наступлением половой зрелости, когда уровни мужских и женских гормонов повышаются во время полового развития и поддержания полового созревания. Более тяжелая форма ПОП может проявляться в младенчестве. EPP может быть вызван воздействием солнца, даже если пациент находится за стеклом. Известно, что даже УФ-излучение при дуговой сварке с использованием полной защитной маски вызывает EPP. ПОП также может проявляться в возрасте от 3 до 6 лет.
Продолжительное пребывание на солнце может привести к отеку рук, лица и ног, редко с образованием пузырей и петехий. Иногда со временем может произойти утолщение кожи.
Люди с ПОП также подвержены повышенному риску развития камни в желчном пузыре.[6] Одно исследование показало, что пациенты с ПОП страдают от дефицита витамина D.[7]
Отказ печени
Протопорфирин накапливается в печени до токсичных уровней у 5–20% пациентов с ПОП, что приводит к печеночной недостаточности. Спектр гепатобилиарной болезни, связанной с EPP, широк. Он включает холелитиаз, паренхиматозное заболевание печени легкой степени, прогрессирующее гепатоцеллюлярное заболевание и терминальное заболевание печени.[4]
Отсутствие диагностических маркеров печеночной недостаточности затрудняет прогнозирование того, у каких пациентов может развиться печеночная недостаточность, а механизм печеночной недостаточности плохо изучен. Ретроспективное европейское исследование выявило 31 пациента с эпилепсией, перенесших трансплантацию печени в период с 1983 по 2008 год, с фототоксическими реакциями у 25% пациентов, которые не были защищены хирургическими светофильтрами. В том же исследовании отмечено 69% рецидивов заболевания в трансплантированном органе. В период с 1987 по 2009 год в Великобритании было выявлено пять трансплантатов печени для лечения EPP. Пациентам с EPP рекомендуется частое тестирование печени, у которых на сегодняшний день не было выявлено эффективных методов лечения печеночной недостаточности.[нужна цитата ]
Беременность
Сообщается, что симптомы фоточувствительности к EPP уменьшаются у некоторых пациенток во время беременности и менструации, хотя это явление не является постоянным, и механизм не изучен.[8]
Генетика
Большинство случаев ПОП являются результатом врожденных нарушений обмена веществ.[2] но у некоторых пациентов метаболический дефект может быть приобретенным.[9] Мутация гена, кодирующего феррохелатазу в длинном плече хромосомы 18, обнаруживается в большинстве случаев. Феррохелатаза (FECH) катализирует внедрение двухвалентного железа в кольцо протопорфирина IX с образованием гема. EPP демонстрирует как рецессивные, так и доминантные паттерны наследования и высокую степень аллельной гетерогенности с неполной пенетрантностью. У большинства гетерозигот симптомы отсутствуют. Симптомы не возникают, если активность FECH составляет менее 30% от нормы, но такие низкие уровни отсутствуют у большинства пациентов.[10]
Патофизиология
Клетки, синтезирующие гем, представляют собой преимущественно эритробласты / ретикулоциты костного мозга (80%) и гепатоциты (20%). Дефицит FECH приводит к повышенному высвобождению протопорфирина, который связывается с альбумином в плазме и впоследствии подвергается печеночной экстракции. Обычно большая часть протопорфирина в гепатоцитах выделяется с желчью; остаток превращается в гем. Некоторое количество протопорфирина с желчью возвращается в печень в результате энтерогепатического кровообращения; оставшийся в кишечнике протопорфирин подвергается фекальной экскреции. Протопорфирин нерастворим и, следовательно, не выводится почками. При EPP субнормальная биотрансформация протопорфирина в гем приводит к накоплению протопорфирина в гепатоцитах.[11]
Поскольку дефицит FECH связан с повышенными концентрациями протопорфирина в эритроцитах, плазме, коже и печени, задержка протопорфирина в коже предрасполагает к острой фоточувствительности. В результате поглощения ультрафиолетового и видимого света (пиковая чувствительность при 400 нм, с меньшими пиками между 500-625 нм[12]) протопорфирином в плазме и эритроцитах, когда кровь циркулирует по сосудам дермы, образуются свободные радикалы, эритроциты становятся нестабильными и вызывается повреждение кожи.[4]
Значительное увеличение гепатобилиарной экскреции протопорфирина может привести к повреждению печени как из-за холестатических явлений, так и из-за окислительного стресса.[11] - предрасположенность к гепатобилиарным заболеваниям различной степени тяжести[13][14]
Диагностика
EPP обычно подозревается по наличию острой светочувствительности кожи и может быть подтвержден обнаружением пика плазменной флуоресценции при 634 нм. Также полезно обнаружить повышенный уровень протопорфирина в кале и демонстрацию избытка свободного протопорфирина в эритроцитах.[15]
Скрининг на FECH мутация на одном аллеле или мутация увеличения функции синтазы 2 аминолевулиновой кислоты у выбранных членов семьи могут быть полезны, особенно при генетическом консультировании.
Биопсия печени подтверждает заболевание печени при ПОП по наличию отложений протопорфирина в гепатоцитах, которые можно наблюдать в виде коричневого пигмента в желчных канальцах и портальных макрофагах. Макроскопически цирротическая печень может иметь черный цвет из-за отложений протопорфирина. Используя поляризованный свет, можно обнаружить характерную мальтийскую форму креста двулучепреломляющих кристаллических отложений пигмента. Исследование ткани печени под Лампа Вуда проявляет красную флуоресценцию из-за протопорфирина. Биопсия печени не помогает оценить прогноз заболевания печени.[13]
Уход
От этого расстройства нет лекарства; тем не менее, симптомы обычно можно контролировать, ограничивая дневное солнце и некоторые виды искусственного освещения. Большинство типов искусственного освещения излучают свет с проблемными длинами волн, причем люминесцентное освещение является худшим нарушителем. Цветовая температура может быть хорошим индикатором того, какой свет является наиболее вредным, поскольку чем выше цветовая температура, тем больше излучается фиолетового света (380–450 нм). Лампы накаливания и светодиодное освещение в мягком белом диапазоне (2700-3000K) дают наименее проблемный свет. Кроме того, выбор ламп с меньшей мощностью может снизить общий световой поток.
Поскольку светочувствительность обусловлена светом в видимом спектре, большинство солнцезащитные кремы малопригодны (за исключением нано оксид цинка который обеспечивает равномерную защиту в диапазоне 290-400 нм и некоторую защиту до 700 нм[16]). Защитная одежда от солнца также может быть очень полезным, хотя одежда со значениями UPF оценивается только на основе их защиты от ультрафиолета (до 400 нм), а не на основе их защиты от видимого спектра. Некоторые производители солнцезащитной одежды используют оксид цинка в своих тканях, например, линия Coolibar ZnO Suntect, которая обеспечивает защиту от видимого света.
Некоторые пациенты постепенно создают защитный слой из меланин регулярно подвергая себя непродолжительному воздействию ультрафиолетового излучения.[нужна цитата ]
Оконные пленки, которые блокируют УФ и видимый свет до 450 нм, могут облегчить симптомы при нанесении на окна автомобиля и дома пациента. Примером может быть Мадико Эмбер 81 который может защищать в диапазоне 500 нм.
Синие защитные пленки для экрана могут помочь облегчить симптомы, вызванные экранами телевизоров, телефонов, планшетов и компьютеров.
EPP считается одним из наименее тяжелых порфирий. Если нет печеночной недостаточности, это не опасное для жизни заболевание.
Утвержденные методы лечения
Афамеланотид, разработанный австралийской компанией Clinuvel Pharmaceuticals, был одобрен в Европе в декабре 2014 года для лечения или профилактики фототоксичности у взрослых с EPP.[17]
Использование не по назначению
Используются несколько препаратов не по этикетке пациентами с ПОП:
- Урсодезоксихолевая кислота это желчная кислота который вводится для стимуляции секреции протопорфирина желчью. Результаты его использования в ПОП противоречивы. Однако известно, что он изменяет состав желчи, защищает гепатоциты от цитотоксического действия гидрофобных желчных кислот и стимулирует секрецию желчи с помощью нескольких различных механизмов.[18][19]
- Гематин по-видимому, снижает избыточную продукцию протопорфирина в костном мозге. Его назначают пациентам с EPP (3-4 мг / кг внутривенно), у которых развился криз после трансплантации печени.[20]
- Плазмаферез может также снизить уровень протопорфирина в плазме, однако его использование при лечении острых эпизодов вызывает споры.[21]
- Холестирамин вводится перорально смола который снижает уровень циркулирующего протопорфирина за счет связывания с протопорфирином в кишечнике и, следовательно, прерывания энтерогепатической циркуляции. Обычно он используется в сочетании с другими подходами к лечению.[22]
- Активированный уголь, как и холестирамин, связывается с протопорфирином в кишечнике и препятствует его всасыванию. Это дешево и легко доступно. Кажется, он эффективен для снижения уровня циркулирующего протопорфирина.[23]
Трансплантация костного мозга, трансплантация печени, ацетилцистеин, экстракорпоральный альбумин диализ, парентеральное введение железа и переливание эритроцитов являются альтернативными планами лечения EEP.
Безрецептурные добавки
Некоторые безрецептурные добавки могут помочь:
- Проферрин представляет собой пероральную добавку гема, которая может действовать аналогично гематину.
- Б. subtilis (грамположительный почвенный пробиотик) производит феррохелатазу,[24] который может преобразовывать часть протопорфирина в кишечнике в гем.
- Бета-каротин, хотя недавний метаанализ лечения каротином поставил под сомнение его эффективность.[25]
Эпидемиология
Сообщения о случаях предполагают, что ПОП распространено во всем мире. В распространенность оценивается между 1 из 75 000 и 1 из 200 000[26] однако было отмечено, что распространенность ПОП может увеличиваться из-за лучшего понимания болезни и улучшения диагностики.[27] По оценкам, 5 000–10 000 человек во всем мире имеют EPP.[требуется медицинская цитата ] ЭПП считается наиболее частой формой порфирии у детей.[28] Распространенность в Швеции была опубликована как 1: 180 000.[29]
История
Эритропоэтическая протопорфирия была впервые описана в 1953 году Косеновым и Трейбсом.[30] и завершен в 1960 году Магнусом и другие. на Институт дерматологии Святого Иоанна В Лондоне.[31]
Смотрите также
Рекомендации
- ^ ЗАЩИЩЕНО, INSERM US14 - ВСЕ ПРАВА. «Орфанет: Аутосомная эритропоэтическая протопорфирия». orpha.net. Получено 17 апреля 2019.
- ^ а б Казанова-Гонсалес, Мария Хосе; Траперо-Маруган, Мария; Джонс, Э. Энтони; Морено-Отеро, Рикардо (28 сентября 2010 г.). «Заболевание печени и эритропоэтическая протопорфирия: краткий обзор». Всемирный журнал гастроэнтерологии. 16 (36): 4526–4531. Дои:10.3748 / wjg.v16.i36.4526. ISSN 2219-2840. ЧВК 2945483. PMID 20857522.
- ^ Сигер, М. Дж .; Whatley, S.D .; Ансти, А. В .; Миллард, Т. П. (2014). «Х-сцепленная доминантная протопорфирия: новая порфирия». Клиническая и экспериментальная дерматология. 39 (1): 35–7. Дои:10.1111 / ced.12202. PMID 24131146.
- ^ а б c Цубои, Хироми; Ёнемото, Кодзох; Кацуока, Кенсей (01.11.2007). «Эритропоэтическая протопорфирия с глазными осложнениями». Журнал дерматологии. 34 (11): 790–794. Дои:10.1111 / j.1346-8138.2007.00386.x. ISSN 0385-2407. PMID 17973823.
- ^ По-Фитцпатрик, М. Б. (1986-06-01). «Молекулярно-клеточные механизмы фотосенсибилизации порфиринов». Фото-дерматология. 3 (3): 148–157. ISSN 0108-9684. PMID 3529055.
- ^ 12-160d. в Руководство по диагностике и терапии Merck Домашняя версия
- ^ Пишется, JM; Де Ройдж, ФВ; Wilson, JH; Зандберген, AA (2010). «Дефицит витамина D у больных эритропоэтической протопорфирией». Журнал наследственных метаболических заболеваний. 33 Дополнение 3: S1–4. Дои:10.1007 / s10545-008-1037-0. PMID 24137761. S2CID 22847583.
- ^ Wahlin, S .; Marschall, H.-U .; Фишлер, Б. (2013). «Материнский и плодный исход у шведских женщин с эритропоэтической протопорфирией». Британский журнал дерматологии. 168 (6): 1311–5. Дои:10.1111 / bjd.12242. PMID 23738640.
- ^ Благоевич, Даниэль; Шенк, Томас; Хаас, Оскар; Цирхофер, Бриджит; Коннарис, Христофор; Траутингер, Франц (2009). «Приобретенная эритропоэтическая протопорфирия». Анналы гематологии. 89 (7): 743–4. Дои:10.1007 / s00277-009-0859-7. PMID 19902211. S2CID 36170513.
- ^ Конг, Сяо-Фэй; Е, Цзин; Гао, Де-Юн; Гун, Ци-Мин; Чжан, Донг-Хуа; Лу, Чжи-Мэн; Лу, И-Мин; Чжан, Синь-Синь (01.02.2008). «Идентификация мутации феррохелатазы в китайской семье с эритропоэтической протопорфирией». Журнал гепатологии. 48 (2): 375–379. Дои:10.1016 / j.jhep.2007.09.013. ISSN 0168-8278. PMID 18160121.
- ^ а б Холм, С. Александр; Ворвуд, Марк; Ансти, Александр В .; Старейшина, Джордж Х .; Бадминтон, Майкл Н. (2007-12-01). «Эритропоэз и метаболизм железа при доминирующей эритропоэтической протопорфирии». Кровь. 110 (12): 4108–4110. Дои:10.1182 / кровь-2007-04-088120. ISSN 0006-4971. PMID 17804693.
- ^ Магнус, И. А. (февраль 1968 г.). «Фотобиологические аспекты порфирии». Труды Королевского медицинского общества. 61: 196–198. Дои:10.1177/003591576806100233. PMID 5688974.
- ^ а б Леха, Марио; Пюи, Эрве; Дейбах, Жан-Шарль (01.01.2009). «Эритропоэтическая протопорфирия». Журнал редких заболеваний Orphanet. 4: 19. Дои:10.1186/1750-1172-4-19. ISSN 1750-1172. ЧВК 2747912. PMID 19744342.
- ^ Bruguera, M .; Эрреро, К. (2005-12-01). «[Заболевание печени при эритропоэтической протопорфирии]». Gastroenterología y Hepatología. 28 (10): 632–636. Дои:10.1016 / s0210-5705 (05) 71529-6. ISSN 0210-5705. PMID 16373015.
- ^ Ансти, А. В .; Хифт, Р. Дж. (2007-07-01). «Заболевание печени при эритропоэтической протопорфирии: выводы и значение для лечения». Кишечник. 56 (7): 1009–1018. Дои:10.1136 / gut.2006.097576. ISSN 0017-5749. ЧВК 1994365. PMID 17360790.
- ^ «Оксид цинка - физический солнцезащитный крем UVA + UVB». smartskincare.com. Получено 2019-04-02.
- ^ «Общественный регистр лекарственных средств для использования человеком». http://ec.europa.eu. Европейская комиссия. Получено 24 декабря 2014. Внешняя ссылка в
| сайт =(помощь) - ^ Пирлич, М .; Lochs, H .; Шмидт, Х. Х. (2001-12-01). «Цирроз печени при эритропоэтической протопорфирии: улучшение функции печени с помощью урсодезоксихолевой кислоты». Американский журнал гастроэнтерологии. 96 (12): 3468–3469. ISSN 0002-9270. PMID 11774991.
- ^ Паумгартнер, Густав; Бойерс, Ульрих (01.09.2002). «Урсодезоксихолевая кислота при холестатической болезни печени: пересмотр механизмов действия и терапевтического использования». Гепатология. 36 (3): 525–531. Дои:10.1053 / jhep.2002.36088. ISSN 0270-9139. PMID 12198643.
- ^ Potter, C .; Толаймат, Н .; Бобо, Р .; Sharp, H .; Ранг, Дж .; Блумер, Дж. (1996-11-01). «Гематинотерапия у детей с протопорфирической болезнью печени». Журнал детской гастроэнтерологии и питания. 23 (4): 402–407. Дои:10.1097/00005176-199611000-00006. ISSN 0277-2116. PMID 8956175.
- ^ Tung, B. Y .; Фаррелл, Ф. Дж .; McCashland, T. M .; Gish, R.G .; Bacon, B.R .; Keeffe, E. B .; Каудли, К. В. (1999-09-01). «Долгосрочное наблюдение после трансплантации печени у пациентов с перегрузкой печеночного железа». Трансплантация и хирургия печени. 5 (5): 369–374. Дои:10.1002 / л.500050503. ISSN 1074-3022. PMID 10477837.
- ^ McCullough, A.J .; Barron, D .; Mullen, K. D .; Петрелли, М .; Парк, М. С .; Mukhtar, H .; Бикерс, Д. Р. (1988-01-01). «Фекальная экскреция протопорфирина при эритропоэтической протопорфирии: влияние холестирамина и кормления желчной кислотой». Гастроэнтерология. 94 (1): 177–181. Дои:10.1016/0016-5085(88)90627-0. ISSN 0016-5085. PMID 3335288.
- ^ Горчейн, А .; Фостер, Г. Р. (1999-03-01). «Печеночная недостаточность при протопорфирии: длительное лечение углем для приема внутрь». Гепатология. 29 (3): 995–996. Дои:10.1002 / hep.510290314. ISSN 0270-9139. PMID 10189233.
- ^ Hansson, M .; Хедерштедт, Л. (1994-02-15). «Очистка и характеристика водорастворимой феррохелатазы из Bacillus subtilis». Европейский журнал биохимии. 220 (1): 201–208. Дои:10.1111 / j.1432-1033.1994.tb18615.x. ISSN 0014-2956. PMID 8119288.
- ^ Minder, EI; Шнайдер-Инь, X; Steurer, J; Бахманн, LM (2009). «Систематический обзор вариантов лечения кожной фоточувствительности при эритропоэтической протопорфирии». Клеточная и молекулярная биология. 55 (1): 84–97. PMID 19268006.
- ^ Арчечи, Роберт .; Ханн, Ян М .; Смит, Оуэн П. (2006). Детский гематолог. Мальден, Массачусетс: Blackwell Pub. ISBN 978-1-4051-3400-2.[страница нужна ]
- ^ Старший, Джордж; Харпер, Полина; Бадминтон, Майкл; Сандберг, Сверре; Дейбах, Жан-Шарль (2012). «Заболеваемость наследственными порфириями в Европе». Журнал наследственных метаболических заболеваний. 36 (5): 849–57. Дои:10.1007 / s10545-012-9544-4. PMID 23114748. S2CID 20442163.
- ^ Michaels, BD; Дель Россо, JQ; Mobini, N; Майклс, младший (2010). «Эритропоэтическая протопорфирия: клинический случай и обзор литературы». Журнал клинической и эстетической дерматологии. 3 (7): 44–8. ЧВК 2921755. PMID 20725556.
- ^ Wahlin, S .; Floderus, Y .; Stål, P .; Харпер, П. (2011). «Эритропоэтическая протопорфирия в Швеции: демографические, клинические, биохимические и генетические характеристики». Журнал внутренней медицины. 269 (3): 278–88. Дои:10.1111 / j.1365-2796.2010.02236.x. PMID 20412370.
- ^ Косенов, W; Treibs, A (1953). «Световая гиперчувствительность и порфиринемия». Zeitschrift für Kinderheilkunde. 73 (1): 82–92. Дои:10.1007 / BF00438257. PMID 13103364. S2CID 46459771.
- ^ Магнус, я; Джарретт, А; Prankerd, TA; Римингтон, К. (1961). «Эритропоэтическая протопорфирия. Новый синдром порфирии с солнечной крапивницей из-за протопорфиринемии». Ланцет. 278 (7200): 448–51. Дои:10.1016 / S0140-6736 (61) 92427-8. PMID 13765301.
внешняя ссылка
- Эритропоэтическая протопорфирия в NLM Домашний справочник по генетике
| Классификация | |
|---|---|
| Внешние ресурсы |
