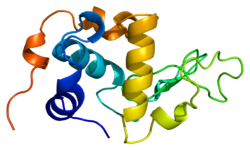
Альфа-лактальбумин - Alpha-lactalbumin
Лактальбумин, альфа-, также известный как ЛАЛБА, это белок что у людей кодируется ЛАЛБА ген.[5][6][7]
Функция
α-лактальбумин белок, регулирующий выработку лактозы в молоке почти всех млекопитающее разновидность.[8] У приматов экспрессия альфа-лактальбумина повышается в ответ на гормон. пролактин и увеличивает производство лактоза.[9]
α-лактальбумин образует регуляторную субъединицу лактозосинтаза (LS) гетеродимер и β-1,4-галактозилтрансфераза (beta4Gal-T1) образует каталитический компонент. Вместе эти белки позволяют LS производить лактоза путем передачи галактоза части для глюкоза. Как мультимер, альфа-лактальбумин прочно связывает ионы кальция и цинка и может обладать бактерицидным или противоопухолевым действием. Складывающийся вариант альфа-лактальбумина человека, который может образовываться в кислой среде, такой как желудок, называется ГАМЛЕТ, вероятно, вызывает апоптоз в опухолевых и незрелых клетках.[5] Таким образом, соответствующая динамика сворачивания альфа-лактальбумина весьма необычна.[10]
При образовании комплекса с Gal-T1, галактозилтрансфераза, α-лактальбумин, увеличивает сродство фермента к глюкоза примерно в 1000 раз и подавляет способность полимеризовать несколько галактоза единицы. Это открывает путь для формирования лактоза преобразовав Гал-ТИ в Лактозосинтаза.
Физические свойства
Структура альфа-лактальбумина хорошо известна и состоит из 123 аминокислот и 4 дисульфидных мостиков. Молекулярная масса составляет 14178 Да, а изоэлектрическая точка составляет от 4,2 до 4,5. Одно из основных конструктивных отличий от бета-лактоглобулин в том, что в нем нет бесплатных тиоловая группа что может служить отправной точкой для реакции ковалентной агрегации. В результате чистый α-лактальбумин не образует гелей при денатурация и подкисление.
Эволюция
Сравнение последовательностей α-лактальбумина показывает сильное сходство с последовательностью лизоцимы, в частности Ca2+-связывающий с-лизоцим.[11] Итак, ожидаемая эволюционная история такова, что за дупликацией гена с-лизоцима следовала мутация.[8] Этот ген предшествует последнему общему предку млекопитающих и птиц, что, вероятно, предполагает его происхождение примерно 300 млн лет назад.[12]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000167531 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000022991 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б «Энтрез Ген: лактальбумин LALBA, альфа».
- ^ Холл L, Дэвис М.С., Крейг Р.К. (январь 1981 г.). «Конструирование, идентификация и характеристика плазмид, содержащих последовательности кДНК альфа-лактальбумина человека». Нуклеиновые кислоты Res. 9 (1): 65–84. Дои:10.1093 / nar / 9.1.65. ЧВК 326669. PMID 6163135.
- ^ Холл L, Эмери, округ Колумбия, Дэвис М.С., Паркер Д., Крейг Р.К. (март 1987 г.). «Организация и последовательность гена альфа-лактальбумина человека». Biochem. J. 242 (3): 735–42. Дои:10.1042 / bj2420735. ЧВК 1147772. PMID 2954544.
- ^ а б Касба П.К., Кумар С. (1997). «Молекулярная дивергенция лизоцимов и альфа-лактальбумина». Крит. Rev. Biochem. Мол. Биол. 32 (4): 255–306. Дои:10.3109/10409239709082574. PMID 9307874.
- ^ Клейнберг JL, Тодд J, Бабицкий G (1983). «Ингибирование эстрадиолом лактогенного действия пролактина в ткани молочной железы приматов: обращение антиэстрогенов LY 156758 и тамоксифена». PNAS. 80 (13): 4144–4148. Дои:10.1073 / pnas.80.13.4144. ЧВК 394217. PMID 6575400.
- ^ Бу, З .; Cook, J .; Каллавей, Д. Дж. Э. (2001). «Динамические режимы и коррелированная структурная динамика в нативном и денатурированном альфа-лактальбумине». J. Mol. Биол. 312 (4): 865–873. Дои:10.1006 / jmbi.2001.5006. PMID 11575938.
- ^ Ачарья К.Р., Стюарт Д.И., Уокер Н.П., Льюис М., Филлипс, округ Колумбия (1989). «Уточненная структура альфа-лактальбумина павиана при разрешении 1,7 A. Сравнение с лизоцимом C-типа». J. Mol. Биол. 208 (1): 99–127. Дои:10.1016/0022-2836(89)90091-0. PMID 2769757.
- ^ Прагер Э.М., Уилсон А.С. (1988). «Древнее происхождение лактальбумина из лизоцима: анализ ДНК и аминокислотных последовательностей». J. Mol. Evol. 27 (4): 326–35. Дои:10.1007 / BF02101195. PMID 3146643. S2CID 10039589.
дальнейшее чтение
- Heine WE, Klein PD, Reeds PJ (1991). «Важность альфа-лактальбумина в детском питании». J. Nutr. 121 (3): 277–83. Дои:10.1093 / jn / 121.3.277. PMID 2002399.
- Пермяков Е.А., Берлинер LJ (2000). «Альфа-лактальбумин: структура и функции». FEBS Lett. 473 (3): 269–74. Дои:10.1016 / S0014-5793 (00) 01546-5. PMID 10818224. S2CID 83964232.
- Холл Л., Эмери Д.К., Дэвис М.С. и др. (1987). «Организация и последовательность гена альфа-лактальбумина человека». Biochem. J. 242 (3): 735–42. ЧВК 1147772. PMID 2954544.
- Дэвис М.С., Вест Л.Ф., Дэвис М.Б. и др. (1987). «Ген альфа-лактальбумина человека отнесен к хромосоме 12q13». Анна. Гм. Genet. 51 (Pt 3): 183–8. Дои:10.1111 / j.1469-1809.1987.tb00869.x. PMID 3479943. S2CID 37901087.
- Финдли Дж. Б., Варка К. (1972). «Полная аминокислотная последовательность лактальбумина человека». Евро. J. Biochem. 27 (1): 65–86. Дои:10.1111 / j.1432-1033.1972.tb01812.x. PMID 5049057.
- Холл L, Крейг Р.К., Эдбрук М.Р., Кэмпбелл П.Н. (1982). «Сравнение нуклеотидной последовательности кДНК пре-альфа-лактальбумина человека и морской свинки с таковой кДНК пре-лизоцима цыпленка предполагает эволюцию от общего предкового гена». Нуклеиновые кислоты Res. 10 (11): 3503–3515. Дои:10.1093 / nar / 10.11.3503. ЧВК 320727. PMID 6285305.
- Хоканссон А., Животовский Б., Оррениус С. и др. (1995). «Апоптоз, индуцированный белком грудного молока». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 92 (17): 8064–8068. Дои:10.1073 / пнас.92.17.8064. ЧВК 41287. PMID 7644538.
- Стейси А., Шниеке А., Керр М. и др. (1995). «Лактация нарушена из-за дефицита альфа-лактальбумина и может быть восстановлена заменой человеческого гена альфа-лактальбумина у мышей». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 92 (7): 2835–2839. Дои:10.1073 / пнас.92.7.2835. ЧВК 42313. PMID 7708733.
- Fujiwara Y, Miwa M, Takahashi R и др. (1997). «Позиционно-независимая и высокоуровневая экспрессия человеческого альфа-лактальбумина в молоке трансгенных крыс, несущих ДНК YAC 210 kb». Мол. Репрод. Dev. 47 (2): 157–63. Дои:10.1002 / (SICI) 1098-2795 (199706) 47: 2 <157 :: AID-MRD5> 3.0.CO; 2-L. PMID 9136116.
- Линднер Р.А., Капур А., Карвер Дж. А. (1997). «Взаимодействие молекулярного шаперона, альфа-кристаллина, с состояниями расплавленных глобул бычьего альфа-лактальбумина». J. Biol. Chem. 272 (44): 27722–9. Дои:10.1074 / jbc.272.44.27722. PMID 9346914.
- Джуффрида М.Г., Кавалетто М., Джунта С. и др. (1998). «Необычный триплет аминокислот Asn-Ile-Cys является консенсусным сайтом гликозилирования в альфа-лактальбумине человека». J. Protein Chem. 16 (8): 747–53. Дои:10.1023 / А: 1026359715821. PMID 9365923. S2CID 42107172.
- Чандра Н., Брю К., Ачарья К.Р. (1998). «Структурные доказательства наличия вторичного сайта связывания кальция в альфа-лактальбумине человека». Биохимия. 37 (14): 4767–4772. Дои:10.1021 / bi973000t. PMID 9537992.
- Хоканссон А., Андреассон Дж., Животовский Б. и др. (1999). «Мультимерный альфа-лактальбумин из грудного молока вызывает апоптоз за счет прямого воздействия на ядра клеток». Exp. Cell Res. 246 (2): 451–60. Дои:10.1006 / excr.1998.4265. PMID 9925761.
- Свенссон М., Сабхарвал Х., Хоканссон А. и др. (1999). «Молекулярная характеристика вариантов сворачивания альфа-лактальбумина, которые вызывают апоптоз в опухолевых клетках». J. Biol. Chem. 274 (10): 6388–6396. Дои:10.1074 / jbc.274.10.6388. PMID 10037730.
- Харата К., Абэ Й., Мураки М. (1999). «Кристаллографическая оценка внутреннего движения альфа-лактальбумина человека, уточненного полноматричным методом наименьших квадратов». J. Mol. Биол. 287 (2): 347–58. Дои:10.1006 / jmbi.1999.2598. PMID 10080897.
- Последний AM, Шульман Б.А., Робинсон CV, Редфилд С. (2001). «Исследование тонких различий в поведении водородного обмена вариантов расплавленной глобулы альфа-лактальбумина человека с использованием масс-спектрометрии». J. Mol. Биол. 311 (4): 909–19. Дои:10.1006 / jmbi.2001.4911. PMID 11518539.
- Бай П, Пэн Зи (2001). «Кооперативное сворачивание изолированного альфа-спирального домена лизоцима куриного яйца». J. Mol. Биол. 314 (2): 321–9. Дои:10.1006 / jmbi.2001.5122. PMID 11718563.
- Эндрюс П. (1970). «Очистка белка лактозосинтетазы из грудного молока и демонстрация его взаимодействия с альфа-лактальбумином». Письма FEBS. 9 (5): 297–300. Дои:10.1016/0014-5793(70)80382-9. PMID 11947697. S2CID 23041445.
внешняя ссылка
- альфа-лактальбумин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Человек ЛАЛБА расположение генома и ЛАЛБА страница сведений о генах в Браузер генома UCSC.