SN2 реакция - SN2 reaction

В SN2 реакция это тип механизм реакции это распространено в органическая химия. В этом механизме одна связь разрывается, а одна образуется синхронно, то есть за один шаг. SN2 - это своего рода нуклеофильное замещение механизм реакции, название относится к Символ Хьюза-Ингольда механизма. С два реагирующие виды участвуют в медленных (ставка определения ) шаг, это приводит к члену sучреждение пуклеофильный (би-молекулярный ) или же SN2; другой основной вид SN1.[1] Многие другие более специализированные механизмы описывают реакции замещения.
Тип реакции настолько распространен, что имеет другие названия, например «бимолекулярное нуклеофильное замещение» или, среди химиков-неоргаников, »ассоциативная замена "или" механизм обмена ".
Механизм реакции
Чаще всего реакция возникает при алифатический зр3 углеродный центр с электроотрицательный, прикрепленная к нему стабильная уходящая группа (часто обозначаемая X), которая часто является галогенид атом. Разрыв связи C – X и образование новой связи (часто обозначаемой C – Y или C – Nu) происходят одновременно через переходное состояние в котором углерод, подвергающийся нуклеофильной атаке, пятикоординатный, и примерно sp2 гибридизированный. Нуклеофил атакует углерод под углом 180 ° к уходящая группа, так как это обеспечивает лучшее перекрытие неподеленной пары нуклеофила и антисвязывающей орбитали C – X σ *. Затем уходящая группа отодвигается с противоположной стороны, и продукт формируется с инверсия тетраэдрической геометрии на центральном атоме.
Если субстрат под нуклеофильной атакой хиральный, то это часто приводит к обращению конфигурация (стереохимия ), названный Инверсия Уолдена.
На примере SN2 реакция, атака Br− (нуклеофил) на этилхлорид (электрофил) приводит к этилбромид, с хлористый изгнан как уходящая группа.
 SN2 реакция хлорэтана с бромид-ионом
SN2 реакция хлорэтана с бромид-ионом
SN2 атака происходит, если обратный путь атаки не стерически затрудненный к заместители на субстрат (вышеупомянутым субстратом является этилхлорид). Следовательно, это механизм обычно происходит беспрепятственно первичный и вторичный углерод центры. Если на субстрате есть стерическое скопление рядом с уходящей группой, например, в третичном углеродном центре, замещение будет включать SN1, а не букву SN2, (SN1 также будет более вероятным в этом случае, потому что достаточно стабильный карбокатион посредник может быть сформирован).
Факторы, влияющие на скорость реакции
На скорость реакции влияют четыре фактора:[2][3]
Субстрат
Субстрат играет наиболее важную роль в определении скорости реакции. Это происходит потому, что нуклеофил атакует с обратной стороны субстрата, тем самым разрывая связь уходящей углеродной группы и образуя связь углерод-нуклеофил. Следовательно, чтобы максимизировать скорость SN2, обратная сторона субстрата должна быть максимально беспрепятственной. В целом это означает, что метильный и первичный субстраты реагируют быстрее всего, за ним следуют вторичные субстраты. Третичные субстраты не участвуют в SN2 реакции, из-за стерическое препятствие. Структуры, которые могут образовывать высокостабильные катионы за счет простой потери уходящей группы, например, в виде резонансно-стабилизированного карбокатиона, особенно склонны реагировать через SN1 путь в конкуренции с SN2.
Нуклеофил
Как и субстрат, стерические препятствия влияют на силу нуклеофила. В метоксид анион, например, является одновременно сильным основанием и нуклеофилом, потому что он является метилнуклеофилом и, таким образом, очень беспрепятственно. терт-Бутоксид, с другой стороны, является сильным основанием, но плохим нуклеофилом из-за его трех метильных групп, препятствующих его приближению к углероду. На прочность нуклеофилов также влияют заряд и электроотрицательность: нуклеофильность увеличивается с увеличением отрицательного заряда и уменьшением электроотрицательности. Например, OH− является лучшим нуклеофилом, чем вода, и я− является лучшим нуклеофилом, чем Br− (в полярных протонных растворителях). В полярном апротонном растворителе нуклеофильность увеличивается вверх по столбцу периодической таблицы, поскольку нет водородной связи между растворителем и нуклеофилом; в этом случае нуклеофильность отражает основность. я− следовательно, будет более слабым нуклеофилом, чем Br− потому что это более слабая база. Вердикт: сильный / анионный нуклеофил всегда предпочитает SN2 способ нуклеофильного замещения.
Растворитель
Растворитель влияет на скорость реакции, поскольку растворители могут окружать или не окружать нуклеофил, тем самым затрудняя или не препятствуя его приближению к атому углерода.[4] Полярные апротонные растворители, например тетрагидрофуран, являются лучшими растворителями для этой реакции, чем полярные протонные растворители потому что полярные протонные растворители будут водородная связь к нуклеофилу, не давая ему атаковать углерод с уходящей группой. Полярный апротонный растворитель с низкой диэлектрической проницаемостью или с затрудненным дипольным концом будет благоприятствовать SN2 способ реакции нуклеофильного замещения. Примеры: диметилсульфоксид, диметилформамид, ацетон и Т. Д.
Выход из группы
Стабильность уходящей группы как аниона и прочность ее связи с атомом углерода влияют на скорость реакции. Чем более стабильно сопряженное основание уходящей группы, тем более вероятно, что оно возьмет два электрона своей связи с углеродом во время реакции. Следовательно, чем слабее уходящая группа в виде конъюгированного основания и, следовательно, чем сильнее ее соответствующая кислота, тем лучше уходящая группа. Поэтому примерами хороших уходящих групп являются галогениды (за исключением фторида из-за его прочной связи с атомом углерода) и тозилат, тогда как HO− и H2N− не.
Кинетика реакции
Скорость SN2 реакция второго порядка, как этап определения ставки зависит от концентрации нуклеофила, [Nu−], а также концентрацию субстрата [RX].[5]
- р = k [RX] [Nu−]
Это ключевое различие между SN1 и SN2 механизма. В SN1 нуклеофил атакует после завершения лимитирующей стадии, тогда как в SN2, нуклеофил отталкивает уходящую группу на лимитирующей стадии. Другими словами, скорость SN1 реакции зависят только от концентрации субстрата, а реакция SN2 скорость реакции зависит от концентрации как субстрата, так и нуклеофила.[5]
Было показано[6] что за исключением редких (но предсказуемых случаев) первичные и вторичные субстраты идут исключительно через SN2, в то время как третичные субстраты проходят через SN1 реакция. Есть два фактора, которые затрудняют определение механизма реакций нуклеофильного замещения у вторичных атомов углерода:
1) Многие изученные реакции являются реакциями сольволиза, в которых молекула растворителя - часто спирт - является нуклеофилом. Хотя механически все еще протекает реакция второго порядка, кинетически реакция первого порядка, поскольку концентрация нуклеофила-молекулы растворителя во время реакции эффективно постоянна. Этот тип реакции часто называют реакцией псевдопервого порядка.
2) В реакциях, где уходящая группа также является хорошим нуклеофил-бромидом, например, уходящая группа может выполнять SN2 реакция на молекулу субстрата. Если субстрат хиральный, это меняет конфигурацию субстрата перед сольволизом, что приводит к рацемизированному продукту - продукту, которого можно было бы ожидать от SN1 механизм. В случае уходящей группы бромида в спиртовом растворителе Cowdrey et al.[7] показали, что бромид может иметь SN2 константа скорости в 100-250 раз превышает константу скорости для этанола. Таким образом, после сольволиза энантиоспецифического субстрата всего на несколько процентов он становится рацемическим.
Примеры в учебниках вторичных субстратов по стандарту SN1 механизм неизменно включает использование бромида (или другого хорошего нуклеофила), поскольку уходящая группа запутала понимание реакций алкилнуклеофильного замещения у вторичных атомов углерода в течение 80 лет.[3]. Работа с 2-адамантильной системой (SN2 невозможно) Шлейером и его сотрудниками,[8] использование азида (отличный нуклеофил, но очень плохая уходящая группа) Weiner и Sneen,[9][10] разработка уходящих сульфонатных групп (ненуклеофильные хорошие уходящие группы) и демонстрация значительных экспериментальных проблем в первоначальной заявке на SN1 механизм сольволиза оптически активного 2-бромоктана Hughes et al.[11][3] убедительно продемонстрировали, что вторичные субстраты поступают исключительно (за исключением необычных, но предсказуемых случаев) SN2 механизм.
E2 соревнование
Обычный побочная реакция происходит с SN2 реакции это E2 устранение: входящий анион может действовать как основание, а не как нуклеофил, абстрагируя протон и приводя к образованию алкен. Этот путь предпочтителен для стерически затрудненных нуклеофилов. Реакции элиминации обычно протекают при повышенных температурах.[12] из-за увеличения энтропия. Этот эффект можно продемонстрировать в газофазной реакции между сульфонат и простой алкилбромид происходит внутри масс-спектрометр:[13][14]
С этилбромид, продукт реакции является преимущественно продуктом замещения. В качестве стерическое препятствие вокруг электрофильного центра увеличивается, как при изобутил бромид, замещение нежелательно, и преобладающей реакцией является отщепление. Другими факторами, способствующими устранению, являются прочность основы. С менее основными бензоат субстрат, изопропилбромид реагирует с замещением 55%. В общем, газофазные реакции и реакции в фазе раствора этого типа следуют одним и тем же тенденциям, хотя в первом случае эффекты растворителя устранены.
Круговой механизм
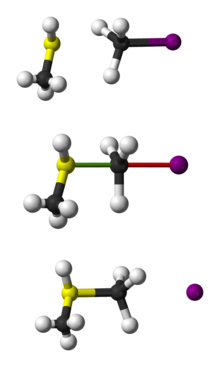
В 2008 году внимание привлекла разработка SN2 обходной механизм наблюдается в газофазной реакции между хлорид-ионами и метилиодид со специальной техникой, называемой визуализация скрещенных молекулярных пучков. Когда ионы хлорида имеют достаточную скорость, их первоначальное коллозирование с молекулой йодистого метила заставляет йодистый метил один раз вращаться до фактического SN2 механизма перемещения.[15][16][17]
Смотрите также
- Реакция замещения
- SN1 реакция
- SNя
- Нуклеофильное ароматическое замещение
- Нуклеофильное ацильное замещение
- Участие в соседней группе
- Реакция Финкельштейна
- Кристофер Келк Ингольд
- Нажатие стрелы
Рекомендации
- ^ Макмерри, Джон Э. (1992), Органическая химия (3-е изд.), Belmont: Wadsworth, ISBN 0-534-16218-5
- ^ Смит, Майкл Б .; Марш, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Hamlin, Trevor A .; Сварт, Марсель; Бикельгаупт, Ф. Матиас (2018). «Нуклеофильное замещение (SN2): зависимость от нуклеофила, уходящей группы, центрального атома, заместителей и растворителя». ХимФисХим. 19 (11): 1315–1330. Дои:10.1002 / cphc.201701363. ISSN 1439-7641. ЧВК 6001448. PMID 29542853.
- ^ Hamlin, Trevor A .; ван Бик, Бас; Wolters, Lando P .; Бикельгаупт, Ф. Матиас (2018). «Нуклеофильная замена в растворе: анализ штамма активации слабого и сильного действия растворителя». Химия - Европейский журнал. 24 (22): 5927–5938. Дои:10.1002 / chem.201706075. ISSN 1521-3765. ЧВК 5947303. PMID 29457865.
- ^ а б Клейден, Джонатан; Гривс, Ник; Уоррен, Стюарт (2012). Органическая химия (2-е изд.). Оксфорд: Издательство Оксфордского университета. п. 330. ISBN 978-0-19-927029-3.
- ^ Отсутствие SN1 Участие в сольволизе вторичных алкильных соединений, T. J. Murphy, J. Chem. Образов .; 2009; 86 (4), стр. 519-24; (Статья) doi: 10.1021 / ed041p678
- ^ Связь стерической ориентации с механизмом замещения с участием атомов галогена и простых или замещенных гидроксильных групп, W. A. Cowdrey, E. D. Hughes, C. K. Ingold, S. Masterman, A. D. Scott, J. Chem. Soc .; 1937; 1252–1271. 10.1039 / JR9370001252
- ^ 2-Адамантильная система, стандарт для ограничения сольволиза во вторичном субстрате J. L. Fry, C. J. Lancelot, L. K. M. Lam, J. M. Harris, R.C.Bingham, D. J. Raber, R. E. Hill, P. v. R. Schleyer, J. Am. Chem. Soc.,; 1970; 92, pp. 1240-42 (статья); DOI: 10.1021 / ja00478a031
- ^ Уточнение механизма сольволиза 2-октилсульфонатов. Стереохимические соображения; Х. Вайнер, Р. А. Снин, J. Am. Chem. Soc.,; 1965; 87 стр. 287–91; (Статья) doi: 10.1021 / ja01080a026
- ^ Уточнение механизма сольволиза 2-октилсульфонатов. Кинетические соображения; Х. Вайнер, Р. А. Снин, J. Am. Chem. Soc .; 1965; 87 стр. 292-96; (Статья) doi: 10.1021 / ja01080a027
- ^ Гомогенный гидролиз и алкоголиз β-н-октилгалогенидов, E. D. Hughes, C. K. Ingold, S. Masterman, J. Chem. Soc .; 1937; pp 1196–1201; (Статья) doi: 10.1039 / JR9370001196
- ^ «Реакциям на удаление способствует тепло - мастер органической химии». www.masterorganicchemistry.com. Получено 13 апреля 2018.
- ^ Газофазные исследования конкуренции между реакциями замещения и отщепления Скотт Гронерт Соотв. Chem. Res.; 2003; 36 (11), стр. 848–857; (Статья) Дои:10.1021 / ar020042n
- ^ Используемая техника ионизация электрораспылением и поскольку для обнаружения требуются заряженные продукты реакции, нуклеофил снабжен дополнительной анионной сульфонатной группой, неактивной и хорошо отделенной от другого аниона. Соотношение продуктов замещения и элиминирования можно измерить по интенсивности их относительных молекулярных ионов.
- ^ Визуализация динамики нуклеофильного замещения Дж. Микош, С. Триппель, К. Эйххорн, Р. Отто, У. Лурдерадж, Дж. Х. Чжан, В. Л. Хасе, М. Вайдемюллер и Р. Вестер Сайенс 11 января 2008 319: 183-186 Дои: 10.1126 / наука.1150238 (в отчетах)
- ^ ПЕРСПЕКТИВЫ ХИМИЯ: Не все так просто Джон И. Брауман (11 января 2008 г.) Science 319 (5860), 168. Дои:10.1126 / science.1152387
- ^ Сюрприз из снимков SN2 Измерения скорости ионов раскрывают дополнительный непредвиденный механизм Кармен Драл Новости химии и машиностроения 14 января, 2008 Том 86, номер 2 стр. 9 http://pubs.acs.org/cen/news/86/i02/8602notw1.html, видео включено


