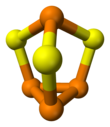
Сесквисульфид фосфора - Phosphorus sesquisulfide
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Трисульфид тетрафосфора или 3,5,7-тритиа-1,2,4,6-тетрафосфатрицикло [2.2.1.02,6]гептан | |||
| Другие имена трисульфид фосфора, полуторный сульфид фосфора, сульфид фосфора | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.013.860 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| п4S3 | |||
| Молярная масса | 220,093 г / моль | ||
| Внешность | Желтое, желто-зеленое или серое твердое вещество | ||
| Плотность | 2,08 г. см3,[1] твердый | ||
| Температура плавления | 172,5 ° С (342,5 ° F, 445,6 К) | ||
| Точка кипения | 408 ° С (766 ° F, 681 К) | ||
| Структура | |||
| ромбический, Обозначение Шенфлиса D2ч | |||
| Pmnb | |||
| C3в | |||
| Родственные соединения | |||
Родственные соединения | п4S10 п4О6 | ||
| Опасности | |||
| Главный опасности | Раздражающий | ||
| Пиктограммы GHS |  | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Сесквисульфид фосфора это неорганическое соединение с формула п4S3. Он был разработан Анри Севен и Эмиль Дэвид Кахен в 1898 году в рамках их изобретения фрикционные спички которые не представляют опасности для здоровья белый фосфор.[2][3] Это твердое вещество желтого цвета - одно из двух производимых серийно сульфиды фосфора. Это составная часть матчей типа «забей куда угодно».
В зависимости от чистоты образцы могут иметь вид от желто-зеленого до серого. Соединение было обнаружено Г. Лемуаном и впервые безопасно произведено в коммерческий количества в 1898 г. Олбрайт и Уилсон. Он растворяется в равной массе сероуглерод (CS2), а в весовом соотношении 1:50 бензол. В отличие от некоторых других сульфидов фосфора, P4S3 медленно гидролизуется и имеет четко определенную температуру плавления.
Структура и синтез
В молекуле C3в симметрия. Это производная от тетраэдра (P4) от внедрения серы в три связи P-P. Расстояния P-S и P-P составляют 2,090 и 2,235 Å соответственно. п4Se3 и P4S3 принять те же структуры.[1] Эти соединения могут плавиться вместе и образовывать смешанные кристаллы, один растворенный в другом.[4] При более высоких температурах смешанные молекулы халькогенидов P4S2Se и P4SSe2 сформируется.[5]
п4S3 образуется при реакции красного или белого фосфора с серой. Избыток серы дает пентасульфид фосфора (П4S10). По оценкам, в 1989 году было произведено 150 тонн в год.[6]
Приложения
п4S3 и хлорат калия, вместе с другими материалами, составляет главу "забастовки везде" совпадения ".[7]
Безопасность
Его температура вспышки составляет около 100 ° C.[8]
Влияние на здоровье
Воздействие спичек, содержащих полуторный сульфид фосфора, может вызвать контактный дерматит, обычно в области карманов, но также и на лице.[9] Длительное воздействие горящих кончиков спичек (содержащих фосфорсесквисульфид) может привести к повторному тяжелому первичному дерматиту вокруг глаз и лица. Сообщалось также о расшатывании зубов, которое могло быть связано с отравлением фосфором.[10]
Рекомендации
- ^ а б Leung, Y.C .; Waser, J .; van Houten, S .; Вос, А .; Wiegers, G.A .; Вибенга, Э. Х. (1957). «Кристаллическая структура P4S3". Acta Crystallographica. 10 (9): 574–582. Дои:10.1107 / S0365110X57002042.
- ^ Патент США 614350, Seyene, H .; Каэн, Э. Д., "Состав спичек", выпущенный 15 ноября 1898 г.
- ^ США 614350
- ^ Бернс, Гэри Р.; Сарфати, Джонатан Д. (1988). "Рамановские спектры триселенида тетрафосфора, допированного трисульфидом тетрафосфора". Твердотельные коммуникации. 66 (4): 347–349. Bibcode:1988SSCom..66..347B. Дои:10.1016 / 0038-1098 (88) 90854-Х.
- ^ Бернс, Гэри Р.; Ролло, Джоанн Р .; Сарфати, Джонатан Д. (1989). «Рамановские спектры клеточных молекул трихалькогенида тетрафосфора P4S2Se и P4SSe2". Неорганика Chimica Acta. 161: 35–38. Дои:10.1016 / S0020-1693 (00) 90111-7.
- ^ Bettermann, G .; Krause, W .; Riess, G .; Хофманн, Т. "Неорганические соединения фосфора". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a19_527.
- ^ Корбридж, Д. Е. С. (1995). Фосфор: краткое описание его химии, биохимии и технологии (5-е изд.). Амстердам: Эльзевир. С. 115–116. ISBN 0-444-89307-5.
- ^ Льюис, Р.Дж. Sr (2007). Краткий химический словарь Хоули (15-е изд.). Нью-Йорк, Нью-Йорк: John Wiley & Sons, Inc. стр. 987.
- ^ Берджесс, Дж. Ф .; Форси, Р. Рой (1951). «Контактный дерматит лица из-за спичек». AMA Arch Derm Syphilol. Американская медицинская ассоциация. 64 (5): 636–637. Дои:10.1001 / archderm.1951.01570110106016.
- ^ Берджесс, Дж. Фредерик (декабрь 1951 г.). «Отравление сесквисульфидом фосфора». Can Med Assoc J. Канадская медицинская ассоциация. 65 (6): 567–568. ЧВК 1822299. PMID 14886853.
Эта статья содержит цитируемый текст из общественного достояния от NOAA.