N-Формилметионин - N-Formylmethionine
 | |
| Имена | |
|---|---|
| Название ИЮПАК (S) -2-Формиламино-4-метилсульфанилбутановая кислота | |
| Другие имена 2-формиламино-4-метилсульфанилмасляная кислота; Формилметионин; N-Формил (метил) гомоцистеин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| Сокращения | fMet |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| Характеристики | |
| C6ЧАС11NО3S | |
| Молярная масса | 177,22 г / моль |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
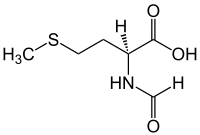
N-Формилметионин (fMet,[1] HCO-Met,[2] For-Met[2]) является производной от аминокислота метионин в котором формил группа добавлена в амино- группа. Он специально используется для инициации синтез белка из бактериальный и органеллар гены и могут быть удалены посттрансляционный.
fMet играет решающую роль в синтезе белка бактериями, митохондрии и хлоропласты. Не используется в цитозольный белковый синтез эукариоты, где эукариотический ядерные гены находятся переведено. Он также не используется Археи. В организме человека fMet распознается иммунной системой как инородный материал или как сигнал тревоги, исходящий от поврежденных клеток, и стимулирует организм бороться с потенциальной инфекцией.
Функция в синтезе белка
fMet - исходный остаток в синтезе белки у бактерий, и, следовательно, находится в N-терминал растущего полипептид. fMet доставляется в рибосома (30S) - комплекс мРНК специализированным тРНК (тРНКfMet) который имеет 3'-UAC-5 ' антикодон способный связываться с началом 5'-AUG-3 ' кодон расположен на мРНК. fMet, таким образом, кодируется тем же кодон как метионин; однако AUG также является перевод кодон инициации. Когда кодон используется для инициации, fMet используется вместо метионина, тем самым образуя первую аминокислоту как пептид цепь синтезируется. Когда тот же кодон появляется позже в мРНК, используется нормальный метионин. Многие организмы используют вариации этого основного механизма.
Присоединение формильной группы к метионину катализируется фермент метионил-тРНК формилтрансфераза. Эта модификация выполняется после того, как метионин был загружен на тРНК.fMet к аминоацил-тРНК синтетаза.
Сам метионин может быть загружен либо на тРНК.fMet или тРНКВстретились. Однако трансформилаза будет катализировать присоединение формильной группы к метионину, только если метионин был загружен на тРНК.fMet, а не на тРНКВстретились.
В N-концевой fMet удаляется из большинства белков, как хозяйских, так и рекомбинантных, в результате последовательности двух ферментативных реакций. Первый, пептид деформилаза деформирует его, превращая остаток обратно в нормальный метионин. потом метионин аминопептидаза (MAP) удаляет остатки из цепочки.[3]
В митохондрии из эукариотический клетки, в том числе человеческие, и хлоропласты из растение клетки также инициируют синтез белка с помощью fMet. Учитывая, что митохондрии и хлоропласты имеют этот начальный синтез белка с fMet, как и бактерии, это было приведено в качестве доказательства эндосимбиотическая теория.[4]
Актуальность в иммунологии
Поскольку fMet присутствует в белках, производимых бактериями, но не в белках, производимых эукариоты (кроме органелл, полученных из бактерий), иммунная система может использовать его, чтобы отличить себя от чужого. Полиморфноядерные клетки может связывать белки, начиная с fMet, и использовать их для привлечения циркулирующей крови лейкоциты а затем стимулировать микробицидную активность, такую как фагоцитоз.[5][6][7]
Поскольку fMet присутствует в белках, созданных митохондриями и хлоропластами, более поздние теории не рассматривают его как молекулу, которую иммунная система может использовать, чтобы отличить себя от чужого.[8] Вместо этого fMet-содержащий олигопептиды и белки, по-видимому, высвобождаются митохондриями поврежденных тканей, а также поврежденными бактериями, и поэтому их можно квалифицировать как «тревожный» сигнал, как обсуждается в Модель опасности иммунитета. Прототипом олигопептида, содержащего fMet, является N-формилметионин-лейцил-фенилаланин (FMLP), который активирует лейкоциты и другие типы клеток, связываясь с этими клетками. рецептор формилового пептида 1 (FPR1) и рецептор формилового пептида 2 (FPR2) G-белковые рецепторы (смотрите также рецептор формилового пептида 3 ). Действуя через эти рецепторы, олигопептиды и белки, содержащие fMet, являются частью врожденная иммунная система; они действуют, чтобы вызвать острые воспаление ответы, но в других условиях действуют, чтобы подавлять и разрешать эти ответы. fMet-содержащие олигопептиды и белки также участвуют в других физиологических и патологических реакциях.
Смотрите также
Рекомендации
- ^ PubChem. «N-Формил-DL-метионин». pubchem.ncbi.nlm.nih.gov. Получено 2020-10-24.
- ^ а б Номенклатура и символика аминокислот и пептидов, 3AA-18 и 3AA-19
- ^ Шерман Ф., Стюарт Дж. В., Цунасава С. (июль 1985 г.). «Метионин или не метионин в начале белка». BioEssays. 3 (1): 27–31. Дои:10.1002 / bies.950030108. PMID 3024631. S2CID 33735710.
- ^ Альбертс, Брюс (18 ноября 2014 г.). Молекулярная биология клетки (Шестое изд.). Нью-Йорк, штат Нью-Йорк. п. 800. ISBN 978-0-8153-4432-2. OCLC 887605755.
- ^ Иммунология в MCG 1 / phagstep
- ^ «Врожденная иммунная система: рецепторы распознавания образов, антиген-неспецифические противомикробные молекулы тела и цитокины». Архивировано из оригинал 27 июля 2010 г.
- ^ Детмерс П.А., Райт С.Д., Олсен Э., Кимбалл Б., Кон З.А. (сентябрь 1987 г.). «Агрегация рецепторов комплемента на нейтрофилах человека в отсутствие лиганда». Журнал клеточной биологии. 105 (3): 1137–45. Дои:10.1083 / jcb.105.3.1137. ЧВК 2114803. PMID 2958480.
- ^ Zhang Q, Raoof M, Chen Y, Sumi Y, Sursal T, Junger W, Brohi K, Itagaki K, Hauser CJ (4 марта 2010 г.). «Циркулирующие митохондриальные DAMPs вызывают воспалительную реакцию на травму». Природа. 464 (7285): 104–107. Bibcode:2010Натура.464..104Z. Дои:10.1038 / природа08780. ЧВК 2843437. PMID 20203610.
внешняя ссылка
- N-Формилметионин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
