Коллективный иммунитет - Herd immunity

Коллективный иммунитет (также называемый стадный эффект, иммунитет сообщества, иммунитет населения, или же социальный иммунитет) является формой косвенной защиты от заразный болезнь, которая возникает, когда достаточный процент населения стал невосприимчивый инфекции, будь то через вакцинация или предыдущие инфекции, тем самым снижая вероятность заражения людей с недостаточным иммунитетом.[1][2] Люди с иммунитетом вряд ли будут способствовать передаче болезни, разрывая цепочки инфекции, которая останавливает или замедляет распространение болезни.[3] Чем больше доля иммунных индивидуумов в сообществе, тем меньше вероятность того, что неиммунные люди вступят в контакт с инфекционным индивидуумом.[1]
Люди могут стать невосприимчивым вылечившись от более раннего заражения или через вакцинация.[3] Некоторые люди не могут получить иммунитет из-за заболеваний, например, иммунодефицит или же иммуносупрессия, и для этой группы коллективный иммунитет является важнейшим методом защиты.[4][5] По достижении порога коллективного иммунитета болезнь постепенно исчезает из популяции.[5] Это устранение, если оно будет достигнуто во всем мире, может привести к необратимому сокращению числа инфекций до нуля, что называется искоренение.[6] Коллективный иммунитет, созданный с помощью вакцинации, в конечном итоге способствовал искоренению оспа в 1977 г. и способствовал сокращению числа других заболеваний.[7] Коллективный иммунитет распространяется только на заразительный болезнь, что означает, что она передается от одного человека к другому.[5] Столбняк, например, является инфекционным, но не заразным, поэтому коллективный иммунитет не применяется.[4]
Коллективный иммунитет был признан естественным явлением в 1930-х годах, когда было обнаружено, что после того, как значительное число детей приобрели иммунитет к корь временно снизилось количество новых случаев инфицирования, в том числе среди непривитых.[8] С тех пор массовая вакцинация для повышения коллективного иммунитета стала обычным явлением и оказалась успешной в предотвращении распространения многих инфекционных заболеваний.[9] Противодействие вакцинации бросает вызов коллективному иммунитету, позволяя предотвращаемым заболеваниям сохраняться или возвращаться в группы населения с недостаточным уровнем вакцинации.[10][11][12]
Точный порог коллективного иммунитета (HIT) варьируется в зависимости от заболевания. Пример заболевания с низким порогом: грипп, с HIT 33–44%. Примером болезни с высоким порогом является корь, с HIT 92–95%.
Последствия
Защита людей без иммунитета
Некоторые люди либо не могут развить иммунитет после вакцинации, либо по медицинским причинам не могут быть вакцинированы.[13][4][14] Новорожденные дети слишком молоды, чтобы получать много вакцин, либо по соображениям безопасности, либо по причине пассивный иммунитет делает вакцину неэффективной.[15] Лица с иммунодефицитом из-за ВИЧ / СПИД, лимфома, лейкемия, Костный мозг рак, ослабленный селезенка, химиотерапия, или же лучевая терапия могли потерять какой-либо иммунитет, который у них был ранее, и вакцины могут быть им бесполезны из-за их иммунодефицита.[4][14][15][16]
У части вакцинированных может не развиться долгосрочный иммунитет.[1][17][18] Вакцина противопоказания может помешать вакцинации некоторых людей.[14] Помимо отсутствия иммунитета, люди в одной из этих групп могут подвергаться большему риску развития осложнений от инфекции из-за своего медицинского статуса, но они все же могут быть защищены, если достаточно большой процент населения имеет иммунитет.[4][14][18][19]
Высокий уровень иммунитета в одной возрастной группе может создать коллективный иммунитет для других возрастных групп.[7] Вакцинация взрослых против коклюш снижает заболеваемость коклюшем у младенцев, слишком маленьких для вакцинации, которые подвергаются наибольшему риску осложнений от болезни.[20][21] Это особенно важно для близких членов семьи, на которых приходится большая часть случаев передачи инфекции младенцам.[7][18] Таким же образом дети, получающие вакцины против пневмококка, снижают заболеваемость пневмококком среди младших, не вакцинированных братьев и сестер.[22] Вакцинация детей от пневмококка и ротавируса привела к снижению пневмококк - и ротавирус - относимые госпитализации для детей старшего возраста и взрослых, которые обычно не получают эти вакцины.[22][23][24] Грипп (грипп) более серьезен у пожилых людей, чем в более молодых возрастных группах, но вакцины против гриппа неэффективность в этой демографической группе из-за ослабления иммунной системы с возрастом.[7][25] Тем не менее, приоритезация детей школьного возраста для вакцинации от сезонного гриппа, которая более эффективна, чем вакцинация пожилых людей, создает определенную степень защиты для пожилых людей.[7][25]
За инфекции, передающиеся половым путем (ИППП) высокий уровень иммунитета у одного пола индуцирует коллективный иммунитет у обоих полов.[9][26][27] Вакцины против ИППП, предназначенные для представителей одного пола, приводят к значительному снижению заболеваемости ИППП у обоих полов, если вакцинация распространяется на людей целевого пола.[26][27][28] Однако коллективный иммунитет от женской вакцинации не распространяется на гомосексуальных мужчин.[27] Если потребление вакцины среди целевого пола низкое, то может потребоваться вакцинация другого пола, чтобы целевой пол мог быть в достаточной степени защищен.[26][27] Поведение, сопряженное с высоким риском, затрудняет устранение ИППП, поскольку, несмотря на то, что большинство инфекций происходит среди лиц с умеренным риском, большинство случаев передачи происходит из-за лиц, ведущих образ жизни с высоким риском.[9] По этим причинам в определенных группах населения может потребоваться иммунизация лиц из группы высокого риска или лиц обоего пола для установления коллективного иммунитета.[9][27]
Эволюционное давление
Коллективный иммунитет сам по себе действует как эволюционное давление на определенные вирусы, влияющие вирусная эволюция путем поощрения производства новых штаммов, в данном случае называемых мутантами-ускользнувшими, которые способны «ускользать» от коллективного иммунитета и легче распространяться.[29][30] На молекулярном уровне вирусы избавляются от коллективного иммунитета через антигенный дрейф, когда мутации накапливаются в части вирусный геном который кодирует поверхность вируса антиген, обычно белок вируса капсид, вызывая изменение вирусного эпитоп.[31][32] В качестве альтернативы, перегруппировка отдельных сегментов вирусного генома, или антигенный сдвиг, что чаще встречается при большом количестве штаммов в обращении, также может давать новые серотипы.[29][33] Когда происходит одно из этих событий, Т-клетки памяти больше не распознают вирус, поэтому люди не застрахованы от доминирующего циркулирующего штамма.[32][33] И для гриппа, и для норовирус, эпидемии временно вызывают коллективный иммунитет, пока не появится новый доминирующий штамм, вызывающий последовательные волны эпидемий.[31][33] Поскольку эта эволюция бросает вызов коллективному иммунитету, широко нейтрализующие антитела и разрабатываются «универсальные» вакцины, которые могут обеспечить защиту, выходящую за рамки определенного серотипа.[30][34][35]
Замена серотипа
Серотип замена или смещение серотипа может произойти, если распространенность определенного серотипа снижается из-за высокого уровня иммунитета, позволяя другим серотипам заменять его.[36][37] Первоначальные вакцины против Пневмококк значительно снижается носоглоточное носительство вакцинных серотипов (VT), в том числе устойчивый к антибиотикам типы,[22][38] только для того, чтобы полностью компенсировать рост числа невакцинных серотипов (NVT).[22][36][37] Это не привело к пропорциональному увеличению заболеваемости, поскольку NVT были менее инвазивными, чем VT.[36] С того времени, пневмококковые вакцины которые обеспечивают защиту от появляющихся серотипов, были внедрены и успешно противодействуют их появлению.[22] Возможность перехода в будущем остается, поэтому дальнейшие стратегии по решению этой проблемы включают расширение охвата ЖТ и разработку вакцин, в которых используется либо убитые целые клетки, которые имеют больше поверхностных антигенов или белков, присутствующих в нескольких серотипах.[22][39]
Искоренение болезней
Если коллективный иммунитет установлен и поддерживается в популяции в течение достаточного времени, болезнь неизбежно исключается - эндемичные передачи больше не происходят.[5] Если элиминация будет достигнута во всем мире, а число случаев навсегда сократится до нуля, то болезнь может быть объявлена искорененной.[6] Искоренение таким образом, можно считать конечным результатом или конечным результатом здравоохранение инициативы по контролю за распространением инфекционных заболеваний.[6][7]
Преимущества искоренения включают прекращение всех болезненность и смертность, вызванная заболеванием, финансовая экономия для отдельных лиц, поставщиков медицинских услуг и правительств, а также предоставление ресурсов, используемых для борьбы с болезнью, для использования в других местах.[6] На сегодняшний день с помощью коллективного иммунитета и вакцинации ликвидированы два заболевания: чума крупного рогатого скота и оспа.[1][7][40] Усилия по искоренению, основанные на коллективном иммунитете, в настоящее время продолжаются. полиомиелит, хотя гражданские волнения и недоверие к современной медицине сделали это трудным.[1][41] Обязательная вакцинация может оказаться полезным для усилий по искоренению, если вакцинацию решит недостаточное количество людей.[42][43][44][45]
Бесплатная езда
Коллективный иммунитет уязвим для проблема безбилетника.[46] Лица, у которых отсутствует иммунитет, особенно те, кто предпочитает не вакцинироваться, бесплатно избавляются от коллективного иммунитета, созданного теми, у кого есть иммунитет.[46] По мере увеличения количества безбилетников в популяции вспышки предотвратимых заболеваний становятся более частыми и более серьезными из-за потери коллективного иммунитета.[10][11][12][43][45] Люди могут выбрать бесплатный проезд по разным причинам, включая убеждение, что вакцины неэффективны,[47] или что риски, связанные с вакцинами, выше, чем риски, связанные с инфекцией,[1][11][12][47] недоверие к вакцинам или чиновникам общественного здравоохранения,[48] увлечение или же групповое мышление,[43][49] социальные нормы или давление сверстников,[47] и религиозные верования.[11] Некоторые люди с большей вероятностью решат не получать вакцины, если уровень вакцинации достаточно высок, чтобы убедить человека в том, что ему или ей может не потребоваться вакцинация, поскольку достаточный процент других уже имеет иммунитет.[1][45]
Механика
| Болезнь | Передача инфекции | р0 | УДАРИТЬ |
|---|---|---|---|
| Корь | В воздухе | 12–18 | 92–95% |
| Коклюш | Капля в воздухе | 12–17[51] | 92–94% |
| Дифтерия | Слюна | 6–7 | 83–86% |
| Краснуха | Капля в воздухе | ||
| Оспа | 5–7 | 80–86% | |
| Полиомиелит | Фекально-оральный путь | ||
| Свинка | Капля в воздухе | 4–7 | 75–86% |
| COVID-19 (COVID-19 пандемия ) | 2.5–4[52][53] | 60–75% | |
| ОРВИ (2002–2004 гг. Вспышка атипичной пневмонии. ) | 2–5[54] | 50–80% | |
| Эбола (Эпидемия вируса Эбола в Западной Африке ) | Телесные жидкости | 1.5–2.5[55] | 33–60% |
| Грипп (пандемии гриппа ) | Капля в воздухе | 1.5–1.8[51] | 33–44% |
Люди, невосприимчивые к заболеванию, действуют как барьер на пути распространения болезни, замедляя или предотвращая передачу болезни другим людям.[3] Иммунитет можно получить путем естественной инфекции или искусственным путем, например, вакцинацией.[3] Когда критическая часть населения приобретает иммунитет, это называется порог коллективного иммунитета (HIT) или уровень коллективного иммунитета (HIL), болезнь может больше не сохраняться в популяции, перестать эндемичный.[5][29]
Критическое значение или порог в данной популяции - это точка, в которой болезнь достигает предела. эндемичное устойчивое состояние, что означает, что уровень заражения не растет и не снижается. экспоненциально. Этот порог может быть рассчитан из эффективное репродуктивное число ре, который получается, если взять произведение базовый номер репродукции р0, среднее количество новых инфекций, вызванных каждым случаем в полностью восприимчивой популяции, которая является однородной или хорошо перемешанной, что означает, что каждый человек может вступить в контакт с любым другим восприимчивым человеком в популяции,[9][29][42] и S, доля населения, восприимчивого к инфекции, и установка этого продукта равным 1:
S можно переписать как (1 - п), куда п доля населения, обладающего иммунитетом, так что п + S равно единице. Затем уравнение можно переставить, чтобы разместить п сам по себе следующим образом:
- так так
С п будучи сам по себе в левой части уравнения, его можно переименовать как пc, представляющий критическую часть населения, которая должна обладать иммунитетом, чтобы остановить передачу болезни, что совпадает с «порогом коллективного иммунитета» HIT.[9] р0 функционирует как мера заразительности, поэтому низкий р0 значения связаны с более низкими HIT, тогда как более высокие р0s приводит к более высоким HIT.[29][42] Например, HIT для болезни с р0 2 составляет теоретически только 50%, тогда как болезнь с р0 из 10 теоретическая HIT составляет 90%.[29]
Когда эффективное число репродукций ре Если инфекционное заболевание снижается до 1 нового человека на инфекцию, то количество случаев заболевания в популяции постепенно уменьшается до тех пор, пока болезнь не будет ликвидирована.[9][29][56] Если население невосприимчиво к заболеванию, превышающему HIT этого заболевания, количество случаев сокращается более быстрыми темпами, вероятность возникновения вспышек еще ниже, а возникающие вспышки меньше, чем они были бы в противном случае.[1][9] Если эффективное число воспроизводимых увеличивается до более чем 1, то болезнь не находится в стабильном состоянии и не уменьшается в заболеваемость, но активно распространяется среди населения и заражает большее количество людей, чем обычно.[43][56]
В этих расчетах предполагается, что популяции однородны или хорошо перемешаны, что означает, что каждый человек вступает в контакт с каждым другим человеком, в то время как в действительности популяции лучше описывать как социальные сети, поскольку люди имеют тенденцию группироваться вместе, оставаясь в относительно тесном контакте. с ограниченным числом других лиц. В этих сетях передача происходит только между теми, кто географически или физически близок друг к другу.[1][42][43] Форма и размер сети, вероятно, изменят HIT заболевания, делая заболеваемость более или менее распространенной.[29][42]
В гетерогенных популяциях р0 считается мерой количества случаев, генерируемых «типичным» заразным человеком, которое зависит от того, как люди в сети взаимодействуют друг с другом.[1] Взаимодействия внутри сетей более обычны, чем между сетями, и в этом случае наиболее тесно связанные сети легче передают болезни, что приводит к более высокому р0 и более высокий HIT, чем требовалось бы в менее подключенной сети.[1][43] В сетях, которые либо предпочитают не приобретать иммунитет, либо недостаточно иммунизированы, заболевания могут сохраняться, несмотря на то, что они не существуют в более иммунизированных сетях.[43]
Перескок
Кумулятивная доля людей, заразившихся во время вспышки болезни, может превышать HIT. Это связано с тем, что HIT не представляет собой точку, в которой болезнь перестает распространяться, а, скорее, точку, в которой каждый инфицированный человек заражает в среднем менее одного дополнительного человека. Когда достигается HIT, количество дополнительных заражений начинает сокращаться, но не сразу падает до нуля. Разница между совокупной долей инфицированных людей и теоретическим HIT известна как превышение.[57][58][59]
Повышает
Вакцинация
Основной способ повысить уровень иммунитета у населения - вакцинация.[1][60] Вакцинация изначально основана на наблюдении, что доярки подвергаются коровья оспа были невосприимчивы к оспе, поэтому практика прививка Люди с вирусом коровьей оспы начинали как средство профилактики оспы.[41] Хорошо разработанные вакцины обеспечивают защиту гораздо более безопасным способом, чем естественные инфекции, поскольку вакцины обычно не вызывают заболеваний, от которых они защищают, а серьезные побочные эффекты встречаются значительно реже, чем осложнения от естественных инфекций.[61][62]
В иммунная система не различает естественные инфекции и вакцины, образуя активный ответ к обоим, поэтому иммунитет, вызванный вакцинацией, аналогичен тому, что произошло бы при заражении и выздоровлении от болезни.[63] Чтобы добиться коллективного иммунитета с помощью вакцинации, производители вакцин стремятся производить вакцины с низким процентом неудач и политики стремятся поощрять их использование.[60] После успешного внедрения и широкого применения вакцины можно наблюдать резкое снижение заболеваемости болезнями, от которых она защищает, что снижает количество госпитализаций и смертей, вызванных такими заболеваниями.[64][65][66]
Если предположить, что вакцина эффективна на 100%, то уравнение, используемое для расчета порога коллективного иммунитета, можно использовать для расчета уровня вакцинации, необходимого для устранения болезни, записанного как Vc.[1] Однако вакцины обычно несовершенны, поэтому эффективность Eвакцины необходимо учитывать:
Из этого уравнения можно заметить, что если E меньше (1 - 1 /р0), то устранить заболевание невозможно, даже если вакцинировано все население.[1] Точно так же ослабление иммунитета, вызванного вакциной, что происходит с бесклеточные коклюшные вакцины, требует более высоких уровней ревакцинации для поддержания коллективного иммунитета.[1][20] Если болезнь перестала быть эндемической для популяции, тогда естественные инфекции больше не способствуют сокращению доли восприимчивой популяции. Только вакцинация способствует этому снижению.[9] Связь между охватом вакциной и ее эффективностью и заболеваемостью может быть продемонстрирована путем вычитания произведения эффективности вакцины на долю вакцинированного населения. пv, из уравнения порога коллективного иммунитета следующим образом:
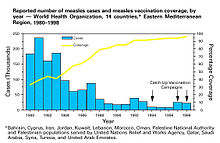
Из этого уравнения видно, что при прочих равных условиях ("при прочих равных условиях "), любое увеличение охвата вакцинацией или эффективности вакцины, включая любое увеличение, превышающее HIT заболевания, дополнительно снижает количество случаев заболевания.[9] Скорость снижения заболеваемости зависит от заболевания. р0, при заболеваниях с нижним р0 значения испытывают более резкое снижение.[9]
Вакцины обычно содержат как минимум один противопоказание для определенной группы населения по медицинским показаниям, но если эффективность и охват достаточно высоки, коллективный иммунитет может защитить этих людей.[13][16][19] На эффективность вакцины часто, но не всегда, отрицательно влияет пассивный иммунитет,[67][68] поэтому для некоторых вакцин рекомендуются дополнительные дозы, в то время как другие не вводятся до тех пор, пока человек не потеряет пассивный иммунитет.[15][19]
Пассивный иммунитет
Индивидуальный иммунитет можно получить и пассивно, если: антитела возбудителю передаются от одного человека к другому. Это может произойти естественным путем, в результате чего материнский антитела, прежде всего иммуноглобулин G антитела, передаются через плацента И в молозиво плодам и новорожденным.[69][70] Пассивный иммунитет можно получить и искусственно, если восприимчивому человеку вводят антитела из сыворотка или же плазма иммунного человека.[63][71]
Защита, создаваемая пассивным иммунитетом, проявляется немедленно, но ослабевает в течение нескольких недель или месяцев, поэтому любой вклад в коллективный иммунитет носит временный характер.[5][63][72] При заболеваниях, которые особенно тяжелы среди плодов и новорожденных, таких как грипп и столбняк, беременных женщин можно иммунизировать, чтобы передать антитела ребенку.[13][73][74] Таким же образом группы высокого риска, которые либо с большей вероятностью переживут инфекцию, либо с большей вероятностью разовьются осложнения от инфекции, могут получать препараты антител для предотвращения этих инфекций или уменьшения тяжести симптомов.[71]
Анализ выгоды и затрат
Коллективный иммунитет часто учитывается при проведении анализ затрат и выгод программ вакцинации. Это рассматривается как положительный внешний эффект высокого уровня иммунитета, что дает дополнительную пользу в виде снижения заболеваемости, чего не произошло бы, если бы в популяции не сформировался коллективный иммунитет.[75][76] Следовательно, включение коллективного иммунитета в анализ затрат и выгод приводит как к более благоприятному соотношению рентабельности или рентабельности, так и к увеличению числа случаев заболеваний, предотвращаемых с помощью вакцинации.[76] Планы исследований, проводимые для оценки пользы коллективного иммунитета, включают регистрацию заболеваемости в домохозяйствах с вакцинированным членом, рандомизацию населения в одном географическом районе, которое будет вакцинировано или нет, и наблюдение за заболеваемостью до и после начала программы вакцинации.[77] Исходя из этого, можно заметить, что заболеваемость может снизиться до уровня, превышающего тот, который можно предсказать на основании одной только прямой защиты, что указывает на то, что коллективный иммунитет внес свой вклад в снижение.[77] Когда замена серотипа учитывается, это снижает прогнозируемые преимущества вакцинации.[76]
История
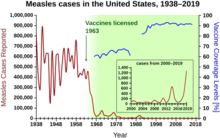
Термин «коллективный иммунитет» был придуман в 1923 году.[78] Коллективный иммунитет был впервые признан естественным явлением в 1930-х годах, когда А. В. Хедрих опубликовал исследование эпидемиология кори в Балтимор и обратили внимание на то, что после того, как многие дети приобрели иммунитет к кори, количество новых инфекций временно снизилось, в том числе среди восприимчивых детей.[79][8] Несмотря на эти знания, попытки контролировать и ликвидировать корь были безуспешными до тех пор, пока массовая вакцинация с использованием вакцина против кори началось в 1960-х годах.[8] Массовая вакцинация, обсуждения искоренения болезней и анализ затрат и выгод вакцинации впоследствии побудили к более широкому использованию этого термина. коллективный иммунитет.[1] В 1970-х годах была разработана теорема, используемая для расчета порога коллективного иммунитета к заболеванию.[1] Вовремя кампания по искоренению оспы в 1960-х и 1970-х годах практика кольцевая вакцинация, неотъемлемой частью которого является коллективный иммунитет, изначально был способом иммунизации каждого человека в «кольце» вокруг инфицированного человека, чтобы предотвратить распространение вспышек.[80]
С момента введения массовой и кольцевой вакцинации возникли сложности и проблемы с коллективным иммунитетом.[1][60] При моделировании распространения инфекционных заболеваний изначально был сделан ряд предположений, а именно, что все популяции восприимчивы и хорошо перемешаны, что не соответствует действительности, поэтому были разработаны более точные уравнения.[1] В последние десятилетия было признано, что доминирующий штамм микроорганизма в циркуляции может измениться из-за коллективного иммунитета, либо из-за коллективного иммунитета, действующего как эволюционное давление, либо из-за того, что коллективный иммунитет против одного штамма позволил распространиться другому уже существующему штамму.[31][37] Возникающие или продолжающиеся опасения и споры по поводу вакцинации привели к снижению или устранению коллективного иммунитета в определенных сообществах, что позволяет предотвратить болезни, сохраняющиеся в этих сообществах или возвращающиеся в них.[10][11][12]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s Хорошо, P .; Eames, K .; Хейманн, Д. Л. (1 апреля 2011 г.). "'Коллективный иммунитет: приблизительное руководство ". Клинические инфекционные болезни. 52 (7): 911–16. Дои:10.1093 / cid / cir007. PMID 21427399.
- ^ Гордис, Л. (2013). Эпидемиология. Elsevier Health Sciences. С. 26–27. ISBN 978-1455742516. Получено 29 марта 2015.
- ^ а б c d Меррилл, Р. М. (2013). Введение в эпидемиологию. Издательство "Джонс и Бартлетт". С. 68–71. ISBN 978-1449645175. Получено 29 марта 2015.
- ^ а б c d е "Коллективный иммунитет". Oxford Vaccine Group, Оксфордский университет. Получено 12 декабря 2017.
- ^ а б c d е ж Somerville, M .; Кумаран, К .; Андерсон, Р. (2012). Обзор общественного здравоохранения и эпидемиологии. Джон Вили и сыновья. С. 58–59. ISBN 978-1118308646. Получено 29 марта 2015.
- ^ а б c d Клифф, А .; Смоллмен-Рейнор, М. (2013). Оксфордский учебник по контролю за инфекционными заболеваниями: географический анализ от средневекового карантина до глобальной ликвидации. Издательство Оксфордского университета. С. 125–36. ISBN 978-0199596614. Получено 29 марта 2015.
- ^ а б c d е ж грамм Kim, T. H .; Jonhstone, J .; Лоеб, М. (сентябрь 2011 г.). «Эффект стада вакцины». Скандинавский журнал инфекционных болезней. 43 (9): 683–89. Дои:10.3109/00365548.2011.582247. ЧВК 3171704. PMID 21604922.
- ^ а б c *Hinman, A. R .; Оренштейн, В. А .; Папания, М. Дж. (1 мая 2004 г.). «Эволюция стратегий элиминации кори в США». Журнал инфекционных болезней. 189 (Приложение 1): S17–22. Дои:10.1086/377694. PMID 15106084.
*Sencer, D. J .; Тупой, H. B .; Ленгмюр, А. Д. (март 1967 г.). «Эпидемиологическая основа искоренения кори в 1967 г.». Отчеты общественного здравоохранения. 82 (3): 253–56. Дои:10.2307/4592985. JSTOR 4592985. ЧВК 1919891. PMID 4960501. - ^ а б c d е ж грамм час я j k Гарнетт, Г. П. (1 февраля 2005 г.). «Роль коллективного иммунитета в определении эффекта вакцин против заболеваний, передающихся половым путем». Журнал инфекционных болезней. 191 (Приложение 1): S97–106. Дои:10.1086/425271. PMID 15627236.
- ^ а б c Квадри-Шериф, М .; Хендрикс, К. С .; Даунс, С. М .; Sturm, L.A .; Zimet, G.D .; Финнелл, С. М. (сентябрь 2012 г.). «Роль коллективного иммунитета в решении родителей вакцинировать детей: систематический обзор». Педиатрия. 130 (3): 522–30. Дои:10.1542 / пед.2012-0140. PMID 22926181.
- ^ а б c d е Dubé, E .; Laberge, C .; Guay, M .; Bramadat, P .; Рой, Р .; Беттингер, Дж. (Август 2013 г.). «Неуверенность в отношении вакцины: обзор». Человеческие вакцины и иммунотерапевтические препараты. 9 (8): 1763–73. Дои:10.4161 / hv.24657. ЧВК 3906279. PMID 23584253.
- ^ а б c d Ропейк Д. (август 2013 г.). «Как общество должно реагировать на риск отказа от вакцины». Человеческие вакцины и иммунотерапевтические препараты. 9 (8): 1815–18. Дои:10.4161 / hv.25250. ЧВК 3906287. PMID 23807359.
- ^ а б c Муньос, Ф. М. (2013). «Материнская иммунизация: обновление для педиатров». Педиатрические анналы. 42 (8): 153–58. Дои:10.3928/00904481-20130723-09. PMID 23910028.
- ^ а б c d Cesaro, S .; Giacchino, M .; Fioredda, F .; и другие. (2014). «Методические указания по вакцинации больных детской гематологией и онкологией». Biomed Res. Int. 2014: 707691. Дои:10.1155/2014/707691. ЧВК 4020520. PMID 24868544.
- ^ а б c Национальный центр иммунизации и респираторных заболеваний (2011 г.). «Общие рекомендации по иммунизации - рекомендации Консультативного комитета по практике иммунизации (ACIP)». MMWR. Рекомендации и отчеты / Центры контроля заболеваний. 60 (2): 1–64. PMID 21293327.
- ^ а б Вулф, Р. М. (2012). «Обновленная информация об иммунизации взрослых». Журнал Американского совета семейной медицины. 25 (4): 496–510. Дои:10.3122 / jabfm.2012.04.100274. PMID 22773718.
- ^ Эспозито, S; Bosis, S; Morlacchi, L; Багги, Э; Сабатини, C; Принципи, Н. (2012). «Можно ли защитить младенцев с помощью материнской вакцинации?». Клиническая микробиология и инфекции. 18 (Дополнение 5): 85–92. Дои:10.1111 / j.1469-0691.2012.03936.x. PMID 22862749.
- ^ а б c Rakel, D .; Ракель, Р. Э. (2015). Учебник семейной медицины. Elsevier Health Sciences. С. 99, 187. ISBN 978-0323313087. Получено 30 марта 2015.
- ^ а б c Тульчинский, Т. Н .; Варавикова, Е. А. (2014). Новое общественное здравоохранение: введение в 21 век. Академическая пресса. С. 163–82. ISBN 978-0124157675. Получено 30 марта 2015.
- ^ а б МакГирр, А; Фисман, Д. Н. (2015). «Продолжительность иммунитета против коклюша после иммунизации DTaP: метаанализ» (PDF). Педиатрия. 135 (2): 331–43. Дои:10.1542 / педы.2014-1729. PMID 25560446. S2CID 8273985.
- ^ Зепп, Ф; Heininger, U; Мертсола, Дж; Bernatowska, E; Guiso, N; Роорд, Дж; Tozzi, A.E .; Ван Дамм, П. (2011). «Обоснование бустерной вакцинации против коклюша на протяжении всей жизни в Европе». Ланцетные инфекционные болезни. 11 (7): 557–70. Дои:10.1016 / S1473-3099 (11) 70007-X. PMID 21600850.
- ^ а б c d е ж Pittet, L.F .; Посфай-Барбе, К. М. (2012). «Пневмококковые вакцины для детей: глобальный приоритет общественного здравоохранения». Клиническая микробиология и инфекции. 18 (Дополнение 5): 25–36. Дои:10.1111 / j.1469-0691.2012.03938.x. PMID 22862432.
- ^ Накагоми, О; Итурриза-Гомара, М; Накагоми, Т; Канлифф, Н. А. (2013). «Включение ротавирусной вакцины в национальный календарь иммунизации в Соединенном Королевстве: обзор». Мнение эксперта по биологической терапии. 13 (11): 1613–21. Дои:10.1517/14712598.2013.840285. PMID 24088009. S2CID 5405583.
- ^ Lopman, B.A .; Payne, D.C .; Tate, J. E .; Patel, M. M .; Cortese, M. M .; Парашар, У. Д. (2012). «Постлицензионный опыт вакцинации против ротавирусной инфекции в странах с высоким и средним уровнем доходов; 2006–2011 годы». Текущее мнение в вирусологии. 2 (4): 434–42. Дои:10.1016 / j.coviro.2012.05.002. PMID 22749491.
- ^ а б Ким, Т. Х. (2014). «Сезонный грипп и эффект стада вакцины». Клинические и экспериментальные исследования вакцин. 3 (2): 128–32. Дои:10.7774 / cevr.2014.3.2.128. ЧВК 4083064. PMID 25003085.
- ^ а б c Lowy, D. R .; Шиллер, Дж. Т. (2012). «Снижение риска рака, связанного с ВПЧ, во всем мире». Исследования по профилактике рака. 5 (1): 18–23. Дои:10.1158 / 1940-6207.CAPR-11-0542. ЧВК 3285475. PMID 22219162.
- ^ а б c d е Лензи, А; Мирон, В; Gentile, V; Bartoletti, R; Ficarra, V; Фореста, С; Мариани, L; Маццоли, S; Parisi, S.G .; Перино, А; Пикардо, М; Зотти, К. М. (2013). "Конференция Римского консенсуса - заявление; болезни вируса папилломы человека у мужчин". BMC Public Health. 13: 117. Дои:10.1186/1471-2458-13-117. ЧВК 3642007. PMID 23391351.
- ^ Гарланд, С. М .; Скиннер, S. R .; Браттон, Дж. М. (2011). «Вакцинация подростков и молодых взрослых против ВПЧ в Австралии: достижения и проблемы». Профилактическая медицина. 53 (Приложение 1): S29–35. Дои:10.1016 / j.ypmed.2011.08.015. PMID 21962468.
- ^ а б c d е ж грамм час Rodpothong, P; Ауеваракул, П (2012). «Вирусная эволюция и эффективность передачи». Всемирный журнал вирусологии. 1 (5): 131–34. Дои:10.5501 / wjv.v1.i5.131. ЧВК 3782273. PMID 24175217.
- ^ а б Corti, D; Ланзавеккья, А (2013). «Широко нейтрализующие противовирусные антитела». Ежегодный обзор иммунологии. 31: 705–42. Дои:10.1146 / аннурев-иммунол-032712-095916. PMID 23330954.
- ^ а б c Bull, R.A .; Уайт, П. А. (2011). «Механизмы эволюции норовируса GII.4». Тенденции в микробиологии. 19 (5): 233–40. Дои:10.1016 / j.tim.2011.01.002. PMID 21310617.
- ^ а б Рамани, S; Атмар, Р. Л .; Эстес, М. К. (2014). «Эпидемиология норовирусов человека и последние данные о разработке вакцин». Текущее мнение в гастроэнтерологии. 30 (1): 25–33. Дои:10.1097 / MOG.0000000000000022. ЧВК 3955997. PMID 24232370.
- ^ а б c Плешка, С (2013). «Обзор вирусов гриппа». Свиной грипп. Актуальные темы микробиологии и иммунологии. 370. С. 1–20. Дои:10.1007/82_2012_272. ISBN 978-3642368707. PMID 23124938.
- ^ Хан, Т; Мараско, В. А. (2011). «Структурные основы нейтрализации вируса гриппа». Летопись Нью-Йоркской академии наук. 1217 (1): 178–90. Bibcode:2011НЯСА1217..178Х. Дои:10.1111 / j.1749-6632.2010.05829.x. ЧВК 3062959. PMID 21251008.
- ^ Reperant, L.A .; Rimmelzwaan, G. F .; Остерхаус, А. Д. (2014). «Достижения в вакцинации против гриппа». Отчеты F1000Prime. 6: 47. Дои:10.12703 / п6-47. ЧВК 4047948. PMID 24991424.
- ^ а б c Weinberger, D. M .; Мэлли, Р. Липсич, М (2011). «Замена серотипа при заболевании после пневмококковой вакцины». Ланцет. 378 (9807): 1962–73. Дои:10.1016 / S0140-6736 (10) 62225-8. ЧВК 3256741. PMID 21492929.
- ^ а б c McEllistrem, M.C .; Нахм, М. Х. (2012). «Новые пневмококковые серотипы 6C и 6D: аномалия или предвестник». Клинические инфекционные болезни. 55 (10): 1379–86. Дои:10.1093 / cid / cis691. ЧВК 3478140. PMID 22903767.
- ^ Даган, Р. (2009). «Влияние пневмококковой конъюгированной вакцины на инфекции, вызванные устойчивостью к антибиотикам. Пневмококк". Клиническая микробиология и инфекции. 15 (Дополнение 3): 16–20. Дои:10.1111 / j.1469-0691.2009.02726.x. PMID 19366365.
- ^ Линч Дж., 3-й; Жанель, Г. Г. (2010). "Пневмококк: Эпидемиология и факторы риска, эволюция устойчивости к противомикробным препаратам и влияние вакцин ». Текущее мнение в области легочной медицины. 16 (3): 217–25. Дои:10.1097 / MCP.0b013e3283385653. PMID 20375783. S2CID 205784538.
- ^ Njeumi, F; Тейлор, Вт; Диалло, А; Миягишима, К; Pastoret, P.P .; Валлат, Б; Траоре, М (2012). «Долгий путь: краткий обзор ликвидации чумы крупного рогатого скота». Revue Scientifique et Technique (Международное бюро эпизоотии). 31 (3): 729–46. PMID 23520729.
- ^ а б Смит, К. А. (2013). «Оспа: можем ли мы извлечь уроки из пути к искоренению?». Индийский журнал медицинских исследований. 137 (5): 895–99. ЧВК 3734679. PMID 23760373.
- ^ а б c d е Перишич, А; Баух, К. Т. (2009). «Социальные сети контактов и искоренение болезней при добровольной вакцинации». PLOS вычислительная биология. 5 (2): e1000280. Bibcode:2009PLSCB ... 5E0280P. Дои:10.1371 / journal.pcbi.1000280. ЧВК 2625434. PMID 19197342.
- ^ а б c d е ж грамм Fu, F; Rosenbloom, D. I .; Ван, L; Новак, М. А. (2011). «Имитационная динамика прививочного поведения в социальных сетях» (PDF). Труды Королевского общества B: биологические науки. 278 (1702): 42–49. Дои:10.1098 / rspb.2010.1107. ЧВК 2992723. PMID 20667876.
- ^ Плетеный, S; Мальтезу, Х. К. (2014). «Болезни, предупреждаемые с помощью вакцин в Европе: где мы находимся?». Экспертный обзор вакцин. 13 (8): 979–87. Дои:10.1586/14760584.2014.933077. PMID 24958075. S2CID 23471069.
- ^ а б c Fukuda, E .; Танимото, Дж. (2014). Влияние упорных лиц на распространение инфекционных заболеваний в рамках политики добровольной вакцинации. Springer. С. 1–10. ISBN 978-3319133591. Получено 30 марта 2015.
- ^ а б Барретт, Скотт (2014). «Глобальные общественные блага и международное развитие». В Дж. Уоррене Эвансе; Робин Дэвис (ред.). Слишком глобален, чтобы потерпеть неудачу: Всемирный банк на пересечении национальной и глобальной государственной политики в 2025 году. Публикации Всемирного банка. С. 13–18. ISBN 978-1464803109.
- ^ а б c Gowda, C; Демпси, А. Ф. (2013). «Рост (и падение?) Нерешительности родителей относительно вакцинации». Человеческие вакцины и иммунотерапевтические препараты. 9 (8): 1755–62. Дои:10.4161 / hv.25085. ЧВК 3906278. PMID 23744504.
- ^ Одзава, S; Стек, М. Л. (2013). «Общественное доверие и признание вакцины - международные перспективы». Человеческие вакцины и иммунотерапевтические препараты. 9 (8): 1774–78. Дои:10.4161 / hv.24961. ЧВК 3906280. PMID 23733039.
- ^ Паркер, А. М .; Vardavas, R; Marcum, C. S .; Гиденгил, К. А. (2013). «Сознательный учет коллективного иммунитета при принятии решений о вакцинации против гриппа». Американский журнал профилактической медицины. 45 (1): 118–21. Дои:10.1016 / j.amepre.2013.02.016. ЧВК 3694502. PMID 23790997.
- ^ Если не указано иное, р0 значения от: История и эпидемиология глобальной ликвидации оспы В архиве 17 марта 2017 в Wayback Machine Из учебного курса «Оспа: болезнь, профилактика и вмешательство». В Центры по контролю и профилактике заболеваний и Всемирная организация здоровья. Слайд 17. Проверено 13 марта 2015 г.
- ^ а б Биггерстафф, М; Cauchemez, S; Рид, C; Гамбхир, М; Финелли, Л. (2014). «Оценки репродуктивной способности сезонного, пандемического и зоонозного гриппа: систематический обзор литературы». BMC Инфекционные болезни. 14: 480. Дои:10.1186/1471-2334-14-480. ЧВК 4169819. PMID 25186370.
- ^ Fontanet A, Cauchemez S (9 сентября 2020 г.). "Коллективный иммунитет от COVID-19: где мы?". Нат Рев Иммунол. 20 (10): 583–584. Дои:10.1038 / s41577-020-00451-5. ЧВК 7480627. PMID 32908300.
- ^ Randolph HE, Barreiro LB (19 мая 2020 г.). «Иммунитет стада: понимание COVID-19». Иммунитет. 52 (5): 737–741. Дои:10.1016 / j.immuni.2020.04.012. ЧВК 7236739. PMID 32433946.
- ^ Валлинга, Дж; Теунис, П. (2004). «Различные эпидемические кривые тяжелого острого респираторного синдрома демонстрируют сходное воздействие мер контроля». Американский журнал эпидемиологии. 160 (6): 509–16. Дои:10.1093 / aje / kwh255. ЧВК 7110200. PMID 15353409.
- ^ Альтхаус, К. Л. (2014). «Оценка репродуктивного числа вируса Эбола (EBOV) во время вспышки 2014 года в Западной Африке». PLOS токи. 6. arXiv:1408.3505. Bibcode:2014arXiv1408.3505A. Дои:10.1371 / current.outbreaks.91afb5e0f279e7f29e7056095255b288. ЧВК 4169395. PMID 25642364.
- ^ а б Даббагян, В .; Маго, В. К. (2013). Теории и моделирование сложных социальных систем. Springer. С. 134–35. ISBN 978-3642391491. Получено 29 марта 2015.
- ^ Гендель, Андреас; Longini, Ira M; Антиа, Рустом (22 марта 2007 г.). «Какова наилучшая стратегия борьбы с множественными вспышками инфекционных заболеваний?». Труды Королевского общества B: биологические науки. 274 (1611): 833–837. Дои:10.1098 / rspb.2006.0015. ISSN 0962-8452. ЧВК 2093965. PMID 17251095.
В целом количество инфицированных растет до тех пор, пока количество восприимчивых не упадет до Sth. На этом этапе среднее количество вторичных инфекций, созданных инфицированным человеком, падает ниже 1, и поэтому количество зараженных начинает уменьшаться. Однако именно в этой точке перегиба присутствует максимальное количество зараженных. Эти зараженные будут создавать в среднем менее 1, но все же более чем ноль новых заражений, что приведет к дополнительному истощению восприимчивых и, следовательно, к перерегулированию.
- ^ Фунг, Исаак Чун-Хай; Антиа, Рустом; Гендель, Андреас (11 июня 2012 г.). «Как минимизировать частоту атак во время множественных вспышек гриппа среди неоднородного населения». PLOS ONE. 7 (6): e36573. Bibcode:2012PLoSO ... 736573F. Дои:10.1371 / journal.pone.0036573. ISSN 1932-6203. ЧВК 3372524. PMID 22701558.
- ^ Bergstrom, Carl T .; Дин, Натали (1 мая 2020 г.). «Мнение: чего не говорят сторонники« естественного »иммунитета стада». Нью-Йорк Таймс. Получено 30 мая 2020.
- ^ а б c Рашид, H; Хандакер, G; Буй, Р. (2012). «Вакцинация и коллективный иммунитет: что еще мы знаем?». Современное мнение об инфекционных заболеваниях. 25 (3): 243–249. Дои:10.1097 / QCO.0b013e328352f727. PMID 22561998. S2CID 19197608.
- ^ Maglione, M.A .; Das, L; Raaen, L; Смит, А; Chari, R; Ньюберри, S; Shanman, R; Перри, Т. Goetz, M. B .; Гиденгил, C (2014). «Безопасность вакцин, используемых для плановой иммунизации детей в США: систематический обзор». Педиатрия. 134 (2): 325–37. Дои:10.1542 / пед.2014-1079. PMID 25086160.
- ^ Ди Пьетрантонж, Карло; Риветти, Алессандро; Маркионе, Паскуале; Дебалини, Мария Грация; Демичели, Витторио (20 апреля 2020 г.). «Вакцины против кори, паротита, краснухи и ветряной оспы у детей». Кокрановская база данных систематических обзоров. 4: CD004407. Дои:10.1002 / 14651858.CD004407.pub4. ISSN 1469-493X. ЧВК 7169657. PMID 32309885.
- ^ а б c Поммервилль, Дж. К. (2014). Основы микробиологии: издание систем организма. Издательство "Джонс и Бартлетт". С. 559–63. ISBN 978-1284057102. Получено 30 марта 2015.
- ^ Папалукас, О; Giannouli, G; Папаевангелу, V (2014). «Успехи и проблемы в вакцине против ветряной оспы». Терапевтические достижения в области вакцин. 2 (2): 39–55. Дои:10.1177/2051013613515621. ЧВК 3991154. PMID 24757524.
- ^ Шенн, Ф (2013). «Неспецифические эффекты вакцин и снижение детской смертности». Клиническая терапия. 35 (2): 109–14. Дои:10.1016 / j.clinthera.2013.01.007. PMID 23375475.
- ^ Visser, A; Хусен, А (2012). "Haemophilus influenzae конъюгированные вакцины типа b - перспективы Южной Африки ». Вакцина. 30 (Дополнение 3): C52–57. Дои:10.1016 / j.vaccine.2012.06.022. HDL:2263/20792. PMID 22939022.
- ^ Leuridan, E; Саббе, М; Ван Дамм, П. (2012). «Вспышка кори в Европе: восприимчивость младенцев, слишком маленьких для иммунизации». Вакцина. 30 (41): 5905–13. Дои:10.1016 / j.vaccine.2012.07.035. PMID 22841972.
- ^ Hodgins, D.C .; Шевен, П. Э. (2012). «Вакцинация новорожденных: проблемы и проблемы». Вакцина. 30 (9): 1541–59. Дои:10.1016 / j.vaccine.2011.12.047. PMID 22189699.
- ^ Chucri, T. M .; Monteiro, J.M .; Lima, A.R .; Salvadori, M. L .; Kfoury Jr, J. R .; Миглино, М.А. (2010). «Обзор иммунного переноса через плаценту». Журнал репродуктивной иммунологии. 87 (1–2): 14–20. Дои:10.1016 / j.jri.2010.08.062. PMID 20956021.
- ^ Palmeira, P; Quinello, C; Silveira-Lessa, A. L .; Zago, C. A.; Carneiro-Sampaio, M (2012). "IgG placental transfer in healthy and pathological pregnancies". Клиническая иммунология и иммунология развития. 2012: 1–13. Дои:10.1155/2012/985646. ЧВК 3251916. PMID 22235228.
- ^ а б Parija, S. C. (2014). Textbook of Microbiology & Immunology. Elsevier Health Sciences. С. 88–89. ISBN 978-8131236246. Получено 30 марта 2015.
- ^ Detels, R .; Gulliford, M.; Karim, Q. A.; Tan, C. C. (2015). Oxford Textbook of Global Public Health. Издательство Оксфордского университета. п. 1490. ISBN 978-0199661756. Получено 30 марта 2015.
- ^ Demicheli, Vittorio; Barale, Antonella; Rivetti, Alessandro (6 July 2015). "Vaccines for women for preventing neonatal tetanus". Кокрановская база данных систематических обзоров (7): CD002959. Дои:10.1002/14651858.CD002959.pub4. ISSN 1469-493X. ЧВК 7138051. PMID 26144877.
- ^ Swamy, G. K.; Garcia-Putnam, R (2013). "Vaccine-preventable diseases in pregnancy". Американский журнал перинатологии. 30 (2): 89–97. Дои:10.1055/s-0032-1331032. PMID 23271378.
- ^ Bärnighausen, T.; Bloom, D. E.; Cafiero-Fonseca, E. T.; O'Brien, J. C. (26 August 2014). "Valuing vaccination". Proc Natl Acad Sci U S A. 111 (34): 12313–19. Bibcode:2014PNAS..11112313B. Дои:10.1073/pnas.1400475111. ЧВК 4151736. PMID 25136129.
- ^ а б c Deogaonkar, R.; Hutubessy, R.; van der Putten I.; Evers S.; Jit M. (16 October 2012). "Systematic review of studies evaluating the broader economic impact of vaccination in low and middle income countries". BMC Public Health. 12: 878. Дои:10.1186/1471-2458-12-878. ЧВК 3532196. PMID 23072714.
- ^ а б Jit, M.; Newall, A. T.; Beutels, P. (April 2013). «Ключевые вопросы оценки воздействия и экономической эффективности стратегий вакцинации против сезонного гриппа». Hum Vaccin Immunother. 9 (4): 834–40. Дои:10.4161 / hv.23637. ЧВК 3903903. PMID 23357859.
- ^ Topley, W. W. C.; Wilson, G. S. (May 1923). "The Spread of Bacterial Infection. The Problem of Herd-Immunity". Журнал гигиены. 21 (3): 243–49. Дои:10.1017/s0022172400031478. ЧВК 2167341. PMID 20474777.
- ^ Hedrich, A. W. (1933). Monthly Estimates of the Child Population Susceptible to Measles, 1900–1931, Baltimore, Md. Американский журнал эпидемиологии, 17(3), 613–636.
- ^ Strassburg, M. A. (1982). "The global eradication of smallpox". Американский журнал инфекционного контроля. 10 (2): 53–59. Дои:10.1016/0196-6553(82)90003-7. PMID 7044193.
внешняя ссылка
| Scholia имеет профиль для коллективный иммунитет (Q736798). |
- Topley, W. W. C.; Wilson, G. S. (May 1923). "The Spread of Bacterial Infection. The Problem of Herd-Immunity". Журнал гигиены. 21 (3): 243–49. Дои:10.1017/s0022172400031478. ЧВК 2167341. PMID 20474777.
- A visual simulation of herd immunity written by Shane Killian and modified by Robert Webb






